一种与放化疗引起的听力损伤相关的SNP标志物及其应用
一种与放化疗引起的听力损伤相关的snp标志物及其应用
技术领域
1.本发明涉及基因工程与肿瘤学技术领域,具体地,涉及一种与放化疗引起的听力损伤相关的snp标志物及其应用。
背景技术:
2.顺铂是世界上使用范围最广泛的化疗药物之一,但同时也是一个已知的强耳毒性药物。此外,对于需要接受头颈部放射治疗的肿瘤患者而言,由于照射部位毗邻听觉器官,射线也会不可避免地损害邻近的听觉器官从而导致听力下降。顺铂化疗和放射治疗均可引起不可逆的感音神经性听力损伤,而接受放疗联合顺铂化疗的肿瘤患者会出现更严重的听力损伤,严重影响肿瘤患者日常生活起居,发病率较高,且通常呈现进行性加重、不可逆性,甚至部分患者会进展为永久性听力损失。然而,临床上暂无特效药物可以治疗放化疗引起的听力损伤,出现严重听力损伤的患者只能靠助听器或耳蜗移植来代偿丢失的听力。永久性听力障碍会严重影响患者的长期生活质量,同时也会造成巨大的疾病负担和社会经济损失。
3.放化疗引起的听力损伤发生风险与年龄、肿瘤t分期、耳蜗照射剂量、顺铂使用剂量等多种因素有关。但是,在考虑了临床、治疗和人口学因素后,放化疗引起的听力损伤在发病率和严重程度上仍然呈现比较大的个体间差异,这提示个体的遗传因素也起到了一定作用。
4.单核苷酸多态性(single nucleotide polymorphism,snp)是引起治疗相关毒副反应的重要的遗传易感因素。现有技术已公开了多种与肿瘤治疗毒副反应相关的遗传分子标志物,如与放射性脑损伤相关的snp标志物(rs162171、rs9304497、rs10501719等),与放射性口腔黏膜炎相关的snp标志物(rs4433399、rs1562524、rs7673990等),并建立了可在临床推广使用的风险预测模型,用于高危人群识别及个体化防治。因此,对于进行放疗联合顺铂化疗的肿瘤患者,如果能早期识别与放疗或化疗所致听力损伤相关的分子标志物并预测发病风险,进而提前采取针对性的预防保护措施,将有望降低该不良反应的发生率。
5.然而,目前尚无可用于临床预测肿瘤患者放化疗引起的听力损伤的分子标志物及其组合,也缺乏对该不良反应的有效风险评估方案。因此,若能成功筛选出与放化疗所致听力损伤发病相关的遗传分子标志物,并研发相应的诊断试剂盒,将有助于识别高危个体,提前采取预防保护措施,实施个体化治疗,提高患者的生存质量。
技术实现要素:
6.为了解决现有技术中尚无可用于临床预测肿瘤患者放化疗引起的听力损伤的分子标志物的问题,本发明提供了一种与放化疗引起的听力损伤相关的snp标志物及其应用。
7.本发明的第一个目的是提供一种与放化疗引起的听力损伤相关的snp标志物的检测试剂。
8.本发明的第二个目的是提供上述检测试剂在制备检测和/或预测肿瘤放化疗引起
听力损伤的风险的试剂盒中的应用。
9.本发明的第三个目的是提供一种放化疗引起的听力损伤的风险评分系统。
10.本发明的第四个目的是提供上述风险评分系统在制备检测和/或预测肿瘤放化疗引起听力损伤的风险的试剂盒中的应用。
11.本发明的第五个目的是提供一种检测和/或预测肿瘤放化疗引起听力损伤的风险的试剂盒。
12.为了实现上述目的,本发明是通过以下方案予以实现的:
13.本发明通过分析接受放疗联合顺铂化疗的鼻咽癌患者放化疗所致听力损伤发生风险与单核苷酸多态性的关联,寻找与放化疗引起的听力损伤高度相关的snp标志物,并研制便于临床应用的可预测肿瘤治疗引起的听力损伤发病风险的检测试剂盒,为识别放化疗相关听力损伤的高危个体提供支持,有助于采取针对性的预防保护措施和个体化治疗,减少听力损伤的发生或降低听力损伤的严重程度,提高患者的长期生存质量。
14.一种与放化疗引起的听力损伤相关的snp标志物的检测试剂,所述检测试剂检测snp标志物1~8,所述snp标志物1为rs1050851;所述snp标志物2为rs117098517;所述snp标志物3为rs1485149、rs11713855、rs73028787、rs9872473、rs6784713、rs36011752、rs34056014、rs66888336、rs869935、rs35486575、rs13072384或rs3864080中的任意一个;所述snp标志物4为rs17010289、rs17010288、rs117227749或rs75222194中的任意一个;所述snp标志物5为rs79938362或rs116989317中的任意一个;所述snp标志物6为rs73335760;所述snp标志物7为rs201061882、rs11700622、rs75423607、rs76415665、rs112894701、rs79765594、rs73354686、rs76372004、rs11702842、rs73193458或rs138904949中的任意一个;所述snp标志物8为rs2275994、rs6996060、rs10104930、rs16868196、rs192243723、rs150249158、rs375127474和rs141273852中的任意一个。
15.rs11713855、rs73028787、rs9872473、rs6784713、rs36011752、rs34056014、rs66888336、rs869935、rs35486575、rs13072384和rs3864080是rs1485149的连锁snp标志物;rs17010288、rs117227749和rs75222194是rs17010289的连锁snp标志物;rs116989317是rs79938362的连锁snp标志物;rs11700622、rs75423607、rs76415665、rs112894701、rs79765594、rs73354686、rs76372004、rs11702842、rs73193458和rs138904949是rs201061882的连锁snp标志物;rs6996060、rs10104930、rs16868196、rs192243723、rs150249158、rs375127474和rs141273852是rs2275994的连锁snp标志物。
16.以人类基因组hg19作为参考基因组:
17.rs1050851位于14号染色体第35872926位碱基,参考等位基因为g,效应等位基因为a;
18.rs117098517位于18号染色体第56986855位碱基,参考等位基因为c,效应等位基因为t;
19.rs1485149位于3号染色体第8013452位碱基,参考等位基因为a,效应等位基因为c;
20.rs11713855位于3号染色体第7992395位碱基,在东亚人种中,其与rs1485149的连锁不平衡((linkage disequilibrium,ld)r2为0.94,参考等位基因为t,效应等位基因为c;
21.rs73028787位于3号染色体第7994403位碱基,其与rs1485149的ld r2为0.91,参
考等位基因为c,效应等位基因为a;
22.rs9872473位于3号染色体第7994673位碱基,其与rs1485149的ld r2为0.94,参考等位基因为g,效应等位基因为a;
23.rs6784713位于3号染色体第7997490位碱基,其与rs1485149的ld r2为0.97,参考等位基因为t,效应等位基因为g;
24.rs36011752位于3号染色体第8000608位碱基,其与rs1485149的ld r2为0.94,参考等位基因为a,效应等位基因为g;
25.rs34056014位于3号染色体第8000863位碱基,其与rs1485149的ld r2为0.94,参考等位基因为c,效应等位基因为t;
26.rs66888336位于3号染色体第8003453位碱基,其与rs1485149的ld r2为0.94,参考等位基因为c,效应等位基因为t;
27.rs869935位于3号染色体第8005225位碱基,其与rs1485149的ld r2为0.97,参考等位基因为a,效应等位基因为g;
28.rs35486575位于3号染色体第8006648位碱基,其与rs1485149的ld r2为0.94,参考等位基因为g,效应等位基因为a;
29.rs13072384位于3号染色体第8007601位碱基,其与rs1485149的ld r2为0.94,参考等位基因为a,效应等位基因为g;
30.rs3864080位于3号染色体第8010700位碱基,其与rs1485149的ld r2为0.97,参考等位基因为t,效应等位基因为a;
31.rs17010289位于2号染色体第124346351位碱基,参考等位基因为a,效应等位基因为g;
32.rs17010288位于2号染色体第124345218位碱基,其与rs17010289的ld r2为0.97,参考等位基因为g,效应等位基因为a;
33.rs117227749位于2号染色体第124378950位碱基,其与rs17010289的ld r2为0.97,参考等位基因为a,效应等位基因为t;
34.rs75222194位于2号染色体第124432237位碱基,其与rs17010289的ld r2为0.87,参考等位基因为t,效应等位基因为c;
35.rs79938362位于13号染色体第110743126位碱基,参考等位基因为c,效应等位基因为t;
36.rs116989317位于13号染色体第110757745位碱基,其与rs79938362的ld r2为0.86,参考等位基因为g,效应等位基因为a;
37.rs73335760位于5号染色体第174470036位碱基,参考等位基因为a,效应等位基因为g;
38.rs201061882位于21号染色体第33360958位碱基,参考等位基因为ttc,效应等位基因为t;
39.rs11700622位于21号染色体第33356500位碱基,其与rs201061882的ld r2为0.87,参考等位基因为g,效应等位基因为a;
40.rs75423607位于21号染色体第33360400位碱基,其与rs201061882的ld r2为0.95,参考等位基因为c,效应等位基因为t;
41.rs76415665位于21号染色体第33361616位碱基,其与rs201061882的ld r2为0.95,参考等位基因为g,效应等位基因为c;
42.rs112894701位于21号染色体第33365503位碱基,其与rs201061882的ld r2为0.95,参考等位基因为c,效应等位基因为t;
43.rs79765594位于21号染色体第33367264位碱基,其与rs201061882的ld r2为0.95,参考等位基因为a,效应等位基因为g;
44.rs73354686位于21号染色体第33367365位碱基,其与rs201061882的ld r2为0.95,参考等位基因为a,效应等位基因为g;
45.rs76372004位于21号染色体第33367519位碱基,其与rs201061882的ld r2为0.95,参考等位基因为c,效应等位基因为t;
46.rs11702842位于21号染色体第33368355位碱基,其与rs201061882的ld r2为1.00,参考等位基因为g,效应等位基因为a;
47.rs73193458位于21号染色体第33375476位碱基,其与rs201061882的ld r2为0.91,参考等位基因为g,效应等位基因为a;
48.rs138904949位于21号染色体第33375702位碱基,其与rs201061882的ld r2为0.95,参考等位基因为at,效应等位基因为a;
49.rs2275994位于8号染色体第102700230位碱基,参考等位基因为c,效应等位基因为t;
50.rs6996060位于8号染色体第102675564位碱基,其与rs2275994的ld r2为0.89,参考等位基因为g,效应等位基因为a;
51.rs10104930位于8号染色体第102681820位碱基,其与rs2275994的ld r2为0.92,参考等位基因为a,效应等位基因为t;
52.rs16868196位于8号染色体第102682242位碱基,其与rs2275994的ld r2为0.92,参考等位基因为c,效应等位基因为t;
53.rs192243723位于8号染色体第102684646位碱基,其与rs2275994的ld r2为0.92,参考等位基因为a,效应等位基因为c;
54.rs150249158位于8号染色体第102686533位碱基,其与rs2275994的ld r2为0.92,参考等位基因为c,效应等位基因为t;
55.rs375127474位于8号染色体第102688459位碱基,其与rs2275994的ld r2为0.92,参考等位基因为g,效应等位基因为a;
56.rs141273852位于8号染色体第102690577位碱基,其与rs2275994的ld r2为0.92,参考等位基因为c,效应等位基因为t。
57.所述snp标志物1~8的基因型分型具体为:
58.针对所述snp标志物1:
59.rs1050851的纯合保护型为gg,杂合型为ag或ga,纯合危险型为aa;
60.针对所述snp标志物2:
61.rs117098517的纯合保护型为cc,杂合型为tc或ct,纯合危险型为tt;
62.针对所述snp标志物3:
63.rs1485149的纯合保护型为aa,杂合型为ca或ac,纯合危险型为cc;
64.rs11713855的纯合保护型为tt,杂合型为ct或tc,纯合危险型为cc;
65.rs73028787的纯合保护型为cc,杂合型为ac或ca,纯合危险型为aa;
66.rs9872473的纯合保护型为gg,杂合型为ag或ga,纯合危险型为aa;
67.rs6784713的纯合保护型为tt,杂合型为gt或tg,纯合危险型为gg;
68.rs36011752的纯合保护型为aa,杂合型为ga或ag,纯合危险型为gg;
69.rs34056014的纯合保护型为cc,杂合型为tc或ct,纯合危险型为tt;
70.rs66888336的纯合保护型为cc,杂合型为tc或ct,纯合危险型为tt;
71.rs869935的纯合保护型为aa,杂合型为ga或ag,纯合危险型为gg;
72.rs35486575的纯合保护型为gg,杂合型为ag或ga,纯合危险型为aa;
73.rs13072384的纯合保护型为aa,杂合型为ga或ag,纯合危险型为gg;
74.rs3864080的纯合保护型为tt,杂合型为at或ta,纯合危险型为aa;
75.针对所述snp标志物4:
76.rs17010289的纯合保护型为aa,杂合型为ga或ag,纯合危险型为gg;
77.rs17010288的纯合保护型为gg,杂合型为ag或ga,纯合危险型为aa;
78.rs117227749的纯合保护型为aa,杂合型为ta或at,纯合危险型为tt;
79.rs75222194的纯合保护型为tt,杂合型为ct或tc,纯合危险型为cc;
80.针对所述snp标志物5:
81.rs79938362的纯合保护型为cc,杂合型为tc或ct,纯合危险型为tt;
82.rs116989317的纯合保护型为gg,杂合型为ag或ga,纯合危险型为aa;
83.针对所述snp标志物6:
84.rs73335760的纯合保护型为aa,杂合型为ga或ag,纯合危险型为gg;
85.针对所述snp标志物7:
86.rs201061882的纯合保护型为ttcttc,杂合型为tttc或ttct,纯合危险型为tt;
87.rs11700622的纯合保护型为gg,杂合型为ag或ga,纯合危险型为aa;
88.rs75423607的纯合保护型为cc,杂合型为tc或ct,纯合危险型为tt;
89.rs76415665的纯合保护型为gg,杂合型为cg或gc,纯合危险型为cc;
90.rs112894701的纯合保护型为cc,杂合型为tc或ct,纯合危险型为tt;
91.rs79765594的纯合保护型为aa,杂合型为ga或ag,纯合危险型为gg;
92.rs73354686的纯合保护型为aa,杂合型为ga或ag,纯合危险型为gg;
93.rs76372004的纯合保护型为cc,杂合型为tc或ct,纯合危险型为tt;
94.rs11702842的纯合保护型为gg,杂合型为ag或ga,纯合危险型为aa;
95.rs73193458的纯合保护型为gg,杂合型为ag或ga,纯合危险型为aa;
96.rs138904949的纯合保护型为atat,杂合型为aat或ata,纯合危险型为aa;
97.针对所述snp标志物8:
98.rs2275994的纯合保护型为cc,杂合型为tc或ct,纯合危险型为tt;
99.rs6996060的纯合保护型为gg,杂合型为ag或ga,纯合危险型为aa;
100.rs10104930的纯合保护型为aa,杂合型为ta或at,纯合危险型为tt;
101.rs16868196的纯合保护型为cc,杂合型为tc或ct,纯合危险型为tt;
102.rs192243723的纯合保护型为aa,杂合型为ca或ac,纯合危险型为cc;
103.rs150249158的纯合保护型为cc,杂合型为tc或ct,纯合危险型为tt;
104.rs375127474的纯合保护型为gg,杂合型为ag或ga,纯合危险型为aa;
105.rs141273852的纯合保护型为cc,杂合型为tc或ct,纯合危险型为tt;
106.snp标志物1~8的基因型分型中,纯合保护型为携带两个致放化疗引起的听力损伤风险低的等位基因,即携带两个参考等位基因;杂合型为同时携带一个致听力损伤风险低和一个致听力损伤风险高的等位基因,即携带一个参考等位基因和一个效应等位基因;纯合危险型为携带两个致听力损伤风险高的等位基因,即携带两个效应等位基因。
107.优选地,所述检测试剂检测rs1050851、rs117098517、rs1485149、rs17010289、rs79938362、rs73335760、rs201061882或rs2275994中的任意一种或几种。
108.优选地,所述检测试剂包含引物和/或探针。
109.更优选地,所述引物为以下的一种或几种:
110.检测rs1050851的引物,核苷酸序列如seq id no:1~2所示;
111.检测rs117098517的引物,核苷酸序列如seq id no:5~6所示;
112.检测rs1485149的引物,核苷酸序列如seq id no:9~10所示;
113.检测rs11713855的引物,核苷酸序列如seq id no:13~14所示;
114.检测rs73028787的引物,核苷酸序列如seq id no:17~18所示;
115.检测rs9872473的引物,核苷酸序列如seq id no:21~22所示;
116.检测rs6784713的引物,核苷酸序列如seq id no:25~26所示;
117.检测rs36011752的引物,核苷酸序列如seq id no:29~30所示;
118.检测rs34056014的引物,核苷酸序列如seq id no:33~34所示;
119.检测rs66888336的引物,核苷酸序列如seq id no:37~38所示;
120.检测rs869935的引物,核苷酸序列如seq id no:41~42所示;
121.检测rs35486575的引物,核苷酸序列如seq id no:45~46所示;
122.检测rs13072384的引物,核苷酸序列如seq id no:49~50所示;
123.检测rs3864080的引物,核苷酸序列如seq id no:53~54所示;
124.检测rs17010289的引物,核苷酸序列如seq id no:57~58所示;
125.检测rs17010288的引物,核苷酸序列如seq id no:61~62所示;
126.检测rs117227749的引物,核苷酸序列如seq id no:65~66所示;
127.检测rs75222194的引物,核苷酸序列如seq id no:69~70所示;
128.检测rs79938362的引物,核苷酸序列如seq id no:73~74所示;
129.检测rs116989317的引物,核苷酸序列如seq id no:77~78所示;
130.检测rs73335760的引物,核苷酸序列如seq id no:81~82所示;
131.检测rs201061882的引物,核苷酸序列如seq id no:85~86所示;
132.检测rs11700622的引物,核苷酸序列如seq id no:89~90所示;
133.检测rs75423607的引物,核苷酸序列如seq id no:93~94所示;
134.检测rs76415665的引物,核苷酸序列如seq id no:97~98所示;
135.检测rs112894701的引物,核苷酸序列如seq id no:101~102所示;
136.检测rs79765594的引物,核苷酸序列如seq id no:105~106所示;
137.检测rs73354686的引物,核苷酸序列如seq id no:109~110所示;
138.检测rs76372004的引物,核苷酸序列如seq id no:113~114所示;
139.检测rs11702842的引物,核苷酸序列如seq id no:117~118所示;
140.检测rs73193458的引物,核苷酸序列如seq id no:121~122所示;
141.检测rs138904949的引物,核苷酸序列如seq id no:125~126所示;
142.检测rs2275994的引物,核苷酸序列如seq id no:129~130所示;
143.检测rs6996060的引物,核苷酸序列如seq id no:133~134所示;
144.检测rs10104930的引物,核苷酸序列如seq id no:137~138所示;
145.检测rs16868196的引物,核苷酸序列如seq id no:141~142所示;
146.检测rs192243723的引物,核苷酸序列如seq id no:145~146所示;
147.检测rs150249158的引物,核苷酸序列如seq id no:149~150所示;
148.检测rs375127474的引物,核苷酸序列如seq id no:153~154所示;
149.检测rs141273852的引物,核苷酸序列如seq id no:157~158所示。
150.更优选地,所述探针为以下的一种或几种:
151.检测rs1050851的探针,核苷酸序列如seq id no:3~4所示;
152.检测rs117098517的探针,核苷酸序列如seq id no:7~8所示;
153.检测rs1485149的探针,核苷酸序列如seq id no:11~12所示;
154.检测rs11713855的探针,核苷酸序列如seq id no:15~16所示;
155.检测rs73028787的探针,核苷酸序列如seq id no:19~20所示;
156.检测rs9872473的探针,核苷酸序列如seq id no:23~24所示;
157.检测rs6784713的探针,核苷酸序列如seq id no:27~28所示;
158.检测rs36011752的探针,核苷酸序列如seq id no:31~32所示;
159.检测rs34056014的探针,核苷酸序列如seq id no:35~36所示;
160.检测rs66888336的探针,核苷酸序列如seq id no:39~40所示;
161.检测rs869935的探针,核苷酸序列如seq id no:43~44所示;
162.检测rs35486575的探针,核苷酸序列如seq id no:47~48所示;
163.检测rs13072384的探针,核苷酸序列如seq id no:51~52所示;
164.检测rs3864080的探针,核苷酸序列如seq id no:55~56所示;
165.检测rs17010289的探针,核苷酸序列如seq id no:59~60所示;
166.检测rs17010288的探针,核苷酸序列如seq id no:63~64所示;
167.检测rs117227749的探针,核苷酸序列如seq id no:67~68所示;
168.检测rs75222194的探针,核苷酸序列如seq id no:71~72所示;
169.检测rs79938362的探针,核苷酸序列如seq id no:75~76所示;
170.检测rs116989317的探针,核苷酸序列如seq id no:79~80所示;
171.检测rs73335760的探针,核苷酸序列如seq id no:83~84所示;
172.检测rs201061882的探针,核苷酸序列如seq id no:87~88所示;
173.检测rs11700622的探针,核苷酸序列如seq id no:91~92所示;
174.检测rs75423607的探针,核苷酸序列如seq id no:95~96所示;
175.检测rs76415665的探针,核苷酸序列如seq id no:99~100所示;
176.检测rs112894701的探针,核苷酸序列如seq id no:103~104所示;
177.检测rs79765594的探针,核苷酸序列如seq id no:107~108所示;
178.检测rs73354686的探针,核苷酸序列如seq id no:111~112所示;
179.检测rs76372004的探针,核苷酸序列如seq id no:115~116所示;
180.检测rs11702842的探针,核苷酸序列如seq id no:119~120所示;
181.检测rs73193458的探针,核苷酸序列如seq id no:123~124所示;
182.检测rs138904949的探针,核苷酸序列如seq id no:127~128所示;
183.检测rs2275994的探针,核苷酸序列如seq id no:131~132所示;
184.检测rs6996060的探针,核苷酸序列如seq id no:135~136所示;
185.检测rs10104930的探针,核苷酸序列如seq id no:139~140所示;
186.检测rs16868196的探针,核苷酸序列如seq id no:143~144所示;
187.检测rs192243723的探针,核苷酸序列如seq id no:147~148所示;
188.检测rs150249158的探针,核苷酸序列如seq id no:151~152所示;
189.检测rs375127474的探针,核苷酸序列如seq id no:155~156所示;
190.检测rs141273852的探针,核苷酸序列如seq id no:159~160所示。
191.任一上述检测试剂在制备检测和/或预测肿瘤放化疗引起听力损伤的风险的试剂盒中的应用也应在本发明的保护范围之内。
192.利用cox比例风险回归模型构建放化疗引起听力损伤的风险评分系统,以是否发生放化疗引起听力损伤和发生听力损伤的时间作为结局变量,以snp标志物1~8和3个临床因素(诊断年龄、肿瘤t分期和同期化疗顺铂剂量)作为预测变量,进行风险评分模型的拟合,从而获得各预测变量的回归系数。对于发生放化疗引起听力损伤的患者而言,发生听力损伤的时间定义为从肿瘤放疗或化疗开始到首次出现听力损伤症状的时间;对于未发生放化疗引起听力损伤的患者而言,发生听力损伤的时间定义为从肿瘤放疗或化疗开始到研究结束的时间。
193.将样本随机分为训练集和验证集,利用训练集构建放化疗引起听力损伤的风险评分系统。然后,利用该风险评分系统预测训练集中每个样本在放化疗后5年内发生听力损伤的风险,获得训练集中每个样本的听力损伤危险评分。以训练集中听力损伤危险评分的中位数作为危险评分的阈值。
194.一种放化疗引起的听力损伤的风险评分系统,包含信息采集模块、储存模块、信息分析模块、判断模块和输出模块;
195.所述信息采集模块用于获取待测样本的特征参数,所述特征参数包括上述snp标志物1~8在待测样本基因组dna中的基因型分型及待测样本的诊断年龄和肿瘤t分期和同期化疗顺铂剂量;
196.所述储存模块用于储存信息采集模块中获取的特征参数和判断模块中的危险评分的阈值;
197.所述信息分析模块,用于根据获得的特征参数建立的cox比例风险回归模型分析得到危险评分;
198.所述判断模块,用于根据危险评分及其阈值判断待测样本的放化疗引起的听力损伤的风险;判定标准为:危险评分>危险评分的阈值,则待测样本是放化疗引起听力损伤的高危个体;危险评分≤危险评分的阈值,则待测样本是放化疗引起听力损伤的低危个体;
199.所述输出模块,用于输出待测样本的放化疗引起的听力损伤的风险。
200.优选地,所述风险评分系统,包含信息采集模块、储存模块、信息分析模块、判断模块和输出模块;
201.所述信息采集模块用于获取待测样本的特征参数,所述特征参数包括上述snp标志物1~8在待测样本基因组dna中的基因型分型及待测样本的诊断年龄、肿瘤t分期和同期化疗顺铂剂量;
202.所述储存模块用于储存信息采集模块中获取的特征参数和判断模块中的危险评分的阈值;
203.所述信息分析模块,根据获得的特征参数,通过公式计算得到危险评分;
204.所述判断模块,根据危险评分及其阈值判断待测样本的放化疗引起的听力损伤的风险;判定标准为:危险评分>危险评分的阈值,则待测样本是放化疗引起听力损伤的高危个体;危险评分≤危险评分的阈值,则待测样本是放化疗引起听力损伤的低危个体。
205.所述公式为:危险评分=(0.5616
×
诊断年龄的评分)+(0.5433
×
肿瘤t分期的评分)+(0.5211
×
同期化疗顺铂剂量的评分)+(a
×
snp标志物1的基因型分型的评分)+(b
×
snp标志物2的基因型分型的评分)+(c
×
snp标志物3的基因型分型的评分)+(d
×
snp标志物4的基因型分型的评分)+(e
×
snp标志物5的基因型分型的评分)+(f
×
snp标志物6的基因型分型的评分)+(g
×
snp标志物7的基因型分型的评分)+(h
×
snp标志物8的基因型分型的评分);
206.所述诊断年龄的评分为:诊断年龄《50岁=“0”;诊断年龄≥50岁=“1”;
207.所述肿瘤t分期的评分为:t1~t2期=“0”;t3~t4期=“1”;
208.所述同期化疗顺铂剂量的评分为:同期化疗顺铂剂量《155mg/m2=“0”,同期化疗顺铂剂量≥155mg/m2=“1”;
209.所述snp标志物1~8的基因型分型的评分为:纯合保护型=“0”;杂合型=“1”;纯合危险型=“2”;
210.所述a、b、c、d、e、f、g和h分别为snp标志物1~8的回归系数;
211.所述snp标志物1~8的基因型分型具体为:
212.针对所述snp标志物1:
213.rs1050851的纯合保护型为gg,杂合型为ag或ga,纯合危险型为aa;
214.针对所述snp标志物2:
215.rs117098517的纯合保护型为cc,杂合型为tc或ct,纯合危险型为tt;
216.针对所述snp标志物3:
217.rs1485149的纯合保护型为aa,杂合型为ca或ac,纯合危险型为cc;
218.rs11713855的纯合保护型为tt,杂合型为ct或tc,纯合危险型为cc;
219.rs73028787的纯合保护型为cc,杂合型为ac或ca,纯合危险型为aa;
220.rs9872473的纯合保护型为gg,杂合型为ag或ga,纯合危险型为aa;
221.rs6784713的纯合保护型为tt,杂合型为gt或tg,纯合危险型为gg;
222.rs36011752的纯合保护型为aa,杂合型为ga或ag,纯合危险型为gg;
223.rs34056014的纯合保护型为cc,杂合型为tc或ct,纯合危险型为tt;
224.rs66888336的纯合保护型为cc,杂合型为tc或ct,纯合危险型为tt;
225.rs869935的纯合保护型为aa,杂合型为ga或ag,纯合危险型为gg;
226.rs35486575的纯合保护型为gg,杂合型为ag或ga,纯合危险型为aa;
227.rs13072384的纯合保护型为aa,杂合型为ga或ag,纯合危险型为gg;
228.rs3864080的纯合保护型为tt,杂合型为at或ta,纯合危险型为aa;
229.针对所述snp标志物4:
230.rs17010289的纯合保护型为aa,杂合型为ga或ag,纯合危险型为gg;
231.rs17010288的纯合保护型为gg,杂合型为ag或ga,纯合危险型为aa;
232.rs117227749的纯合保护型为aa,杂合型为ta或at,纯合危险型为tt;
233.rs75222194的纯合保护型为tt,杂合型为ct或tc,纯合危险型为cc;
234.针对所述snp标志物5:
235.rs79938362的纯合保护型为cc,杂合型为tc或ct,纯合危险型为tt;
236.rs116989317的纯合保护型为gg,杂合型为ag或ga,纯合危险型为aa;
237.针对所述snp标志物6:
238.rs73335760的纯合保护型为aa,杂合型为ga或ag,纯合危险型为gg;
239.针对所述snp标志物7:
240.rs201061882的纯合保护型为ttcttc,杂合型为tttc或ttct,纯合危险型为tt;
241.rs11700622的纯合保护型为gg,杂合型为ag或ga,纯合危险型为aa;
242.rs75423607的纯合保护型为cc,杂合型为tc或ct,纯合危险型为tt;
243.rs76415665的纯合保护型为gg,杂合型为cg或gc,纯合危险型为cc;
244.rs112894701的纯合保护型为cc,杂合型为tc或ct,纯合危险型为tt;
245.rs79765594的纯合保护型为aa,杂合型为ga或ag,纯合危险型为gg;
246.rs73354686的纯合保护型为aa,杂合型为ga或ag,纯合危险型为gg;
247.rs76372004的纯合保护型为cc,杂合型为tc或ct,纯合危险型为tt;
248.rs11702842的纯合保护型为gg,杂合型为ag或ga,纯合危险型为aa;
249.rs73193458的纯合保护型为gg,杂合型为ag或ga,纯合危险型为aa;
250.rs138904949的纯合保护型为atat,杂合型为aat或ata,纯合危险型为aa;
251.针对所述snp标志物8:
252.rs2275994的纯合保护型为cc,杂合型为tc或ct,纯合危险型为tt;
253.rs6996060的纯合保护型为gg,杂合型为ag或ga,纯合危险型为aa;
254.rs10104930的纯合保护型为aa,杂合型为ta或at,纯合危险型为tt;
255.rs16868196的纯合保护型为cc,杂合型为tc或ct,纯合危险型为tt;
256.rs192243723的纯合保护型为aa,杂合型为ca或ac,纯合危险型为cc;
257.rs150249158的纯合保护型为cc,杂合型为tc或ct,纯合危险型为tt;
258.rs375127474的纯合保护型为gg,杂合型为ag或ga,纯合危险型为aa;
259.rs141273852的纯合保护型为cc,杂合型为tc或ct,纯合危险型为tt;
260.所述判断模块,根据危险评分判断待测样本的放化疗引起的听力损伤的风险,判定标准为:危险评分>危险评分的阈值,则待测样本是放化疗引起听力损伤的高危个体;危险评分≤危险评分的阈值,则待测样本是放化疗引起听力损伤的低危个体;
261.所述输出模块,用于输出待测样本的放化疗引起的听力损伤的风险。
262.更优选地,所述snp标志物1为rs1050851;snp标志物2为rs117098517;snp标志物3为rs1485149;snp标志物4为rs17010289;snp标志物5为rs79938362;snp标志物6为rs73335760;snp标志物7为rs201061882;snp标志物8为rs2275994;
263.所述snp标志物1~8的回归系数,a为0.8548,b为1.7102;c为1.2895;d为1.1940;e为1.8931;f为1.2720;g为1.5115;h为1.4220;
264.所述危险评分的阈值为0.9598;危险评分>0.9598,则判断待测样本是放化疗引起听力损伤的高危个体;危险评分≤0.9598,则判断待测样本是放化疗引起听力损伤的低危个体。
265.上述风险评分系统在制备检测和/或预测肿瘤放化疗引起听力损伤的风险的试剂盒中的应用也应在本发明的保护范围之内。
266.一种检测和/或预测肿瘤放化疗引起听力损伤的风险的试剂盒,包含上述检测试剂。
267.优选地,所述检测试剂为上述检测所述snp标志物的引物和/或探针。
268.更优选地,所述检测试剂为检测rs1050851、rs117098517、rs1485149、rs17010289、rs79938362、rs73335760、rs201061882和rs2275994的引物和探针。
269.进一步优选地,所述检测试剂为核苷酸序列如seq id no:1~12、seq id no:57~60、seq id no:73~76、seq id no:81~88和seq id no:129~132所示的引物及探针。
270.优选地,所述试剂盒还包含搭载上述风险评分系统的载体。
271.优选地,所述试剂盒还包含阳性对照,即确定snp标志物基因型的标准品,其核苷酸序列如seq id no:161~240所示。
272.更优选地,所述阳性对照的核苷酸序列如seq id no:161~166、seq id no:189~190、seq id no:197~198、seq id no:201~204和seq id no:225~226所示。
273.更优选地,所述试剂盒还包含空白对照,即双蒸水。
274.更优选地,所述试剂盒还包含10mm dntp混合液、25mm mgcl2溶液、pcr反应缓冲液、pcr反应酶。
275.优选地,所述试剂盒还包含说明书,所述说明书记载危险评分的计算公式和肿瘤放化疗引起听力损伤的风险的判断方法:所述计算公式为:危险评分=(0.5616
×
诊断年龄的评分)+(0.5433
×
肿瘤t分期的评分)+(0.5211
×
同期化疗顺铂剂量的评分)+(0.8548
×
snp标志物1的基因型分型的评分)+(1.7102
×
snp标志物2的基因型分型的评分)+(1.2895
×
snp标志物3的基因型分型的评分)+(1.1940
×
snp标志物4的基因型分型的评分)+(1.8931
×
snp标志物5的基因型分型的评分)+(1.2720
×
snp标志物6的基因型分型的评分)+(1.5115
×
snp标志物7的基因型分型的评分)+(1.4220
×
snp标志物8的基因型分型的评分);
276.所述诊断年龄的评分为:诊断年龄《50岁=“0”;诊断年龄≥50岁=“1”;所述肿瘤t分期的评分为:t1~t2期=“0”;t3~t4期=“1”;所述同期化疗顺铂剂量的评分为:同期化疗顺铂剂量《155mg/m2=“0”,同期化疗顺铂剂量≥155mg/m2=“1”;所述snp标志物1~8的基因型分型的评分为:纯合保护型=“0”;杂合型=“1”;纯合危险型=“2”;
277.所述snp标志物1~8的基因型分型具体为:
278.针对所述snp标志物1:
279.rs1050851的纯合保护型为gg,杂合型为ag或ga,纯合危险型为aa;
280.针对所述snp标志物2:
281.rs117098517的纯合保护型为cc,杂合型为tc或ct,纯合危险型为tt;
282.针对所述snp标志物3:
283.rs1485149的纯合保护型为aa,杂合型为ca或ac,纯合危险型为cc;
284.针对所述snp标志物4:
285.rs17010289的纯合保护型为aa,杂合型为ga或ag,纯合危险型为gg;
286.针对所述snp标志物5:
287.rs79938362的纯合保护型为cc,杂合型为tc或ct,纯合危险型为tt;
288.针对所述snp标志物6:
289.rs73335760的纯合保护型为aa,杂合型为ga或ag,纯合危险型为gg;
290.针对所述snp标志物7:
291.rs201061882的纯合保护型为ttcttc,杂合型为tttc或ttct,纯合危险型为tt;
292.针对所述snp标志物8:
293.rs2275994的纯合保护型为cc,杂合型为tc或ct,纯合危险型为tt;
294.所述肿瘤放化疗引起听力损伤的风险的判断方法为:危险评分>0.9598,则判断待测样本是放化疗引起听力损伤的高危个体;危险评分≤0.9598,则判断待测样本是放化疗引起听力损伤的低危个体。
295.所述试剂盒的使用方法为:
296.s1.提取待测样本的基因组dna;
297.s2.以步骤s1所得基因组dna为模板,核苷酸序列如seq id no:1~12、seq id no:57~60、seq id no:73~76、seq id no:81~88和seq id no:129~132所示的引物及探针进行pcr扩增,分析扩增结果,得到上述snp标志物的基因型分型:
298.具体地,针对snp标志物1:rs1050851,
299.上游扩增引物:tcagaaaggatctggggtga(seq id no:1),
300.下游扩增引物:ctctcttccccacaggttcc(seq id no:2),
301.探针1:ttgaggaaggccaggtctccc(seq id no:3),检测参考等位基因g,
302.探针2:ttgaggaaagccaggtctccc(seq id no:4),检测效应等位基因a;
303.针对snp标志物2:rs117098517,
304.上游扩增引物:gtggggtgggaaggaag(seq id no:5),
305.下游扩增引物:gagaccatttaagcagcattt(seq id no:6),
306.探针1:ctttatatattttatcgtctgctttccctt(seq id no:7)检测参考等位基因c,
307.探针2:ctttatatattttattgtctgctttccctt(seq id no:8)检测效应等位基因t;
308.针对snp标志物3:rs1485149,
309.上游扩增引物:taggagaagattacaggtccatt(seq id no:9),
310.下游扩增引物:tagttgtggctgggaagata(seq id no:10),
311.探针1:ttcaacttttggaatatcacaataatttgg(seq id no:11)检测参考等位基因a,
312.探针2:ttcaacttttggcatatcacaataatttgg(seq id no:12)检测效应等位基因c;
313.针对snp标志物4:rs17010289,
314.上游扩增引物:gttctttctactgtgtattctcca(seq id no:57),
315.下游扩增引物:atgacatggaatggaatagct(seq id no:58),
316.探针1:tccaaagaaaccacatcactatttcttattg(seq id no:59)检测参考等位基因a,
317.探针2:tccaaagaaaccacatcactgtttcttattg(seq id no:60)检测效应等位基因g;
318.针对snp标志物5:rs79938362,
319.上游扩增引物:aaggggagtttcaaccaaga(seq id no:73),
320.下游扩增引物:aaagtgggaggggaggc(seq id no:74),
321.探针1:ctgagactccacagttctcagacggg(seq id no:75)检测参考等位基因c,
322.探针2:ctgagactccacagttctcagatggg(seq id no:76)检测效应等位基因t;
323.针对snp标志物6:rs73335760,
324.上游扩增引物:ttcttcccacatccttcctt(seq id no:81),
325.下游扩增引物:atggctttgcccattctg(seq id no:82),
326.探针1:ccctgttatccctcactccagcttt(seq id no:83)检测参考等位基因a,
327.探针2:ccctgttatccctcgctccagcttt(seq id no:84)检测效应等位基因g;
328.针对snp标志物7:rs201061882,
329.上游扩增引物:cctgtgtgtgtatctgtgtccc(seq id no:85),
330.下游扩增引物:gggagggagggaaggaaa(seq id no:86),
331.探针1:tccctccctcatttttctctcttttctc(seq id no:87)检测参考等位基因ttc,
332.探针2:tccctccctcatttttctcttttctc(seq id no:88)检测效应等位基因t;
333.针对snp标志物8:rs2275994,
334.上游扩增引物:gcacggcaatggaaaatac(seq id no:129),
335.下游扩增引物:gggagccaggtctggaata(seq id no:130),
336.探针1:ttgatgactgcccaacctctgattct(seq id no:131)检测参考等位基因c,
337.探针2:ttgatgactgcccaatctctgattct(seq id no:132)检测效应等位基因t;
338.s3.使用所述危险评分的计算公式得到危险评分,使用所述肿瘤放化疗引起听力损伤的风险的判断方法判定待测样本的放化疗引起的听力损伤发生风险。
339.本发明试剂盒对样本的来源没有特殊限定,全血、血凝块、血清、血浆、唾液、口咽拭子、鼻咽拭子、鼻咽镜取材样本、尿液、粪便等含有人体dna的生物标本均可作为待测样本。
340.优选地,步骤s2中,以核苷酸序列如seq id no:1~12、seq id no:57~60、seq id no:73~76、seq id no:81~88和seq id no:129~132所示的引物及探针进行pcr扩增。
341.优选地,步骤s2中,所述pcr扩增的反应体系为:10μm待检测snp标志物的上游扩增引物,0.1μl;10μm待检测snp标志物的下游扩增引物,0.1μl;10μm待检测snp标志物的探针1,0.1μl;10μm待检测snp标志物的探针2,0.1μl;10mm dntp混合液,0.2μl;25mm mgcl2溶液,0.4μl;pcr反应缓冲液,1μl;pcr反应酶,0.1μl;双蒸水,1.9μl;模板,1μl。
342.优选地,步骤s2中,所述pcr扩增的反应条件为:60℃30秒;95℃10分钟;95℃15秒,60℃1分钟,循环45次;60℃30秒。
343.优选地,所述放化疗的治疗药物为顺铂。
344.优选地,所述肿瘤为适用于放疗联合顺铂化疗的肿瘤。
345.与现有技术相比,本发明具有以下有益效果:
346.snp作为一种新型的基因生物标志物,区别于传统生物标志物,具有稳定、微创、易于检测的优点,本发明提供的一组snp标志物具有高灵敏度和高特异度的特点,为放化疗引起的听力损伤发病风险提供更加准确高效的评估。
347.本发明提供了一种系统、高效的诊断试剂盒,可快速准确地评估接受放疗联合顺铂化疗的肿瘤患者发生听力损伤的风险,有助于及时采取预防保护措施,尽可能减少肿瘤治疗后听力损伤的发生。
348.本发明采取严谨的验证和评价体系,采用大样本的全基因组关联研究,构建得到高灵敏度和高特异度的放化疗引起的听力损伤的风险评分系统,并明确其评估效果以确保其在临床上的有效应用。
附图说明
349.图1为rs1050851的生物信息学分析结果;a为rs1050851基因型与放化疗所致听力损伤的关联;b为rs1050851基因型与nfkbia基因表达在小脑皮质组织中的相关性;c为rs1050851所在区域的染色质状态;d为在中枢神经系统肿瘤细胞系中,nfkbia基线表达水平与顺铂敏感性的关联;e为在12种肿瘤细胞系中,nfkbia基因表达水平与顺铂敏感性的关联。
350.图2为rs2275994的生物信息学分析结果;a为rs2275994基因型与放化疗所致听力损伤的关联;b为rs2275994基因型与grhl2基因表达在颞叶皮质组织中的相关性;c为rs2275994所在区域的染色质状态;d为在中枢神经系统肿瘤细胞系中,grhl2基线表达水平与放射敏感性的关联;e为在12种肿瘤细胞系中,grhl2基因表达水平与放射敏感性的关联。
351.图3为联合单个snp标志物和3个临床因素(诊断年龄、肿瘤t分期和同期化疗顺铂剂量)预测验证集人群放化疗引起的听力损伤发生风险的roc曲线;a为联合snp标志物1:rs1050851和临床因素的危险评分系统的roc曲线;b为联合snp标志物2:rs117098517和临床因素的危险评分系统的roc曲线;c为联合snp标志物3:rs1485149和临床因素的危险评分系统的roc曲线;d为联合snp标志物4:rs17010289和临床因素的危险评分系统的roc曲线;e为联合snp标志物5:rs79938362和临床因素的危险评分系统的roc曲线;f为联合snp标志物6:rs73335760和临床因素的危险评分系统的roc曲线;g为联合snp标志物7:rs201061882和临床因素的危险评分系统的roc曲线;h为联合snp标志物8:rs2275994和临床因素的危险评分系统的roc曲线。
352.图4为联合单个snp标志物和3个临床因素(诊断年龄、肿瘤t分期和同期化疗顺铂剂量)预测验证集人群放化疗引起的听力损伤发生风险的效果;a为联合snp标志物1:rs1050851和临床因素的危险评分与放化疗所致听力损伤的关联;b为联合snp标志物2:rs117098517和临床因素的危险评分与放化疗所致听力损伤的关联;c为联合snp标志物3:rs1485149和临床因素的危险评分与放化疗所致听力损伤的关联;d为联合snp标志物4:rs17010289和临床因素的危险评分与放化疗所致听力损伤的关联;e为联合snp标志物5:rs79938362和临床因素的危险评分与放化疗所致听力损伤的关联;f为联合snp标志物6:rs73335760和临床因素的危险评分与放化疗所致听力损伤的关联;g为联合snp标志物7:rs201061882和临床因素的危险评分与放化疗所致听力损伤的关联;h为联合snp标志物8:
rs2275994和临床因素的危险评分与放化疗所致听力损伤的关联。
353.图5为联合snp标志物1~8(snp标志物1:rs1050851、snp标志物2:rs117098517、snp标志物3:rs1485149、snp标志物4:rs17010289、snp标志物5:rs79938362、snp标志物6:rs73335760、snp标志物7:rs201061882和snp标志物8:rs2275994)和3个临床因素(诊断年龄、肿瘤t分期和同期化疗顺铂剂量)预测验证集人群放化疗引起的听力损伤发生风险的效果;a为危险评分系统的roc曲线;b为危险评分与放化疗所致听力损伤的关联。
具体实施方式
354.下面结合说明书附图及具体实施例对本发明作出进一步地详细阐述,所述实施例只用于解释本发明,并非用于限定本发明的范围。下述实施例中所使用的试验方法如无特殊说明,均为常规方法;所使用的材料、试剂等,如无特殊说明,为可从商业途径得到的试剂和材料。
355.实施例1基于全基因组关联分析发现遗传易感位点
356.一、实验方法
357.1、样本收集
358.于2009年~2015年,在中山大学肿瘤防治中心生物标本库收集血液标本,并系统收集相应信息,根据以下标准筛选后续研究的样本:
359.(1)明确病理诊断及临床分期的鼻咽癌患者;
360.(2)诊断年龄≥18岁;
361.(3)初诊时肿瘤无远处转移;
362.(4)在接受放疗或化疗前无听力下降;
363.(5)治疗模式为同期放化疗;
364.(6)完成全程放疗,且放疗技术为调强放疗(intensity-modulated radiotherapy,imrt)
365.(7)自愿参加且签署知情同意书;
366.同时,排除出现以下任一情况的患者:
367.(1)在听力损伤发生前因肿瘤复发或远处转移接受了二程放疗或化疗;
368.(2)在随访过程中出现听力恢复。
369.共筛选得到777例符合标准的样本。
370.2、dna提取与基因分型
371.通过定期的门诊随访(随访时间至2021年7月31日),上述777例样本中,共有132例发生了放化疗引起的听力损伤,645例未发生放化疗引起的听力损伤。
372.针对777例研究对象的血液标本进行全基因组dna提取以及使用illumina infinium global screening array-24v1芯片进行基因分型检测。具体步骤如下:
373.(1)用edta抗凝管采集3ml外周血,3500转/分钟离心10分钟,吸出血浆;
374.(2)去除红细胞:在剩余血液成分中加入等体积红细胞裂解液,充分混匀,4000转/分钟离心10分钟,弃去上清;再加入5ml红细胞裂解液,充分混匀,4000转/分钟离心10分钟,弃去上清;
375.(3)去除有核细胞:加入1ml白细胞裂解液、10g rna酶和10g蛋白酶k,充分混匀后,
65℃水浴30分钟,期间每隔5分钟混匀1次;
376.(4)去除蛋白质:加入1ml饱和酚溶液,充分混匀后,12000转/分钟离心10分钟,吸取上层水相转移至新的ep管中;加入等体积氯仿-异戊醇混合液,充分混匀后,12000转/分钟离心10分钟,吸取上层水相转移至新的ep管中;
377.(5)dna沉淀:加入1/10体积的醋酸钠和等体积预冷的异丙醇,轻轻混匀后可见白色絮状物,12000转/分钟离心5分钟,弃去上清;
378.(6)dna漂洗:加入1ml 75%乙醇,上下颠倒,12000转/分钟离心5分钟,弃去上清;此步骤重复两次;
379.(7)干燥dna:开盖静置5分钟后,加入50μl te缓冲液溶解dna。用nanodrop2000测定dna浓度和纯度;将质检合格的dna的浓度调整至50ng/μl。
380.(8)基因分型:采用illumina infinium global screening array-24v1芯片进行全基因组扫描,利用成熟的illumina iscan芯片扫描系统分析每个样本各位点的基因型。
381.3、基因型数据质量控制
382.对基因分型数据进行质量控制,剔除不合格的研究对象和snp标志物,具体流程如下:
383.个体水平的质控:(1)剔除分型成功率小于95%的样本;(2)剔除预测性别与临床信息不一致的个体;(3)剔除杂合率偏离均值
±
6倍标准差的样本;(4)计算个体间的亲缘关系,对于血缘同源(identity by descent,ibd)大于0.25的关系对,剔除基因分型成功率较低的样本;(5)对于前10个遗传主成分,剔除每个主成分中偏离均值
±
6倍标准差的个体;
384.snp标志物的质控:(1)保留常染色体上的变异位点;(2)剔除分型成功率小于95%的位点;(3)剔除最小等位基因频率(minor allele frequency,maf)小于0.01的位点;(4)剔除hardy-weinberg平衡检验p值小于1.0
×
10-12
的位点;
385.以千人基因组(1000genome phase iii integrated variant set)中所有样本的基因型数据作为参考,利用shapeit2软件和impute2软件填补未检测位点的基因型;对填补后的位点进行进一步质控,剔除info值小于0.8、分型成功率小于95%或maf小于0.01的snp标志物。
386.4、统计分析
387.单因素和多因素cox比例风险回归分析,以检验人口统计学变量(诊断年龄、性别、吸烟、饮酒、高血压和糖尿病)和临床因素(肿瘤t/n/总体分期、治疗前ebv dna载量、治疗模式、原发灶照射剂量、诱导化疗顺铂剂量和同期化疗顺铂剂量)与放化疗所致听力损伤的关联。
388.在加性效应的假设下,采用cox比例风险回归模型来评估每个snp标志物对放化疗引起的听力损伤发病的效应,同时校正诊断年龄(《50岁或≥50岁)、肿瘤t分期(t1~t2或t3~t4)、同期化疗顺铂剂量(《155mg/m2或≥155mg/m2)和前两个遗传主成分(pc1和pc2)。
389.二、实验结果
390.单因素和多因素cox回归分析均显示,诊断年龄、肿瘤t分期和同期化疗顺铂剂量与放化疗引起的听力损伤发生风险显著相关。
391.多因素cox回归分析显示,与诊断年龄《50岁的患者相比,诊断年龄≥50岁的患者发生放化疗所致听力损伤的风险更高(hr=1.72,95%ci:1.19~2.49,p=0.004);与低肿
瘤t分期(t1~t2)相比,高肿瘤t分期(t3~t4)的患者发生听力损伤的风险更高(hr=1.66,95%ci:1.12~2.46,p=0.012);与接受较低剂量(《155mg/m2)的同期顺铂化疗相比,接受较高剂量(≥155mg/m2)的同期顺铂化疗的患者发生听力损伤的风险更高(hr=1.46,95%ci:1.01~2.12,p=0.046)。
392.在校正诊断年龄、肿瘤t分期、同期化疗顺铂剂量和前两个遗传主成分(pc1和pc2)后,经过全基因组关联分析共得到15个p《1.0
×
10-06
的snp标志物。
393.对这15个snp标志物进行独立性筛选,保留相互之间连锁不平衡ld r2<0.1的snp标志物,最后得到7个snp标志物。snp标志物之间的连锁不平衡关系利用plink软件基于千人基因组计划第三阶段东亚人群(1000genomes phase iii eas population)计算得出。这7个snp标志物及与其高度连锁(ld r2>0.8)的其他snp标志物的关联分析结果如表1所示。rs1050851的p值最小,是最显著的遗传易感位点。
394.表1 7个snp标志物及其连锁snp标志物的关联分析结果
[0395][0396][0397]
实施例2遗传性耳聋基因富集分析识别遗传易感位点
[0398]
一、实验方法
[0399]
从hereditary hearing loss homepage网站(https://hereditaryhearingloss.org/)获取149个常染色体遗传的遗传性耳聋基因,以基因上下游50kb的范围作为提取snp标志物的关键区域,共得到56040个snp标志物。
[0400]
固定每个个体和snp基因型对应关系不变,将snp基因型与表型(放化疗相关听力损伤的结局与时间、诊断年龄、肿瘤t分期和同期化疗顺铂剂量)的对应关系随机打乱重组,对重组的数据进行关联分析;此步骤重复1000次。
[0401]
设置不同的gwas显著性阈值(p《5.0
×
10-02
,1.0
×
10-02
,5.0
×
10-03
,1.0
×
10-03
,5.0
×
10-04
,1.0
×
10-04
,5.0
×
10-05
,1.0
×
10-05
,5.0
×
10-06
),计算每次关联分析中超过阈值的snp个数(称为试验值),获得1000个试验值的经验分布。
[0402]
计算超过阈值的snp个数(称为观察值),计算1000个试验值中大于或等于观察值的次数,并与试验次数进行比较,从而获得经验p值(empirical p-value)。
[0403]
二、实验结果
[0404]
在149个遗传性耳聋基因中,有118个基因的上下游50kb的区域中至少含有一个gwas p值小于0.05的snp标志物。
[0405]
当gwas显著性阈值为p
gwas
《1.0
×
10-04
,经验p值=0.034;当gwas显著性阈值为p
gwas
《5.0
×
10-05
,经验p值=0.016;当gwas显著性阈值为p
gwas
《1.0
×
10-05
,经验p值=0.033;当gwas显著性阈值设为p
gwas
《5.0
×
10-06
时,经验p值=0.027。表明上述149个遗传性耳聋基因中位于关键区域的snp标志物显著富集于gwas显著信号中。
[0406]
其中,位于遗传性耳聋基因上下游50kb区域内、与放化疗所致听力损伤发生最显著相关的snp标志物是rs2275994。rs2275994及与其高度连锁(ld r2>0.8)的其他snp标志物的关联分析结果如表2所示。
[0407]
表2rs2275994及其连锁snp标志物的关联分析结果
[0408][0409]
实施例3snp标志物的生物信息学分析
[0410]
一、实验方法
[0411]
1、snp标志物功能预测评分注释
[0412]
对实施例1中最显著的遗传易感位点rs1050851和实施例2中的rs2275994,进行cadd评分的注释。cadd评分是一个综合了63种功能注释的指标,与突变致病性、疾病严重程度、实验调控效应和复杂性状关联等相关,可预测变异位点的有害性。
[0413]
2、snp标志物表达数量性状基因座分析
[0414]
脑组织表达数据库uk brain expression consortium(ukbec)收集了134名无神经退行性疾病的参与者12个大脑区域的基因表达芯片数据,其对应的在线网站braineac(http://www.braineac.org/)提供了10个不同脑区(小脑皮质、额叶皮质、海马体、下橄榄核髓质、枕叶皮质、硬脑膜、黑质、颞叶皮质、丘脑和小叶区白质)的snp-基因关系对表达数量性状基因座(expression quantitative trait loci,eqtl)分析结果。利用braineac公共数据库提供的信息,确定rs1050851和rs2275994的基因型与靶基因表达水平的关联。
[0415]
3、染色质状态注释
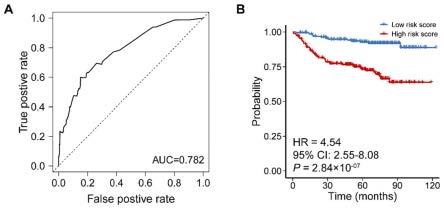
[0416]
从roadmap数据库和encode公共数据库中获得15种组织或细胞系(神经节隆起来源的神经球组织、大脑皮层来源的神经球组织、脑海马体组织、脑黑质组织、脑前叶组织、脑扣带回组织、脑颞叶组织、脑角回组织、脑背外侧前额叶皮质组织、脑生发基质组织、胎儿脑
组织、h1来源的神经元祖细胞系、h9来源的神经元祖细胞系、h9来源的神经元细胞系和人淋巴母细胞系)的组蛋白修饰标记(h3k27ac、h3k4me1和h3k4me3)和dnase i超敏感位点(dhs)的信息,对rs1050851和rs2275994进行染色质状态注释。
[0417]
4、rs1050851和rs2275994所在基因的表达情况与细胞敏感性分析
[0418]
选取分别来自膀胱或尿道癌组织、骨肿瘤组织、大肠癌组织、乳腺癌组织、中枢神经系统(central nervous system,cns)肿瘤组织、肾肿瘤组织、肺癌组织、卵巢癌组织、胰腺癌组织、外周神经系统肿瘤组织、皮肤癌组织和软组织肿瘤组织,共12种癌症组织类型的肿瘤细胞系。
[0419]
从“pharmacogx”r软件包中提取上述肿瘤细胞系的基因表达数据和细胞顺铂敏感性(采用ic
50
值)信息,进行基因表达水平与细胞顺铂敏感性的关联分析。
[0420]
采用肿瘤细胞在2gyγ射线照射下的存活比例(即sf2值)评价细胞放射敏感性,从“radiogx”r软件包中提取上述肿瘤细胞系的基因表达数据和细胞放射敏感性信息,进行基因表达水平与细胞放射敏感性的关联分析。
[0421]
二、实验结果
[0422]
rs1050851是gwas发现的最显著的遗传易感位点(hr=5.46,95%ci:2.93~10.18,p=9.51
×
10-08
),接近gwas显著性水平(p《5.0
×
10-08
)。如图1中的a所示,携带rs1050851效应等位基因a的患者发生放化疗所致听力损伤的风险更高。而且,cadd功能预测评分注释显示,rs1050851的cadd评分为17.10,远高于参考值12.37,所以rs1050851是一个有害突变位点。
[0423]
如图1中的b所示,在小脑皮质组织中,rs1050851的效应等位基因a与nfkbia基因高表达相关。如图1中的c所示,在神经节隆起来源的神经球组织、脑扣带回组织和人淋巴母细胞系中,rs1050851位于增强子和启动子组蛋白修饰(h3k27ac,h3k4me1和h3k4me3)区域;在人淋巴母细胞系中,rs1050851位于dhs标记区域。这些结果提示,rs1050851可能通过影响nfkbia基因启动子或增强子活性、或染色质可及性来调控该基因的表达水平,从而影响放化疗所致听力损伤的发生风险。
[0424]
如图1中的d所示,细胞顺铂敏感性分析结果显示,在cns肿瘤细胞系中,nfkbia基因的基线表达水平与细胞对顺铂的耐受性呈显著负相关。而且,如图1中的e所示,未在其他组织类型的肿瘤细胞系中观察到nfkbia表达与细胞顺铂耐受性的显著关联,这一显著关联特异性地存在于cns肿瘤细胞系中。
[0425]
综上所述,携带rs1050851效应等位基因a的个体,其nfkbia基因高表达,对顺铂的耐受性较低,更容易受到顺铂损害,因此发生放化疗所致听力损伤的风险更高。
[0426]
rs2275994是遗传性耳聋基因区域内与放化疗所致听力损伤发生最显著相关的遗传易感位点(hr=3.85,95%ci:2.24~6.61,p=1.10
×
10-06
)。如图2中的a所示,携带rs2275994效应等位基因t的患者发生放化疗所致听力损伤的风险更高。cadd功能预测评分注释显示,rs2275994的cadd评分为7.12。
[0427]
如图2中的b所示,在颞叶皮质组织中,rs2275994的效应等位基因t与grhl2基因低表达相关。如图2中的c所示,在人淋巴母细胞系中,rs2275994位于dhs标记区域。这些结果提示,rs2275994可能通过影响grhl2基因染色质可及性来调控该基因的表达水平,从而影响放化疗所致听力损伤的发生风险。
[0428]
如图2中的d和e所示,细胞放射敏感性分析结果显示,在cns肿瘤细胞系中,grhl2基因的基线表达水平与细胞对射线的耐受性具有显著正相关关系,且这一显著关联也特异性地存在于cns肿瘤细胞系中。
[0429]
综上所述,携带rs2275994效应等位基因t的个体,其grhl2基因低表达,对放疗的耐受性较低,更容易受到射线损害,因此发生放化疗所致听力损伤的风险升高。
[0430]
实施例4放化疗引起听力损伤的风险评分系统的建立
[0431]
一、实验方法
[0432]
1、放化疗引起听力损伤的风险评分系统的构建
[0433]
(1)snp标志物分组
[0434]
将实施例1~2中的40个snp标志物分为8个组,分别记为snp标志物1~8。
[0435]
其中,snp标志物1:rs1050851;
[0436]
snp标志物2:rs117098517;
[0437]
snp标志物3:rs1485149或其连锁snp位点(rs11713855、rs73028787、rs9872473、rs6784713、rs36011752、rs34056014、rs66888336、rs869935、rs35486575、rs13072384和rs3864080)中的任意一个;
[0438]
snp标志物4:rs17010289或其连锁snp位点(rs17010288、rs117227749和rs75222194)中的任意一个;
[0439]
snp标志物5:rs79938362或其连锁snp位点(rs116989317)中的任意一个;
[0440]
snp标志物6:rs73335760;
[0441]
snp标志物7:rs201061882或其连锁snp位点(rs11700622、rs75423607、rs76415665、rs112894701、rs79765594、rs73354686、rs76372004、rs11702842、rs73193458和rs138904949)中的任意一个;
[0442]
snp标志物8:rs2275994或其连锁snp位点(rs6996060、rs10104930、rs16868196、rs192243723、rs150249158、rs375127474和rs141273852)中的任意一个。
[0443]
(2)回归系数及阈值的确定
[0444]
利用cox比例风险回归模型构建放化疗引起听力损伤的风险评分系统,以是否发生放化疗引起听力损伤和发生听力损伤的时间作为结局变量,以snp标志物1~8和3个临床因素(诊断年龄、肿瘤t分期和同期化疗顺铂剂量)作为预测变量,进行风险评分模型的拟合,从而获得各预测变量的回归系数。对于发生放化疗引起听力损伤的患者而言,发生听力损伤的时间定义为从肿瘤放疗或化疗开始到首次出现听力损伤症状的时间;对于未发生放化疗引起听力损伤的患者而言,发生听力损伤的时间定义为从肿瘤放疗或化疗开始到研究结束的时间。
[0445]
将实施例1中的777例样本随机分为训练集(n=389)和验证集(n=388),利用训练集(n=389)构建放化疗引起听力损伤的风险评分系统。然后,利用该风险评分系统预测训练集中每个样本在放化疗后5年内发生听力损伤的风险,获得训练集中每个样本的听力损伤危险评分。以训练集中听力损伤危险评分的中位数作为听力损伤危险评分的阈值。
[0446]
(3)联合单个snp标志物和3个临床因素的放化疗引起听力损伤的风险评分系统
[0447]
将实施例1中的777例样本随机分为训练集(n=389)和验证集(n=388),结合snp标志物1~8和3个临床因素(诊断年龄、肿瘤t分期和同期化疗顺铂剂量),利用训练集(n=
389)分别构建联合单个snp标志物和3个临床因素的放化疗引起听力损伤的风险评分系统。
[0448]
其中,snp标志物1~8以rs1050851、rs117098517、rs1485149、rs17010289、rs79938362、rs73335760、rs201061882和rs2275994为例构建了放化疗引起听力损伤的风险评分系统。
[0449]
对于联合单个snp标志物(snp标志物1~8)和3个临床因素构建的放化疗引起听力损伤的风险评分系统,设置snp标志物1~8的基因型分型及对应回归系数如表3所示。表3用于构建联合单个snp标志物和3个临床因素的风险评分系统的snp标志物1~8的基因型分型和回归系数
[0450][0451]
snp标志物的基因型分型中,纯合保护型为携带两个致放化疗引起的听力损伤风险低的等位基因(即携带两个参考等位基因);杂合型为同时携带一个致听力损伤风险低和一个致听力损伤风险高的等位基因(即携带一个参考等位基因和一个效应等位基因);纯合危险型为携带两个致听力损伤风险高的等位基因(即携带两个效应等位基因)。
[0452]
联合单个snp标志物和3个临床因素的风险评分系统的具体计算公式如下:
[0453]
①
联合snp标志物1(rs1050851)和3个临床因素的风险评分系统的具体计算公式如下:
[0454]
危险评分=(0.5785
×
诊断年龄的评分)+(0.2721
×
肿瘤t分期的评分)+(0.4092
×
同期化疗顺铂剂量的评分)+(2.1895
×
snp标志物1的基因型分型的评分);
[0455]
其中,诊断年龄的评分为:诊断年龄《50岁=“0”;诊断年龄≥50岁=“1”;
[0456]
肿瘤t分期的评分为:t1~t2期=“0”;t3~t4期=“1”;
[0457]
同期化疗顺铂剂量的评分为:同期化疗顺铂剂量《155mg/m2=“0”,同期化疗顺铂剂量≥155mg/m2=“1”;
[0458]
snp标志物1的基因型分型的评分为:纯合保护型=“0”;杂合型=“1”;纯合危险型=“2”;
[0459]
根据公式计算得到的危险评分,当危险评分>0.5785时,判定检测对象是放化疗所致听力损伤的高危个体;当危险评分≤0.5785时,判定检测对象是放化疗所致听力损伤的低危个体。
[0460]
②
联合snp标志物2(rs117098517)和3个临床因素的风险评分系统的具体计算公式如下:
[0461]
危险评分=(0.6828
×
诊断年龄的评分)+(0.3467
×
肿瘤t分期的评分)+(0.4150
×
同期化疗顺铂剂量的评分)+(2.3685
×
snp标志物2的基因型分型的评分);
[0462]
其中,诊断年龄的评分为:诊断年龄《50岁=“0”;诊断年龄≥50岁=“1”;
[0463]
肿瘤t分期的评分为:t1~t2期=“0”;t3~t4期=“1”;
[0464]
同期化疗顺铂剂量的评分为:同期化疗顺铂剂量《155mg/m2=“0”,同期化疗顺铂剂量≥155mg/m2=“1”;
[0465]
snp标志物2的基因型分型的评分为:纯合保护型=“0”;杂合型=“1”;纯合危险型=“2”;
[0466]
根据公式计算得到的危险评分,当危险评分>0.6828时,判定检测对象是放化疗所致听力损伤的高危个体;当危险评分≤0.6828时,判定检测对象是放化疗所致听力损伤的低危个体。
[0467]
③
联合snp标志物3(rs1485149)和3个临床因素的风险评分系统的具体计算公式如下:
[0468]
危险评分=(0.5666
×
诊断年龄的评分)+(0.3074
×
肿瘤t分期的评分)+(0.3446
×
同期化疗顺铂剂量的评分)+(1.1087
×
snp标志物3的基因型分型的评分);
[0469]
其中,诊断年龄的评分为:诊断年龄《50岁=“0”;诊断年龄≥50岁=“1”;
[0470]
肿瘤t分期的评分为:t1~t2期=“0”;t3~t4期=“1”;
[0471]
同期化疗顺铂剂量的评分为:同期化疗顺铂剂量《155mg/m2=“0”,同期化疗顺铂剂量≥155mg/m2=“1”;
[0472]
snp标志物3的基因型分型的评分为:纯合保护型=“0”;杂合型=“1”;纯合危险型=“2”;
[0473]
根据公式计算得到的危险评分,当危险评分>0.5666时,判定检测对象是放化疗所致听力损伤的高危个体;当危险评分≤0.5666时,判定检测对象是放化疗所致听力损伤的低危个体。
[0474]
④
联合snp标志物4(rs17010289)和3个临床因素的风险评分系统的具体计算公式如下:
[0475]
危险评分=(0.7010
×
诊断年龄的评分)+(0.2712
×
肿瘤t分期的评分)+(0.3631
×
同期化疗顺铂剂量的评分)+(1.3741
×
snp标志物4的基因型分型的评分);
[0476]
其中,诊断年龄的评分为:诊断年龄《50岁=“0”;诊断年龄≥50岁=“1”;
[0477]
肿瘤t分期的评分为:t1~t2期=“0”;t3~t4期=“1”;
[0478]
同期化疗顺铂剂量的评分为:同期化疗顺铂剂量《155mg/m2=“0”,同期化疗顺铂剂量≥155mg/m2=“1”;
[0479]
snp标志物4的基因型分型的评分为:纯合保护型=“0”;杂合型=“1”;纯合危险型=“2”;
[0480]
根据公式计算得到的危险评分,当危险评分>0.6343时,判定检测对象是放化疗所致听力损伤的高危个体;当危险评分≤0.6343时,判定检测对象是放化疗所致听力损伤的低危个体。
[0481]
⑤
联合snp标志物5(rs79938362)和3个临床因素的风险评分系统的具体计算公式如下:
[0482]
危险评分=(0.5798
×
诊断年龄的评分)+(0.3667
×
肿瘤t分期的评分)+(0.3349
×
同期化疗顺铂剂量的评分)+(1.8981
×
snp标志物5的基因型分型的评分);
[0483]
其中,诊断年龄的评分为:诊断年龄《50岁=“0”;诊断年龄≥50岁=“1”;
[0484]
肿瘤t分期的评分为:t1~t2期=“0”;t3~t4期=“1”;
[0485]
同期化疗顺铂剂量的评分为:同期化疗顺铂剂量《155mg/m2=“0”,同期化疗顺铂剂量≥155mg/m2=“1”;
[0486]
snp标志物5的基因型分型的评分为:纯合保护型=“0”;杂合型=“1”;纯合危险型=“2”;
[0487]
根据公式计算得到的危险评分,当危险评分>0.5798时,判定检测对象是放化疗所致听力损伤的高危个体;当危险评分≤0.5798时,判定检测对象是放化疗所致听力损伤的低危个体。
[0488]
⑥
联合snp标志物6(rs73335760)和3个临床因素的风险评分系统的具体计算公式如下:
[0489]
危险评分=(0.7039
×
诊断年龄的评分)+(0.2124
×
肿瘤t分期的评分)+(0.4126
×
同期化疗顺铂剂量的评分)+(1.4411
×
snp标志物6的基因型分型的评分);
[0490]
其中,诊断年龄的评分为:诊断年龄《50岁=“0”;诊断年龄≥50岁=“1”;
[0491]
肿瘤t分期的评分为:t1~t2期=“0”;t3~t4期=“1”;
[0492]
同期化疗顺铂剂量的评分为:同期化疗顺铂剂量《155mg/m2=“0”,同期化疗顺铂剂量≥155mg/m2=“1”;
[0493]
snp标志物6的基因型分型的评分为:纯合保护型=“0”;杂合型=“1”;纯合危险型=“2”;
[0494]
根据公式计算得到的危险评分,当危险评分>0.5064时,判定检测对象是放化疗所致听力损伤的高危个体;当危险评分≤0.5064时,判定检测对象是放化疗所致听力损伤的低危个体。
[0495]
⑦
联合snp标志物7(rs201061882)和3个临床因素的风险评分系统的具体计算公式如下:
[0496]
危险评分=(0.6711
×
诊断年龄的评分)+(0.3257
×
肿瘤t分期的评分)+(0.4106
×
同期化疗顺铂剂量的评分)+(1.1470
×
snp标志物7的基因型分型的评分);
[0497]
其中,诊断年龄的评分为:诊断年龄《50岁=“0”;诊断年龄≥50岁=“1”;
[0498]
肿瘤t分期的评分为:t1~t2期=“0”;t3~t4期=“1”;
[0499]
同期化疗顺铂剂量的评分为:同期化疗顺铂剂量《155mg/m2=“0”,同期化疗顺铂剂量≥155mg/m2=“1”;
[0500]
snp标志物7的基因型分型的评分为:纯合保护型=“0”;杂合型=“1”;纯合危险型=“2”;
[0501]
根据公式计算得到的危险评分,当危险评分>0.6711时,判定检测对象是放化疗所致听力损伤的高危个体;当危险评分≤0.6711时,判定检测对象是放化疗所致听力损伤的低危个体。
[0502]
⑧
联合snp标志物8(rs2275994)和3个临床因素的风险评分系统的具体计算公式如下:
[0503]
危险评分=(0.6548
×
诊断年龄的评分)+(0.3675
×
肿瘤t分期的评分)+(0.4401
×
同期化疗顺铂剂量的评分)+(1.5321
×
snp标志物8的基因型分型的评分);
[0504]
其中,诊断年龄的评分为:诊断年龄《50岁=“0”;诊断年龄≥50岁=“1”;
[0505]
肿瘤t分期的评分为:t1~t2期=“0”;t3~t4期=“1”;
[0506]
同期化疗顺铂剂量的评分为:同期化疗顺铂剂量《155mg/m2=“0”,同期化疗顺铂剂量≥155mg/m2=“1”;
[0507]
snp标志物8的基因型分型的评分为:纯合保护型=“0”;杂合型=“1”;纯合危险型=“2”;
[0508]
根据公式计算得到的危险评分,当危险评分>1.5321时,判定检测对象是放化疗所致听力损伤的高危个体;当危险评分≤1.5321时,判定检测对象是放化疗所致听力损伤的低危个体。
[0509]
(4)联合snp标志物1~8和3个临床因素的风险评分系统
[0510]
将实施例1中的777例样本随机分为训练集(n=389)和验证集(n=388),结合snp标志物1~8和3个临床因素(诊断年龄、肿瘤t分期和同期化疗顺铂剂量),利用训练集(n=389)构建联合snp标志物1~8和3个临床因素的风险评分系统。
[0511]
对于联合snp标志物1~8和3个临床因素的风险评分系统,设置snp标志物1~8的基因型分型及对应回归系数如表4所示。
[0512]
表4用于构建联合snp标志物1~8和3个临床因素的风险评分系统的snp标志物1~8的基因型分型和回归系数
[0513][0514]
snp标志物的基因型分型中,纯合保护型为携带两个致放化疗引起的听力损伤风险低的等位基因(即携带两个参考等位基因);杂合型为同时携带一个致听力损伤风险低和一个致听力损伤风险高的等位基因(即携带一个参考等位基因和一个效应等位基因);纯合危险型为携带两个致听力损伤风险高的等位基因(即携带两个效应等位基因)。
[0515]
在多因素模型下,综合考虑每个预测因子,以各预测因子的回归系数为权重,构建联合snp标志物1~8和3个临床因素的风险评分系统,具体计算公式如下:
[0516]
危险评分=(0.5616
×
诊断年龄的评分)+(0.5433
×
肿瘤t分期的评分)+(0.5211
×
同期化疗顺铂剂量的评分)+(0.8548
×
snp标志物1的基因型分型的评分)+(1.7102
×
snp标志物2的基因型分型的评分)+(1.2895
×
snp标志物3的基因型分型的评分)+(1.1940
×
snp标志物4的基因型分型的评分)+(1.8931
×
snp标志物5的基因型分型的评分)+(1.2720
×
snp标志物6的基因型分型的评分)+(1.5115
×
snp标志物7的基因型分型的评分)+(1.4220
×
snp标志物8的基因型分型的评分);
[0517]
其中,诊断年龄的评分为:诊断年龄《50岁=“0”;诊断年龄≥50岁=“1”;
[0518]
肿瘤t分期的评分为:t1~t2期=“0”;t3~t4期=“1”;
[0519]
同期化疗顺铂剂量的评分为:同期化疗顺铂剂量《155mg/m2=“0”,同期化疗顺铂剂量≥155mg/m2=“1”;
[0520]
snp标志物1~8的基因型分型的评分为:纯合保护型=“0”;杂合型=“1”;纯合危
险型=“2”;
[0521]
根据公式计算得到的危险评分,当危险评分>0.9598时,判定检测对象是放化疗所致听力损伤的高危个体;当危险评分≤0.9598时,判定检测对象是放化疗所致听力损伤的低危个体。
[0522]
2、放化疗引起听力损伤的风险评分系统的应用
[0523]
将实施例1中的777例样本随机分为训练集(n=389)和验证集(n=388)。在训练集中,使用cox回归模型构建危险评分模型,预测放化疗后5年内听力损伤发生率;在验证集中,使用上述放化疗引起听力损伤的风险评分系统,进行放化疗引起的听力损伤的风险预测。绘制roc曲线以及评估风险预测的灵敏度和特异度,确定放化疗引起听力损伤的风险评分系统的预测效果。
[0524]
二、实验结果
[0525]
如图3中的a所示,在验证集中,联合snp标志物1(rs1050851)和3个临床因素的风险评分系统的曲线下面积(area under the curve,auc)为0.633;当灵敏度为72.1%时,特异度为47.9%。
[0526]
如图3中的b所示,在验证集中,联合snp标志物2(rs117098517)和3个临床因素的风险评分系统的auc为0.620;当灵敏度为73.7%时,特异度为48.5%。
[0527]
如图3中的c所示,在验证集中,联合snp标志物3(rs1485149)和3个临床因素的风险评分系统的auc为0.634;当灵敏度为73.6%时,特异度为47.8%。
[0528]
如图3中的d所示,在验证集中,联合snp标志物4(rs17010289)和3个临床因素的风险评分系统的auc为0.630;当灵敏度为79.9%时,特异度为43.8%。
[0529]
如图3中的e所示,在验证集中,联合snp标志物5(rs79938362)和3个临床因素的风险评分系统的auc为0.655;当灵敏度为77.2%时,特异度为48.9%。
[0530]
如图3中的f所示,在验证集中,联合snp标志物6(rs73335760)和3个临床因素的风险评分系统的auc为0.571;当灵敏度为73.7%时,特异度为41.1%。
[0531]
如图3中的g所示,在验证集中,联合snp标志物7(rs201061882)和3个临床因素的风险评分系统的auc为0.652;当灵敏度为76.5%时,特异度为48.7%。
[0532]
如图3中的h所示,在验证集中,联合snp标志物8(rs2275994)和3个临床因素的风险评分系统的auc为0.619;当灵敏度为72.4%时,特异度为47.3%。具体结果整理如表5所示。
[0533]
表5放化疗引起听力损伤的风险评分系统的预测效果
[0534][0535]
如图4中的a所示,以0.5785作为危险评分的截断值,联合snp标志物1(rs1050851)
和3个临床因素的风险评分系统可以区分容易发生放化疗所致听力损伤的高危人群与不太容易发生听力损伤的低危人群(hr=2.33,95%ci:1.36~4.01,p=2.23
×
10-03
)。
[0536]
如图4中的b所示,以0.6828作为危险评分的截断值,联合snp标志物2(rs117098517)和3个临床因素的风险评分系统可以区分容易发生放化疗所致听力损伤的高危人群与不太容易发生听力损伤的低危人群(hr=2.58,95%ci:1.48~4.48,p=7.90
×
10-04
)。
[0537]
如图4中的c所示,以0.5666作为危险评分的截断值,联合snp标志物3(rs1485149)和3个临床因素的风险评分系统可以区分容易发生放化疗所致听力损伤的高危人群与不太容易发生听力损伤的低危人群(hr=2.52,95%ci:1.45~4.37,p=1.06
×
10-03
)。
[0538]
如图4中的d所示,以0.6343作为危险评分的截断值,联合snp标志物4(rs17010289)和3个临床因素的风险评分系统尚不能区分容易发生放化疗所致听力损伤的高危人群与不太容易发生听力损伤的低危人群(hr=1.64,95%ci:1.00~2.69,p=5.03
×
10-02
)。
[0539]
如图4中的e所示,以0.5798作为危险评分的截断值,联合snp标志物5(rs79938362)和3个临床因素的风险评分系统可以区分容易发生放化疗所致听力损伤的高危人群与不太容易发生听力损伤的低危人群(hr=3.05,95%ci:1.71~5.43,p=1.52
×
10-04
)。
[0540]
如图4中的f所示,以0.5064作为危险评分的截断值,联合snp标志物6(rs73335760)和3个临床因素的风险评分系统尚不能区分容易发生放化疗所致听力损伤的高危人群与不太容易发生听力损伤的低危人群(hr=1.33,95%ci:0.80~2.20,p=0.27)。
[0541]
如图4中的g所示,以0.6711作为危险评分的截断值,联合snp标志物7(rs201061882)和3个临床因素的风险评分系统可以区分容易发生放化疗所致听力损伤的高危人群与不太容易发生听力损伤的低危人群(hr=3.04,95%ci:1.71~5.41,p=1.60
×
10-04
)。
[0542]
如图4中的h所示,以1.5321作为危险评分的截断值,联合snp标志物8(rs2275994)和3个临床因素的风险评分系统可以区分容易发生放化疗所致听力损伤的高危人群与不太容易发生听力损伤的低危人群(hr=2.51,95%ci:1.45~4.37,p=1.08
×
10-03
)。
[0543]
如图5中的a所示,在验证集中,联合8个snp标志物和3个临床因素的放化疗引起听力损伤的风险评分系统的auc为0.782;当灵敏度为70.7%时,特异度为69.8%。
[0544]
如图5中的b所示,以0.9598作为危险评分的截断值,该放化疗引起听力损伤的风险评分系统可以清晰地区分容易发生放化疗所致听力损伤的高危人群与不太容易发生听力损伤的低危人群(hr=4.54,95%ci:2.55~8.08,p=2.84
×
10-07
)。
[0545]
上述结果表明,联合8个snp标志物与3个临床因素建立的放化疗引起听力损伤的风险评分系统,可以有效地预测鼻咽癌患者因放化疗导致发生听力损伤的风险。
[0546]
实施例5放化疗引起听力损伤的风险评分系统
[0547]
本发明提供一种放化疗引起的听力损伤的风险评分系统,所述系统包含:信息采集模块、储存模块、信息分析模块、判断模块和输出模块。
[0548]
所述信息采集模块获取待测样本的特征参数,所述特征参数包括snp标志物1~8在待测样本基因组dna中的基因型分型,以及待测样本的诊断年龄、肿瘤t分期和同期化疗
顺铂剂量。
[0549]
其中,snp标志物1:rs1050851;
[0550]
snp标志物2:rs117098517;
[0551]
snp标志物3:rs1485149或其连锁snp标志物(rs11713855、rs73028787、rs9872473、rs6784713、rs36011752、rs34056014、rs66888336、rs869935、rs35486575、rs13072384和rs3864080)中的任意一个;
[0552]
snp标志物4:rs17010289或其连锁snp标志物(rs17010288、rs117227749和rs75222194)中的任意一个;
[0553]
snp标志物5:rs79938362或其连锁snp标志物(rs116989317)中的任意一个;
[0554]
snp标志物6:rs73335760;
[0555]
snp标志物7:rs201061882或其连锁snp标志物(rs11700622、rs75423607、rs76415665、rs112894701、rs79765594、rs73354686、rs76372004、rs11702842、rs73193458和rs138904949)中的任意一个;
[0556]
snp标志物8:rs2275994或其连锁snp标志物(rs6996060、rs10104930、rs16868196、rs192243723、rs150249158、rs375127474和rs141273852)中的任意一个。
[0557]
所述储存模块用于储存信息采集模块中获取的特征参数和判断模块中的危险评分的阈值。
[0558]
所述信息分析模块,根据获得的特征参数,通过公式计算得到危险评分;所述公式为:危险评分=(0.5616
×
诊断年龄的评分)+(0.5433
×
肿瘤t分期的评分)+(0.5211
×
同期化疗顺铂剂量的评分)+(a
×
snp标志物1的基因型分型的评分)+(b
×
snp标志物2的基因型分型的评分)+(c
×
snp标志物3的基因型分型的评分)+(d
×
snp标志物4的基因型分型的评分)+(e
×
snp标志物5的基因型分型的评分)+(f
×
snp标志物6的基因型分型的评分)+(g
×
snp标志物7的基因型分型的评分)+(h
×
snp标志物8的基因型分型的评分);
[0559]
所述诊断年龄的评分为:诊断年龄《50岁=“0”;诊断年龄≥50岁=“1”;所述肿瘤t分期的评分为:t1~t2期=“0”;t3~t4期=“1”;所述同期化疗顺铂剂量的评分为:同期化疗顺铂剂量《155mg/m2=“0”,同期化疗顺铂剂量≥155mg/m2=“1”;snp标志物1~8的基因型分型的评分为:纯合保护型=“0”;杂合型=“1”;纯合危险型=“2”;
[0560]
a、b、c、d、e、f、g和h分别为snp标志物1~8的回归系数,回归系数的值由实施例4的步骤2的方法得到。
[0561]
所述snp标志物1~8的基因型分型,具体为:
[0562]
针对所述snp标志物1:
[0563]
rs1050851的纯合保护型为gg,杂合型为ag或ga,纯合危险型为aa;
[0564]
针对所述snp标志物2:
[0565]
rs117098517的纯合保护型为cc,杂合型为tc或ct,纯合危险型为tt;
[0566]
针对所述snp标志物3:
[0567]
rs1485149的纯合保护型为aa,杂合型为ca或ac,纯合危险型为cc;
[0568]
rs11713855的纯合保护型为tt,杂合型为ct或tc,纯合危险型为cc;
[0569]
rs73028787的纯合保护型为cc,杂合型为ac或ca,纯合危险型为aa;
[0570]
rs9872473的纯合保护型为gg,杂合型为ag或ga,纯合危险型为aa;
[0571]
rs6784713的纯合保护型为tt,杂合型为gt或tg,纯合危险型为gg;
[0572]
rs36011752的纯合保护型为aa,杂合型为ga或ag,纯合危险型为gg;
[0573]
rs34056014的纯合保护型为cc,杂合型为tc或ct,纯合危险型为tt;
[0574]
rs66888336的纯合保护型为cc,杂合型为tc或ct,纯合危险型为tt;
[0575]
rs869935的纯合保护型为aa,杂合型为ga或ag,纯合危险型为gg;
[0576]
rs35486575的纯合保护型为gg,杂合型为ag或ga,纯合危险型为aa;
[0577]
rs13072384的纯合保护型为aa,杂合型为ga或ag,纯合危险型为gg;
[0578]
rs3864080的纯合保护型为tt,杂合型为at或ta,纯合危险型为aa;
[0579]
针对所述snp标志物4:
[0580]
rs17010289的纯合保护型为aa,杂合型为ga或ag,纯合危险型为gg;
[0581]
rs17010288的纯合保护型为gg,杂合型为ag或ga,纯合危险型为aa;
[0582]
rs117227749的纯合保护型为aa,杂合型为ta或at,纯合危险型为tt;
[0583]
rs75222194的纯合保护型为tt,杂合型为ct或tc,纯合危险型为cc;
[0584]
针对所述snp标志物5:
[0585]
rs79938362的纯合保护型为cc,杂合型为tc或ct,纯合危险型为tt;
[0586]
rs116989317的纯合保护型为gg,杂合型为ag或ga,纯合危险型为aa;
[0587]
针对所述snp标志物6:
[0588]
rs73335760的纯合保护型为aa,杂合型为ga或ag,纯合危险型为gg;
[0589]
针对所述snp标志物7:
[0590]
rs201061882的纯合保护型为ttcttc,杂合型为tttc或ttct,纯合危险型为tt;
[0591]
rs11700622的纯合保护型为gg,杂合型为ag或ga,纯合危险型为aa;
[0592]
rs75423607的纯合保护型为cc,杂合型为tc或ct,纯合危险型为tt;
[0593]
rs76415665的纯合保护型为gg,杂合型为cg或gc,纯合危险型为cc;
[0594]
rs112894701的纯合保护型为cc,杂合型为tc或ct,纯合危险型为tt;
[0595]
rs79765594的纯合保护型为aa,杂合型为ga或ag,纯合危险型为gg;
[0596]
rs73354686的纯合保护型为aa,杂合型为ga或ag,纯合危险型为gg;
[0597]
rs76372004的纯合保护型为cc,杂合型为tc或ct,纯合危险型为tt;
[0598]
rs11702842的纯合保护型为gg,杂合型为ag或ga,纯合危险型为aa;
[0599]
rs73193458的纯合保护型为gg,杂合型为ag或ga,纯合危险型为aa;
[0600]
rs138904949的纯合保护型为atat,杂合型为aat或ata,纯合危险型为aa;
[0601]
针对所述snp标志物8:
[0602]
rs2275994的纯合保护型为cc,杂合型为tc或ct,纯合危险型为tt;
[0603]
rs6996060的纯合保护型为gg,杂合型为ag或ga,纯合危险型为aa;
[0604]
rs10104930的纯合保护型为aa,杂合型为ta或at,纯合危险型为tt;
[0605]
rs16868196的纯合保护型为cc,杂合型为tc或ct,纯合危险型为tt;
[0606]
rs192243723的纯合保护型为aa,杂合型为ca或ac,纯合危险型为cc;
[0607]
rs150249158的纯合保护型为cc,杂合型为tc或ct,纯合危险型为tt;
[0608]
rs375127474的纯合保护型为gg,杂合型为ag或ga,纯合危险型为aa;
[0609]
rs141273852的纯合保护型为cc,杂合型为tc或ct,纯合危险型为tt。
[0610]
所述判断模块,根据危险评分判断待测样本的放化疗引起的听力损伤的风险,判定标准为:危险评分>危险评分的阈值,则待测样本是放化疗引起听力损伤的高危个体;危险评分≤危险评分的阈值,则待测样本是放化疗引起听力损伤的低危个体。危险评分的阈值由实施例4的步骤2的方法得到。
[0611]
所述输出模块,用于输出待测样本的放化疗引起的听力损伤的风险。
[0612]
上述实施例中,所包括的各个模块只是按照功能逻辑进行划分的,但并不局限于上述的划分,只要能够实现相应的功能即可;另外,各功能模块的具体名称也只是为了便于相互区分,并不用于限制本发明的保护范围。
[0613]
实施例6放化疗引起听力损伤的风险评分系统
[0614]
本发明提供一种放化疗引起的听力损伤的风险评分系统,所述系统包含:信息采集模块、储存模块、信息分析模块、判断模块和输出模块。
[0615]
所述信息采集模块获取待测样本的特征参数,所述特征参数包括snp标志物1~8在待测样本基因组dna中的基因型分型,以及待测样本的诊断年龄、肿瘤t分期和同期化疗顺铂剂量。
[0616]
其中,snp标志物1:rs1050851;
[0617]
snp标志物2:rs117098517;
[0618]
snp标志物3:rs1485149;
[0619]
snp标志物4:rs17010289;
[0620]
snp标志物5:rs79938362
[0621]
snp标志物6:rs73335760;
[0622]
snp标志物7:rs201061882;
[0623]
snp标志物8:rs2275994。
[0624]
所述储存模块用于储存信息采集模块中获取的特征参数和判断模块中的危险评分的阈值(0.9598)。
[0625]
所述信息分析模块,根据获得的特征参数,通过公式计算得到危险评分;所述公式为:危险评分=(0.5616
×
诊断年龄的评分)+(0.5433
×
肿瘤t分期的评分)+(0.5211
×
同期化疗顺铂剂量的评分)+(0.8548
×
snp标志物1的基因型分型的评分)+(1.7102
×
snp标志物2的基因型分型的评分)+(1.2895
×
snp标志物3的基因型分型的评分)+(1.1940
×
snp标志物4的基因型分型的评分)+(1.8931
×
snp标志物5的基因型分型的评分)+(1.2720
×
snp标志物6的基因型分型的评分)+(1.5115
×
snp标志物7的基因型分型的评分)+(1.4220
×
snp标志物8的基因型分型的评分);所述诊断年龄的评分为:诊断年龄《50岁=“0”;诊断年龄≥50岁=“1”;所述肿瘤t分期的评分为:t1~t2期=“0”;t3~t4期=“1”;所述同期化疗顺铂剂量的评分为:同期化疗顺铂剂量《155mg/m2=“0”,同期化疗顺铂剂量≥155mg/m2=“1”;snp标志物1~8的基因型分型的评分为:纯合保护型=“0”;杂合型=“1”;纯合危险型=“2”。
[0626]
所述snp标志物1~8的基因型分型如实施例4中表4所示,具体为:
[0627]
rs1050851的纯合保护型为gg,杂合型为ag或ga,纯合危险型为aa;
[0628]
rs117098517的纯合保护型为cc,杂合型为tc或ct,纯合危险型为tt;
[0629]
rs1485149的纯合保护型为aa,杂合型为ca或ac,纯合危险型为cc;
[0630]
rs17010289的纯合保护型为aa,杂合型为ga或ag,纯合危险型为gg;
[0631]
rs79938362的纯合保护型为cc,杂合型为tc或ct,纯合危险型为tt;
[0632]
rs73335760的纯合保护型为aa,杂合型为ga或ag,纯合危险型为gg;
[0633]
rs201061882的纯合保护型为ttcttc,杂合型为tttc或ttct,纯合危险型为tt;
[0634]
rs2275994的纯合保护型为cc,杂合型为tc或ct,纯合危险型为tt。
[0635]
所述判断模块,根据危险评分判断待测样本的放化疗引起的听力损伤的风险,判定标准为:危险评分>0.9598,则待测样本是放化疗引起听力损伤的高危个体;危险评分≤0.9598,则待测样本是放化疗引起听力损伤的低危个体。
[0636]
所述输出模块,用于输出待测样本的放化疗引起的听力损伤的风险。
[0637]
上述实施例中,所包括的各个模块只是按照功能逻辑进行划分的,但并不局限于上述的划分,只要能够实现相应的功能即可;另外,各功能模块的具体名称也只是为了便于相互区分,并不用于限制本发明的保护范围。
[0638]
实施例7一种检测肿瘤放化疗引起听力损伤的风险的试剂盒
[0639]
一、组成
[0640]
试剂盒的主要成分包含如表6所示的pcr扩增引物及探针,还包括相应pcr技术所需的常用试剂:如dntp混合液、mgcl2溶液、pcr反应缓冲液、pcr反应酶、双蒸水、空白对照及阳性对照。空白对照即为双蒸水;阳性对照即为如表7所示的8个snp标志物及其连锁snp标志物确定基因型的标准品,浓度为50ng/μl。
[0641]
表6 8个snp标志物及其连锁snp标志物的pcr扩增引物及探针
[0642]
[0643]
[0644][0645]
表7 8个snp标志物及其连锁snp标志物确定基因型的标准品
[0646]
[0647]
[0648]
[0649]
[0650]
[0651]
[0652][0653][0654]
表中方框标出的碱基即为各snp标志物的参考等位基因和效应等位基因。
[0655]
二、使用方法
[0656]
1、待测样本基因组dna的提取
[0657]
本试剂盒对样本的来源没有特殊限定,全血、血凝块、血清、血浆、唾液、口咽拭子、鼻咽拭子、鼻咽镜取材样本、尿液、粪便等含有人体dna的生物标本均可作为待测样本。
[0658]
本试剂盒对待测样本基因组dna的提取方法没有指定要求,一般可用实验室常规方法(酚-氯仿抽提法)或试剂盒提取。
[0659]
测定dna的浓度和纯度,将常规质检合格的dna的浓度调整至50ng/μl用于后续检测。
[0660]
2、pcr反应
[0661]
设置空白对照、阳性对照和待测样本三管,空白对照的扩增模板为双蒸水,阳性对照的扩增模板为表7所示的序列(seq id no:161~240),待测样本的扩增模板为上一步提取得到的待测样本基因组dna。根据针对检测的snp标志物,选择表6中对应的扩增引物及探针,配制如表8所示的pcr反应体系。
[0662]
表8pcr反应体系
[0663][0664]
pcr反应扩增条件为:60℃30秒;95℃10分钟;95℃15秒,60℃1分钟,循环45次;60℃30秒。
[0665]
使用上述pcr反应体系和扩增条件进行荧光定量pcr反应,收集pcr反应过程中的荧光变化信息。
[0666]
三、结果判读
[0667]
根据实施例4中表4所示的基因型分型,分析判定各样本snp标志物1~8的基因型分型,结合对应样本的诊断年龄、肿瘤t分期和同期化疗顺铂剂量,使用实施例5中放化疗引起听力损伤的风险评分系统进行计算和判定。
[0668]
实施例8一种检测肿瘤放化疗引起听力损伤的风险的试剂盒
[0669]
一、组成
[0670]
试剂盒的主要成分包含如表9所示的pcr扩增引物及探针,还包括相应pcr技术所需的常用试剂:如dntp混合液、mgcl2溶液、pcr反应缓冲液、pcr反应酶、双蒸水、空白对照及阳性对照。空白对照即为双蒸水;阳性对照即为如表10所示的8个snp标志物确定基因型的标准品,浓度为50ng/μl。
[0671]
表9 8个snp标志物的pcr扩增引物及探针
[0672][0673]
表10 8个snp标志物确定基因型的标准品
[0674]
[0675]
[0676][0677]
表中方框标出的碱基即为各snp标志物的参考等位基因和效应等位基因。
[0678]
二、使用方法
[0679]
1、待测样本基因组dna的提取
[0680]
本试剂盒对样本的来源没有特殊限定,全血、血凝块、血清、血浆、唾液、口咽拭子、鼻咽拭子、鼻咽镜取材样本、尿液、粪便等含有人体dna的生物标本均可作为待测样本。
[0681]
本试剂盒对待测样本基因组dna的提取方法没有指定要求,一般可用实验室常规方法(酚-氯仿抽提法)或试剂盒提取。
[0682]
测定dna的浓度和纯度,将常规质检合格的dna的浓度调整至50ng/μl用于后续检测。
[0683]
2、pcr反应
[0684]
设置空白对照、阳性对照和待测样本三管,空白对照的扩增模板为双蒸水,阳性对照的扩增模板为表10所示的序列,待测样本的扩增模板为上一步提取得到的待测样本基因组dna。根据针对检测的snp标志物,选择表9中对应的扩增引物及探针,配制如表11所示的pcr反应体系。
[0685]
表11pcr反应体系
[0686][0687]
pcr反应扩增条件为:60℃30秒;95℃10分钟;95℃15秒,60℃1分钟,循环45次;60℃30秒。
[0688]
使用上述pcr反应体系和扩增条件进行荧光定量pcr反应,收集pcr反应过程中的荧光变化信息。
[0689]
三、结果判读
[0690]
根据实施例4中表4所示的基因型分型,分析判定各样本snp标志物1~8的基因型分型,结合对应样本的诊断年龄、肿瘤t分期和同期化疗顺铂剂量,使用实施例6中放化疗引
起听力损伤的风险评分系统进行计算和判定。
[0691]
实施例9检测肿瘤放化疗引起听力损伤的风险的试剂盒的应用
[0692]
一、实验方法
[0693]
使用实施例8的试剂盒,预测5名鼻咽癌患者因放化疗引起听力损伤的风险。5名鼻咽癌患者的临床信息如表12所示。
[0694]
表12 5名鼻咽癌患者的临床信息
[0695][0696]
二、实验结果
[0697]
5名鼻咽癌患者snp标志物1~8(snp标志物1:rs1050851、snp标志物2:rs117098517、snp标志物3:rs1485149、snp标志物4:rs17010289、snp标志物5:rs79938362、snp标志物6:rs73335760、snp标志物7:rs201061882和snp标志物8:rs2275994)的基因分型结果如表13所示。
[0698]
表13试剂盒检测5名鼻咽癌患者snp标志物的基因分型结果
[0699][0700]
根据临床信息和snp标志物1~8的基因分型结果,计算得到5名鼻咽癌患者的危险评分如表14所示。
[0701]
表14 5名鼻咽癌患者的危险评分
[0702][0703][0704]
结果显示,这5名鼻咽癌患者的危险评分均大于0.9598,所以这5名患者为放化疗所致听力损伤的高危个体。
[0705]
最后所应当说明的是,以上实施例仅用以说明本发明的技术方案而非对本发明保
护范围的限制,对于本领域的普通技术人员来说,在上述说明及思路的基础上还可以做出其它不同形式的变化或变动,这里无需也无法对所有的实施方式予以穷举。凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明权利要求的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1