基于DNA四面体局部结构降解的miRNA检测传感器、试剂盒及检测方法
基于dna四面体局部结构降解的mirna检测传感器、试剂盒及检测方法
技术领域
1.本发明涉及生物医药技术领域,特别涉及一种基于dna四面体局部结构降解的mirna检测传感器、试剂盒及检测方法。
背景技术:
2.microrna(mirna)是一种非编码单链rna,大小约为18~25个核苷酸,是多种细胞过程(如细胞增殖、分裂、分化和凋亡)的重要调控因子,通过转录后调节相应的基因表达。在多种疾病的发展进程中起到特定的调节作用。例如,mir-141和mir-200a能够调节与肿瘤生长相关的氧化应激反应;mir-200-zeb1在调节上皮-间质转化促进癌症的进展和转移中起关键作用。因此,检测mirna对于研究相关疾病的调节通路至关重要。在传统的检测方法中,逆转录定量聚合酶链式反应是mirna分析的技术标准。然而,由于mirna的尺寸小,引物设计复杂,这种方法存在一些局限性。而其他一些常用的mirna测定方法,例如northern印迹和微阵列法,也存在灵敏度不足和技术复杂的弊端。因此仍需开发新型的超灵敏mirna检测方案。
技术实现要素:
3.本发明所要解决的技术问题在于针对上述现有技术中的不足,提供一种基于dna四面体局部结构降解的mirna检测传感器、试剂盒及检测方法。本发明构建了一种新的mirna检测策略,通过目标mirna与特殊构造的dna四面体反应,来形成部分dna/rna杂合体,在触发双链特异性核酸酶(dsn)的活性进行切割后,可实现dna四面体局部结构的降解,同时释放用于捕获银纳米颗粒(agnps)信号探针的单链区域,实现mirna的高灵敏度、高特异性电化学检测。并据此形成了mirna检测传感器、试剂盒以及对应的检测方法。
4.为实现上述目的,本发明采用的技术方案是:提供一种基于dna四面体局部结构降解的mirna检测传感器,包括:侧链上具有茎环结构序列的dna四面体以及修饰在所述dna四面体上的连接基团和捕获基团,所述连接基团用于与电极偶联,所述捕获基团用于捕获电化学探针;
5.所述mirna检测传感器的检测原理为:在存在目标mirna、电化学探针和双链特异性核酸酶的体系中,所述mirna检测传感器中的茎环结构序列与目标mirna特异性杂交反应打开dna四面体的结构,dna四面体中与目标mirna杂交部分的dna序列被双链特异性核酸酶降解,释放的目标mirna用于循环反应,dna四面体上暴露出捕获基团,捕获基团捕获体系中的电化学探针,通过对体系进行电化学信号测量实现目标mirna含量的检测。
6.优选的是,所述连接基团为巯基或生物素或其他可以与电极界面作用的基团。
7.优选的是,所述电化学探针为银纳米颗粒或铜纳米颗粒或其他具备电化学响应信号的材料。
8.优选的是,所述捕获基团为氨基或巯基或其他可以与所述电化学探针结合的基
团。
9.优选的是,所述mirna检测传感器的组装方法为:将等体积的四种探针:probe ta、probe tb、probe tc、probe td加入到氯化钠和磷酸盐缓冲液的混合液中,加热到95℃,反应5min,得到所述mirna检测传感器。
10.优选的是,其中的四种探针:probe ta、probe tb、probe tc、probe td的序列如下:
11.probe ta的序列为:
[0012]5’‑
sh-c
6-acattcctaagtctgaaacattacagcatgctacacgaga agagccaccatagta-3’;
[0013]
probe tb的序列为:
[0014]5’‑
tatcaccaagcagttgacagtgtagcaagctgtaatagatgcga ggtaggttgaactatacaacctactacctca-3’;
[0015]
probe tc的序列为:
[0016]5’‑
sh-c
6-tcaactgcatggtgataaaacgacactacgtgggaatcta ctatggaggctcttc-3’;
[0017]
probe td的序列为:
[0018]5’‑
sh-c
6-tttctcgcatttcagactaaggaatgtgcttcccacgaag tgtcgttttgaggta-nh2-3’;
[0019]
目标mirna的序列为:5
’‑
ugagguaguagguuguauaguu-3’。
[0020]
本发明还提供一种基于dna四面体局部结构降解的mirna检测试剂盒,其包括如上所述的mirna检测传感器、电化学探针和双链特异性核酸酶。
[0021]
优选的是,所述连接基团为巯基基团,所述电化学探针为银纳米颗粒,所述捕获基团为氨基。
[0022]
本发明还提供一种基于dna四面体局部结构降解的mirna检测方法,其采用如上所述的mirna检测试剂盒进行目标mirna的检测,具体包括以下步骤:
[0023]
1)电极的预处理;
[0024]
2)合成银纳米颗粒;
[0025]
3)组装mirna检测传感器:将等体积的四种探针:probe ta、probe tb、probe tc、probe td加入到氯化钠和磷酸盐缓冲液的混合液中,加热到95℃,反应5min并冷却至室温,得到所述mirna检测传感器。
[0026]
4)dsn催化解链反应:将含目标mirna的待测样品与mirna检测传感器共孵育,接着加入双链特异性核酸酶,加热条件下进行降解反应;然后将预处理后的电极插入反应产物中,反应,再使用纯水冲洗干净电极,之后将电极浸泡入银纳米颗粒;
[0027]
5)对步骤4)得到的电极进行电化学检测,最后根据电极的电化学信号强度,结合预先建立的表征目标mirna浓度与电化学信号强度关系的标准曲线计算出待测样品中目标mirna的浓度。
[0028]
优选的是,该方法具体包括以下步骤:
[0029]
1)电极的预处理:
[0030]
将金电极浸泡在水虎鱼溶液中放置5min,然后用砂纸对金电极进行电极界面的抛光并冲洗;接着通过氧化铝浆液对金电极进行进一步抛光,最终得到镜面状态的平整电极表面;将金电极分别在乙醇和双蒸馏水中进行超声处理,随后,在0.5m硫酸中使用循环伏安
法对电极进行电化学清洗,最后用超纯水冲洗再用氮气干燥,得到预处理后的金电极;
[0031]
2)合成银纳米颗粒:
[0032]
配制浓度为0.25mm的硝酸银溶液和浓度为0.25mm的柠檬酸三钠溶液,混合后,再加入浓度为10mm的硼氢化钠溶液,搅拌,30分钟后,12000rpm下离心30分钟,弃上清,并将沉淀重悬,得到银纳米颗粒重悬液;
[0033]
3)组装mirna检测传感器:将等体积的四种探针probe ta、probe tb、probe tc、probe td加入到氯化钠和磷酸盐缓冲液的混合液中,加热到95℃,反应5min并冷却至室温,得到所述mirna检测传感器;
[0034]
4)dsn催化解链反应:将含目标mirna的待测样品与mirna检测传感器共孵育,接着加入浓度为3u/ml的双链特异性核酸酶,50℃下反应2小时;然后将预处理后的金电极插入反应产物中,反应8小时,再使用纯水冲洗干净电极,之后将电极浸泡入银纳米颗粒重悬液中反应20分钟;
[0035]
5)对步骤4)得到的电极进行电化学检测,最后根据金电极的电化学信号强度,结合预先建立的表征目标mirna浓度与电化学信号强度关系的标准曲线计算出待测样品中目标mirna的浓度。
[0036]
本发明的有益效果是:
[0037]
本发明成果构建了一种新的mirna检测策略,通过目标mirna与特殊构造的dna四面体反应,来形成部分dna/rna杂合体,在触发双链特异性核酸酶(dsn)的活性进行切割后,可实现dna四面体局部结构的降解,同时释放用于捕获银纳米颗粒(agnps)信号探针的单链区域,实现mirna的高灵敏度、高特异性电化学检测;并据此形成了mirna检测传感器、试剂盒以及对应的检测方法。
附图说明
[0038]
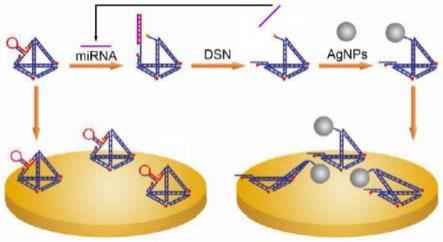
图1为本发明的基于dna四面体局部结构降解的mirna检测传感器的检测原理示意图;
[0039]
图2为本发明的实施例1中对mirna检测传感器可行性的验证结果:图2a为凝胶电泳表征结果,图2b-2d为采用循环伏安法、交流阻抗及线性伏安扫描法研究电极界面上的组装及反应进程的结果;
[0040]
图3为本发明的实施例1中获取的不同浓度mirna与检测传感器反应后得到的电化学分析结果:图3a为不同浓度mirna的线性伏安扫描曲线,图3b为mirna浓度对数值与峰电流关系的拟合曲线。
具体实施方式
[0041]
下面结合实施例对本发明做进一步的详细说明,以令本领域技术人员参照说明书文字能够据以实施。
[0042]
应当理解,本文所使用的诸如“具有”、“包含”以及“包括”术语并不排除一个或多个其它元件或其组合的存在或添加。
[0043]
下列实施例中所使用的试验方法如无特殊说明,均为常规方法。下列实施例中所用的材料试剂等,如无特殊说明,均可从商业途径得到。下列实施例中未注明具体条件者,
按照常规条件或者制造商建议的条件进行。所用试剂或仪器未注明生产厂商者,均为可以通过市售购买获得的常规产品。
[0044]
实施例1
[0045]
本实施例提供一种基于dna四面体局部结构降解的mirna检测传感器,其包括:侧链上具有茎环结构序列的dna四面体以及修饰在所述dna四面体上的连接基团和捕获基团,所述连接基团用于与电极偶联,所述捕获基团用于捕获电化学探针;
[0046]
参照图1,所述mirna检测传感器的检测原理为:在存在目标mirna、电化学探针和双链特异性核酸酶(dsn)的体系中,所述mirna检测传感器中的茎环结构序列与目标mirna特异性杂交反应打开dna四面体的结构,dna四面体中与目标mirna杂交部分的dna序列被双链特异性核酸酶降解,释放的目标mirna用于循环反应,局部降解后的dna四面体上暴露出捕获基团,捕获基团捕获体系中的电化学探针,通过对体系进行电化学信号测量实现目标mirna含量的检测。
[0047]
本实施例中,所述连接基团为巯基基团,可以理解的是,也可以采用其他能够使dna四面体偶联到电极上的基团或方案,例如:电极首先修饰抗生物素蛋白,同时将dna四面体底部的巯基基团替换为生物素,即可通过抗生物素蛋白-生物素之间特异性的反应实现dna四面体的修饰。
[0048]
本实施例中,所述电化学探针为银纳米颗粒,对应的所述捕获基团为氨基,可以理解的是,电化学探针与用于捕获其的捕获基团也可以是其他组合,例如:炔基修饰的二茂铁纳米颗粒(电化学探针)与暴露出的叠氮基团(捕获基团)之间的点击化学反应可实现快速连接。
[0049]
本实施例中,所述mirna检测传感器的组装方法为:将等体积的四种探针:probe ta、probe tb、probe tc、probe td加入到氯化钠和磷酸盐缓冲液的混合液中,加热到95℃,反应5min,得到所述mirna检测传感器。
[0050]
本实施例中,为便于进行说明,提供了具体的四种探针以及对应的目标mirna,四种探针:probe ta、probe tb、probe tc、probe td的序列如下:
[0051]
probe ta的序列为:
[0052]
seq id no.1:
[0053]5’‑
sh-c
6-acattcctaagtctgaaacattacagcatgctacacgagaagagccaccatagta-3’;
[0054]
probe tb的序列为:
[0055]
seq id no.2:
[0056]5’‑
tatcaccaagcagttgacagtgtagcaagctgtaatagatgcgaggtaggttgaactatacaacctactacctca-3’;
[0057]
probe tc的序列为:
[0058]
seq id no.3:
[0059]5’‑
sh-c
6-tcaactgcatggtgataaaacgacactacgtgggaatctactatggaggctcttc-3’;
[0060]
probe td的序列为:
[0061]
seq id no.5:
[0062]5’‑
sh-c
6-tttctcgcatttcagactaaggaatgtgcttcccacgaagtgtcgttttgaggta-nh2-3’;
[0063]
目标mirna的序列为:
[0064]
seq id no.6:5
’‑
ugagguaguagguuguauaguu-3’。
[0065]
以下对本发明提供的mirna检测传感器的可行性等相关性能进行了验证与研究,具体如下。
[0066]
1、参照图2a,为通过聚丙烯酰胺凝胶电泳对dna组装进行表征的结果,其中a-d泳道为探针probe ta、probe tb、probe tc、probe td进行dna四面体组装获得的杂合体的结果,随着dna四面体组装的dna链条数的增加,可以观察到形成了分子量更大的新条带,表明形成了相应的结构。e泳道为只有探针probe tb的结果,f泳道为探针probe tb与mirna杂交的杂合体的结果,说明探针tb与mirna杂交形成更大分子量的杂合体;g泳道为探针probe tb、mirna与dsn混合的结果,当其中加入dsn后,双链条带消失,形成了一个较小的条带,表明dsn对双链的高效消化活性。
[0067]
2、参照图2b-2d,为采用循环伏安法、交流阻抗及线性伏安扫描法研究电极界面上的组装及反应进程结果;图2b为循环伏安图,可以看出,裸电极(bare electrode)的电流峰最高,当电极修饰dna四面体后(tdna),由于其磷酸骨架能够有效排斥电信号分子[fe(cn)6]
3-/4-,因此循环伏安峰显著降低,而当mirna与dsn作用后(mirna+dsn),dna四面体结构发生破坏且电负性降低,因而循环伏安峰电流强度有所恢复;
[0068]
图2c显示了相应的交流阻抗谱,裸电极不包含任何半圆区域,这反映了电极良好的导电性。经dna四面体修饰后,出现了一个显著的半圆区域,表面阻抗值的增加。由于靶mirna启动的dsn裂解反应,半圆区域直径较小,表明电极表面电负性程度得以降低,与循环伏安图的结论吻合;
[0069]
图2d中测量并比较了银纳米颗粒的线性伏安扫描响应,分析了裸电极(bare electrode)、dna四面体修饰电极(tdna)、mirna与dsn反应后的电极(mirna+dsn),由于完整结构的dna四面体中氨基基团被封闭在内,无法与银纳米颗粒有效接触,因此裸电极及dna四面体修饰电极的线性伏安扫描图中不存在或只存在非常小的溶出伏安峰;当dna四面体结构被部分降解后,氨基暴露可以有效捕获银纳米颗粒,因此可以通过电化学检测看到尖锐的溶出伏安峰。
[0070]
3、参照图3a和图3b,本发明中检测获取了不同浓度mirna与本发明的检测传感器反应后得到的电化学分析结果,图3a为不同浓度mirna的线性伏安扫描曲线,mirna浓度的增加导致更多的部分降解dna四面体及暴露出的氨基基团,与agnps反应进行信号输出后,所得的电流峰强度更高。图3b为mirna浓度对数值与峰电流关系的拟合曲线,从10am到100fm的线性范围,回归方程如下:
[0071]
y=100.849+5.796x(n=3;r2=0.995)
[0072]
其中y表示峰值电流的强度,x表示对数mirna浓度。检测限lod计算为3.1am(s/n=3),低于大多数报道的mirna检测方法。
[0073]
实施例2
[0074]
本实施例提供一种基于dna四面体局部结构降解的mirna检测试剂盒,其包括实施例1的mirna检测传感器、电化学探针和双链特异性核酸酶。其中,所述连接基团为巯基基团,所述电化学探针为银纳米颗粒,所述捕获基团为氨基。
[0075]
实施例3
[0076]
本实施例提供一种基于dna四面体局部结构降解的mirna检测方法,其采用实施例2的mirna检测试剂盒进行目标mirna的检测,具体包括以下步骤:
[0077]
1)电极的预处理:
[0078]
将金电极浸泡在水虎鱼溶液(98%硫酸:30%过氧化氢=3:1)中放置5min,然后用p5000砂纸对金电极进行电极界面的抛光并冲洗;接着通过氧化铝浆液(1,0.3,0.05μm)对金电极进行进一步抛光,最终得到镜面状态的平整电极表面;将金电极分别在乙醇和双蒸馏水中进行超声处理,随后,在0.5m硫酸中使用循环伏安法对电极进行电化学清洗,最后用超纯水冲洗再用氮气干燥,得到预处理后的金电极;
[0079]
2)合成银纳米颗粒:
[0080]
配制浓度为0.25mm的硝酸银溶液和浓度为0.25mm的柠檬酸三钠溶液,混合为100ml体积后,再加入3ml冰冷的浓度为10mm的硼氢化钠溶液,剧烈搅拌,30分钟后,12000rpm下离心30分钟进行纯化,弃上清,并将沉淀重悬,得到银纳米颗粒重悬液;
[0081]
3)组装mirna检测传感器:将等体积的四种探针probe ta、probe tb、probe tc、probe td加入到含有0.25m氯化钠(ph 7.0)的10mm磷酸盐缓冲液(pbs)中,四种探针的浓度均为4μm,加热到95℃,反应5min并冷却至室温,得到所述mirna检测传感器;
[0082]
4)dsn催化解链反应:将含目标mirna的待测样品与mirna检测传感器共孵育,接着加入浓度为3u/ml的双链特异性核酸酶,50℃下反应2小时;然后将预处理后的金电极插入反应产物中,反应8小时,再使用纯水冲洗干净电极,之后将金电极浸泡入银纳米颗粒重悬液中反应20分钟;
[0083]
5)对步骤4)得到的电极进行电化学检测:采用chi660d电化学工作站进行电化学信号的测量。电化学体系中包含铂对电极、ag/agcl参比电极及金工作电极(步骤4得到的电极)。循环伏安参数:0.6到-0.2v扫描范围,50mv/s扫描速度;交流阻抗参数:振幅5mv,频率范围0.1hz到100000hz;线性伏安扫描参数:扫描范围0.65到-0.4v。交流阻抗法的电解液为5mm铁氰化钾;线性伏安扫描法的电解液为0.1m kcl;
[0084]
最后根据金电极的电化学信号强度,结合预先建立的表征目标mirna浓度与电化学信号强度关系的标准曲线(例如实施例1中图3b所示的拟合曲线)计算出待测样品中目标mirna的浓度。
[0085]
尽管本发明的实施方案已公开如上,但其并不仅仅限于说明书和实施方式中所列运用,它完全可以被适用于各种适合本发明的领域,对于熟悉本领域的人员而言,可容易地实现另外的修改,因此在不背离权利要求及等同范围所限定的一般概念下,本发明并不限于特定的细节。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1