一类双青蒿素衍生物及其制备方法与应用
1.本发明涉及抗肿瘤药物技术领域,具体涉及到一类双青蒿素衍生物在制备抗肿瘤药物中的应用。
背景技术:
2.青蒿素是一种从甜蒿植物黄花蒿l.中提取的天然倍半萜内酯类化合物,已在中药中使用了数千年的治疗发烧和寒战。20世纪70年代,屠呦呦研究小组发现青蒿素作为一种抗疟药物可以有效地杀死疟疾寄生虫,拯救了全世界数百万人的生命。此外,青蒿素在临床上被用于治疗咳嗽、感冒和腹泻,以及对抗细菌、真菌和病毒感染。不仅如此,早在1995年,华盛顿大学的研究人员发现,青蒿素可以杀死某些类型的癌细胞。在体外实验中,青蒿素证明了对所有测试的癌细胞的细胞毒性。在过去的五年中,大量新的研究也表明,青蒿素及其衍生物可以选择性地杀死多种癌细胞。然而,青蒿素的单体衍生物在癌细胞中表现出相对较低的细胞毒性,且在体内中的半衰期较短。近年来,有研究表明,青蒿素二聚体即双青蒿素,明显比单体更有效,单体可以抑制肿瘤生长,其活性比单体高几个数量级。
3.蛋白水解靶向嵌合分子(protac)是一种可以募集靶蛋白和靶蛋白降解酶的杂合双功能化合物,它是由一个可以识别靶标蛋白的配体和一个e3连接酶配体组成,protac分子可以使poi和e3泛素连接酶接近,并诱导poi发生泛素化,然后通过泛素-蛋白酶体降解系统(ups)促进poi降解。该技术具有靶向性广、细胞通透性好、组织特异性好、选择性高、口服生物利用度高、可控等优点。
技术实现要素:
4.本发明的目的是:为了获得抗肿瘤活性更高且机理明确的青蒿素衍生物,本发明利用protac技术将双青蒿素与不同e3泛素连接酶配体通过不同linker共价连接,设计了一类双青蒿素衍生物,它们能在血液瘤细胞中有效降解与肿瘤相关的蛋白信号分子,表现出更强的细胞毒性,是一种优秀的抗肿瘤候选化合物。
5.本发明涉及的一类双青蒿素衍生物,该化合物具有如下通式:
[0006][0007]
所述的一类双青蒿素衍生物的制备方法,其合成路线如下:
[0008][0009]
具体合成步骤分为两步:
[0010]
步骤1:若e3泛素连接酶小分子配体含羧基(r-cooh)或氟取代基(r-f)时,将e3泛素连接酶小分子配体和含末端的氨基羧酸linker溶于n,n-二甲基乙酰胺(dma)中;若e3泛素连接酶小分子配体含氨基(r-nh2)时,将e3泛素连接酶小分子配体和含末端的二羧酸linker溶于n,n-二甲基乙酰胺(dma)中,随后加入n,n-二异丙基乙胺(diea),90℃回流6h,
tlc检测反应完成,用水洗和乙酸乙酯萃取反应液,饱和食盐水萃取乙酸乙酯层2-3遍,无水硫酸钠干燥,旋干有机层过柱得中间体linker-r;
[0011]
步骤2:将化合物linker-r溶解在四氢呋喃(thf)中,5min后加入n,n-二异丙基乙胺(diea),继续反应10min留样后加入双青蒿素,室温反应4h,tlc检测反应完成。旋干thf,用适量二氯甲烷溶解,盐水萃取二氯甲烷层2-3遍,无水硫酸钠干燥,旋干有机层过柱得所述的一类双青蒿素衍生物。
[0012]
以其中一种双青蒿素衍生物为例,该化合物具有如下通式之一:
[0013][0014]
式中,n为自然数,n=1、2、3、4。
[0015]
所述的双青蒿素衍生物的制备方法,其合成路线如下:
[0016][0017]
上述路线中,n为自然数,n=1、2、3、4。
[0018]
具体合成步骤如下:
[0019]
步骤1:将化合物1和2溶于n,n-二甲基乙酰胺(dma)中,随后加入n,n-二异丙基乙胺(diea),90℃回流6h,tlc检测反应完成,用水洗和乙酸乙酯萃取反应液,饱和食盐水萃取乙酸乙酯层2-3遍,无水硫酸钠干燥,旋干有机层过柱得产物3;
[0020]
步骤2:将化合物3溶解在四氢呋喃(thf)中,5min后加入n,n-二异丙基乙胺(diea),继续反应10min留样后加入化合物4,室温反应4h,tlc检测反应完成。旋干thf,用适量二氯甲烷溶解,盐水萃取二氯甲烷层2-3遍,无水硫酸钠干燥,旋干有机层过柱得产物ar1-4;
[0021]
上述双青蒿素衍生物能够用于制备抗肿瘤的药物。
[0022]
优选的,所述肿瘤为血液瘤。
[0023]
通过采用上述技术方案,本发明通过protac技术设计合成的双青蒿素衍生物,对多种癌细胞具有抑制作用,且对血液瘤的抗肿瘤活性明显,是对血液瘤具有治疗作用的新型双青蒿素衍生物。
[0024]
化合物ar1-4的
13
c-nmr、1h-nmr数据:
[0025]
化合物ar1:1h nmr(400mhz,dmso-d6)δ8.36(d,j=14.5hz,1h),7.48(dd,j=8.4,7.2hz,1h),7.07(d,j=6.9hz,1h),6.87(d,j=8.5hz,1h),6.25(t,j=5.3hz,1h),5.37
–
5.27(m,2h),4.89(dd,j=12.1,5.4hz,1h),4.76(dd,j=9.8,3.5hz,2h),4.03
–
3.88(m,2h),3.74(m,j=13.4,8.1,5.0hz,1h),3.63(dd,j=14.2,9.1hz,1h),3.55
–
3.36(m,4h),3.28(q,j=6.1hz,2h),2.87(dd,j=14.5,3.5hz,1h),2.75
–
2.69(m,1h),2.66
–
2.55(m,2h),2.36(m,j=17.8,13.4,5.1hz,4h),2.14
–
2.07(m,1h),2.01(d,j=14.5hz,2h),1.89
–
1.81(m,3h),1.62(m,j=22.2,10.2,6.0hz,10h),1.51
–
1.36(m,10h),1.33
–
1.16(m,6h),0.93
–
0.84(m,12h).
13
c nmr(100mhz,dmso-d6)δ172.46,171.23,169.51,168.46,167.69,146.91,136.25,132.55,116.68,111.56,109.96,104.36,104.23,102.54,102.30,87.90,81.05,80.96,66.52,66.27,66.18,52.53,52.46,48.93,47.81,45.16,45.11,44.36,44.19,42.64,38.70,37.55,36.44,36.39,34.67,34.56,33.02,31.52,30.80,30.72,29.79,29.40,29.17,26.22,24.75,24.71,24.62,24.55,22.88,22.65,20.46,13.14,13.11.
[0026]
化合物ar2:1h nmr(400mhz,dmso-d6)δ8.38(s,1h),7.50
–
7.44(m,1h),7.07(d,j=7.1hz,1h),6.86(d,j=8.6hz,1h),6.21(t,j=5.4hz,1h),5.37
–
5.27(m,2h),4.89(dd,j=11.9,5.4hz,1h),4.76(dd,j=9.5,3.3hz,2h),4.03
–
3.88(m,2h),3.78
–
3.69(m,1h),3.66
–
3.58(m,1h),3.55
–
3.37(m,4h),3.26(dd,j=12.8,6.6hz,2h),2.90
–
2.82(m,1h),2.75(dd,j=6.7,2.7hz,1h),2.62(m,j=15.4,9.8,5.9hz,2h),2.40
–
2.26(m,4h),2.11(m,j=10.2,3.8hz,1h),2.05
–
1.97(m,2h),1.91
–
1.81(m,3h),1.72
–
1.56(m,10h),1.42(dd,j=12.2,4.2hz,12h),1.29
–
1.14(m,6h),0.93
–
0.82(m,12h).
13
c nmr(100mhz,dmso-d6)δ172.77,171.22,169.55,168.48,167.70,146.99,136.23,132.53,116.72,111.51,109.91,104.35,104.23,102.54,102.29,87.90,81.06,80.97,66.56,66.34,66.29,52.54,52.48,48.92,47.86,45.17,44.37,44.20,42.46,38.70,37.56,36.44,36.39,34.68,34.57,33.35,31.51,30.80,30.73,29.26,29.23,26.84,26.21,24.91,24.75,24.71,24.61,24.55,22.88,20.46,13.15,13.10.
[0027]
化合物ar3:1h nmr(400mhz,dmso-d6)δ8.27(s,1h),7.48(m,j=8.2,7.4hz,1h),7.07(d,j=7.0hz,1h),6.87(d,j=8.5hz,1h),6.21(t,j=5.4hz,1h),5.32(dd,j=16.7,6.9hz,2h),4.90(dd,j=12.0,5.3hz,1h),4.76(dd,j=9.8,3.3hz,2h),4.03
–
3.89(m,2h),3.78
–
3.68(m,1h),3.66
–
3.56(m,1h),3.54
–
3.38(m,4h),3.25(dd,j=12.8,6.7hz,2h),2.97
–
2.82(m,1h),2.75
–
2.70(m,1h),2.66
–
2.56(m,2h),2.35(dd,j=14.8,9.9hz,4h),2.15
–
2.07(m,1h),2.02(d,j=13.5hz,2h),1.82(d,j=24.1hz,3h),1.65(m,j=24.1,13.0,3.3hz,12h),1.40(t,j=7.3hz,12h),1.27
–
1.16(m,6h),0.94
–
0.84(m,12h).13c nmr(100mhz,dmso-d6)δ172.99,171.19,169.55,168.47,167.72,147.03,136.23,132.53,116.73,111.48,109.88,104.35,104.22,102.55,102.30,87.91,81.07,80.98,77.46,77.35,77.14,76.83,66.53,66.33,52.54,52.48,48.92,47.85,45.12,44.37,44.21,42.66,38.70,37.56,36.44,36.40,34.68,34.57,33.40,31.51,30.81,30.74,29.79,29.28,29.21,27.01,26.23,25.20,24.75,24.71,24.61,24.55,22.88,20.48,13.16,13.11.
[0028]
化合物ar4:1h nmr(400mhz,dmso-d6)δ11.12(s,1h),7.56(m,j=7.6hz,1h),7.04
(dd,j=24.7,7.7hz,2h),6.51(t,j=5.2hz,1h),5.24(d,j=8.5hz,2h),5.03(dd,j=12.6,5.2hz,1h),4.66(d,j=12.9hz,2h),3.83
–
3.74(m,2h),3.44
–
3.36(m,6h),3.27(d,j=6.2hz,2h),2.92
–
2.80(m,1h),2.58(d,j=18.5hz,1h),2.31(dd,j=21.9,14.9hz,5h),2.15(t,j=13.6hz,2h),1.98(t,j=15.2hz,4h),1.83
–
1.70(m,3h),1.67
–
1.36(m,14h),1.26(s,12h),1.20
–
1.00(m,4h),0.84(dd,j=14.0,7.0hz,12h).
13
c nmr(100mhz,dmso-d6)δ173.43,172.83,170.62,169.46,167.85,146.91,136.84,132.65,117.67,110.94,109.42,103.90,103.86,101.61,101.29,87.41,80.95,80.88,65.98,65.54,52.45,49.02,47.53,44.62,44.24,44.09,42.30,37.27,37.22,36.49,34.61,33.24,31.47,30.88,30.84,29.35,29.29,29.20,26.85,26.81,26.10,25.39,24.79,24.52,24.43,22.67,20.67,13.24,13.13.
附图说明
[0029]
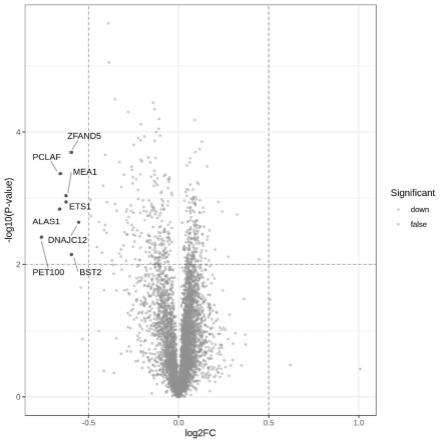
图1是通过蛋白组学分析靶标蛋白得到的火山图。
[0030]
图2是通过western blot验证降解的相关靶标蛋白。
具体实施方式
[0031]
为了使本领域技术人员更好地理解本发明的技术方案能予以实施。下面结合具体实例和附图对本发明作进一步说明,但所举实施例不作为对本发明的限定。
[0032]
下述方法中所涉及配料或材料,如无特殊说明,均为商业途径可获得。相关实验方法中如无特殊说明均为本技术领域现有常规方法。
[0033]
实施例1:双青蒿素衍生物在不同细胞系的毒性
[0034]
采用公认的可用于大规模抗肿瘤药物筛选、细胞毒性试验测定的cck-8法,评价ar1-4和母体化合物4对于rpmi8226(人多发性骨髓瘤外周血b淋巴细胞)、rs4;11(人急性淋巴白血病细胞)和u266(人骨髓瘤细胞)的细胞毒性种人癌细胞株的抗细胞增殖活性;阴性对照组为不加药组。
[0035]
细胞增殖抑制率=(阴性对照组0d值-药物组0d值)*100%/阴性对照组0d值。通过化合物不同浓度的抑制率由graphpad prism 5模拟曲线得出ic50值(单位为nm)。
[0036]
表1.对于三种不同血液瘤的细胞的ic50
[0037][0038][0039]
由表1可知,所设计的化合物在rs4;11细胞具有一个较强的细胞毒性,其中化合物ar4达到50.6nm,比母体化合物毒性高出10倍。然而随着linker长度的增加,活性依次降低。
[0040]
实施例2:蛋白组学进一步分析与靶标相关蛋白
[0041]
该实验基于tmt/itraq标记的定量蛋白质组学技术对化合物4和ar4两组样品间的
蛋白进行相对定量比较,筛选差异表达的蛋白,并进行后续的生物信息学分析,结果如图1。
[0042]
如图1所示,化合物ar4显著下调了9个蛋白,其中我们筛选了四个与肿瘤有关的蛋白进行进一步验证
[0043]
实施例3:通过western blot验证降解的相关靶标蛋白
[0044]
与肿瘤相关的被下调的蛋白为:alas1、ets1、zfand5、pclaf
[0045]
用浓度为100nm的ar4和5μm的蛋白酶体抑制剂处理rs4;11细胞12h,收集细胞,提取总蛋白,然后对alas1、ets1、zfand5、pclaf四个抗体进行western blot检测,结果如图2。
[0046]
结果发现,除了alas1,其余三个蛋白都被降解,并且加入mg132组都阻断了降解趋势,进一步说明ets1、zfand5、pclaf可能是化合物ar4的靶标蛋白。
[0047]
在此有必要指出的是,以上实施例和试验例仅限于对本发明技术方案做进一步阐述和理解,不能理解为对本发明的技术方案做进一步的限定,本领域技术人员作出的非突出实质性特征和显著进步的发明创造,仍然属于本发明的保护范畴。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1