一种SHP2抑制剂的可药用盐、晶型及其制备方法与流程
本公开涉及一种咪唑并嘧啶衍生物的晶型及其制备方法,属于制药领域。
背景技术:
1、shp2(含sh2结构域的蛋白酪氨酸磷酸酶2)也称为ptpn1 1(蛋白酪氨酸磷酸酶,非受体1 1型)是由ptpn1 1基因编码的胞质酪氨酸激酶。shp2可以被广泛的细胞因子和生长因子激活,并通过调节关键的细胞内信号传导途径(如ras丝裂原活化激酶(mapk)途径)在发育和体内平衡中发挥重要作用。
2、shp2蛋白包含两个n末端sh2域和一个c末端磷酸酶域。sh2结构域充当构象开关,控制shp2的激活和亚细胞定位。shp2的sh2结构域以其自身抑制形式结合并物理上封闭了催化位点。sh2结构域与磷蛋白的结合将shp2切换为开放构象,使底物能够进入催化位点。shp2 c末端尾部的两个酪氨酸残基的磷酸化可以募集重要的下游信号传导蛋白,因此shp2具有催化和支架功能。在少年骨髓单核细胞白血病(jmml),急性白血病中发现了破坏自我抑制的shp2体细胞突变,在神经母细胞瘤,aml/mds,cmml,黑素瘤和肺,乳腺,结肠癌中很少发现。在大约一半的noonan综合征患者和大多数leopard综合征患者中发现了shp2的种系突变。因此,代表了开发用于治疗各种疾病的新疗法的目标。
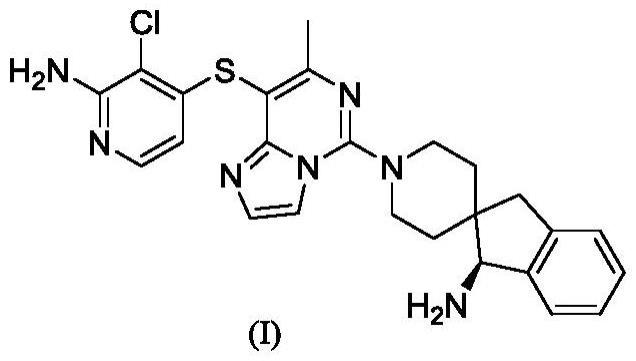
3、wo2020094104a公开了一种式(i)所示的咪唑并嘧啶衍生物,作为药用活性成
4、
5、分的晶型结构往往影响到该药物的化学稳定性,结晶条件及储存条件的不同有可能导致化合物的晶型结构的变化,有时还会伴随着产生其他形态的晶型。一般来说,无定形的药物产品没有规则的晶型结构,往往具有其它缺陷,比如产物稳定性较差,析晶较细,过滤较难,易结块,流动性差等。药物的多晶型对产品储存、生产及放大有不同的要求。因此,深入研究式(i)化合物的晶型及相关制备方法,改善式(i)所示化合物的各方面性质是很有必要的。
技术实现思路
1、本公开提供一种式(i)所示化合物的可药用盐,所述的可药用盐选自盐酸盐、硫酸盐、磷酸盐、乙酸盐、酒石酸盐、马来酸盐、苹果酸盐、柠檬酸盐、甲磺酸盐、对甲苯磺酸盐、富马酸盐、琥珀酸盐、马尿酸盐、氢溴酸盐,
2、
3、可选的实施方案中,本公开提供的式(i)所示化合物的可药用盐,其中式(i)所示化合物与酸分子的比例选自5:1-1:5;具体可选5:1、4:1、3:1、2:1、1:1、1:2、1:3、1:4或1:5,或者任意两个数之间的点值。
4、一些实施方案中,本公开提供一种式(i)所示化合物的盐酸盐的i晶型,以衍射角2θ角度表示的x-射线粉末衍射图谱,在5.0、12.1、13.8、14.6、19.0、22.2处有特征峰;可选地,在5.0、10.9、12.1、12.4、13.8、14.6、17.6、18.3、19.0、22.2、24.3处有特征峰;可选地,在5.0、8.1、10.9、12.1、12.4、13.8、14.6、17.6、18.3、19.0、22.2、24.3、28.7处有特征峰。
5、一些实施方案中,本公开提供一种式(i)所示化合物的盐酸盐的ii晶型,以衍射角2θ角度表示的x-射线粉末衍射图谱,在5.0、11.3、13.6、14.2、18.3、25.4处有特征峰;可选地,在5.0、11.3、12.7、13.6、14.2、16.8、18.3、21.2、22.8、25.4处有特征峰;可选地,在5.0、11.3、12.7、13.6、14.2、15.6、16.8、18.3、19.6、21.2、22.0、22.8、24.2、25.4、28.7、31.1处有特征峰。
6、一些实施方案中,本公开提供一种式(i)所示化合物的硫酸盐的i晶型,以衍射角2θ角度表示的x-射线粉末衍射图谱,在10.1、12.0、15.3、16.1、17.0、24.7处有特征峰;可选地,在10.1、12.0、15.3、16.1、17.0、18.5、24.7、27.4、33.4处有特征峰;可选地,在10.1、12.0、15.3、16.1、17.0、18.5、20.0、20.8、23.1、24.7、27.4、30.2、32.1、33.4处有特征峰。
7、一些实施方案中,本公开提供一种式(i)所示化合物的磷酸盐的i晶型,以衍射角2θ角度表示的x-射线粉末衍射图谱,在9.8、12.0、13.7、17.6、18.9、22.4处有特征峰;可选地,在4.9、8.1、9.8、10.8、12.0、13.7、14.5、17.6、18.9、22.4、24.3处有特征峰;可选地,在4.9、8.1、9.8、10.8、12.0、13.7、14.5、17.6、18.1、18.9、22.4、23.4、24.3、28.6、29.2、31.7处有特征峰。
8、一些实施方案中,本公开提供一种式(i)所示化合物的磷酸盐的ii晶型,以衍射角2θ角度表示的x-射线粉末衍射图谱,在6.8、9.5、10.5、14.3、21.1处有特征峰;可选地,在6.8、9.5、10.5、13.7、14.3、15.5、19.1、20.7、21.1、22.5处有特征峰;可选地,在6.6、6.8、9.5、10.5、13.7、14.3、15.5、16.7、18.0、19.1、20.7、21.1、21.8、22.5、24.4、26.3、27.4处有特征峰。
9、一些实施方案中,本公开提供一种式(i)所示化合物的乙酸盐的i晶型,以衍射角2θ角度表示的x-射线粉末衍射图谱,在5.0、5.4、10.9、11.2、15.7处有特征峰;可选地,在5.0、5.4、10.9、11.2、12.2、15.3、15.7、22.2处有特征峰;可选地,在5.0、5.4、10.9、11.2、12.2、12.6、13.7、14.3、15.3、15.7、18.4、20.1、22.2、24.9处有特征峰。
10、一些实施方案中,本公开提供一种式(i)所示化合物的乙酸盐的ii晶型,以衍射角2θ角度表示的x-射线粉末衍射图谱,在5.2、6.3、11.3、16.4、18.3、22.9处有特征峰;可选地,在5.2、6.3、11.3、16.4、18.3、20.0、22.4、22.9、23.6、24.5处有特征峰;可选地,在5.2、6.3、11.3、12.8、14.0、15.2、15.6、16.4、18.3、20.0、22.4、22.9、23.6、24.5、26.3、28.1、28.8、29.9、32.0、34.1处有特征峰。
11、一些实施方案中,本公开提供一种式(i)所示化合物的乙酸盐的iii晶型,以衍射角2θ角度表示的x-射线粉末衍射图谱,在5.0、11.1、11.6、12.6、22.3、22.8处有特征峰;可选地,在5.0、11.1、11.6、12.6、13.6、18.6、19.0、22.3、22.8、23.6、29.0处有特征峰;可选地,在5.0、11.1、11.6、12.6、13.6、18.6、19.0、22.3、22.8、23.6、29.0、29.5、33.6、34.6处有特征峰。
12、一些实施方案中,本公开提供一种式(i)所示化合物的乙酸盐的iv晶型,以衍射角2θ角度表示的x-射线粉末衍射图谱,在5.7、10.9、11.2、12.3、22.6、23.4、28.7处有特征峰;可选地,在5.7、10.9、11.2、12.3、18.3、19.1、21.9、22.6、23.4、24.0、28.7处有特征峰;可选地,在5.7、10.9、11.2、12.3、13.4、14.9、15.1、15.9、18.3、19.1、19.9、21.9、22.6、23.4、24.0、28.7、29.9、33.1、33.7、34.1处有特征峰。
13、一些实施方案中,本公开提供一种式(i)所示化合物的酒石酸盐的i晶型,以衍射角2θ角度表示的x-射线粉末衍射图谱,在4.6、9.0、11.7、14.8处有特征峰;可选地,在4.6、9.0、10.9、11.7、14.8、18.4、22.7、24.8、28.8处有特征峰。
14、一些实施方案中,本公开提供一种式(i)所示化合物的酒石酸盐的ii晶型,以衍射角2θ角度表示的x-射线粉末衍射图谱,在5.0、10.0、12.1、15.0、19.1处有特征峰。
15、一些实施方案中,本公开提供一种式(i)所示化合物的马来酸盐的i晶型,以衍射角2θ角度表示的x-射线粉末衍射图谱,在4.8、9.6、11.7、14.2、18.6、22.4处有特征峰;可选地,在4.8、9.6、11.7、14.2、18.6、20.8、22.4、24.5、25.1、28.9处有特征峰。
16、一些实施方案中,本公开提供一种式(i)所示化合物的马来酸盐的ii晶型,以衍射角2θ角度表示的x-射线粉末衍射图谱,在4.4、8.8、13.3、14.3、18.0、22.6处有特征峰;可选地,在4.4、8.8、12.0、13.3、14.3、16.0、18.0、20.6、22.6、24.0、26.8、28.5处有特征峰,可选地,在4.4、8.8、11.5、12.0、13.3、14.3、16.0、18.0、19.3、20.6、22.6、23.1、24.0、24.7、25.7、26.8、28.5、28.8、34.4处有特征峰。
17、一些实施方案中,本公开提供一种式(i)所示化合物的苹果酸盐的i晶型,以衍射角2θ角度表示的x-射线粉末衍射图谱,在4.9、12.0、13.7、18.9、22.6、24.2处有特征峰;可选地,在4.9、9.8、12.0、13.7、14.6、18.9、22.2、22.6、24.2处有特征峰;可选地,在4.9、9.8、12.0、13.7、14.6、17.6、18.9、22.2、22.6、24.2、26.4、27.2、27.7、29.4、31.7处有特征峰。
18、一些实施方案中,本公开提供一种式(i)所示化合物的柠檬酸盐的i晶型,以衍射角2θ角度表示的x-射线粉末衍射图谱,在5.0、10.1、13.3、17.0、23.7处有特征峰;可选地,在5.0、10.1、11.3、13.3、15.0、17.0、18.6、22.3、23.7处有特征峰;可选地,在5.0、10.1、11.3、13.3、15.0、17.0、18.6、19.9、20.4、22.3、23.7、27.4、29.4、29.7处有特征峰。
19、一些实施方案中,本公开提供一种式(i)所示化合物的柠檬酸盐的ii晶型,以衍射角2θ角度表示的x-射线粉末衍射图谱,在5.0、10.1、12.5、14.5、17.2、22.8处有特征峰;可选地,在5.0、10.1、11.1、12.5、14.5、17.2、17.8、18.4、21.6、22.8、25.4、27.6处有特征峰;可选地,在5.0、10.1、11.1、12.5、14.5、17.2、17.8、18.4、19.6、20.5、21.6、22.8、25.4、27.6、28.6、29.2、29.6、30.9、32.1处有特征峰。
20、一些实施方案中,本公开提供一种式(i)所示化合物的柠檬酸盐的iii晶型,以衍射角2θ角度表示的x-射线粉末衍射图谱,在9.5、11.9、13.7、17.3、19.0、23.9处有特征峰;可选地,在9.5、11.9、13.7、17.3、19.0、21.3、22.7、23.9、26.2、27.4、29.3、30.8处有特征峰。
21、一些实施方案中,本公开提供一种式(i)所示化合物的甲磺酸盐的i晶型,以衍射角2θ角度表示的x-射线粉末衍射图谱,在10.3、12.5、16.2、17.5、21.1处有特征峰;可选地,在5.2、10.3、12.5、16.2、17.5、19.0、21.1、25.1处有特征峰;可选地,在5.2、10.3、12.5、16.2、17.5、19.0、19.9、21.1、22.9、25.1、29.9处有特征峰。
22、一些实施方案中,本公开提供一种式(i)所示化合物的甲磺酸盐的ii晶型,以衍射角2θ角度表示的x-射线粉末衍射图谱,在4.7、11.3、12.9、18.8、22.7、24.5处有特征峰;可选地,在4.7、8.2、11.3、12.9、13.7、16.2、16.8、18.8、19.7、22.7、24.5处有特征峰;可选地,在4.7、8.2、9.6、11.3、12.9、13.7、14.2、16.2、16.8、18.8、19.7、21.0、22.7、24.5、26.6、31.9处有特征峰。
23、一些实施方案中,本公开提供一种式(i)所示化合物的甲磺酸盐的iii晶型,以衍射角2θ角度表示的x-射线粉末衍射图谱,在5.6、11.8、15.4、18.8、24.1处有特征峰;可选地,在5.6、11.8、13.2、13.7、14.1、15.4、18.8、20.6、22.3、23.0、23.7、24.1、29.1处有特征峰。
24、一些实施方案中,本公开提供一种式(i)所示化合物的对甲苯磺酸盐的i晶型,以衍射角2θ角度表示的x-射线粉末衍射图谱,在8.1、9.2、11.4、13.7、15.8、22.1处有特征峰;可选地,在4.7、8.1、9.2、11.4、13.7、15.8、19.0、22.1、22.5、23.1、24.3、26.6处有特征峰;可选地,在4.7、8.1、9.2、11.4、13.7、15.8、16.7、18.0、18.4、19.0、19.8、22.1、22.5、23.1、24.3、26.6、27.9、29.5、31.4处有特征峰。
25、一些实施方案中,本公开提供一种式(i)所示化合物的富马酸盐的i晶型,以衍射角2θ角度表示的x-射线粉末衍射图谱,在9.7、12.0、14.6、19.0、22.0、24.2处有特征峰;可选地,在9.7、11.0、12.0、13.7、14.6、17.6、19.0、22.0、24.2处有特征峰。
26、一些实施方案中,本公开提供一种式(i)所示化合物的富马酸盐的ii晶型,以衍射角2θ角度表示的x-射线粉末衍射图谱,在5.0、11.3、14.3、16.6、18.3、22.3处有特征峰;可选地,在5.0、11.3、12.9、14.3、14.8、16.6、17.1、18.3、22.3、27.8、28.8处有特征峰;可选地,在5.0、11.3、12.9、14.3、14.8、16.6、17.1、18.3、20.5、21.2、22.3、25.0、26.0、27.8、28.8处有特征峰。
27、一些实施方案中,本公开提供一种式(i)所示化合物的琥珀酸盐的i晶型,以衍射角2θ角度表示的x-射线粉末衍射图谱,在5.0、9.5、11.7、17.6、22.8、24.4处有特征峰。
28、一些实施方案中,本公开提供一种式(i)所示化合物的琥珀酸盐的ii晶型,以衍射角2θ角度表示的x-射线粉末衍射图谱,在5.0、10.1、17.4、18.4、23.0、25.7处有特征峰;可选地,在5.0、10.1、11.1、12.7、14.5、17.4、18.4、20.5、23.0、23.4、25.7处有特征峰;可选地,在5.0、10.1、11.1、12.7、14.5、17.4、18.4、20.5、21.9、23.0、23.4、25.2、25.7、27.8、28.9、30.1、32.4、33.2、34.6处有特征峰。
29、一些实施方案中,本公开提供一种式(i)所示化合物的马尿酸盐的i晶型,以衍射角2θ角度表示的x-射线粉末衍射图谱,在14.0、17.8、21.9、23.5、28.0处有特征峰;可选地,在11.2、14.0、16.1、17.8、21.3、21.9、22.7、23.5、28.0处有特征峰;可选地,在11.2、12.3、12.9、14.0、16.1、17.8、20.3、21.3、21.9、22.7、23.5、23.9、24.3、25.2、28.0、28.6、30.6、31.0、32.8、34.0处有特征峰。
30、一些实施方案中,本公开提供一种式(i)所示化合物的马尿酸盐的ii晶型,以衍射角2θ角度表示的x-射线粉末衍射图谱,在8.9、11.6、13.8、22.7、23.4处有特征峰;可选地,在8.9、11.6、13.8、15.5、19.1、21.8、22.7、23.4、24.0、24.8、28.0处有特征峰;可选地,在5.5、8.9、11.6、13.8、15.5、16.8、18.1、19.1、21.8、22.7、23.4、24.0、24.8、25.9、26.6、28.0、29.5、30.4、32.9处有特征峰。
31、一些实施方案中,本公开提供一种式(i)所示化合物的氢溴酸盐的i晶型,以衍射角2θ角度表示的x-射线粉末衍射图谱,在11.2、16.8、18.6、23.8、26.1处有特征峰;可选地,在11.2、11.9、16.8、18.6、22.5、23.8、26.1、27.1处有特征峰;可选地,在10.1、11.2、11.9、13.6、15.7、16.8、18.6、22.5、23.8、26.1、27.1、27.4、28.5、29.6、31.7、33.0、34.1处有特征峰。
32、一些实施方案中,本公开提供一种式(i)所示化合物的氢溴酸盐的ii晶型,以衍射角2θ角度表示的x-射线粉末衍射图谱,在12.0、19.9、22.5、23.7、26.1处有特征峰;可选地,在12.0、17.0、18.9、19.9、22.5、23.7、24.3、26.1、28.5、31.5处有特征峰。
33、可选的实施方案中,本公开提供的式(i)所示化合物的可药用盐的晶型,其中,所述2θ角度的误差范围为±0.2。
34、本公开另一方面提供一种式(i)所示化合物的可药用盐或式(i)所示化合物的可药用盐的晶型的制备方法,包括式(i)所示化合物与酸反应的步骤,所述酸选自盐酸、硫酸、磷酸、乙酸、酒石酸、马来酸、苹果酸、柠檬酸、甲磺酸、对甲苯磺酸、富马酸、琥珀酸、马尿酸、氢溴酸。
35、本公开提供一种式(i)所示化合物盐酸盐i晶型的制备方法,包括:
36、方法一:
37、1)将式(i)所示化合物与溶剂a混合;
38、2)加入盐酸溶液;
39、析晶,收集固体;所述的溶剂a选自乙腈、丙酮、四氢呋喃中的至少一种。
40、方法二:
41、1)将式(i)所示化合物与甲醇混合,加入盐酸溶液;
42、2)加水析晶,收集固体。
43、本公开提供一种式(i)所示化合物硫酸盐i晶型的制备方法,包括:
44、方法一:
45、1)将式(i)所示化合物与溶剂a混合;
46、2)加入硫酸溶液;
47、析晶,收集固体;所述的溶剂a选自乙腈、丙酮、四氢呋喃的至少一种。
48、方法二:
49、1)将式(i)所示化合物与甲醇溶液混合,加入硫酸溶液
50、2)降温析晶,收集固体。
51、本公开提供一种式(i)所示化合物磷酸盐i晶型的制备方法,将式(i)所示化合物与甲醇溶液混合,加入磷酸溶液,析晶,收集固体。
52、本公开提供一种式(i)所示化合物磷酸盐ii晶型的制备方法,将式(i)所示化合物与溶剂a混合,加入磷酸溶液析晶,收集固体,所述溶剂a可选甲醇或四氢呋喃。
53、本公开提供一种式(i)所示化合物乙酸盐i晶型的制备方法,将式(i)所示化合物与丙酮混合,加入乙酸溶液,析晶,收集固体。
54、本公开提供一种式(i)所示化合物乙酸盐ii晶型的制备方法,将式(i)所示化合物与乙腈混合,加入乙酸溶液,析晶,收集固体。
55、本公开提供一种式(i)所示化合物乙酸盐iii晶型的制备方法,将式(i)所示化合物与四氢呋喃混合,加入乙酸溶液,析晶,收集固体。
56、本公开提供一种式(i)所示化合物乙酸盐iv晶型的制备方法,将式(i)所示化合物与四氢呋喃混合,加入乙酸溶液,析晶,干燥后收集固体。
57、本公开提供一种式(i)所示化合物酒石酸盐i晶型的制备方法,将式(i)所示化合物与甲醇混合,加入酒石酸溶液,析晶,收集固体。
58、本公开提供一种式(i)所示化合物酒石酸盐ii晶型的制备方法,将式(i)所示化合物与溶剂a混合,加入酒石酸溶液,析晶,收集固体,所述溶剂a可选甲醇或丙酮。
59、本公开提供一种式(i)所示化合物马来酸盐i晶型的制备方法,包括:
60、1)将式(i)所示化合物与溶剂a混合;
61、2)加入马来酸溶液;
62、析晶,收集固体;所述溶剂a选自丙酮、甲醇、乙腈、四氢呋喃的至少一种。
63、本公开提供一种式(i)所示化合物马来酸盐ii晶型的制备方法,将式(i)所示化合物与四氢呋喃混合,加入马来酸溶液,析晶,收集固体。
64、本公开提供一种式(i)所示化合物苹果酸盐i晶型的制备方法,包括:
65、1)将式(i)所示化合物与溶剂a混合;
66、2)加入苹果酸溶液;
67、析晶,收集固体;所述溶剂a为丙酮、乙腈、四氢呋喃中的至少一种。
68、本公开提供一种式(i)所示化合物柠檬酸盐i晶型的制备方法,将式(i)所示化合物与甲醇混合,加入柠檬酸溶液,析晶,收集固体。
69、本公开提供一种式(i)所示化合物柠檬酸盐ii晶型的制备方法,将式(i)所示化合物与甲醇混合,加入柠檬酸溶液,析晶,收集固体。
70、本公开提供一种式(i)所示化合物柠檬酸盐iii晶型的制备方法,将式(i)所示化合物与甲醇混合,加入柠檬酸溶液,析晶,收集固体。
71、本公开提供一种式(i)所示化合物甲磺酸盐i晶型的制备方法,包括:
72、1)将式(i)所示化合物与溶剂a混合;
73、2)加入甲磺酸溶液;
74、析晶,收集固体;所述溶剂a选自乙酸乙酯或乙腈的至少一种。
75、本公开提供一种式(i)所示化合物甲磺酸盐ii晶型的制备方法,将式(i)所示化合物与丙酮混合,加入甲磺酸溶液,析晶,收集固体。
76、本公开提供一种式(i)所示化合物甲磺酸盐iii晶型的制备方法,将式(i)所示化合物与丙酮混合,加入甲磺酸溶液,析晶,收集固体。
77、本公开提供一种式(i)所示化合物对甲苯磺酸盐i晶型的制备方法,包括:
78、1)将式(i)所示化合物与溶剂a混合;
79、3)加入对甲苯磺酸溶液;
80、析晶,收集固体;所述溶剂a选自乙酸乙酯、丙酮、乙腈、四氢呋喃中的至少一种。
81、本公开提供一种式(i)所示化合物富马酸盐i晶型的制备方法,将式(i)所示化合物与丙酮混合,加入富马酸,析晶,收集固体。
82、本公开提供一种式(i)所示化合物富马酸盐ii晶型的制备方法,将式(i)所示化合物与四氢呋喃混合,加入富马酸,析晶,收集固体。
83、本公开提供一种式(i)所示化合物琥珀酸盐i晶型的制备方法,将式(i)所示化合物与溶剂a混合,加入琥珀酸,析晶,收集固体,所述溶剂a选自乙腈或丙酮中的至少一种。
84、本公开提供一种式(i)所示化合物琥珀酸盐ii晶型的制备方法,将式(i)所示化合物与四氢呋喃混合,加入琥珀酸,析晶,收集固体。
85、本公开提供一种式(i)所示化合物马尿酸盐i晶型的制备方法,将式(i)所示化合物与溶剂a混合,加入马尿酸,析晶,收集固体,所述溶剂a选自甲基叔丁基醚或乙腈中的至少一种。
86、本公开提供一种式(i)所示化合物马尿酸盐ii晶型的制备方法,将式(i)所示化合物的马尿酸盐i晶型放置于92.5%rh 7天;或将式(i)所示化合物的马尿酸盐i晶型置于dvs后转晶,收集固体。
87、本公开提供一种式(i)所示化合物氢溴酸盐i晶型的制备方法,将式(i)所示化合物与溶剂a混合,加入氢溴酸溶液,析晶,收集固体,所述溶剂a选自四氢呋喃、乙醇、甲基叔丁基醚、丙酮中的至少一种。
88、本公开提供一种式(i)所示化合物氢溴酸盐ii晶型的制备方法,将式(i)所示化合物与四氢呋喃混合,加入氢溴酸溶液析晶,收集固体。
89、在某些实施方案中,本公开所述的晶型的制备方法还包括过滤、洗涤或干燥步骤。
90、本公开还提供了由前述式(i)所示化合物的晶型制备得到的药物组合物。
91、本公开还提供了一种药物组合物,含前述式(i)所示化合物的可药用盐、可药用盐的晶型或其混合物,或由前述方法制备得到的式(i)所示化合物的可药用盐、可药用盐的晶型,和任选自药学上可接受的赋形剂。
92、本公开还提供了一种药物组合物的制备方法,包括将前述式(i)所示化合物的可药用盐、可药用盐的晶型或其混合物,或由前述方法制备得到的式(i)所示化合物的可药用盐、可药用盐的晶型与药学上可接受的赋形剂混合的步骤。
93、本公开还提供了式(i)所示化合物的可药用盐、可药用盐的晶型或其混合物,或由前述方法制备得到的可药用盐、可药用盐的晶型或其混合物,或前述组合物,或由前述方法制备得到的组合物在制备治疗与shp2调节有关的疾病或病症的药物中的用途。
94、本公开还提供了式(i)所示化合物的可药用盐、可药用盐的晶型或其混合物,或由前述方法制备得到的可药用盐、可药用盐的晶型或其混合物,或前述组合物,或由前述方法制备得到的组合物在制备noonan综合征、豹综合症、少年骨髓单核细胞白血病(jmml)、神经母细胞瘤、黑素瘤、急性髓细胞性白血病(aml)、骨髓增生异常综合症(mds)、b细胞急性淋巴细胞性白血病(b-all)、乳腺癌、食道癌、肺癌、结肠癌、头癌、胃癌、头颈部鳞状细胞癌、间变性大细胞淋巴瘤和胶质母细胞瘤的药物中的用途。
95、本公开所述的“2θ或2θ角度”是指衍射角,θ为布拉格角,单位为°或度;每个特征峰2θ的误差范围为±0.20(包括超过1位小数的数字经过四舍五入后的情况),具体为-0.20、-0.19、-0.18、-0.17、-0.16、-0.15、-0.14、-0.13、-0.12、-0.11、-0.10、-0.09、-0.08、-0.07、-0.06、-0.05、-0.04、-0.03、-0.02、-0.01、0.00、0.01、0.02、0.03、0.04、0.05、0.06、0.07、0.08、0.09、0.10、0.11、0.12、0.13、0.14、0.15、0.16、0.17、0.18、0.19、0.20。
96、本公开所述的“结晶析出”或“析晶”包括但不限于搅拌结晶、打浆结晶、冷却结晶和挥发结晶。
97、本公开中所述的“差示扫描量热分析或dsc”是指在样品升温或恒温过程中,测量样品与参考物之间的温度差、热流差,以表征所有与热效应有关的物理变化和化学变化,得到样品的相变信息。
98、本公开中所述干燥温度一般为25℃-100℃,优选40℃-70℃,可以常压干燥,也可以减压干燥。
99、本公开中所述的“药学上可接受的赋形剂”包括但不限于任何已经被美国食品和药物管理局批准对于人类或家畜动物使用可接受的任何助剂、载体、助流剂、甜味剂、稀释剂、防腐剂、染料/着色剂、增香剂、表面活性剂、润湿剂、分散剂、助悬剂、稳定剂、等渗剂或乳化剂。
- 还没有人留言评论。精彩留言会获得点赞!