一种人诱导性多潜能干细胞诱导分化为多巴胺能神经元祖细胞的方法
本发明涉及干细胞诱导分化与移植治疗的,具体来说涉及一种人诱导性多潜能干细胞诱导分化为多巴胺能神经元祖细胞的方法。
背景技术:
1、帕金森病(parkinson’s disease,pd)是仅次于阿尔茨海默病的第二大常见的神经系统退行性疾病,全球65岁以上的老年群体中约有1~2%的个体为帕金森病患者,预计2030年患病比例会达到现在的一倍之多。其主要的病理改变是因中脑黑质-纹状体通路的多巴胺能神经元(dans)变性大量死亡,导致脑内多巴胺合成减少,而引起的一系列神经功能障碍,现已成为神经系统疾病治疗的热点之一。目前针对pd的主要治疗方法,包括l-左旋多巴(l-dopa)等药物治疗或深部脑刺激等手术治疗,侧重于减轻症状,不能使受损的神经元再生,无法从根本上治疗帕金森病。
2、近年来,通过细胞移植替代损失的多巴胺神经元(da神经元)以恢复神经传递,保护残留的da神经元,成为治疗pd的重要手段。从人类腹侧中脑(vm)中分离出的da能神经元祖细胞可以在pd患者脑内存活并发挥修复作用。但人类胎儿vm组织细胞数量有限,阻碍了其临床应用。因此,寻找一种获得多巴胺能神经元祖细胞的方法至关重要。
技术实现思路
1、为解决上述技术问题,本发明提供了一种人诱导性多潜能干细胞诱导分化为多巴胺能神经元祖细胞的方法,得到的多巴胺能神经元祖细胞在帕金森大鼠脑微环境中可长期存活,并对大鼠运动功能障碍具有明显的修复效应,为治疗相关神经退行性疾病提供了事实依据和理论基础。
2、本发明的第一个目的是提供了一种诱导多能干细胞分化为多巴胺能神经元祖细胞的方法,包括如下步骤:
3、s1,人诱导性多潜能干细胞的体外培养:复苏人诱导多能干细胞系并进行体外培养;
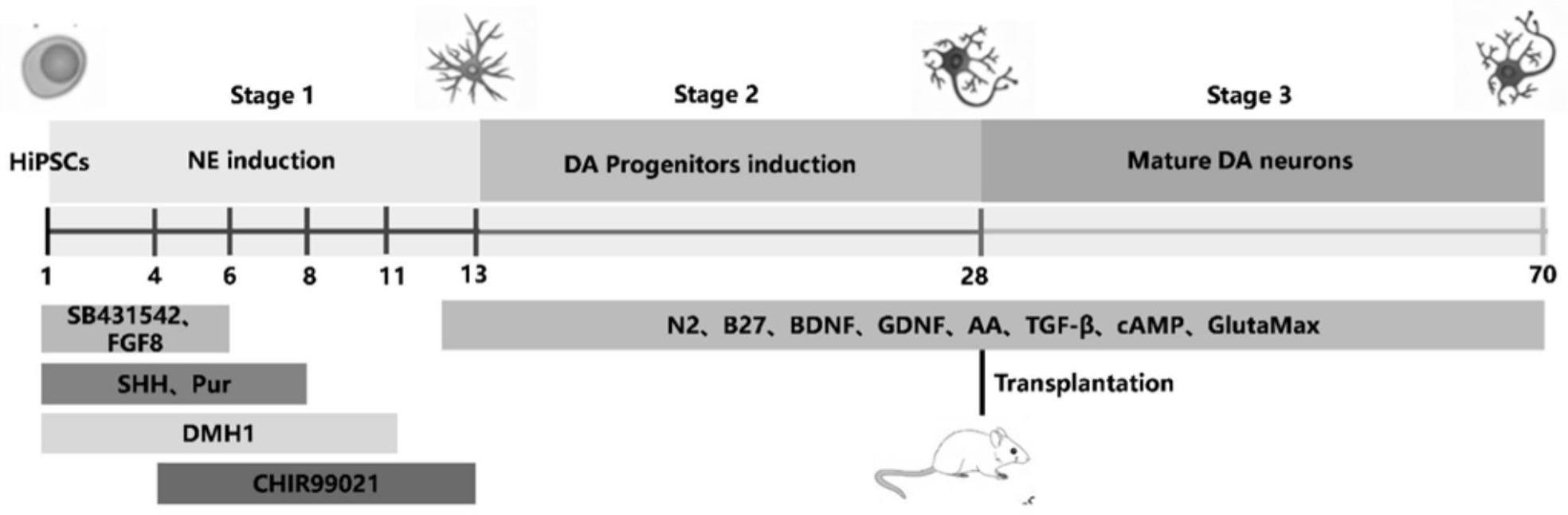
4、s2,人诱导性多潜能干细胞在添加剂sb431542、dmh1、shh、fgf8b、purmorphamine及chir99021的作用下诱导分化为原始神经上皮细胞;
5、s3,利用添加剂bdnf、gdnf、aa、n2、b27、camp及glutamax对中间态细胞原始神经上皮细胞进行持续诱导分化,获得多巴胺能神经元祖细胞。
6、进一步地,s1中,培养过程为:细胞接种于mtesrtm basal medium培养基,加入y27632使其终浓度为10μm,次日弃除旧培养基,更换为新的mtesrtm basal medium培养基培养,每2天更换一次培养液,更换2次后可进行传代。
7、进一步地,s2中,具体诱导分化过程为:s1中培养获得的人诱导性多潜能干细胞克隆增殖至融合度为30%后,在添加10mm dmh1、10mm sb431542、shh、fgf8b、purmorphamine的mtesrtm basal medium上培养至第3天,继续添加chir99021培养至第5天,然后将培养基更换为神经诱导培养基nim培养至第7天,然后去除shh和purmorphamine培养至第11天,更换为神经分化培养基nem培养至第13天,获得原始神经上皮细胞;
8、所述神经诱导培养基nim为dmem/f12培养基添加1%n2、10mm dmh1、200ng/mlshh、2μm purmorphamine、3μm chir99021。
9、进一步地,s2中,所述神经分化培养基nem为neurobasal medium添加1%n2、2%b27(不添加维生素a)、10ng/ml bdnf、10ng/ml gdnf、200μm aa、tgf-β、1μm camp、1%glutamax和3μm chir99021。
10、进一步地,s3中,具体诱导分化过程为:在获得的原始神经上皮细胞中加入iv型胶原酶进行消化,然后弃去ⅳ型胶原酶,收集细胞,采用neurobasal medium培养液贴壁培养至第28天,获得多巴胺能神经元祖细胞;
11、所述neurobasal medium培养液为neurobasal medium添加1%n2、2%b27、10ng/ml bdnf、10ng/ml gdnf、200μm aa、1ng/ml tgf-β、1μm camp、1%glutamax。
12、进一步地,s3中,消化条件为:5%co2,37℃,消化30s。
13、进一步地,s3中,贴壁培养前吹打成单细胞。
14、进一步地,s3中,加入的iv型胶原酶的量为700μl。
15、进一步地,s3中,贴壁培养过程中,每2天更换一次新鲜的培养液。
16、进一步地,s1-s3中,所有的培养基和添加剂均为临床级别的。
17、与现有技术相比,本发明的有益效果在于:
18、1、本发明在第一阶段将sb431542、dmh1、shh、fgf8b、purmorphamine及chir99021诱导12天产生中间态细胞,降低了因多能性被激活而出现致瘤性的风险;第二阶段对中间态细胞进行诱导直至第28天即可得到高纯度的多巴胺能神经元祖细胞(93.3-96.7%)。
19、2、本发明采用双重smad抑制(暴露于dmh1和sb431542),并将处理时间缩短为6天增强ipscs向中脑daps的分化。选择性骨形态发生蛋白(bmp)抑制剂dmh1替换了ldn193189,一方面可以显著降低表达多能性标记蛋白oct4和nanog的细胞百分比,从而降低了细胞因多能性被激活而出现致瘤性的风险,另一方面能够显著提高神经祖细胞标记pax6表达,促进向神经祖细胞转换;sb431542是tgf-β/smad通路抑制剂,可有效抑制由tgfβ1诱导的细胞迁移和侵袭的进程,并促进sox2和myc依赖的功能来促进重编程。
20、3、与传统的2d单层培养方法相比,我们改进的方法更为有效,通过purmorphamine激活sonic hedgehog(shh)信号通路特异分化为底板细胞和chir99021(gsk3抑制剂)激活wnt通路促进中脑细胞分化,诱导生成daps比例更高,产量更高(th+、foxa2+、lmx1a+和nurr1+细胞占93.3%-96.7%),显著高于目前同类研究85%左右的foxa2+/tuj1+阳性细胞率。
21、值得注意的是,在诱导的第一阶段,chir99021通过抑制gsk3-β激活β-catenin/c-jun/wnt信号通路,是诱导lmx1a共表达的关键因素,促进ipsc衍生的中脑向da神经元命运的神经源性转化。而且,purmorphamine作为shh受体激动剂,其与重组shh组合强烈激活sonic hedgehog(shh)信号通路,诱导foxa2/lmx1a的共表达,并改善mda神经元生存。fgf8是产生多巴胺神经元的必要条件,可改善mda神经元的分布,减少了丘脑下核神经元的数量。bdnf通过激活wnt/β-连环蛋白和erk5信号通路来促进ipscs分化为神经前体细胞,进而分化为成熟神经元。camp可上调th合成,促进神经元分化/存活。tgf-β促进神经突生长和神经元存活。另外双重smad抑制也确保产生foxa2/lmx1a1表达的daps细胞。
22、4、本发明提供的将人诱导性多潜能干细胞高效分化为中脑多巴胺能神经元祖细胞的方法可以得到中脑多巴胺能神经元祖细胞,为神经元损伤缺失后的补充来源提供了保障,也为用干细胞移植治疗神经退行性疾病,如帕金森病、阿尔茨海默疾病等疾病奠定了基础。
23、5、本发明通过脑切片he染色、免疫组化法检测酪氨酸羟化酶表达,有效验证了移植的多巴胺能神经元祖细胞在宿主脑内存活、迁移和分化;使用阿扑吗啡诱导旋转实验、旷场实验、水迷宫实验和疲劳转棒实验,有效表明移植的多巴胺能神经元祖细胞对帕金森病大鼠具有显著疗效。利用本发明提供的方法得到的多巴胺能神经元祖细胞在帕金森大鼠脑微环境中可长期存活,并对大鼠运动功能障碍具有明显的修复效应,为用干细胞移植治疗如帕金森病和阿尔茨海默症等神经退行性疾病奠定了基础。
- 还没有人留言评论。精彩留言会获得点赞!