一种用于食管鳞状细胞癌及癌前病变的诊断或辅助诊断的试剂及检测试剂盒的制作方法
1.本发明属于生物医药技术领域,更具体地,涉及一种用于食管鳞状细胞癌及癌前病变的诊断或辅助诊断的试剂及检测试剂盒。
背景技术:
2.食管鳞状细胞癌(escc)是食管恶性肿瘤的两种主要亚型之一,是由于食管上皮细胞的恶性转化而发生的,多发于老年人,同时已知其发病与饮食生活习惯密切相关,包括烫食、热茶、饮酒、吸烟等,此外还包括食品霉变、炭烤或烟熏制备方式、饮用水、土壤成分或环境微生物菌群等因素。中国部分地区位于“食管癌带”,escc患者通常表现为吞咽困难和体重减轻,出现相应症状时通常处于疾病晚期,所以针对食管鳞癌的早诊早治是非常必要的。
3.目前escc的主要检查方式有三种:
4.1、内镜检查
5.内镜检查是通过电子镜头或内窥镜对消化器官黏膜进行直接检查,可直观了解病灶部位、大小、扩散情况、表面形状、病灶数量、颜色、浸润深度等。缺点在于,内镜具有侵入性,患者依从性低。
6.2、食道x线钡餐检查
7.食道x线钡餐检查即消化道钡剂造影,是指用硫酸钡作为造影剂,在x线照射下显示消化道有无病变的一种检查方法。食管癌早期的病人,可以见到食管黏膜皱襞的紊乱、粗糙、中断的现象,以及小的充盈缺损,还有局限性的管壁僵硬、蠕动中断,而且伴有小的龛影。除具有一定的放射性外,x线钡餐检查结果仅能作为诊断参考,不能直接判断是否为癌。
8.3、鳞状细胞癌抗原检测
9.鳞状细胞癌抗原(scc),是多年前日本研究人员发现的一种肿瘤标志物,是从子宫颈鳞状上皮中分离出来的鳞状上皮细胞相关抗原ta-4的亚单位,是一种糖蛋白。多数研究显示,scc与鳞状细胞癌的侵袭、转移、复发和预后密切相关,是反映鳞状细胞癌生物学特性的重要标志物。当恶性肿瘤发生的时候,scc可通过细胞增殖后释放入血,使得血清中scc浓度增高。然而,scc检测可检测多种鳞状细胞癌,例如:肺癌,头颈鳞癌,宫颈上皮癌等,不具备检测食管鳞癌的单一性;同时,术前麻醉等影响会使scc检测值升高,使得scc检测的准确度有待商榷。
10.近年来分子生物学方面的进展为开发简便、有效的早期诊断方法提供了新的方向,食管癌组织中存在多基因、多位点的甲基化,并且在食管癌发生的早期即出现dna甲基化的改变,因此,甲基化改变有望作为食管癌早期诊断的标志物,从dna甲基化角度探索食管鳞癌诊断策略已成为一种新的思路。
11.一般而言,与癌症相关的dna甲基化改变指的是cpg二核苷酸位点的甲基化改变,值得注意的是,尽管cpg岛内包含多个cpg二核苷酸位点,但并非每个位点都与癌症的发生发展有同等的相关性。现有技术中以某基因的dna甲基化水平作为疾病诊断依据时,通常以
基因整体作为靶序列,但这种情况下靶序列中的cpg岛较长,且与疾病的相关性存在差异,导致检测的特异性及灵敏度降低。此外,研究表明,在常规cpg岛区域以外也仍然存在一些cpg位点与疾病的发生呈现强关联性。因此,在开发癌症检测标记物时,需要找到灵敏性和特异性均较好的cpg位点。
12.食管上皮内瘤变(低级别)是指食管黏膜轻度结构紊乱的形态学表现,是食管在炎症等刺激下出现的异常增生,暂时属于良性病变,属于癌前病变,通过检测食管上皮内瘤变(低级别)的甲基化水平,能够有效提高食管癌癌前病变的检出率。现有技术公开了一些用于dna甲基化检测的试剂及食管癌检测试剂盒,对食管癌与非癌的检测具有良好的灵敏性和特异性,但是对于食管癌的瘤前病变,包括食管上皮内瘤变(高级别)和食管上皮内瘤变(低级别),尤其是对食管上皮内瘤变(低级别)的检测灵敏度和检出率偏低。
技术实现要素:
13.针对现有技术的缺陷,本发明的目的在于提供了一种用于食管鳞状细胞癌及癌前病变诊断或辅助诊断的试剂及检测试剂盒,以解决现有技术对食管癌及癌前病变的检出率低、检测的灵敏度欠佳等的技术问题,尤其适用于食管鳞状细胞癌的癌前瘤变的高灵敏度检测。
14.为实现上述目的,本发明提供了一种用于食管鳞状细胞癌及癌前病变诊断或辅助诊断的试剂,包括用于检测生物样本中目标区域甲基化水平的试剂,其中所述目标区域选自如下至少一种目标区域中的全长区域或部分区域:目标区域(a)、目标区域(b)、目标区域(c)、目标区域(d)和目标区域(e);
15.以grch38.p14为参考基因组,所述目标区域(a)选自chr10:101121016-101121513;所述目标区域(b)选自chr12:121580936-121581260;所述目标区域(c)选自chr19:10580847-10581279;所述目标区域(d)选自chr17:9576547-9576756;所述目标区域(e)选自chr11:22829210-22829426。
16.优选地,所述部分区域选自如下至少一种所述目标区域中的任一或多个特定区域:
17.所述目标区域(a)的特定区域包括特定区域1和特定区域2,其中所述特定区域1选自chr10:101121016-101121202正链,所述特定区域2选自chr10:101121313-101121513正链;
18.所述目标区域(b)的特定区域包括特定区域3和特定区域4,其中特定区域3选自chr12:121581057-121581260正链,特定区域4选自chr12:121580936-121581114负链;
19.所述目标区域(c)的特定区域包括特定区域5、特定区域6和特定区域7,其中特定区域5选自chr19:10580847-10581034正链,特定区域6选自chr19:10581089-10581279正链,特定区域7选自chr19:10581005-10581188负链;
20.所述目标区域(d)的特定区域包括特定区域8、特定区域9和特定区域10,其中特定区域8选自chr17:9576553-9576728正链,特定区域9选自chr17:9576547-9576670正链,特定区域10选自chr17:9576593-9576756负链;
21.所述目标区域(e)的特定区域包括特定区域11、特定区域12和特定区域13,其中特定区域11选自chr11:22829233-22829426正链,特定区域12选自chr11:22829210-22829377
正链,特定区域13选自chr11:22829220-22829426正链。
22.优选地,所述试剂包括能够扩增所述特定区域的引物对以及所述引物对对应的探针。
23.进一步优选地,所述引物对以及所述引物对对应的探针选自如下至少一种:所述特定区域1对应的seq id no.27和seq id no.28所示的引物对,以及seq id no.29所示的探针;所述特定区域2对应的seq id no.30和seq id no.31所示的引物对,以及seq id no.32所示的探针;所述特定区域3对应的seq id no.33和seq id no.34所示的引物对,以及seq id no.35所示的探针;所述特定区域4对应的seq id no.36和seq idno.37所示的引物对,以及seq id no.38所示的探针;所述特定区域5对应的seq idno.39和seq id no.40所示的引物对,以及seq id no.41所示的探针;所述特定区域6对应的seq id no.42和seq id no.43所示的引物对,以及seq id no.44所示的探针;所述特定区域7对应的seq id no.45和seq id no.46所示的引物对,以及seq id no.47所示的探针;所述特定区域8对应的seq id no.48和seq id no.49所示的引物对,以及seq id no.50所示的探针;所述特定区域9对应的seq id no.51和seq id no.52所示的引物对,以及seq id no.53所示的探针;所述特定区域10对应的seq id no.54和seq id no.55所示的引物对,以及seq id no.56所示的探针;所述特定区域11对应的seq id no.57和seq id no.58所示的引物对,以及seq id no.59所示的探针;所述特定区域12对应的seq id no.60和seq id no.61所示的引物对,以及seq id no.62所示的探针;所述特定区域13对应的seq id no.63和seq id no.64所示的引物对,以及seq id no.65所示的探针。
24.优选地,所述试剂还包括能够差异修饰甲基化dna和非甲基化dna的反应试剂;进一步优选地,所述反应试剂为亚硫酸氢盐。
25.优选地,所述生物样本为血液样本、唾液样本、组织样本或食管来源的细胞样本;所述生物样本为来源于哺乳动物的离体生物样本。
26.按照本发明的另一个方面,提供了一种用于食管鳞状细胞癌及癌前病变诊断或辅助诊断的检测试剂盒,所述检测试剂盒包括所述的试剂。
27.按照本发明的另一个方面,提供了所述试剂或所述的检测试剂盒在制备食管鳞状细胞癌及癌前病变的诊断或辅助诊断产品中的用途。
28.总体而言,通过本发明所构思的以上技术方案与现有技术相比,具有以下有益效果:
29.(1)本发明提供的一种用于食管鳞状细胞癌及癌前病变的诊断或辅助诊断的试剂,通过检测目标区域的全长区域或部分区域的核苷酸序列的dna甲基化水平,可以对食管鳞状细胞癌进行特异性诊断及辅助诊断,可用于食管鳞癌患者,包括食管鳞状细胞癌、食管上皮内瘤变(高级别)、食管上皮内瘤变(低级别),对食管鳞癌及癌前病变的组织样本均具有较高的诊断灵敏度和特异性。
30.(2)本发明提供的一种用于食管鳞状细胞癌及癌前病变的诊断或辅助诊断的试剂,通过检测目标区域的特定区域的核苷酸序列的dna甲基化水平,相对于现有技术显著提高了食管上皮内瘤变(高级别)和食管上皮内瘤变(低级别)的检测灵敏度和检出率,可以用于食管鳞状细胞癌的早期筛查,对于早日治疗介入及改善患者预后具有重要意义。本发明通过检测目标区域(a)-(e)的单一特定区域的甲基化水平,对食管上皮内瘤变(低级别)的
检测灵敏度可达77%,通过检测任意两个目标区域(a)-(e)的组合特定区域的甲基化水平,对食管上皮内瘤变(低级别)的检测灵敏度可达81%。
31.(3)本发明所述试剂盒包括能够扩增所述目标区域的特定区域的引物对以及所述引物对对应的探针,能够检测特定区域的胞嘧啶的甲基化水平。本发明提供的检测试剂盒可用于不同阶段的食管鳞状细胞癌患者的诊断及辅助诊断,其中对食管癌癌前病变包括食管上皮内瘤变(低级别)具有较高的检测灵敏度。本发明所述试剂盒以所述目标区域(a)-(e)的特定区域作为食管鳞状细胞癌检测诊断的标志物,在食管鳞状细胞癌检测诊断或辅助诊断中作为目标序列,具有较高的诊断灵敏度和特异性。
32.综上所述,本发明提供的试剂及检测试剂盒均可用于不同阶段的食管鳞状细胞癌患者的诊断及辅助诊断,其中对食管上皮内瘤变(低级别)具有较高的检测灵敏度,提高了食管上皮内瘤变(低级别)的检出率,对食管鳞状细胞癌的早期筛查,尤其是癌前病变的早期筛查具有重要意义。
具体实施方式
33.为了使本发明的目的、技术方案及优点更加清楚明白,以下结合实施例,对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅仅用以解释本发明,并不用于限定本发明。
34.除非另有定义,本文所使用的所有的技术和科学术语与属于本发明的技术领域的技术人员通常理解的含义相同。本文中在本发明的说明书中所使用的术语只是为了描述具体的实施例的目的,不是旨在于限制本发明。
35.本发明使用术语“至少一种”、“及/或”或“和/或”均是指包括一个或多个相关的所列项目的任意的和所有的组合。
36.术语“诊断”包括辅助诊断、复发风险评估、癌变风险和癌变程度的评估、预后判断等方面。
37.术语“基因”是指编码产生氨基酸多肽链的dna区段,它包括参与基因转录/翻译和转录/翻译调控的位于编码区和非编码区的序列,以及外显子和内含子序列。
38.术语“寡核苷酸”或“多核苷酸”或“核苷酸”或“核酸”是指具有两个或更多个脱氧核糖核苷酸或核糖核苷酸的分子,优选多于三个,并且通常多于十个。确切的大小将取决于许多因素,而所述因素又取决于寡核苷酸的最终功能或用途。寡核苷酸可以任何方式产生,包括化学合成、dna复制、逆转录或其组合。dna的典型脱氧核糖核苷酸是胸腺嘧啶、腺嘌呤、胞嘧啶和鸟嘌呤。rna的典型核糖核苷酸是尿嘧啶、腺嘌呤、胞嘧啶和鸟嘌呤。
39.术语“甲基化”为dna化学修饰的一种形式,能够在不改变dna序列的前提下,改变遗传表现。dna甲基化是指在dna甲基转移酶的作用下,在基因组cpg二核苷酸的胞嘧啶第5号碳位共价结合一个甲基基团。dna甲基化能引起染色质结构、dna构象、dna稳定性及dna与蛋白质相互作用方式的改变,从而控制基因表达。
40.术语“甲基化水平”指的是一段dna序列中一个或多个cpg二核苷酸中的胞嘧啶是否发生甲基化、或发生甲基化的频率/比例/百分数,既代笔定性的概念又代表定量的概念。在实际应用中,可根据实际情况采用不同的检测指标比较dna甲基化水平。如在一些情况下,可根据样本检测的ct值进行比较;在一些情况下,可计算样本中基因甲基化的比例,即
甲基化分子数/(甲基化分子数+非甲基化分子数)
×
100,然后再进行比较;在一些情况下,还需要对各个指标进行统计学上的分析整合,得出最终的判定指标。
41.术语“引物”是指可以用在扩增方法(例如聚合酶链式反应pcr)中,基于与目标基因或其一部分区域相对应的多核苷酸序列来扩增目的序列的寡核苷酸。通常,用于扩增多核苷酸序列的pcr引物中的至少一个对于该多核苷酸序列是序列特异性的。引物的确切长度取决于很多因素,包括温度、引物来源以及所用方法等。例如,对于诊断和预后应用,根据靶序列的复杂度,寡核苷酸引物通常含有至少10、15、20、25或更多个核苷酸,但是也可以含有更少的核苷酸。在本发明公开内容中,术语“引物”是指能与目标dna分子的双链杂交或能与目标dna分子中位于待扩增核苷酸序列两翼的区域杂交的一对引物。
42.本发明提供了一种用于食管鳞状细胞癌及癌前病变诊断或辅助诊断的试剂,包括能够特异性检测生物样本中目标区域的甲基化水平的试剂,其中所述目标区域选自如下至少一种目标区域中的全长区域或部分区域:目标区域(a)、目标区域(b)、目标区域(c)、目标区域(d)和目标区域(e);
43.所述目标区域(a)选自chr10:101121016-101121513;所述目标区域(b)选自chr12:121580936-121581260;所述目标区域(c)选自chr19:10580847-10581279;所述目标区域(d)选自chr17:9576547-9576756;所述目标区域(e)选自chr11:22829210-22829426,区域所在位置参考的人类基因组的版本号为grch38.p14。
44.可以理解,上述目标区域的部分区域是指相应目标区域中的一个特定区域,该部分区域至少包括一个cpg二核苷酸位点。
45.一些实施例中,所述部分区域选自如下至少一种所述目标区域(a)-(e)的特定区域,所述目标区域(a)的特定区域包括但不限于特定区域1、特定区域2,其中特定区域1选自chr10:101121016-101121202正链,特定区域2选自chr10:101121313-101121513正链;
46.所述目标区域(b)的特定区域包括但不限于特定区域3、特定区域4,其中特定区域3选自chr12:121581057-121581260正链,特定区域4选自chr12:121580936-121581114负链。
47.所述目标区域(c)的特定区域包括但不限于特定区域5、特定区域6、特定区域7,其中特定区域5选自chr19:10580847-10581034正链,特定区域6选自chr19:10581089-10581279正链,特定区域7选自chr19:10581005-10581188负链。
48.所述目标区域(d)的特定区域包括但不限于特定区域8、特定区域9、特定区域10,其中特定区域8选自chr17:9576553-9576728正链,特定区域9选自chr17:9576547-9576670正链,特定区域10选自chr17:9576593-9576756负链。
49.所述目标区域(e)的特定区域包括但不限于特定区域11、特定区域12、特定区域13,其中特定区域11选自chr11:22829233-22829426正链,特定区域12选自chr11:22829210-22829377正链,特定区域13选自chr11:22829220-22829426正链。
50.发明人研究发现:目标区域(a)-(e)的特定区域的甲基化水平在食管鳞状细胞癌样本中的甲基化水平显著高于正常样本,通过检测上述目标区域(a)-(e)的特定区域的甲基化水平,可以为受试者(对象)是否存在食管鳞状细胞癌的风险或者是否存在食管鳞状细胞癌早期病变、或者是否已经发生食管鳞状细胞癌病变提供参考,为食管鳞状细胞癌及癌前病变的诊断或辅助诊断提供参考。
51.本发明较佳的目标区域的部分区域为特定区域1、特定区域2、特定区域4、特定区域6、特定区域7、特定区域9、特定区域10和特定区域11中的至少一者。实验中将本发明目标区域的特定区域进行两两组合或多个组合作为甲基化标志物进行检测时,实验发现将本发明特定区域进行组合检测食管鳞癌患者及癌前病变患者生物样本的灵敏度均高于单特定区域的检测结果。较佳的特定区域组合为特定区域1、特定区域2、特定区域4、特定区域6、特定区域9和特定区域11中任意两者的组合,包括但不限于特定区域1和特定区域4的组合、特定区域1和特定区域6的组合、特定区域1和特定区域9的组合、特定区域1和特定区域11的组合、特定区域4和特定区域6的组合、特定区域4和特定区域9的组合、特定区域4和特定区域11的组合、特定区域6和特定区域9的组合、特定区域6和特定区域11的组合以及特定区域9和特定区域11的组合。更佳实施例中,组合特定区域包括但不限于特定区域1和特定区域4的组合、特定区域4和特定区域9的组合、特定区域4和特定区域11的组合以及特定区域9和特定区域11的组合。
52.一些实施例中,所述特定区域1的核苷酸序列为seq id no.1,所述特定区域2的核苷酸序列为seq id no.3,所述特定区域3的核苷酸序列为seq id no.5,所述特定区域4的核苷酸序列为seq id no.7,特定所述区域5的核苷酸序列为seq id no.9,特定所述区域6的核苷酸序列为seq id no.11,所述特定区域7的核苷酸序列为seq idno.13,所述特定区域8的核苷酸序列为seq id no.15,所述特定区域9的核苷酸序列为seq id no.17,所述特定区域10的核苷酸序列为seq id no.19,所述特定区域11的核苷酸序列为seq id no.21,所述特定区域12的核苷酸序列为seq id no.23,所述特定区域13的核苷酸序列为seq id no.25。
53.本领域技术人员可以理解,由于个体差异的不同,在同一染色体的相同区域,基因的碱基序列可能存在细微差别。因此,与目标区域(a)-(e)的特定区域所示的核苷酸序列、或其互补序列、或前述两者的部分区域存在不同位点,但具有较高同一性的序列仍可作为本发明中dna甲基化检测的目标序列。
54.所述试剂可采用本领域已知的方法检测上述目标区域(a)-(e)的特定区域核苷酸序列的dna甲基化水平,包括甲基化特异性pcr、定量甲基化特异性pcr、亚硫酸氢盐测序法、甲基化特异性微阵列法、全基因组甲基化测序法、焦磷酸测序法、甲基化特异性高效液相层析法、数字pcr法、甲基化特异性高分辨率溶解曲线法、甲基化敏感性限制性内切酶法和荧光定量法。本领域技术人员可根据已知方法所需的试剂和工具确定并制备所述检测试剂。
55.一些实施例中,所述检测试剂包括如下至少一种能够扩增所述目标区域(a)-(e)的特定区域的引物对以及所述引物对对应的探针:所述特定区域1对应的seq id no.27和seq id no.28所示的引物对,以及seq id no.29所示的探针;所述特定区域2对应的seq id no.30和seq id no.31所示的引物对,以及seq id no.32所示的探针;所述特定区域3对应的seq id no.33和seq id no.34所示的引物对,以及seq id no.35所示的探针;所述特定区域4对应的seq id no.36和seq id no.37所示的引物对,以及seq id no.38所示的探针;所述特定区域5对应的seq id no.39和seq id no.40所示的引物对,以及seq id no.41所示的探针;所述特定区域6对应的seq id no.42和seq idno.43所示的引物对,以及seq id no.44所示的探针;所述特定区域7对应的seq idno.45和seq id no.46所示的引物对,以及seq id no.47所示的探针;所述特定区域8对应的seq id no.48和seq id no.49所示的引
物对,以及seq id no.50所示的探针;所述特定区域9对应的seq id no.51和seq id no.52所示的引物对,以及seq id no.53所示的探针;所述特定区域10对应的seq id no.54和seq id no.55所示的引物对,以及seq id no.56所示的探针;所述特定区域11对应的seq id no.57和seq id no.58所示的引物对,以及seq id no.59所示的探针;所述特定区域12对应的seq id no.60和seq id no.61所示的引物对,以及seq id no.62所示的探针;所述特定区域13对应的seq id no.63和seq id no.64所示的引物对,以及seq id no.65所示的探针。本技术中,所述试剂所包括的引物对及探针没有特别的限定,本领域技术人员在确定目标区域(a)-(e)的特定区域的核苷酸序列作为目标序列之后,可根据本领域已知的方法和工具设计特异性引物对及探针,只要可以实现检测特定cpg位点是否发生甲基化的目的即可。
56.本发明所述试剂能够检测所述特定区域中一个或多个胞嘧啶的甲基化,一些实施例中,本发明所述试剂能够检测特定区域1正链上的chr10:101121016、chr10:101121056、chr10:101121076、chr10:101121185和chr10:101121194至少一个位置上的胞嘧啶的甲基化。
57.一些实施例中,本发明所述试剂能够检测特定区域2正链上的chr10:101121313、chr10:101121325、chr10:101121328、chr10:101121331、chr10:101121357、chr10:101121496、chr10:101121498和chr10:101121507至少一个位置上的胞嘧啶的甲基化。
58.一些实施例中,本发明所述试剂能够检测特定区域3正链上的chr12:121581057、chr12:121581067、chr12:121581074、chr12:121581171、chr12:121581175、chr12:121581241、chr12:121581248和chr12:121581258至少一个位置上的胞嘧啶的甲基化。
59.一些实施例中,本发明所述试剂能够检测特定区域4负链上的chr12:121580952、chr12:121580994、chr12:121581058、chr12:121581068和chr12:121581075至少一个位置上的胞嘧啶的甲基化。
60.一些实施例中,本发明所述试剂能够检测特定区域5正链上的chr19:10580847、chr19:10580941、chr19:10581022和chr19:10581024至少一个位置上的胞嘧啶的甲基化。
61.一些实施例中,本发明所述试剂能够检测特定区域6正链上的chr19:10581089、chr19:10581160、chr19:10581164、chr19:10581265和chr19:10581278至少一个位置上的胞嘧啶的甲基化。
62.一些实施例中,本发明所述试剂能够检测特定区域7负链上的chr19:10581023、chr19:10581025、chr19:10581090、chr19:10581165、chr19:10581179和chr19:10581186至少一个位置上的胞嘧啶的甲基化。
63.一些实施例中,本发明所述试剂能够检测特定区域8正链上的chr17:9576569、chr17:9576575、chr17:9576593、chr17:9576595、chr17:9576599、chr17:9576712和chr17:9576715至少一个位置上的胞嘧啶的甲基化。
64.一些实施例中,本发明所述试剂能够检测特定区域9正链上的chr17:9576569、chr17:9576612、chr17:9576618、chr17:9576622、chr17:9576626和chr17:9576648至少一个位置上的胞嘧啶的甲基化。
65.一些实施例中,本发明所述试剂能够检测特定区域10负链上的chr17:9576594、chr17:9576596、chr17:9576600、chr17:9576613、chr17:9576619、chr17:9576623、chr17:
9576627、chr17:9576638、chr17:9576747、chr17:9576750和chr17:9576756至少一个位置上的胞嘧啶的甲基化。
66.一些实施例中,本发明所述试剂能够检测特定区域11正链上的chr11:22829234、chr11:22829242、chr11:22829250、chr11:22829305、chr11:22829320、chr11:22829406、chr11:22829421和chr11:22829424至少一个位置上的胞嘧啶的甲基化。
67.一些实施例中,本发明所述试剂能够检测特定区域12正链上的chr11:22829220、chr11:22829232、chr11:22829234、chr11:22829340、chr11:22829342和chr11:22829368至少一个位置上的胞嘧啶的甲基化。
68.一些实施例中,本发明所述试剂能够检测特定区域13正链上的chr11:22829220、chr11:22829232、chr11:22829234、chr11:22829380、chr11:22829382、chr11:22829386、chr11:22829396、chr11:22829400、chr11:22829403、chr11:22829406、chr11:22829421和chr11:22829424至少一个位置上的胞嘧啶的甲基化。
69.一些实施例中,所述试剂还包括能够差异修饰甲基化dna和非甲基化dna的反应试剂。在用所述反应试剂处理来自生物样本的样本dna之后,所述检测试剂能确定上述目标区域(a)-(e)的特定区域的核苷酸序列中的特定的cpg位点是甲基化的还是非甲基化的,进而可分析所述样本dna的甲基化水平。
70.一些实施例中,所述反应试剂是选自以下方法的一个或多个所用的试剂:基于重亚硫酸盐转化的pcr(例如甲基化特异性pcr)、dna测序(如亚硫酸氢盐测序、全基因组甲基化测序、简化甲基化测序)、焦磷酸测序法、甲基化敏感的限制性内切酶分析法、荧光定量法、甲基化敏感性高分辨率熔解曲线法、数字pcr法等所需的试剂等。一些实施例中,所述反应试剂为亚硫酸氢盐。
71.一些实施例中,所述生物样本为血液样本、唾液样本、组织样本或食管来源的细胞样本;所述生物样本为来源于对象的离体生物样本。本技术中,“对象”或“患者”或“受试者”包括人类患者和其它哺乳类动物,还包括患有或患有过食管癌的任何个体,或者希望使用本发明方法进行分析或治疗的任何个体。落入本发明范围内的合适的哺乳类动物包括但不限于:灵长类、家畜(例如绵羊、牛、马、猴、猪)、实验室试验动物(例如兔、小鼠、大鼠、豚鼠、仓鼠)、宠物(例如猫、狗)和圈养野生动物(例如狐狸、鹿、澳洲野狗)。优选地,患者为人类患者。
72.本发明还提供一种用于食管癌诊断或辅助诊断的检测试剂盒,其包括所述的试剂,还包括扩增试剂、扩增内参基因的引物对以及所述引物对对应的探针、dna提取试剂、dna纯化试剂和质控品中的一种或者多种。
73.一些实施例中,所述扩增试剂包括扩增缓冲液、dntps、dna聚合酶和mg
2+
中的一种或者多种。
74.一些实施例中,所述内参基因可以为actb,所述扩增内参基因actb的引物对包括上游扩增引物和下游扩增引物,其中上游扩增引物为:aaggtggttgggtggttgttttg(seq id no:66),下游扩增引物为:aataacacccccaccctgc(seq id no:67);所述扩增内参基因actb的引物对对应的探针为:ggagtggtttttgggtttg(seq idno:68)。
75.一些实施例中,本发明所用检测探针均为taqman探针,目标区域的检测探针5’端的荧光报告基团为fam,3’端的荧光淬灭基团为mgb,actb基因的检测探针5’端的荧光报告
基团为vic,3’端的荧光淬灭基团为bhq-1。
76.在本发明一些实施例中,“taqman探针”是指包含5’荧光基团和3’淬灭基团的一段寡核苷酸序列。当探针与dna上的相应位点结合时,因为荧光基团附近存在淬灭基团,探针不会发出荧光。在扩增过程中,如果探针与被扩增的链结合,dna聚合酶(如taq酶)的5
’‑3’
核酸外切酶活性会消化探针,荧光基团远离淬灭基团,其能量不被吸收,即产生荧光信号。每经过一个pcr循环,荧光信号也和目的片段一样,有一个同步的指数增长的过程。
77.本发明提供的试剂或检测试剂盒可用于制备食管鳞状细胞癌及癌前病变的诊断或辅助诊断产品,产品可以为如下中的至少一种:试剂、试剂盒、芯片和测序文库等。可选地,所述试剂可以是冻干粉状、溶液、悬浮液、乳液等产品形态。
78.本技术进一步提供上述检测试剂盒的使用方法,包括:将来源于生物样本的dna序列用所述反应试剂处理,随后加入所述检测试剂,进行pcr反应,测得所述dna序列中dna甲基化的水平。
79.需要说明的是,本发明提供的试剂和检测试剂盒均能够用于食管鳞状细胞癌及癌前病变诊断或辅助诊断,并不限于上述所列举的试剂、试剂盒,只要能满足食管鳞状细胞癌或癌前病变的诊断或辅助诊断的需求均在本发明的保护范围内。本技术提供了可作为食管鳞状细胞癌检测诊断标志物的目标区域(a)-(e)的特定区域的核苷酸序列,其可在食管鳞状细胞癌检测诊断或辅助诊断中作为目标序列,并进一步提供了检测上述核苷酸序列的试剂及方法。本发明所提供的试剂和试剂盒适用于食管鳞状细胞癌的检测诊断或辅助诊断。本发明的检测试剂盒可用于不同阶段的食管鳞状细胞癌的诊断及辅助诊断,包括食管上皮内瘤变(高级别)、食管上皮内瘤变(低级别),因而,本技术的检测试剂盒可用于食管鳞状细胞癌的早期筛查,尤其是癌前病变筛查,其灵敏度可达81%。需要说明的是,基于人类疾病诊断的复杂性,本技术所述的食管鳞状细胞癌检测试剂盒所获得的结果仅作为食管鳞状细胞癌诊断的中间结果或提示患者患有食管癌的可能性或风险,还需结合个体的临床表现及其他生理指标最终得出是否罹患食管癌的结论。
80.以下结合具体实施例,对上述技术方案详细说明。
81.本实施例中,所用试剂如无特殊说明,均为市售产品。
82.以下为实施例:
83.实施例1
84.1.样本dna提取
85.组织样本均为福尔马林浸泡、石蜡包埋的样本,使用qiaamp dnaffpe tissue kit(cat:56404)提取组织样本的dna。
86.血浆样本用天根生化科技(北京)有限公司的磁珠法血清/血浆游离dna(cfdna)提取试剂盒(dp709)进行血浆cfdna提取。
87.具体dna提取操作均参见试剂盒说明书。
88.2.样本dna的转化和纯化
89.样本dna的转化和纯化所用试剂盒均为武汉艾米森生命科技有限公司核酸转化试剂(鄂汉械备20200843号),具体操作步骤参见试剂盒说明书。
90.3.甲基化特异性荧光定量pcr
91.1)甲基化引物对和检测探针设计:
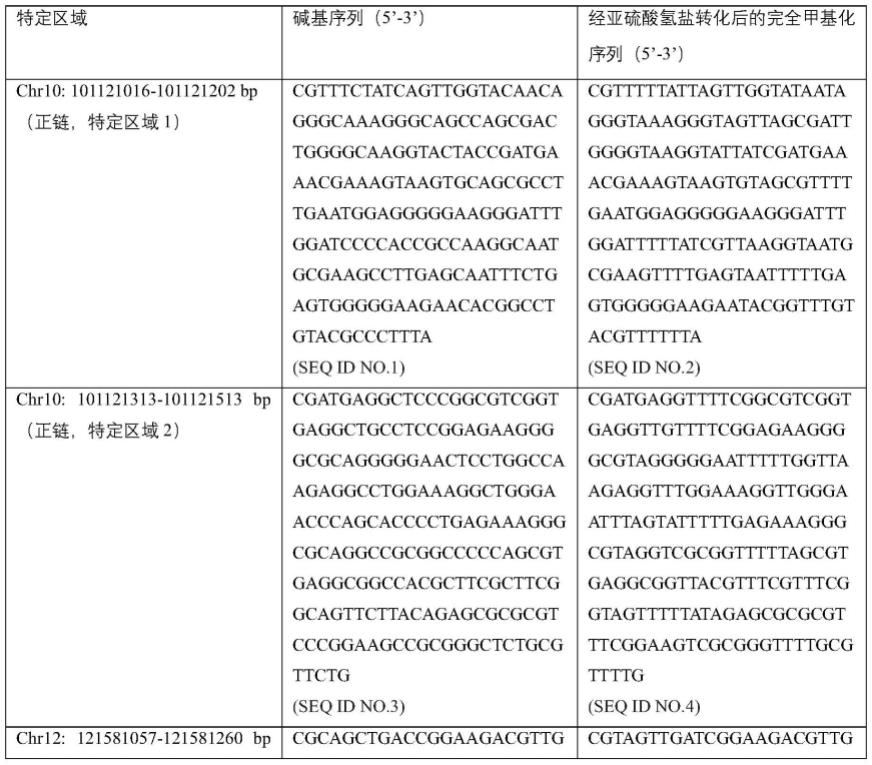
92.分别以经亚硫酸氢盐转化后的dna序列为模板,设计甲基化引物对和检测探针用以检测特定区域的甲基化水平。具体的,目标区域chr10:101121016-101121513bp包括两个特定区域,针对特定区域所在的正链dna分子,共设计2对甲基化引物对和检测探针;目标区域chr12:121580936-121581260bp包括两个特定区域,针对特定区域所在的正/负链dna分子,共设计2对甲基化引物对和检测探针;目标区域chr19:10580847-10581279bp包括三个特定区域,针对特定区域所在的正/负链dna分子共设计3对甲基化引物对和检测探针;目标区域chr17:9576547-9576756bp包括三个特定区域,针对特定区域所在的正/负链dna分子共设计3对甲基化引物对和检测探针;目标区域chr11:22829210-22829426bp包括三个特定区域,针对特定区域所在的正链dna分子共设计3对甲基化引物对和检测探针。特定区域的dna序列及经亚硫酸氢盐转化后的序列如表1所示,用以扩增特定区域的甲基化引物对、检测探针的序列以及可检测的甲基化的胞嘧啶位点如表2所示。
93.2)pcr扩增:
94.pcr反应体系中用到的引物对和检测探针如表2所示,用到的模板为从各个样本中提取的且经亚硫酸氢盐转化的dna,如表1所示。在每个pcr管中,除加入目标区域的引物对和检测探针以外,还需加入内参基因actb的引物对和检测探针。内参基因actb的上游扩增引物为:aaggtggttgggtggttgttttg(seq id no:66),下游扩增引物为:aataacacccccaccctgc(seq id no:67),检测探针为:ggagtggtttttgggtttg(seq id no:68)。上述检测探针均为taqman探针,目标区域的检测探针5’端的荧光报告基团为fam,3’端的荧光淬灭基团为mgb,actb基因的检测探针5’端的荧光报告基团为vic,3’端的荧光淬灭基团为bhq-1。反应体系和反应程序如下表3和表4所示。
95.3)阴性对照和阳性对照:
96.在进行pcr反应检测样本时,阴性对照和阳性对照也应同时进行检测,阴性对照管的dna模板为te缓冲液。阳性对照管的dna模板的制备方法为:将actb基因扩增区域对应的经亚硫酸氢盐完全转化后的序列进行人工合成,并克隆至载体上,形成人工合成质粒;将经亚硫酸氢盐完全转化后的目标区域的特定区域进行人工合成,并分别克隆至载体,形成人工合成质粒。若只检测单一区域的甲基化水平,阳性对照dna模板为103拷贝/微升的含转化后actb的人工合成质粒、103拷贝/微升的含检测区域的人工合成质粒,二者1:1混合而成;若检测组合物的甲基化水平,则阳性对照dna模板为103拷贝/微升的含转化后actb的人工合成质粒、含各目标区域的特定区域的人工合成质粒分别为103拷贝/微升,等体积混合。
97.4)ct值读取:
98.pcr完成后,调整基线,将一次pcr中样本最小ct值提前1-2个循环前的荧光值设置为基线值,将阈值设置在s型扩增曲线的拐点处,得到样本各个基因的ct值。
99.5)质量控制:
100.阴性对照要无扩增,阳性对照要有明显的指数增长期,且阳性对照各基因的ct值应在26-30之间。待检样本的内参基因的ct值应≤35,阴性对照、阳性对照及内参基因均满足上述要求后,表明本次实验有效,可进行下一步样本结果的判定。否则,当次实验无效,须重新进行检测。
101.4.pcr结果分析
102.根据各个目的区域检测的ct值来判断待测样本的甲基化水平。对于组织样本,若
扩增某一区域的ct值≤38,则认为该样本中此区域为甲基化阳性,若扩增某一区域的ct值>38,则认为该样本中此区域为甲基化阴性。对于血浆样本,若扩增某一区域的ct值≤45时,即认为该样本在此区域为甲基化阳性,若扩增某一区域的ct值》45,则认为该样本在此区域为甲基化阴性。在检测单一区域时,若待测样本在该区域为甲基化阳性,则该样本为癌症阳性样本,若待测样本在该区域为甲基化阴性,则该样本为癌症阴性样本。在检测组合物时,若待测样本在组合物中至少一个区域为甲基化阳性,则该样本为癌症阳性样本,仅当待测样本在构成组合物的两个区域均为甲基化阴性,则该样本为癌症阴性样本。
103.将样本的甲基化检测结果同病理结果进行对比,计算甲基化检测的灵敏度和特异性。灵敏度=甲基化阳性个数/(病理检测结果为阳性的个数),特异性为=甲基化阴性个数/(癌旁样本or健康人样本)。
104.表1特定区域的dna序列及经亚硫酸氢盐转化后的序列
105.106.107.[0108][0109]
表2特定区域的引物、探针序列以及可检测的甲基化的胞嘧啶位点
[0110]
[0111][0112]
表3qmsp反应体系
[0113][0114]
表4qmsp反应程序
[0115][0116]
实施例2
[0117]
共收集了65例经病理检测确诊为食管鳞癌患者的癌组织样本和对应的癌旁正常组织样本65例,食管上皮内瘤变(高级别)组织样本57例,食管上皮内瘤变(低级别)组织样本48例。所有样本的收集过程经过伦理委员会的审批,所有志愿者都签署了知情同意书,所有样本均采用匿名化处理。
[0118]
将样本按照实施例中1所述方法进行基因组提取、亚硫酸氢盐转化,并用转化后的dna作为模板分别检测特定区域1-13,以及区域组合的甲基化状态。
[0119]
表5特定区域1-13在组织样本中的甲基化状态及诊断的灵敏度和特异性
[0120]
[0121][0122]
由表5的结果可知,特定区域1-2对于食管鳞癌组织样本的检测灵敏度均在86%以上,对于癌前病变甚至是低级别瘤变组织样本的检测灵敏度也在75%以上,对于癌旁正常组织的检测特异性均在87%以上;特定区域3-4对于食管鳞癌组织样本的检测灵敏度均在86%以上,其对于高级别的癌前病变组织样本的检测灵敏度达到75%以上,其对于低级别的癌前病变组织样本的检测灵敏度达到66%以上,其对于癌旁正常组织的检测特异性均在86%以上;特定区域5-7对于食管鳞癌组织样本的检测灵敏度均在86%以上,其对于高级别的癌前病变组织样本的检测灵敏度达到75%以上,其对于低级别的癌前病变组织样本的检测灵敏度达到66%以上,最高达到72.92%,其对于癌旁正常组织的检测特异性均在87%以上;特定区域8-10对于食管鳞癌组织样本的检测灵敏度均在83%以上,其对于高级别的癌前病变组织样本的检测灵敏度达到78%以上,其对于低级别的癌前病变组织样本的检测灵敏度达到68%以上,其对于癌旁正常组织的检测特异性均在86%以上;特定区域11-13对于食管鳞癌组织样本的检测灵敏度均在87%以上,对于高级别的癌前病变组织样本的检测灵敏度达到80%以上,对于低级别的癌前病变组织样本的检测灵敏度达到75%以上,对于癌旁正常组织的检测特异性均在84%以上。总体来说,特定区域1-13对食管癌及癌前病变的组织样本均具有较高的诊断灵敏度和特异性,也就是说,以上任意特定区域都可以作为标志物,通过检测标志物的甲基化水平从而区分健康样本和食管鳞癌样本。
[0123]
表6组合特定区域在组织样本中的甲基化状态及诊断的灵敏度和特异性
[0124]
[0125][0126]
由表6所示,选取特定区域1、特定区域4、特定区域6、特定区域9以及特定区域11任意组合用来检测组织样本食管鳞癌以及癌前病变的灵敏度、癌旁正常组织的特异性结果均显示在表格中。区域两两组合进行检测时,组合物对于食管鳞癌、高级别及低级别的食管鳞癌癌前病变组织样本的检测灵敏度均显示出等于或高于单区域检测的最高灵敏度的水平,且不同组合之间的差距不大,均显示较高水平。食管鳞癌组织样本的检测灵敏度均大于90.77%,最高检测灵敏度为特定区域1+特定区域4的组合,其检测灵敏度为达到93.85%;检测高级别瘤变的组织样本的检测灵敏度大于82.46%,其最高检测灵敏度为特定区域1+特定区域11以及特定区域4+特定区域9的组合,达到85.96%;低级别瘤变的组织样本的检测灵敏度大于77.08%,其最高检测灵敏度为81.25%;检测癌旁正常组织样本的特异性略低于单特定区域的检测水平,其特异性均高于81.54%,但依然处于较高水平。综合来看,目标区域(a)-(e)任意两区域组合的特定区域的组合检测效果优于单特定区域检测。
[0127]
实施例3
[0128]
利用甲基化荧光定量pcr法分析单特定区域及组合特定区域诊断食管鳞癌及癌前病变患者血浆样本的性能
[0129]
共收集食管鳞癌患者血浆样本65例,食管上皮内瘤变(高级别)患者血浆43例,食管上皮内瘤变(低级别)患者血浆46例,健康人血浆样本110例。所有样本由专业医务人员收集并经过伦理委员会的审批,所有志愿者都签署了知情同意书,所有样本均采用匿名化处理。
[0130]
将此部分样本按照实施例中1所述方法进行基因组提取、亚硫酸氢盐转化,并用转化后的dna作为模板分别检测特定区域1-13,以及目标区域(a)-(e)任意两区域组合的特定区域的甲基化状态。
[0131]
表7特定区域1-13在血浆样本中的甲基化状态及诊断的灵敏度和特异性
[0132][0133]
从表7可以看出,在血浆样本中检测特定区域1-13的甲基化水平对食管鳞癌、高级别和低级别的癌前病变以及健康人可以实现较好的区分。其各区域检测食管鳞癌血浆样本的灵敏度多在80%以上,其中,特定区域1、特定区域4、特定区域10、特定区域12和特定区域13的检测灵敏度最高,可以达到84.62%。同时,各特定区域检测高级别癌前病变血浆样本的灵敏度均在69.77%以上,最高检测灵敏度可达79.07%;对于低级别的癌前病变血浆样本的检测,其检测灵敏度也多大于67.57%,最高检测灵敏度达到71.74%;对于健康人血浆的特异性检测表现较好,特定区域7、10、11均能达到100%的检测特异性。
[0134]
表8组合特定区域在血浆样本中的甲基化状态及诊断的灵敏度和特异性
[0135]
[0136][0137]
由表8可以看出,组合特定区域在血浆样本中的检测结果与在组织样本中的检测结果趋势类似,组合特定区域检测食管鳞癌患者及癌前病变患者血浆样本的灵敏度均高于单特定区域的检测结果。目标区域(a)-(e)任意两两组合进行检测时,检测食管鳞癌血浆样本的灵敏度均大于87.69%,总体检测灵敏度与单特定区域检测最高灵敏度持平或高于,其检测高级别瘤变血浆样本的灵敏度大于79.07%,其检测低级别瘤变血浆样本的灵敏度大于71.74%;检测健康人血浆的特异性略低于单区域的检测水平,其检测特异性均高于94.55%。综合来看,对于血浆样本,目标区域(a)-(e)任意两区域组合的特定区域的组合检测效果优于单特定区域检测效果。
[0138]
本领域的技术人员容易理解,以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1