分拣蛋白活性调节剂的制作方法
本发明涉及式(i)化合物,其是分拣蛋白活性的调节剂。本发明还涉及包含这些化合物的药物组合物以及这些化合物在治疗或预防其中调节分拣蛋白活性是有益的医学病症中的用途。此类医学病症包括神经退行性疾病、炎症性疾病、癌症、疼痛、糖尿病、糖尿病视网膜病变、青光眼、葡萄膜炎、心血管疾病、遗传性眼部疾病或听力损失。
背景技术:
1、分拣蛋白(sortilin,由sort1编码)是空泡蛋白分拣10蛋白(vps10p)分拣受体家族中的1型膜受体,在中枢神经系统、内耳和一些参与代谢控制的外周组织中大量表达1,2,3,4。分拣蛋白具有根据seq id no:1的氨基酸序列,并且包括信号肽、前肽、vps10p结构域、10cc结构域(10cca+10cb)、跨膜结构域和大的细胞质尾部。分拣蛋白的管腔结构域具有6个潜在的n-连接糖基化位点,而细胞质尾部能够募集各种接头蛋白。
2、分拣蛋白与大量配体和膜受体结合,从而参与已知在细胞信号传导和分拣中重要的功能。例如,分拣蛋白参与神经营养因子前体:分别为神经生长因子的前体形式(prongf)、脑源性神经营养因子的前体形式(probdnf)和神经营养因子-3的前体形式(pront3)的信号传导。据报道,在与p75ntr蛋白(p75神经营养因子受体)的复合物中,分拣蛋白形成神经营养因子前体介导的凋亡效应的受体,导致细胞和动物模型中的变性和细胞死亡5,6,7。
3、先前的研究表明,分拣蛋白在与糖尿病和肥胖症等疾病相关的细胞分拣和信号传导中发挥作用(huang等人,2013 mol biol cell oct;24(19):3115-22)8。分拣蛋白促进glut4向质膜的易位,并将其从溶酶体中的降解中拯救出来(pan等人mol biol cell.2017jun 15;28(12):1667-1675)9。分拣蛋白水平已被证明受与这些疾病相关的炎症水平的调节。促炎细胞因子tnfα降低了培养的小鼠和人类脂肪细胞中分拣蛋白的mrna水平和蛋白质水平,以及注射到小鼠体内时的分拣蛋白水平(kaddai等人,diabetologia 52:932-40,2009)10。分拣蛋白也可以影响细胞因子分泌:已提出在免疫细胞中靶向分拣蛋白以减轻炎症并减少动脉粥样硬化疾病进展(mortensen等人,j clin invest 124(12):5317-22,2014)11。此外,us2016/0331746描述了能够与分拣蛋白活性位点结合的各种小分子支架。分拣蛋白参与葡萄糖摄取的调节(shi&kandror.developmental cell 9:99-108,2005)12和脂质紊乱疾病的发展(gao等人dnaand cell biology 36(12):1050-61,2017)13。
4、此外,据报道,血浆分拣蛋白水平是识别冠心病或糖尿病患者的潜在生物标志物(oh等人,cardiovascular diabetology 16:92,2017)14。血浆中分拣蛋白水平升高的患者,因此可识别为患有上述疾病,其血糖水平也升高,表明分拣蛋白是治疗这些疾病的治疗靶点。
5、鉴于上述情况,对新化合物的需求尚未得到满足,所述新化合物可用于治疗和预防对调节分拣蛋白有益的疾病,例如神经退行性疾病、炎症性疾病、癌症、疼痛、糖尿病、糖尿病视网膜病变、青光眼、葡萄膜炎、心血管疾病、遗传性眼部疾病或听力损失。神经退行性疾病可以选自额颞叶痴呆、阿尔茨海默病、帕金森病和脊髓损伤;炎症性疾病可以选自炎症性疾病和神经炎症;癌症可选自乳腺癌、肺癌、卵巢癌、前列腺癌、甲状腺癌、胰腺癌、胶质母细胞瘤和结直肠癌;听力损失可选自噪声引起的听力损失、耳毒性引起的听力损失、年龄引起的听力损失、特发性听力损失、耳鸣和突发性听力损失。
技术实现思路
1、在第一方面,本发明提供了式(i)的化合物
2、
3、或其药学上可接受的盐、溶剂合物、水合物、互变异构体、光学异构体、n-氧化物和/或前药;其中
4、r1、r2和r3各自独立地选自卤素、h、(c1-c4)烷基、卤代-(c1-c4)烷基、(c2-c4)烯基和卤代-(c2-c4)烯基;
5、r4选自h、(c1-c10)烷基、卤代-(c1-c10)烷基、(c2-c10)烯基、卤代-(c2-c10)烯基、(c3-c8)芳基、卤代-(c3-c8)芳基、(c3-c8)杂芳基、卤代-(c3-c8)杂芳基、(c1-c6)亚烷基-(c3-c20)芳基、(c1-c6)亚烷基-(c3-c20)杂芳基、(c1-c6)亚烷基-(3至10元杂环);
6、其中(c1-c6)-亚烷基-(c3-c20)芳基中的芳基、(c1-c6)-亚烷基-(c3-c20)杂芳基中的杂芳基或(c1-c6)亚烷基-(3至10元杂环)中的杂环任选地被一个或多个取代基取代,所述取代基独立地选自卤素、h、-oh、(c1-c4)烷基、卤代-(c1-c4)烷基、(c1-c4)烷氧基、卤代-(c1-c4)烷氧基;
7、r5选自h、(c1-c10)烷基和(c2-c10)烯基;
8、其中烷基和烯基任选地被卤素、酰氨基和酚基取代;且
9、r6选自(c1-c10)烷基、卤代-(c1-c10)烷基、(c2-c10)烯基、卤代-(c2-c10)烯基和3至10元杂环;
10、其中,所述杂环任选地被一个或多个取代基取代,所述取代基独立地选自卤素、h、-oh、(c1-c4)烷基、卤代-(c1-c10)烷基、乙酰基、(c1-c4)烷氧基、卤代-(c1-c4)烷氧基。
11、已发现,式(i)化合物抑制或拮抗分拣蛋白,因此在分拣蛋白抑制有益的病症可能有用。这种病症包括神经退行性疾病、炎症性疾病、癌症、疼痛、糖尿病、糖尿病视网膜病变、青光眼、葡萄膜炎、心血管疾病、遗传性眼部疾病或听力损失。神经退行性疾病可以选自额颞叶痴呆、阿尔茨海默病、帕金森病和脊髓损伤;炎症性疾病可以选自炎症性疾病和神经炎症;癌症可选自乳腺癌、肺癌、卵巢癌、前列腺癌、甲状腺癌、胰腺癌、胶质母细胞瘤和结直肠癌;听力损失可选自噪声引起的听力损失、耳毒性引起的听力损失、年龄引起的听力损失、特发性听力损失、耳鸣和突发性听力损失。
12、如本文所用,术语“分拣蛋白”可指全长分拣蛋白(也称为未成熟分拣蛋白),其包含信号肽、前肽、vps10p结构域、10cc结构域、跨膜结构域和大细胞质尾部,具有根据seq idno:1或seq id no:2的氨基酸序列,或者分拣蛋白可指成熟分拣蛋白,其包含vps10p结构域、10cc结构域、跨膜结构域和大的细胞质尾区,具有根据seq id no:3的氨基酸序列,或其天然存在的片段、同源物或变体。术语“分拣蛋白”或“分拣蛋白分子”在本文中可互换使用。据了解,分拣蛋白能够与神经营养因子前体分子相互作用,形成分拣蛋白/神经营养因子前体复合物。该分拣蛋白/神经营养因子前体复合物可能能够或可能不能够与p75ntr分子相互作用以形成包含分拣蛋白、神经营养原和p75ntr的三聚体复合物。据了解,这种三聚体复合物可能是不良生物反应(例如刺激视网膜和神经节细胞的凋亡,以及控制突起轴突的生长锥回缩)的原因5,7,15,16。
13、如本文所用,术语“神经营养因子前体”是指神经营养因子的较大前体,其经历蛋白水解切割以产生成熟形式的神经营养因子。神经营养因子是一个诱导神经元生存、发育和功能的蛋白质家族,通常被称为生长因子。神经营养因子前体具有生物活性,与相应的神经营养因子相比具有不同的作用,如诱导细胞凋亡。神经营养因子前体的实例包括prongf、probdnf、pront3和pront4。神经营养因子前体也可能控制突触可塑性。尽管成熟的神经营养因子诱导突触强度,但在其前体形式,它们可能削弱突触。
14、本发明的化合物可以是分拣蛋白抑制剂或拮抗剂。如本文所用,术语“分拣蛋白拮抗剂”是指干扰、阻断或以其他方式减弱分拣蛋白蛋白与神经营养因子前体(例如prongf、pront3、probdnf)结合的作用并防止分拣蛋白、p75ntr和前神经营养因子之间形成三聚复合物的物质。术语“分拣蛋白拮抗剂”还包括干扰高亲和力三聚体复合物形成的物质或试剂。在后一种情况下,可以认识到可以形成三聚复合物,因为分拣蛋白可以结合p75ntr(但不能结合prongf),p75ntr可以同时结合prongf的ngf结构域。然而,所得到的三聚体复合物可能对其受体具有较低的亲和力,因此通过上述机制刺激细胞凋亡的能力显著降低。skeldal等人(j.biol.chem.2012dec21;287(52):43798-809)17证明,当分拣蛋白在其细胞内结构域中缺失时,三聚体复合物的凋亡功能被消除。术语“分拣蛋白拮抗剂”还包括干扰、阻断或以其他方式减弱与p75ntr相互作用的分拣蛋白蛋白的作用的物质或试剂。这种相互作用可以被完全阻止(在这种情况下阻止三聚复合物的形成),或者仅部分阻止(在这种情况下可以形成三聚复合物),但可能具有降低的生物效力。skeldal等人表明,分拣蛋白和p75ntr之间的复合物形成依赖于受体细胞外结构域中的接触点,并且相互作用主要依赖于p75ntr的细胞外近膜23个氨基酸的序列。因此,分拣蛋白拮抗剂可能干扰分子中的这23个氨基酸序列或近端序列。
15、优选r1、r2和r3各自独立地选自卤素、(c1-c2)烷基和卤代-(c1-c2)烷基。
16、在本发明的优选方面中,r1、r2和r3各自独立地选自f、ch3和cf3。最优选地,r1、r2和r3是相同的。例如,在本发明的示例性化合物中,r1、r2和r3可以各自为f、ch3或cf3。
17、在本发明的另一个优选方面中,r4选自h、(c1-c6)烷基、卤代-(c1-c6)烷基、(c3-c10)芳基、(c1-c3)亚烷基-(c3-c10)芳基、(c1-c3)亚烷基-(c3-c10)杂芳基和(c1-c3)亚烷基-(3至10元杂环)。(c1-c3)-亚烷基-(c3-c10)芳基中的芳基、(c1-c4)亚烷基-(c3-c10)杂芳基或(c1-c3亚烷基)(3至10元杂环)中的杂环任选地被一个或多个取代基取代,所述取代基独立地选自卤素、-h、-oh、(c1-c3)烷基、卤代-(c1-c3)烷基、(c1-c3)烷氧基和卤代-(c1-c3)烷氧基。
18、烷基、卤代烷基、烯基、卤代烯基和烷基、卤代基、烷氧基和卤代烷氧基取代基可以是直链或支链的。
19、取代基可以连接在芳基、杂芳基或杂环的任何位置。一个或多个取代基可以连接到碳原子、杂原子或其组合。优选地,不存在取代基或取代基为一至三个。
20、杂芳基或杂环可以包含一个、两个或更多个杂原子。优选地,杂芳基或杂环包含一个或两个杂原子。杂原子可以选自n、s或o。在存在多于一个杂原子的基团中,杂原子可以相同或不同。
21、杂环可以是脂肪族的。它可以是单环的、双环的或三环的。优选地,杂环是单环的或双环的。优选地,杂环为5-10元环,优选5-9元环。
22、芳基和杂芳基也可以是单环的、双环的或三环的。优选地,单环的或双环的。优选地,芳基和杂芳基大小为5-10元,更优选为5-9元。
23、在一些优选实施方案中,r4选自:
24、
25、与r4连接的式(i)的碳的手性是(r)或(s)。优选地,当基团(ii)-(xii)包含在式(i)中时,该碳的手性为(s);并且当基团(i)包含在式(i)时,该碳的手性为(s)或(r)。
26、在本发明的另一个优选方面中,r5选自h和(c1-c4)烷基,所述烷基任选地被卤素、酰氨基和酚基取代。
27、优选地,r5选自
28、
29、在本发明的另一个优选方面中,r6选自(c1-c3)烷基、卤代-(c1-c3)烷基和3-8元杂环。所述杂环任选地被独立地选自卤素、-oh、(c1-c4)烷基和乙酰基的取代基取代。
30、最优选地,r6选自:
31、
32、本发明的特定化合物如下所列。
33、(2s)-2-[(2s)-2-[(2s)-3-(4-羟基苯基)-2-{[(2s)-吡咯烷-2-基]甲酰氨基}丙酰氨基]-3-(1-甲基-1h-咪唑-4-基)丙酰氨基]-5,5-二甲基己酸;
34、(2s)-2-[(2s)-2-[(2s)-3-(4-羟基苯基)-2-{[(2s)-吡咯烷-2-基]甲酰氨基}丙酰氨基]-3-(1,3-噻唑-4-基)丙酰氨基]-5,5-二甲基己酸;
35、(2s)-2-[(2s)-2-[(2s)-4-氨基甲酰基-2-{[(2s)-吡咯烷-2-基]甲酰氨基}丁酰氨基]-3-(1,3-噻唑-4-基)丙酰氨基]-5,5-二甲基己酸;
36、(2s)-2-[(2s)-2-[(2s)-3-(4-羟基苯基)-2-{[(2s)-吡咯烷-2-基]甲酰氨基}丙酰氨基]-3-(1h-吲哚-3-基)丙酰氨基]-5,5-二甲基己酸;
37、(2s)-2-[(2s,3s)-2-[(2s)-3-(4-羟基苯基)-2-{[(2s)-吡咯烷-2-基]甲酰氨基}丙酰氨基]-3-甲基戊酰氨基]-5,5-二甲基己酸;
38、(2s)-2-[(2s,3s)-2-[(2s)-3-(4-羟基苯基)-2-{[(2r)-吗啉-2-基]甲酰氨基}丙酰氨基]-3-甲基戊酰氨基]-5,5-二甲基己酸;
39、(2s)-2-[(2s)-2-[(2s)-3-(4-羟基苯基)-2-{[(2s)-吡咯烷-2-基]甲酰氨基}丙酰氨基]-3-(1-甲基-1h-咪唑-5-基)丙酰氨基]-5,5-二甲基己酸;
40、(2s)-2-[(2s,3s)-2-[(2s)-3-(4-羟基苯基)-2-{[(2r)-吡咯烷-2-基]甲酰氨基}丙酰氨基]-3-甲基戊酰氨基]-5,5-二甲基己酸;
41、(2s)-2-[(2s)-2-[(2s)-3-氨基甲酰基-2-{[(2s)-吡咯烷-2-基]甲酰氨基}丙酰氨基]-3-(1,3-噻唑-4-基)丙酰氨基]-5,5-二甲基己酸;
42、(2s)-2-[(2s)-2-[(2s)-3-(4-羟基苯基)-2-{[(2s)-吡咯烷-2-基]甲酰氨基}丙酰氨基]-3-(吗啉-4-基)丙酰氨基]-5,5-二甲基己酸;
43、(2s)-2-[(2s)-2-[(2s)-3-(4-羟基苯基)-2-{[(2s)-吡咯烷-2-基]甲酰氨基}丙酰氨基]-3-(吡啶-2-基)丙酰氨基]-5,5-二甲基己酸;
44、(2s)-2-[(2s,3s)-2-[(2s)-2-乙酰氨基-3-(4-羟基苯基)丙酰氨基]-3-甲基戊酰氨基]-5,5-二甲基己酸;
45、(2s)-2-[(2s,3s)-2-[(2s)-3-(4-羟基苯基)-2-{[(2r)-氧杂戊环-2-基]甲酰氨基}丙酰氨基]-3-甲基戊酰氨基]-5,5-二甲基己酸;
46、(2s)-2-[(2s,3s)-2-[(2s)-3-(4-羟基苯基)-2-{[(2s)-氧杂戊环-2-基]甲酰氨基}丙酰氨基]-3-甲基戊酰氨基]-5,5-二甲基己酸;
47、(2s)-2-[(2s,3s)-2-[(2s)-2-{[(2r)-4-乙酰基吗啉-2-基]甲酰氨基}-3-(4-羟基苯基)丙酰氨基]-3-甲基戊酰氨基]-5,5-二甲基己酸;
48、(2s)-2-[(2s,3s)-2-[(2s)-3-(4-羟基苯基)-2-{[(3s)-吗啉-3-基]甲酰氨基}丙酰氨基]-3-甲基戊酰氨基]-5,5-二甲基己酸;
49、(2s)-2-[(2s,3s)-2-[(2s)-3-(4-羟基苯基)-2-{[(3r)-吗啉-3-基]甲酰氨基}丙酰氨基]-3-甲基戊酰氨基]-5,5-二甲基己酸;
50、(2s)-2-[(2s,3s)-2-[(2s)-3-(4-羟基苯基)-2-{[(2s)-吗啉-2-基]甲酰氨基}丙酰氨基]-3-甲基戊酰氨基]-5,5-二甲基己酸;
51、(2s)-2-[(2s)-2-[(2s)-3-(4-羟基苯基)-2-{[(2s)-吡咯烷-2-基]甲酰氨基}丙酰氨基]-3-(吡啶-4-基)丙酰氨基]-5,5-二甲基己酸;
52、(2s)-2-[(2s)-2-[(2s)-3-(4-羟基苯基)-2-{[(2s)-吡咯烷-2-基]甲酰氨基}丙酰氨基]-3-(吡啶-3-基)丙酰氨基]-5,5-二甲基己酸;
53、(2s)-2-[(2s)-2-[(2s)-3-(4-羟基苯基)-2-{[(2s)-吡咯烷-2-基]甲酰氨基}丙酰氨基]-3-(噻吩-3-基)丙酰氨基]-5,5-二甲基己酸;
54、(2s)-2-[(2s,3s)-2-[(2s)-3-(4-羟基苯基)-2-{[(3r)-吡咯烷-3-基]甲酰氨基}丙酰氨基]-3-甲基戊酰氨基]-5,5-二甲基己酸;
55、(2s)-2-[(2s,3s)-2-[(2s)-3-(4-羟基苯基)-2-{[(3s)-吡咯烷-3-基]甲酰氨基}丙酰氨基]-3-甲基戊酰氨基]-5,5-二甲基己酸;
56、(2s)-2-[(2s,3s)-2-[(2s)-3-(4-羟基苯基)-2-{[(2s)-哌嗪-2-基]甲酰氨基}丙酰氨基]-3-甲基戊酰氨基]-5,5-二甲基己酸;
57、(2s)-2-[(2s,3s)-2-[(2s)-3-(4-羟基苯基)-2-{[(2r)-哌嗪-2-基]甲酰氨基}丙酰氨基]-3-甲基戊酰氨基]-5,5-二甲基己酸;
58、(2s)-5,5-二甲基-2-[(2s,3s)-3-甲基-2-[(2s)-2-{[(2s)-吡咯烷-2-基]甲酰氨基}丙酰氨基]戊酰氨基]己酸;
59、(2s)-5,5-二甲基-2-[(2s,3s)-3-甲基-2-(2-{[(2s)-吡咯烷-2-基]甲酰氨基}乙酰氨基)戊酰氨基]己酸;
60、(2s)-5,5-二甲基-2-[(2s,3s)-3-甲基-2-[(2s)-3-甲基-2-{[(2s)-吡咯烷-2-基]甲酰氨基}丁酰氨基]戊酰氨基]己酸;
61、(2s)-5,5,5-三氟-2-[(2s,3s)-2-[(2s)-3-(4-羟基苯基)-2-{[(2r)-氧杂戊环-2-基]甲酰氨基}丙酰氨基]-3-甲基戊酰氨基]戊酸;
62、(2s)-5,5,5-三氟-2-[(2s,3s)-2-[(2s)-3-(4-羟基苯基)-2-{[(2s)-氧杂戊环-2-基]甲酰氨基}丙酰氨基]-3-甲基戊酰氨基]戊酸;
63、(2s)-2-[(2s,3s)-2-[(2s)-2-乙酰氨基-3-(4-羟基苯基)丙酰氨基]-3-甲基戊酰氨基]-5,5,5-三氟戊酸;以及
64、(2s)-2-[(2s,3s)-2-[(2s)-2-{[(2r)-4-乙酰基吗啉-2-基]甲酰氨基}-3-(4-羟基苯基)丙酰氨基]-3-甲基戊酰氨基]-5,5,5-三氟戊酸。
65、本发明式(i)化合物旨在用于治疗或预防神经退行性疾病、炎症性疾病、癌症、疼痛、糖尿病、糖尿病视网膜病变、青光眼、葡萄膜炎、心血管疾病、遗传性眼部疾病或听力损失。
66、优选地,神经退行性疾病选自额颞叶痴呆、阿尔茨海默病、帕金森病和脊髓损伤。
67、优选地,炎症性病症可以选自炎症性疾病和神经炎症;
68、优选地,癌症选自腺癌、肺癌、卵巢癌、前列腺癌、甲状腺癌、胰腺癌、胶质母细胞瘤和结直肠癌。
69、优选地,听力损失选自噪声引起的听力损失、耳毒性引起的听力损失、年龄引起的听力损失、特发性听力损失、耳鸣和突发性听力损失。
70、因此,在一个实施方案中,根据本发明使用的化合物可以破坏分拣蛋白分子和促神经营养因子分子之间的相互作用,或者破坏分拣蛋白分子和p75ntr分子之间的互相作用。所述分拣蛋白分子可以是成熟的分拣蛋白。
71、优选地,本发明的化合物是分拣蛋白抑制剂。如本文所用,术语“分拣蛋白抑制剂”是指与分拣蛋白蛋白结合,从而阻止其与神经营养因子前体或p75ntr分子结合,并阻止上述三聚复合物的形成,或导致形成活性较低或无活性的三聚复合物的化合物。
72、优选地,本发明的化合物防止分拣蛋白分子与神经营养因子前体或p75ntr分子之间的蛋白质-蛋白质相互作用,进一步防止凋亡三聚体复合物的形成,该凋亡三聚体复合物的形成通常在分拣蛋白、神经营养因子前体和p75ntr受体之间形成,或导致低亲和力三聚物的形成,其在生物学上活性较低或无活性或具有最小活性。
73、因此,所述化合物可以与分拣蛋白、神经营养因子前体或p75ntr分子结合。拮抗作用可能是由于蛋白质-蛋白质相互作用的直接阻断,或者当结合在这些蛋白质中除结合位点之外的一个位点时可能是通过空间位阻发生拮抗作用。
74、根据本发明的第二方面,提供了一种药物组合物,其包含根据本发明第一方面的化合物和一种或多种药学上可接受的载体、赋形剂和/或稀释剂。
75、在本发明的第三方面中,提供了用于治疗的根据本发明第一方面的化合物或根据本发明第二方面的药物组合物。
76、根据本发明的第四方面,提供了根据本发明第一方面的化合物或根据本发明第二方面的药物组合物,其用于治疗或预防神经变性病症、炎症病症、癌症、疼痛、糖尿病、糖尿病性视网膜病变、青光眼、葡萄膜炎、心血管疾病、遗传性眼部疾病或听力损失。
77、优选地,神经退行性疾病选自额颞叶痴呆、阿尔茨海默病、帕金森病和脊髓损伤。
78、优选地,听力损失选自噪声引起的听力损失、耳毒性引起的听力损失、年龄引起的听力损失、特发性听力损失、耳鸣和突发性听力损失。
79、优选地,癌症选自腺癌、肺癌、卵巢癌、前列腺癌、甲状腺癌、胰腺癌、胶质母细胞瘤和结直肠癌。
80、优选地,心血管疾病选自动脉粥样硬化、心肌病、心脏病发作、心律失常和冠状动脉疾病。
81、根据本发明的第五方面,提供了根据本发明第一方面的化合物在制备用于治疗或预防神经退行性疾病、炎症性疾病、癌症、疼痛、糖尿病、糖尿病视网膜病变、青光眼、葡萄膜炎、心血管疾病、遗传性眼部疾病或听力损失中的药物的用途。
82、根据本发明的第六方面,提供了一种治疗或预防对分拣蛋白调节有反应的疾病或病症的方法,包括施用有效治疗量的根据本发明第一方面的化合物或根据本发明第二方面的药物组合物。
83、本发明的化合物可以包括同位素标记和/或同位素富集形式的化合物。本文中的本发明化合物可以在构成这样的化合物的一个或多个原子处包含非自然比例的原子同位素。可掺入所公开的化合物中的同位素的实例包括氢、碳、氮、氧、磷、硫、氯的同位素,例如2h、3h、11c、13c、14c、13n、15o、17o、32p、35s、18f、36cl。
84、本发明的化合物可以这样使用,或者在适当的情况下,作为其药理学上可接受的盐(酸或碱加成盐)使用。以下提及的药学上可接受的加成盐是指包含化合物能够形成的具有治疗活性的无毒酸和碱加成盐形式。通过用合适的酸处理碱形式,具有碱性性质的化合物可以转化为其药学上可可接受的酸加成盐。示例性酸包括无机酸,例如氯化氢、溴化氢、碘化氢、硫酸、磷酸;和有机酸如甲酸、乙酸、丙酸、羟基乙酸、乳酸、丙酮酸、乙醇酸、马来酸、丙二酸、草酸、苯磺酸、甲苯磺酸、甲磺酸、三氟乙酸、富马酸、琥珀酸、苹果酸、酒石酸、柠檬酸、水杨酸、对氨基水杨酸、双羟苯甲酸、苯甲酸,抗坏血酸等。具有酸性性质的化合物可以通过用合适的碱处理酸形式而转化为其药学上可接受的碱性加成盐。示例性的碱加成盐形式是钠盐、钾盐、钙盐和与药学上可接受的胺如氨、烷基胺、苄星和如精氨酸和赖氨酸的氨基酸的盐。本文使用的术语加成盐还包括化合物及其盐能够形成的溶剂化物,例如水合物、醇化物等。
85、在整个本公开中,给定的化学式或名称还应包括其所有药学上可接受的盐、溶剂合物、水合物、n-氧化物和/或前药形式。应当理解,本发明的化合物包括化合物式的任何和所有水合物和/或溶剂化物。可以理解,某些官能团,例如羟基、氨基和类似基团,以化合物的各种物理形式与水和/或各种溶剂形成络合物和/或配位化合物。因此,上述式应理解为包括并代表那些各种水合物和/或溶剂化物。
86、本发明的化合物还包括互变异构体形式。互变异构形式是由单键与相邻双键的交换以及伴随的质子迁移产生的。互变异构体形式包括原变异构体,其为具有相同经验式和总电荷的异构质子化态。示例的质子互变异构体包括酮-烯醇对、酰胺-亚胺酸对、内酰胺-丙交酯对、酰胺酰亚胺对、烯胺-亚胺对和环状形式,其中质子可以占据杂环系统的两个或多个位置,例如1h-咪唑和3h-咪唑、1h-1,2,4-三唑、2h-1,2,4-三唑和4h-1,2,4-三唑、1h-异吲哚和2h-异吲哚以及1h-吡唑和2h-吡唑。互变异构体形式可以是平衡的,或者通过适当的取代在空间上锁定为一种形式。
87、本文所述的化合物可以是不对称的(例如具有一个或多个立体中心)。所有立体异构体,如对映体和非对映体,均为预期异构体,除非另有说明。含有不对称取代的碳原子的本发明化合物可以以光学活性或外消旋形式分离。关于如何从光学活性起始材料制备光学活性形式的方法是本领域已知的,例如通过外消旋混合物的拆分或通过立体选择性合成。烯烃的许多几何异构体、c=n双键等也可以存在于本文所述的化合物中,并且在本发明中考虑了所有这些稳定的异构体。描述了本发明化合物的顺式和反式几何异构体,并且可以作为异构体的混合物或分离的异构体形式分离。
88、在含有不对称碳原子的化合物的情况下,本发明涉及d形式、l形式和d,l混合物,并且在存在多于一个不对称碳原子时,还涉及非对映体形式。本发明的那些含有不对称碳原子并且通常以外消旋体形式积累的化合物可以以已知的方式,例如使用光学活性酸,分离成光学活性异构体。然而,也可以从一开始就使用光学活性起始物质,然后获得相应的光学活性或非对映体化合物作为最终产物。
89、术语“前药”是指可以在生理条件下或通过溶剂解转化为本发明的生物活性化合物的化合物。前药在给予有需要的受试者时可能是无活性的,但在体内转化为本发明的活性化合物。前药通常在体内快速转化以产生本发明的母体化合物,例如通过在血液中水解。前药化合物通常在哺乳动物生物体中具有溶解性、组织相容性或延迟释放的优点(参见silverman,r.b.,the organicchemistry of drug design and drug action,第2版,elsevier academic press(2004),498至549页)。本发明化合物的前药可以通过修饰存在于本发明化合物中的官能团如羟基、氨基或巯基来制备,使得所述修饰在常规操作或体内切割成本发明的母体化合物。前药的实例包括但不限于羟基官能团的乙酸盐、甲酸盐和琥珀酸盐衍生物或氨基官能团的苯基氨基甲酸酯衍生物。
90、本文中使用的术语“治疗”可包括预防所命名的紊乱或病症,或在病症建立后改善或消除病症。术语“预防”是指对所命名的紊乱或病症的预防。
91、本文所述的方法包括将受试者确定为需要特定的治疗的方法。识别需要这种治疗的受试者可以由受试者或医疗保健专业人员判断,也可以是主观的(例如意见)或客观的(例如通过测试或诊断方法测定)。
92、在其他方面,本文的方法包括进一步包括监测受试者对治疗给药的反应的方法。这种监测可以包括对受试者组织、液体、标本、细胞、蛋白质、化学标志物、遗传物质等的周期性成像或采样,作为治疗方案的标志物或指标。在其他方法中,通过评估适用于此类治疗的相关标志物或指标,对受试者进行预筛选或确定需要此类治疗。
93、本发明提供了一种监测治疗进展的方法。所述方法包括测定患有或易感于本文所述病症或其症状的受试者的诊断标志物(marker)(例如本文所述的由本文所述化合物调节的任何靶标或细胞类型)或诊断测定(例如筛选、测定)的水平的步骤,其中所述受试者已被施用足以治疗所述疾病或其症状的治疗量的本文化合物。在该方法中确定的标志物水平可以与健康正常对照或其他受折磨患者中的已知标志物水平进行比较,以确定受试者的疾病状态。在优选实施方案中,在比第一水平的确定晚的时间点确定受试者中的第二水平的标志物,并且将这两个水平进行比较以监测病程或治疗的疗效。在某些优选实施方案中,根据本发明,在开始治疗之前测定受试者中标志物的预处理水平;然后可以将该标志物的预处理水平与治疗开始后受试者中的标志物水平进行比较以确定治疗的疗效。
94、受试者中标志物或标志物活性的水平可以至少确定一次。将标志物水平与先前或随后从同一患者、另一患者或正常受试者获得的标志物水平的另一测定值进行比较,可用于确定根据本发明的治疗是否具有期望的效果,从而允许适当地调节剂量水平。标志物水平的测定可以使用本领域已知或本文所述的任何合适的取样/表达测定方法进行。优选地,首先从受试者移除组织或流体样品。合适样品的实例包括血液、尿液、组织、口腔或脸颊细胞以及含有发根的头发样品。本领域技术人员已知其他合适的样品。样品中蛋白质水平和/或mrna水平(例如,标志物水平)的测定可以使用本领域已知的任何合适的技术进行,包括但不限于酶免疫测定、酶联免疫吸附试验、放射性标记/测定技术、印迹/化学发光方法、实时pcr等。
95、对于临床应用,本文公开的化合物被配制成用于各种给药模式的药物组合物(或制剂)。应当理解的是,本发明的化合物可以与生理上可接受的载体、赋形剂和/或稀释剂(即它们中的一种、两种或全部三种)一起给药。本文公开的药物组合物可以通过任何合适的途径给药,优选通过口服、直肠、鼻腔、局部(包括眼科、口腔和舌下)、舌下、透皮、鞘内、透粘膜或胃肠外(包括皮下、肌内、静脉内和皮内)给药。其他制剂可以方便地以单位剂型(例如片剂和缓释胶囊)和脂质体的形式存在,并且可以通过药学领域中公知的任何方法制备。药物制剂通常通过将活性物质或其药学可接受的盐与常规药学可接受载体、稀释剂或赋形剂混合来制备。赋形剂的实例为水、明胶、阿拉伯树胶、乳糖、微晶纤维素、淀粉、乙醇酸淀粉钠、磷酸氢钙、硬脂酸镁、滑石、胶体二氧化硅等。这种制剂还可以含有其他药理学活性剂和常规添加剂,例如稳定剂、润湿剂、乳化剂、调味剂、缓冲剂等。通常,活性化合物的量以重量计在制剂的0.1-95%之间,在胃肠外使用的制剂中优选以重量计0.2-20%,在口服给药的制剂中更优选以重量计1-50%。制剂可通过已知方法进一步制备,例如造粒、压片、微胶囊化、喷雾包衣等。制剂可通过常规方法以片剂、胶囊、颗粒、粉末、糖浆、悬浮液、栓剂或注射剂的剂型制备。液体制剂可以通过将活性物质溶解或悬浮在水中或其他合适的载体中来制备。片剂和颗粒可以以常规方式包衣。为了长时间保持治疗有效的血浆浓度,本文公开的化合物可以掺入缓释制剂中
96、特定化合物的剂量水平和剂量频率将根据多种因素而变化,包括所用特定化合物的效力、该化合物的代谢稳定性和作用时间、患者的年龄、体重、一般健康状况、性别、饮食、给药方式和时间、排泄率、药物组合、要治疗的病症的严重程度以及正在接受治疗的患者。例如,每日剂量可以在每公斤体重约0.001mg至约100mg的范围内,单独给药或多次给药,例如每次约0.01mg至约25mg。通常,这种剂量是口服的,但也可以选择非肠道给药。
97、定义
98、“任选的”或“任选地”是指随后描述的事件或情况可能发生,但不必发生,并且描述包括事件或情况发生的实例和不发生的实例。
99、术语“杂原子”是指o、n或s。
100、术语“(c1-cn)烷基”表示具有1至n个碳原子的直链、支链或环状或部分环状的烷基,即1、2、3、……或n个碳。对于包含环状部分的“(c1-cn)烷基”,它应该由至少三个碳原子形成。对于“(c1-cn)烷基”范围的部分,考虑其所有亚组。例如,在(c1-c6)烷基的范围内,所有的亚组,例如(c1-c5)烷基、(c1-c4)烷基、(c1-c3)烷基、(c1-c2)烷基、(c1)烷基、(c2-c6)烷基、(c2-c5)烷基、(c2-c4)烷基、(c2-c3)烷基、(c2)烷基、(c3-c4)烷基、(c3)烷基、(c4-c6)烷基、(c4-c5)烷基、(c4)烷基、(c5-c6)烷基、(c6)烷基。“c1-c6烷基”的实例包括甲基、乙基、正丙基、异丙基、环丙基、正丁基、异丁基、仲丁基、叔丁基、环丁基、环丙基甲基、支链或环状或部分环状的戊基和己基等。
101、术语“卤代-(c1-cn)烷基”表示如上所述的被至少一个卤原子取代的c1-cn烷基,该卤原子优选为f、cl、br和i,更优选为f和cl,最优选为f。
102、当术语表示一个范围时,例如在(c1-c6)烷基的定义中的“1-6个碳原子”,每个整数被认为是公开的,即1、2、3、4、5和6。
103、术语“(c2-cn)烯基”表示具有至少一个碳-碳双键并具有2-6个碳原子的直链、支链或环状或部分环状的烷基。烯基可以包括由3-6个碳原子形成的环。对于“(c2-cn)烯基”范围的部分,考虑其所有亚组。例如,范围“(c2-c4)烯基”包括(c2-c4)烯基、(c2-c3)烯基和(c2)烯基。“(c2-c4)烯基”的实例包括2-丙烯基、2-丁烯基、3-丁烯基、2-甲基-2-丙烯基等。
104、术语“(c1-c4)烷氧基”表示-o-((c1-c4)烷基),其中(c1-c4)烷基如上所定义,并通过氧原子连接到化合物的其余部分。“(c1-c4)烷氧基”的实例包括甲氧基、乙氧基、正丙氧基、异丙氧基、正丁氧基、异丁氧基、仲丁氧基和叔丁氧基。
105、术语“卤代(c1-c4)烷氧基”表示如上所述的被卤素原子取代的(c1-c4)烷氧基优选为f、cl、br和i,更优选f和cl,最优选f。
106、术语“卤素”是指卤素原子,优选为f、cl、br和i,更优选为f和cl,最优选为f。
107、术语“3至10元杂环”表示具有3至10个环原子的非芳香环体系,其中至少一个环原子是杂原子。
108、“有效量”是指对治疗对象具有治疗效果的本发明化合物的量。治疗效果可以是客观的(即通过某种测试或标志物测定)或主观的(即受试者给出效果的指示或感觉到效果)。
109、如本文所用,术语“给药”或“施用”是指本文公开的化合物的给药途径。示例性给药途径包括但不限于口服、眼内、静脉内、腹膜内、动脉内和肌肉内。优选的给药途径可以根据各种因素而变化,例如包含本文公开的化合物的药物组合物的组分、潜在或实际疾病的部位以及疾病的严重程度。
110、术语“受试者”和“患者”在本文中可互换使用。它们指的是人类或其他哺乳动物(如小鼠、大鼠、兔子、狗、猫、牛、猪、绵羊、马或灵长类动物),可能患有或易患某种疾病或病症,但可能患有或可能没有这种疾病或病症。受试者最好是人类。
111、本发明的化合物可以通过名称或化学结构来公开。如果一种化合物的名称与其相关的化学结构之间存在差异,则以化学结构为准。
112、现将通过以下非限制性实施例来进一步说明本发明。下面的具体示例应被解释为仅仅是说明性的,而不是以任何方式限制本公开的其余部分。在没有进一步阐述的情况下,相信本领域的技术人员可以基于本文的描述,最大限度地利用本发明。本文引用的所有参考文献和出版物通过引用的方式全部并入本文。
113、本发明化合物的制备
114、本发明的化合物可以根据以下通用合成方案,通过本领域熟知和理解的方法制备。通用合成步骤方案1的步骤的合适反应条件在本领域是众所周知的,溶剂和助试剂的适当取代在本领域技术人员的公知常识范围内。同样,本领域技术人员将意识到,合成中间体可以根据需要或需要通过各种众所周知的技术分离和/或纯化,并且经常可以在随后的合成步骤中直接使用各种中间体,而很少或没有纯化。此外,本领域技术人员将理解,在某些情况下,引入部分的顺序并不重要。制备式(i)化合物所需步骤的特定顺序取决于所合成的特定化合物、起始化合物和取代部分的相对可靠性,这是本领域普通技术人员所熟知的,并且所有试剂在本领域中都是公知的和可理解的。
115、通式(i)的化合物可以通过多种程序制备,其中一些程序如下所述。如本领域普通技术人员所熟知和理解的,特别适合制备中小型肽的方法之一是固相肽合成(spps)。
116、合适的起始材料和通式aa-1、int-1、int-2或int-3的受保护氨基酸可商购或可通过多种方法制备。例如,如通用合成步骤方案1所示,可以使用良好建立的程序和试剂,如甲醇和亚硫酰氯的混合物,将通式aa-1的适当取代的氨基酸的羧酸官能团化学选择性地保护为合适的衍生物,例如作为甲酯,以产生通式int-1的化合物。在随后的步骤中,保护int-1中的游离胺官能团,例如酰胺或氨基甲酸酯,如fmoc,得到一般结构int-2的中间体。通式int-3的中间体可以通过使用例如酸性水解对int-2中存在的掩蔽的酸官能团进行选择性脱保护而获得。当使用spps时,int-3可以使用酯形成试剂,例如二异丙基甲烷二亚胺、4-甲基吗啉和n,n-二甲基吡啶-4-胺在二氯甲烷中的混合物,连接到适当官能化的树脂,例如wang树脂上,得到固体负载的通式int-4的中间体。
117、一般合成步骤
118、
119、当需要时,树脂结合的中间体int-4至int-9可以在从树脂裂解后进行分析。或者,可以在不进行分析的情况下在固体支撑件上执行相应的步骤。当例如使用fmoc保护基时,int-4中的胺的保护基可以通过用碱类哌啶处理来去除,从而得到int-5。存在于第二n-保护氨基酸中的游离酸官能度,这里由通式aa-2的化合物表示,可以使用经典的酰胺偶联程序(例如hatu和碱(如在合适的溶剂体系(如dcm-dmf的混合物)中的n-甲基吗啉)的混合物),与存在于通式int-5的中间体中的游离胺偶联,得到int-6。
120、类似地,适当地,胺部分被保护,aa-2可以与int-5偶联以得到int-6。临时胺保护基团可以在随后的步骤中去除,以使用碱类的哌啶得到int-7。int-7中存在的游离碱性胺官能团再次并且如前所述,通过引入另一种适当保护的通式aa-3的氨基酸衍生物(如在一般合成步骤中举例说明的)来扩展,得到int-8。同样,在选择性地去除int-8中的胺的保护基之后,获得的int-9可以使用经典的酰胺偶联程序(例如hatu和碱(例如在合适的溶剂体系(例如dcm-dmf的混合物)中的n-甲基吗啉)的混合物),容易地官能化为酰基衍生物,以产生通式int-10的中间体。通式(i)的最终化合物是通过例如使用诸如三氟乙酸的试剂的酸性水解裂解树脂固体载体和int-10中所示的一般结构的化合物之间的酯键而获得的。
121、从树脂裂解后分析树脂结合的中间体。所有中间体的分析都是游离酸。
122、然后,每个步骤的产物可以通过常规方法回收,所述方法包括提取、蒸发、沉淀、色谱、过滤、研磨、结晶等。
123、本领域技术人员还将理解,并非式(i)化合物中的所有取代基都能耐受用于合成化合物的某些反应条件。这些部分可以在合成中的方便点引入,或者可以根据需要或需要进行保护,然后脱保护,如本领域所熟知的。本领域技术人员将理解,在本发明化合物的合成中,保护基团可以在任何方便的点去除。本发明中使用的引入或去除保护基团的方法在本领域是众所周知的;参见例如greene和wuts,protective groups in organicsynthesis,第4版,johnwiley and sons,new york(2006)18。
124、实施例
125、缩写
126、approx:近似值;aq:水性;br:宽峰;ca:约;cdi:1,1'-羰基二咪唑;d:二重峰;dcm:二氯甲烷;dic:n,n′-二异丙基碳二亚胺;二恶烷:1,4-二恶烷;dipea:二异丙基乙胺;dmf:二甲基甲酰胺;eq.:当量;et3n:三乙胺;etoac:乙酸乙酯;etoh:乙醇;fmoc:芴甲氧羰基;boc:叔丁氧羰基;h:小时;min:分钟:hatu:2-(3h-[1,2,3]三唑并[4,5-b]吡啶-3-基)-1,1,3,3-四甲基异糖醛酸六氟磷酸盐(v);hplc:高效液相色谱法;ipa:异丙醇;lc:液相色谱法;m:多重峰;m:摩尔,分子离子;mecn:乙腈;meoh:甲醇;ms:质谱法;nmr:核磁共振;pda:光电二极管阵列;q:四重峰;rt:室温(约20℃);rt:保留时间;s:单峰,固体;spps:固相肽合成。t:三重峰;tbaf:四丁基氟化铵;tbme:叔丁基甲基醚;tfa:三氟乙酸;thf:四氢呋喃;uplc:超高效液相色谱法;uv:紫外线。
127、其他缩写旨在传达其普遍接受的含义。
128、一般实验条件
129、所有起始材料和溶剂都是从商业来源获得的或根据文献引文制备的。除非另有说明,否则将反应混合物磁力搅拌,并在室温(约20℃)下进行反应。
130、除非另有说明,否则柱色谱是在自动快速色谱系统(如combiflash rf系统)上使用预填充二氧化硅(40μm)柱进行的。
131、在配备有bruker 5mm smartprobetm的bruker avaence iii-500 hd光谱仪上,在500mhz下记录1h nmr光谱。化学位移以百万分之一(ppm)表示,使用残余质子溶剂的中心峰作为参考或相对于四甲基硅烷作为内标。除非另有说明,否则在298k下记录光谱。以下缩写或其组合用于nmr信号的多重性:br=宽峰,d=双重峰,m=多重峰,q=四重峰,quint=五重,s=单峰,t=三重峰。
132、使用waters acquityh-class系统进行分析uplc-ms实验,以确定保留时间和相关质量离子,该系统配备了acquity pda检测器和acquityqda质量检测器,运行下述分析方法之一。
133、使用与agilent 1956、6100或6120系列单重四极杆质谱仪耦合的agilent1200系列hplc系统进行分析lc-ms实验以确定保留时间和相关质量离子,该质谱仪运行下述分析方法之一。
134、使用waters x-select csh c18,5μm,19x50mm柱,使用mecn和水的梯度(均用0.1%v/v甲酸修饰),或在waters x-bridge beh c18、5μm、19x50mm柱子上使用mecn和10mm碳酸氢铵(aq)的梯度进行制备型hplc纯化。在通过可变波长检测器测定的单一波长的uv检测之后收集级分。
135、分析方法
136、方法1-酸性3分钟法
137、色谱柱:waters acquitycsh c18,1.7μm,2.1x30mm,40℃检测:除非另有说明,否则在254nm处进行uv,通过电喷雾电离进行ms
138、溶剂a:水中0.1%v/v甲酸,b:mecn中0.1%v/v甲酸
139、梯度
140、
141、
142、方法2-碱性4分钟法
143、柱:waters x-bridge beh c18,2.5μm,4.6x30mm,40℃
144、溶剂a:10mm碳酸氢铵(aq),b:mecn
145、梯度:
146、 时间 %a %b 流速(ml/min) 0.0 95.0 5.0 2.5 3.0 5.0 95.0 2.5 3.01 5.0 95.0 4.5 3.6 5.0 95.0 4.5 3.7 95.0 5.0 2.5 4.0 95.0 5.0 2.5
147、中间体
148、(s)-2-((((9h-芴-9-基)甲氧基)羰基)氨基)-5,5,5-三氟戊酸(int-11)
149、
150、中间体int-11按照wo 2010/132601中描述的程序制备,以制备5,5,5-三氟戊酸甲酯,随后进行fmoc保护和甲酯水解,如wo 2015/131100中描述的。
151、4-乙酰基-(2r)-2-吗啉羧酸(int-15)
152、
153、(r)-2-(甲氧基羰基)吗啉-4-鎓氯化物(int-13)
154、乙酰氯(7.60ml,107mmol)冷却至0℃,向其中滴加meoh(40ml),并搅拌混合物15分钟。向冷却的混合物中逐份加入(r)-4-(叔丁氧基羰基)吗啉-2-羧酸(int-12,4.50g,19.5mmol)。将反应混合物在2小时内加热至室温,然后加热至70℃过夜。将反应混合物真空浓缩,用tbme(5x 30ml)研制并再次真空浓缩,得到灰白色固体的(r)-2-(甲氧羰基)吗啉-4-鎓氯化物(int-13,3.64g,19.0mmol,98%收率,95%纯度)。1h nmr(500mhz,dmso-d6)δ9.76(s,2h),4.56(dd,j=9.9,3.1hz,1h),4.00(dt,j=12.7,3.3hz,1h),3.88-3.80(m,1h),3.70(s,3h),3.39-3.30(m,1h),3.13-3.19(m,1h),3.11-3.05(m,1h),3.04-3.96(m,1h)。
155、(r)-4-乙酰基吗啉-2-羧酸甲酯(int-14)
156、在0℃下,向(r)-2-(甲氧羰基)吗啉-4-鎓氯化物(int-13,998mg,5.49mmol)和n-甲基吗啉(1.69ml,15.4mmol)的dcm(18ml)溶液中滴加乙酰氯(469μl,6.59mmol),反应混合物过夜加热至室温。过滤反应混合物,用水(20ml)稀释滤液,然后通过加入饱和nahco3水溶液(约10ml)碱化至ph 8。将各层分离,并用dcm(2x20ml)进一步萃取水溶液。合并的有机物用盐水洗涤,用mgso4干燥并浓缩成深橙色油状物。粗产物通过硅胶柱色谱法(40g柱,0-5%meoh在dcm中)纯化,得到棕色油状的(r)-4-乙酰基吗啉-2-羧酸甲酯(int-14,350mg,1.87mmol,34%收率,95%纯度)。1h nmr光谱描述了旋转异构体。
157、1h nmr(500mhz,25℃下,dmso-d6,旋转异构体)δ4.30(dd,j=7.5,3.4hz,0.5h),4.20-4.09(m,1h),3.88(dt,j=11.5,3.4hz,0.5h),3.79-3.70(m,1h),3.68(d,j=14.8hz,3.5h),3.65-3.56(m,0.5h),3.56-3.46(m,1.5h),3.23(dddd,j=28.2,12.5,8.9,3.5hz,1h),3.01(dd,j=13.0,8.8hz,0.5h),2.01(d,j=8.1hz,3h).
158、1h nmr(500mhz,90℃下,dmso-d6)δ4.21-4.18(m,1h),3.87-3.84(m,1h),3.71(s,3h),3.66-3.59(m,1h),3.55(ddd,j=11.6,8.6,3.0hz,1h),3.29(td,j=10.3,9.6,5.1hz,1h),3.01-2.99(m,2h),2.01(s,3h)。
159、(r)-4-乙酰吗啉-2-羧酸(int-15)
160、向(r)-4-乙酰基吗啉-2-羧酸甲酯(int-14,350mg,1 1.87mmol)在水(2.5ml)和thf(2.5ml)中的溶液(冷却至0℃)中逐份加入lioh(42.5mg,1.78mmol)。将反应混合物搅拌3小时,然后用1m hcl(10ml)稀释,并用etoac(20ml×3)萃取。合并有机相,用mgso4干燥并真空浓缩,得到棕色油状物(40.0mg)。水相用4:1=chcl3/ipa(30ml×3)进一步萃取。合并有机相,用mgso4干燥并真空浓缩,得到灰白色固体的(r)-4-乙酰基吗啉-2-羧酸(int-15,202mg,1.10mmol,59%收率,95%纯度)。1h nmr光谱描述了旋转异构体。
161、1h nmr(500mhz,25℃下,dmso-d6,旋转异构体)δ13.01(br s,1h),4.17(dt,j=10.7,3.3hz,1h),3.98(dd,j=9.2,3.4hz,0.5h),3.88(dt,j=11.5,3.4hz,0.5h),3.83-3.75(m,0.5h),3.70(dd,j=13.3,3.4hz,0.5h),3.68-3.61(m,0.5h),3.58(d,j=13.6hz,0.5h),3.49(qd,j=11.8,11.2,2.8hz,1.5h),3.27-3.15(m,1h),2.97(dd,j=13.3,9.2hz,0.5h),2.01(d,j=10.0hz,3h).
162、1h nmr(500mhz,90℃下,dmso-d6)δ4.15-3.93(m,1h),3.93-3.76(m,1h),3.65-3.46(m,2h),3.32-3.17(m,1h),3.13-2.82(m,2h),2.01(s,3h).未看到co2h峰.
163、实施例1
164、(s)-5,5,5-三氟-2-((2s,3s)-2-((s)-3-(4-羟基苯基)-2-(s)-四氢呋喃-2-甲酰氨基)丙酰氨基)-3-甲基戊酰氨基)戊酸
165、
166、(s)-2-((((9h-芴-9-基)甲氧基)羰基)氨基)-5,5,5-三氟戊酸的合成(int-16)
167、将wang树脂(上样量:1.0mmol/g,90.0mg,0.09mmol)在dcm(1ml)中溶胀10分钟并过滤,用dcm(3x 5ml)洗涤。(s)-2-((((9h-芴-9-基)甲氧基)羰基)氨基)-5,5,5-三氟戊酸(int-11,177mg,0.450mmol),1h-苯并[d][1,2,3]三唑-1-醇水合物(69.0mg,0.45mmol)、二异丙基碳二亚胺(70.0μl,0.45mmol),n-二甲基吡啶-4-胺(11.0mg,0.09mmol)和dcm(5ml),并将混合物在室温下搅拌18小时。过滤反应混合物,并用dmf(5ml×3)、dcm(5ml×3)、水(5ml×2)和dmf(5ml×3)洗涤。dcm(5ml)、(s)-2-((((9h-芴-9-基)甲氧基)羰基)氨基)-5,5,5-三氟戊酸(int-11,177mg,0.45mmol)、1h-苯并[d][1,2,3]三唑-1-醇水合物(69.0mg,0.45mol)、4-甲基吗啉(49.0μl,0.45mmol)、二异丙基碳二亚胺(69.7μl,0.45mmol)和将n,n-二甲基吡啶-4-胺(11.0mg,0.09mmol)加入到树脂中,并在室温下将悬浮液再轻轻搅拌12小时。将混合物过滤并用dmf(5ml×3)、dcm(5ml×3)、水(5ml×2)和dmf(5ml×3)洗涤,得到int-16。在这个阶段没有进行任何分析,在下一步中直接使用树脂。
168、(s)-2-[(2s,3s)-2-((((9h-芴-9-基)甲氧基)羰基)氨基)-3-甲基戊酰氨基)-5,5,5-三氟戊酸[树脂结合在c-末端]的合成(int-18)
169、将树脂结合的(s)-2-((((9h-芴-9-基)甲氧基)羰基)氨基)-5,5,5-三氟戊酸(int-16,90.0mg,0.09mmol)在dmf(1ml)中溶胀10分钟并过滤。将20%哌啶在dmf(5ml)中的溶液加入到溶胀的树脂中,并将悬浮液在室温下用氮气搅拌20分钟。过滤悬浮液,加入在dmf(5ml)中的20%哌啶,并在室温下用氮气搅拌悬浮液20分钟。过滤悬浮液,并用dmf(5ml×3)、dcm(5ml×3)、水(5ml×2)和dmf(5ml×3)洗涤。所获得的固体在没有进一步纯化的情况下使用。
170、加入dmf/dcm(1∶1,3ml)的混合物,然后加入(((9h-芴-9-基)甲氧基)羰基)-l-异亮氨酸(int-17,127mg,0.36mmol)、hatu(137mg,0.36mmol)和4-甲基吗啉(40.0μl,0.36mol)。悬浮液在室温下用氮气搅拌2小时,然后过滤并用dmf(5ml×3)、dcm(5ml×3)、水(5ml×2)和dmf(5ml×3)洗涤。加入dmf(3ml),然后加入(((9h-芴-9-基)甲氧基)羰基)-l-异亮氨酸(int-17,127mg,0.36mmol)、hatu(137mg,0.36mmol)和4-甲基吗啉(40.0μl,0.36mol)。悬浮液在室温下用氮气搅拌15小时,然后过滤并用dmf(5ml×3)、dcm(5ml×3)、水(5ml×2)和dmf(5ml×3)洗涤,得到int-18。将一小部分树脂加入0.5ml tfa中,并将悬浮液在室温下放置1小时。将悬浮液在真空中浓缩,得到(s)-2-((2s,3s)-2-([(9h-芴-9-基)甲氧基羰基)氨基]-3-甲基戊酰胺)-5,5,5-三氟戊酸(77%纯度),通过uplc进行分析。lcms(方法1,1.67分钟;m+h=507.4)。
171、(5s,8s,11s)-5-(4-(叔丁氧基)苄基)-8-((s)-仲丁基)-1-(9h-芴-9-基)-3,6,9-三氧基-11-(3,3,3-三氟丙基)-2-氧-4,7,10-三氮杂十二烷-12-酸的合成(int-20)
172、将树脂结合的(s)-2-((2s,3s)-2-((((9h-芴-9-基)甲氧基)羰基)氨基)-3-甲基戊酰胺)-5,5,5-三氟戊酸(int-18,90.0mg,0.09mmol)在dmf(1ml)中溶胀10分钟并过滤。将20%哌啶在dmf(5ml)中的溶液加入到溶胀的树脂中,并将悬浮液在室温下用氮气搅拌20分钟。过滤悬浮液,加入在dmf(5ml)中的20%哌啶,并在室温下用氮气搅拌悬浮液20分钟。过滤悬浮液,并用dmf(5ml×3)、dcm(5ml×3)、水(5ml×2)和dmf(5ml×3)洗涤。所获得的固体在没有进一步纯化的情况下使用。
173、加入dmf/dcm(1∶1,3ml)的混合物,然后加入(s)-2-((((9h-芴-9-基)甲氧基)羰基)氨基)-3-(4-(叔丁氧基)苯基)丙酸(int-19,165mg,0.36mmol)、hatu(137mg,0.36mmol)和4-甲基吗啉(40.0μl,0.36mol)。悬浮液在室温下用氮气搅拌2小时,然后过滤并用dmf(5ml×3)、dcm(5ml×3)、水(5ml×2)和dmf(5ml×3)洗涤。加入dmf(3ml),然后加入(s)-2-((((9h-芴-9-基)甲氧基)羰基)氨基)-3-(4-(叔丁氧基)苯基)丙酸(int-19,165mg,0.36mmol)、4-甲基吗啉(40.0μl,0.36mol)和hatu(137mg,0.36mmol)。将悬浮液在室温下用氮气搅拌16小时,然后过滤并用dmf(5ml×3)、dcm(5ml×3)、水(5ml×2)和dmf(5ml×3)洗涤得到int-20。将一小部分树脂加入0.5ml tfa中,并将悬浮液在室温下放置1小时。过滤悬浮液,并真空浓缩,得到(5s,8s,11s)-8-((s)-仲丁基)-1-(9h-芴-9-基)-5-(4-羟基苄基)-3,6,9-三氧基-11-(3,3,3-三氟丙基)-2-氧杂-4,7,10-三氮杂十二烷-12-酸(69%纯度),通过uplc进行分析。lcms(方法1,1.58分钟;m+h=670.5)。
174、(s)-2-[(2s,3s)-2-((s)-3-(4-(叔丁氧基)苯基)-2-(s)-四氢呋喃-2-甲酰氨基)-3-甲基戊酰氨基)-5,5,5-三氟戊酸[树脂结合在c-末端]的合成(int-22)
175、将树脂结合的(5s,8s,11s)-5-(4-(叔丁氧基)苄基)-8-((s)-仲丁基)-1-(9h-芴-9-基)-3,6,9-三氧基-11-(3,3,3-三氟丙基)-2-氧杂-4,7,10-三氮杂十二烷-12-酸(int-20,90.0mg,0.09mmol)在dmf(1ml)中溶胀10分钟并过滤。将20%哌啶在dmf(5ml)中的溶液加入到溶胀的树脂中,并将悬浮液在室温下用氮气搅拌20分钟。过滤悬浮液,加入在dmf(5ml)中的20%哌啶,并在室温下用氮气搅拌悬浮液20分钟。过滤悬浮液,并用dmf(5ml×3)、dcm(5ml×3)、水(5ml×2)和dmf(5ml×3)洗涤。所获得的固体在没有进一步纯化的情况下使用。
176、加入dmf/dcm(1∶1,3ml)的混合物,然后加入4-甲基吗啉(33.0μl,0.30mmol)、hatu(114mg,0.30mol)和(s)-四氢呋喃-2-羧酸(int-21,29.0μl,0.30mmol)。悬浮液在室温下用氮气搅拌2小时,然后过滤并用dmf(5ml×3)、dcm(5ml×3)、水(5ml×2)和dmf(5ml×3)洗涤。加入dmf(3ml),然后加入4-甲基吗啉(33.0μl,0.30mmol)、hatu(114mg,0.30mol)和(s)-四氢呋喃-2-羧酸(int-21,29.0μl,0.30mmol),并在室温下轻轻搅拌悬浮液12小时。过滤悬浮液并用dmf(5ml×3)、dcm(5ml×3)、水(5ml×2)和dmf(5ml×3)洗涤,得到int-22。在这个阶段没有进行任何分析,在下一步中直接使用树脂。
177、(s)-5,5,5-三氟-2-((2s,3s)-2-((s)-3-(4-羟基苯基)-2-(s)-四氢呋喃-2-甲酰氨基)-3-甲基戊酰氨基)戊酸的合成(实施例1)
178、将tfa/水(95∶5,1ml)的混合物加入树脂结合的(s)-2-((2s,3s)-2-(s)-3-(4-(叔丁氧基)苯基)-2-(四氢呋喃-2-甲酰氨基)-3-甲基戊酰氨基)-5,5,5-三氟戊酸(int-22,80.0mg,0.08mmol)中,并在室温下搅拌3小时。过滤反应混合物,并用dcm(20ml×3)洗涤树脂。将合并的滤液真空浓缩,并与甲苯(15ml×3)共沸。通过制备型hplc纯化粗产物,得到白色固体的(s)-5,5,5-三氟-2-((2s,3s)-2-((s)-3-(4-羟基苯基)-2-(s)-四氢呋喃-2-甲酰氨基)丙酰氨基)-3-甲基戊酰氨基)戊酸(实施例1,2.70mg,4.90μmol,6.5%,1h nmr纯度95%)。lcms 95%纯度(方法1,1.11分钟;m+h=546.7)。1h nmr(500mhz,dmso-d6)δ12.83(s,1h),9.14(s,1h),8.28(s,1h),7.93(d,j=8.6hz,1h),7.62(d,j=8.6hz,1h),6.99-6.88(m,2h),6.66-6.56(m,2h),4.49(td,j=8.8,4.4hz,1h),4.26-4.23(m,1h),4.18(t,j=8.0hz,1h),4.13(dd,j=8.1,4.6hz,1h),3.84(q,j=6.9hz,1h),3.72(dt,j=8.1,6.5hz,1h),2.90(dd,j=14.0,4.4hz,1h),2.76(dd,j=14.0,9.1hz,1h),2.29(ddd,j=50.1,23.9,9.6hz,2h),2.07-1.90(m,2h),1.86-1.77(m,1h),1.77-1.64(m,4h),1.52-1.35(m,1h),1.09(dt,j=14.9,7.9hz,1h),0.94-0.76(m,6h)。
179、
180、
181、
182、实施例5
183、(s)-2-((s)-2-(s)-3-(4-羟基苯基)-2-((s)-吡咯烷-2-甲酰氨基)丙酰氨基)-3-(吡啶-2-基)丙脒基)-5,5-二甲基己酸
184、
185、(s)-2-((((9h-芴-9-基)甲氧基)羰基)氨基)-5,5-二甲基己酸(int-24)的合成wang树脂(上样量:1.0mmol/g,650mg,0.65mmol)在室温下在dcm(30ml)中溶胀10分钟并过滤。加入dcm(30ml),然后加入(s)-2-((((9h-芴-9-基)甲氧基)羰基)氨基)-5,5-二甲基己酸(int-23,0.25g,0.65mmol)、dic(0.31ml,2.00mmol),1h-苯并[d][1,2,3]三唑-1-醇水合物(0.30g,2.0mmol)、4-甲基吗啉(0.21ml,2.00mmol)和dmap(79.0mg,0.65mmol)并将悬浮液在室温下轻轻搅拌16小时。过滤悬浮液,并用dmf(20ml×3)、dcm(20ml×3)、水(20ml×2)、dmf(20mgl×2)和dcm(20ml×2)洗涤。加入dcm/dmf(1∶1,30ml)的混合物,然后加入(s)-2-((((9h-芴-9-基)甲氧基)羰基)氨基)-5,5-二甲基己酸(int-23,0.25g,0.65mmol)、dic(0.31ml,2.00mmol。将悬浮液在室温下搅拌24小时,然后过滤并用dmf(5ml×2)、dcm(5ml×2)、水(5ml×2)、dmf(5ml×2)、dmf(20ml×2)和dcm(20ml×2)洗涤得到int-24。将一小部分树脂加入tfa(0.05ml)中,并将悬浮液在室温下放置1小时。过滤悬浮液,真空浓缩,得到(s)-2-((((9h-芴-9-基)甲氧基)羰基)氨基)-5,5-二甲基己酸(100%纯度),通过lcms进行分析。lcms(方法2,1.53分钟;m+na=404.1)。
186、(s)-2-((s)-2-[(((9h-芴-9-基)甲氧基)羰基)氨基)-3-(吡啶-2-基)丙酰氨基)-5,5-二甲基己酸的合成(int-26)
187、将树脂结合的(s)-2-((((9h-芴-9-基)甲氧基)羰基)氨基)-5,5-二甲基己酸(int-24,100mg,100μmol)在dmf(1ml)中溶胀10分钟,然后过滤。将20%哌啶在dmf(5ml)中的溶液加入到溶胀的树脂中,并将悬浮液在室温下用氮气搅拌20分钟。过滤悬浮液,并用dmf(5ml×2)、dcm(5ml×2)、水(5ml×2)、dcm(5ml×2)和dmf(5ml×2)洗涤。所获得的固体在没有进一步纯化的情况下使用。
188、加入dcm(2.6ml)和dmf(0.4ml),然后加入(s)-2-((((9h-芴-9-基)甲氧基)羰基)氨基)-3-(吡啶-2-基)丙酸(int-25155mg,0.40mmol)、hatu(152mg,0.40mmol)和4-甲基吗啉(44.0μl,0.40mol)。将反应物在室温下在氮气气氛下轻轻搅拌20小时,然后过滤并用dmf(5ml×2)、dcm(5ml×2)、水(5ml×2)、dcm(5ml×2)和dmf(5ml×3)洗涤,得到int-26。将一小部分树脂加入tfa(0.05ml)中,并在室温下搅拌30分钟。过滤悬浮液,用dcm(5ml)洗涤,合并的滤液在真空中浓缩,得到(s)-2-((((9h-芴-9-基)甲氧基)羰基)氨基)-3-(吡啶-2-基)丙酰氨基)-5,5-二甲基己酸(85%纯度),通过lcms分析。(方法2,1.60分钟;m+h=530.2)。
189、(5s,8s,11s)-5-(4-(叔丁氧基)苄基)-11-(3,3-二甲基丁基)-1-(9h-氟-9-基)-3,6,9-三氧代-8-(吡啶-2-基甲基)-2-氧-4,7,10-三氮杂十二烷-12-酸的合成(int-27)。
190、将树脂结合的(s)-2-((s)-2-((((9h-芴-9-基)甲氧基)羰基)氨基)-3-(吡啶-2-基)丙酰氨基)-5,5-二甲基己酸(int-26,50.0mg,50.0μmol)在dmf(1ml)中溶胀10分钟,然后过滤。将20%哌啶在dmf(5ml)中的溶液加入到溶胀的树脂中,并将悬浮液在室温下用氮气搅拌20分钟。过滤悬浮液,并用dmf(5ml×2)、dcm(5ml×2)、水(5ml×2)、dcm(5ml×2)和dmf(5ml×3)洗涤。所获得的固体在没有进一步纯化的情况下使用。
191、加入dcm(2.6ml)和dmf(0.4ml),然后加入(s)-2-((((9h-芴-9-基)甲氧基)羰基)氨基)-3-(4-(叔丁氧基)苯基)丙酸(int-19,92.0mg,0.20mmol)、hatu(76.0mg,0.20mmol)和4-甲基吗啉(22.0μl,0.20mmol)。将反应物在室温下在氮气气氛下轻轻搅拌3天,然后过滤并用dmf(5ml×2)、dcm(5ml×2)、水(5ml×2)、dcm(5ml×2)和dmf(5ml×3)洗涤,得到int-27。将一小部分树脂加入tfa(0.05ml)中,并在室温下搅拌30分钟。悬浮液用dcm(5ml)稀释,过滤,滤液真空浓缩,得到(5s,8s,11s)-11-(3,3-二甲基丁基)-1-(9h-芴-9-基)-5-(4-羟基苄基)-3,6,9-三氧代-8-(吡啶-2-基甲基)-2-氧杂-4,7,10-三氮杂十二烷-12-酸(86%纯度),通过lcms进行分析。lcms(方法2,1.56分钟;m+h=693.3)。
192、(s)-2-((s)-2-[(s)-3-(4-(叔丁氧基)苯基)-2-(s)-1-(叔丁氧基羰基)吡咯烷-2-甲酰氨基)丙酰氨基)-3-(吡啶-2-基)丙脒基)-5,5-二甲基己酸的合成(int-29)
193、将树脂结合的(5s,8s,11s)-5-(4-(叔丁氧基)苄基)-11-(3,3-二甲基丁基)-1-(9h-氟-9-基)-3,6,9-三氧代-8-(吡啶-2-基甲基)-2-氧杂-4,7,10-三氮杂十二烷-12-酸(int-27,50.0mg,0.05mmol)在dmf(5ml)中溶胀10分钟,然后过滤。将20%哌啶在dmf(5ml)中的溶液加入到溶胀的树脂中,并将悬浮液在室温下用氮气搅拌20分钟。过滤悬浮液,并用dmf(5ml x 2)、dcm(5ml×2)、水(5ml x 2)、dcm5ml x 3和dmf(5ml x 3)洗涤。所获得的固体在没有进一步纯化的情况下使用。
194、加入dcm(2.6ml)和dmf(0.4ml),加入(叔丁氧羰基)-l-脯氨酸(int-28,43.0mg,0.20mmol)、hatu(76.0mg,0.20mmol)和4-甲基吗啡(22.0μl,0.20mmol)。将反应物在氮气气氛下轻轻搅拌20小时。将悬浮液过滤并用dmf(5ml x 2)、dcm(5ml×2)、水(5ml x 2)、dcm[5ml×3]和dmf(5ml x 3)洗涤得到int-29。在这个阶段没有进行分析,在下一步中直接使用树脂。
195、(s)-2-((s)-2-[(s)-3-(4-羟基苯基)-2-(s)-吡咯烷-2-甲酰氨基)丙酰氨基)-3-(吡啶-2-基)丙脒基)-5,5-二甲基己酸的合成(实施例5)
196、将tfa(0.38ml,5.00mmol)加入到树脂结合的(s)-2-((s)-2-((s,(s)-3-(4-(叔丁氧基)苯基)-2-(s)-1-(叔丁氧基羰基)吡咯烷-2-甲酰氨基)丙酰氨基)-3-(吡啶-2-基)丙酰氨基)-5,5-二甲基己酸中(int-29,50.0mg,50.0μmol),并在室温下搅拌3小时。过滤悬浮液,用dcm(5ml×3)洗涤,滤液真空浓缩并与甲苯(5ml×3)共沸。通过制备型hplc纯化粗产物,得到无色固体的(s)-2-((s)-3-(4-羟基苯基)-2-(s)-吡咯烷-2-甲酰氨基)丙酰氨基)-3-(吡啶-2-基)丙脒基)-5,5-二甲基己酸(实施例5,2.00mg,3.00μmol,7.0%收率,1h nmr纯度97%)。由于发色团较弱,lcms纯度未得到确认。(方法2,1.18分钟;m+h=568.3)。1hnmr(500mhz,dmso-d6)δ12.70(s,1h),9.21(s,1h),9.13(s,1h),8.57(d,j=8.5hz,1h),8.46-8.43(m,2h),8.41-8.38(m,1h),8.36(d,j=8.4hz,1h),8.30(d,j=7.7hz,1h),7.29(d,j=5.9hz,1h),7.01(d,j=8.5hz,2h),6.64-6.61(m,2h),4.73-4.65(m,1h),4.50-4.43(m,1h),4.21-4.13(m,1h),4.07-4.01(m,1h),3.24-3.10(m,3h),3.07(dd,j=14.0,4.4hz,1h),2.88(dd,j=14.1,4.0hz,1h),2.82(dd,j=14.0,9.5hz,1h),2.64-2.54(m,1h),2.26-2.16(m,1h),1.91-1.65(m,3h),1.64-1.54(m,1h),1.27-1.17(m,2h),0.86(s,9h)。
197、
198、
199、
200、
201、
202、
203、
204、
205、
206、
207、
208、
209、
210、
211、
212、
213、
214、
215、
216、
217、
218、
219、
220、
221、
222、
223、
224、
225、
226、
227、
228、
229、
230、
231、
232、
233、生物学数据
234、神经降压素闪烁邻近测定
235、在神经降压素(nts)闪烁邻近测定(spa)中测试的示例性本发明化合物的数据。ic50数据如下表6所示。nts是一种13个氨基酸的神经肽,是分拣蛋白配体。ic50是抑制nts与分拣蛋白结合50%所需的化合物量的量度。本领域技术人员将认识到,ic50值越低,实现所需效果所需的化合物就越少,因此,降低了不希望的脱靶效果的几率。
236、通过以spa形式测定[3h]神经降压素与h分拣蛋白结合的位移来测定化合物亲和力。在含有100mm nacl、2.0mm cacl2、0.1%bsa和0.1%吐温-20的50mm hepes ph 7.4测定缓冲液中的总体积为40μl。在添加5nm[3h]-神经降压素和ni螯合物成像珠(perkin-elmer)之前,化合物在室温下用150nm的6his-分拣蛋白预孵育30分钟,在viewlux上以360s的暴露时间读取6小时的板。使用8种浓度的药物(覆盖30年)对化合物进行剂量反应评估。ic50值通过非线性回归使用s型浓度响应(可变斜率)使用cdd-vault软件计算。报告的所有值均为至少2次测定的平均值。
237、下表6中的数据表明本文公开的化合物是分拣蛋白抑制剂。
238、表6
239、
240、
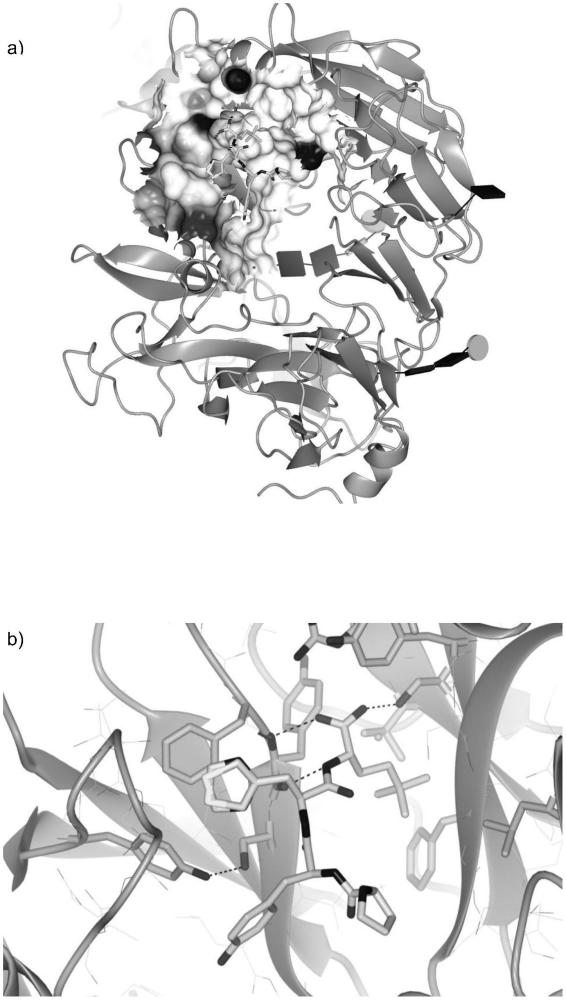
241、结合h-分拣蛋白的实施例12的化合物的x-射线衍生照片
242、材料和方法
243、ssortilin,分拣蛋白的管腔结构域,按如前所述获得(andersen等人,actacrystal.d,2017)19。结晶前,12μl的在50mm ph 8.0的tris-hcl,150mm nacl中的4mg/mlssortilin,与1.2μl的分别以16.7mm和13.2mm的浓度溶解在dmso中两种化合物ins1767和ins1783混合。
244、通过添加2μl分拣蛋白配体混合物至2μl由100mm hepes ph 7.3、400mm丙二酸ph7.3、8%v/v甘油、22.5%w/v peg3350组成的储备液设置坐滴。通过用500μl储备液蒸汽扩散进行坐滴的平衡。
245、在没有进一步冷冻保护的情况下将晶体安装在石蜡环中,并在液氮中快速冷却。
246、在光束线p13(embl/desy,汉堡)收集衍射数据,并使用xds软件包(kabsch,w.,acta cryst.d,2010)18进行加工(表1)。使用分拣蛋白的已知结构(pdb条目:3f6k)作为搜索模型和在phenix软件包(afonine等人,acta crystal.d,2012)21中实现的程序phaser,通过分子置换获得结构因子的相位。通过在coot(emsley p.等人,acta cryst.d,2010)22中的几个模型构建周期和使用phenix的最大似然精化来获得精化模型。得到的实施例12化合物与h-分拣蛋白结合的x射线衍生照片如图1a)和1b)所示。下表7显示了精化统计数据以及模型与标准几何结构的一致性。
247、表7:精化统计以及模型与标准几何结构的和一致性(括号中显示了最高分辨率范围的统计信息)
248、
249、
250、
251、参考文献
252、1.tauris,j.,et al.,proneurotrophin-3may induce sortilin-dependentdeath in inner ear neurons.eur j neuroscience(2020),33(4),pp.622-31.
253、2.goettsch,c.,et al.,sortilin and its multiple roles incardiovascular and metabolic diseases.atherosclerosis,thrombosis and vascularbiology(2017),38(1),pp.19-25.
254、3.willnow,t.e.,et al.,sortilins:new players in lipoproteinmetabolism.current opinion in lipidology(2011),22(2),pp.79-85.
255、4.kjolby,m.,et al.,sort1,encoded by the cardiovascular risk locus1p13.3,is a regulator of hepatic lipoprotein export.cell metabolism(2010),12(3),pp.213-223.
256、5.jansen,p.,et al.,roles for the pro-neurotrophin receptor sortilinin neuronal development,aging and brain injury.nature neuroscience(2007),10(11),pp.1449-1457.
257、6.tenk,h.k.,et al.,probdnf induces neuronal apoptosis via activationof a receptor complex of p75ntr and sortilin.j neuroscience(2005),10(11),pp.1449-1457.
258、7.nykjaer,a.,et al.,sortilin is essential for prongf-induced neuronalcell death.nature(2004),427(6977),pp.843-848.
259、8.huang,g.et al.,insulin responsiveness of glucose transporter 4in3t3-l1cells depends on the presence of sortilin.mol biol cell(2013),24(19),pp.3115-3122.
260、9.pan,x.et al.,sortilin and retromer mediate retrograde transport ofglut4 in 3t3-l1 adipocytes.mol biol cell(2017),28(12),pp.1667-1675.
261、10.kaddai,v.et al.involvement of tnf-αin abnormal adipocyte andmuscle sortilin expression in obese mice and humans.diabetologia(2009)52,pp.932-940.
262、11.mortensen,m.b.et al.,targeting sortilin in immune cells reducesproinflammatory cytokines and atherosclerosis.j clin invest(2014),124(12),pp.5317-5322.
263、12.shi,j.&kandror,k.v.,sortilin is essential and sufficient for theformation of glut4 storage vesicles in 3t3-l1 adipocytes.developmental cell(2005),9,pp.99-108.
264、13.gao,a.et al.,implications of sortilin in lipid metabolism andlipid disorder diseases.dna and cell biology(2017),36(12),pp.1050-1061.
265、14.oh,t.j.et al.,circulating sortilin level as a potential biomarkerfor coronary atherosclerosis and diabetes mellitus.cardiovascular diabetology(2017),16(92).
266、15.santos,a.m.et al.,sortilin participates in light-dependentphotoreceptor degeneration in vivo.plos one(2012),7(4),pp.e36243-e36243.16.kuruvilla,r.et al.,a neurotrophin signaling cascade coordinatessympathetic neuron development through differential control of trkatrafficking and retrograde signalling.cell(2004),118(2),pp.243-255.
267、17.skeldal,s.et al.,mapping of the interaction site between sortilinand the p75 neurotrophin receptor reveals a regulatory role for the sortilinintracellular domain in p75 neurotrophin receptor shedding and apoptosis.jbiol chem(2012),21(287),pp.43798-43809.
268、18.wuts,p.g.m.and greene,t.w,greene’s protective groups in organicsynthesis,4th edition,john wiley and sons,new york(2006).
269、19.andersen,k r et al.,introducing site-specific cysteines intonanobodies for mercury labelling allows de novo phasing of their crystalstructures.acta crystallographia section.d(2017),73(1),pp.804-813.
270、20.kabsch,w,xds.acta crystallographia section.d(2010),66(2),pp.125-132.
271、21.afonine,p v et al.,acta crystallographia section.d(2012),68(4),pp.352-367.
272、22.emsley,p.et al.,acta crystallographia section.d(2010),66(4),pp.486-501.整个说明书中引用的序列,并构成说明书的一部分seq id no:1(全长分拣蛋白异构体1)
273、
274、seq id no:2(全长分拣蛋白异构体2)
275、
276、
277、seq id no:3(成熟分拣蛋白)
278、
279、 序列表
280、<110> 因苏森斯有限公司
281、<120> 化合物
282、<130> rmc00233wo
283、<150> ep21173972.7
284、<151> 2021-05-14
285、<160> 3
286、<170> patentin version 3.5
287、<210> 1
288、<211> 831
289、<212> prt
290、<213> 智人(homo sapiens)
291、<400> 1
292、met glu arg pro trp gly ala ala asp gly leu ser arg trp pro his
293、1 5 10 15
294、gly leu gly leu leu leu leu leu gln leu leu pro pro ser thr leu
295、 20 25 30
296、ser gln asp arg leu asp ala pro pro pro pro ala ala pro leu pro
297、 35 40 45
298、arg trp ser gly pro ile gly val ser trp gly leu arg ala ala ala
299、 50 55 60
300、ala gly gly ala phe pro arg gly gly arg trp arg arg ser ala pro
301、65 70 75 80
302、gly glu asp glu glu cys gly arg val arg asp phe val ala lys leu
303、 85 90 95
304、ala asn asn thr his gln his val phe asp asp leu arg gly ser val
305、 100 105 110
306、ser leu ser trp val gly asp ser thr gly val ile leu val leu thr
307、 115 120 125
308、thr phe his val pro leu val ile met thr phe gly gln ser lys leu
309、 130 135 140
310、tyr arg ser glu asp tyr gly lys asn phe lys asp ile thr asp leu
311、145 150 155 160
312、ile asn asn thr phe ile arg thr glu phe gly met ala ile gly pro
313、 165 170 175
314、glu asn ser gly lys val val leu thr ala glu val ser gly gly ser
315、 180 185 190
316、arg gly gly arg ile phe arg ser ser asp phe ala lys asn phe val
317、 195 200 205
318、gln thr asp leu pro phe his pro leu thr gln met met tyr ser pro
319、 210 215 220
320、gln asn ser asp tyr leu leu ala leu ser thr glu asn gly leu trp
321、225 230 235 240
322、val ser lys asn phe gly gly lys trp glu glu ile his lys ala val
323、 245 250 255
324、cys leu ala lys trp gly ser asp asn thr ile phe phe thr thr tyr
325、 260 265 270
326、ala asn gly ser cys lys ala asp leu gly ala leu glu leu trp arg
327、 275 280 285
328、thr ser asp leu gly lys ser phe lys thr ile gly val lys ile tyr
329、 290 295 300
330、ser phe gly leu gly gly arg phe leu phe ala ser val met ala asp
331、305 310 315 320
332、lys asp thr thr arg arg ile his val ser thr asp gln gly asp thr
333、 325 330 335
334、trp ser met ala gln leu pro ser val gly gln glu gln phe tyr ser
335、 340 345 350
336、ile leu ala ala asn asp asp met val phe met his val asp glu pro
337、 355 360 365
338、gly asp thr gly phe gly thr ile phe thr ser asp asp arg gly ile
339、 370 375 380
340、val tyr ser lys ser leu asp arg his leu tyr thr thr thr gly gly
341、385 390 395 400
342、glu thr asp phe thr asn val thr ser leu arg gly val tyr ile thr
343、 405 410 415
344、ser val leu ser glu asp asn ser ile gln thr met ile thr phe asp
345、 420 425 430
346、gln gly gly arg trp thr his leu arg lys pro glu asn ser glu cys
347、 435 440 445
348、asp ala thr ala lys asn lys asn glu cys ser leu his ile his ala
349、 450 455 460
350、ser tyr ser ile ser gln lys leu asn val pro met ala pro leu ser
351、465 470 475 480
352、glu pro asn ala val gly ile val ile ala his gly ser val gly asp
353、 485 490 495
354、ala ile ser val met val pro asp val tyr ile ser asp asp gly gly
355、 500 505 510
356、tyr ser trp thr lys met leu glu gly pro his tyr tyr thr ile leu
357、 515 520 525
358、asp ser gly gly ile ile val ala ile glu his ser ser arg pro ile
359、 530 535 540
360、asn val ile lys phe ser thr asp glu gly gln cys trp gln thr tyr
361、545 550 555 560
362、thr phe thr arg asp pro ile tyr phe thr gly leu ala ser glu pro
363、 565 570 575
364、gly ala arg ser met asn ile ser ile trp gly phe thr glu ser phe
365、 580 585 590
366、leu thr ser gln trp val ser tyr thr ile asp phe lys asp ile leu
367、 595 600 605
368、glu arg asn cys glu glu lys asp tyr thr ile trp leu ala his ser
369、 610 615 620
370、thr asp pro glu asp tyr glu asp gly cys ile leu gly tyr lys glu
371、625 630 635 640
372、gln phe leu arg leu arg lys ser ser met cys gln asn gly arg asp
373、 645 650 655
374、tyr val val thr lys gln pro ser ile cys leu cys ser leu glu asp
375、 660 665 670
376、phe leu cys asp phe gly tyr tyr arg pro glu asn asp ser lys cys
377、 675 680 685
378、val glu gln pro glu leu lys gly his asp leu glu phe cys leu tyr
379、 690 695 700
380、gly arg glu glu his leu thr thr asn gly tyr arg lys ile pro gly
381、705 710 715 720
382、asp lys cys gln gly gly val asn pro val arg glu val lys asp leu
383、 725 730 735
384、lys lys lys cys thr ser asn phe leu ser pro glu lys gln asn ser
385、 740 745 750
386、lys ser asn ser val pro ile ile leu ala ile val gly leu met leu
387、 755 760 765
388、val thr val val ala gly val leu ile val lys lys tyr val cys gly
389、 770 775 780
390、gly arg phe leu val his arg tyr ser val leu gln gln his ala glu
391、785 790 795 800
392、ala asn gly val asp gly val asp ala leu asp thr ala ser his thr
393、 805 810 815
394、asn lys ser gly tyr his asp asp ser asp glu asp leu leu glu
395、 820 825 830
396、<210> 2
397、<211> 830
398、<212> prt
399、<213> 智人(homo sapiens)
400、<400> 2
401、met glu arg pro trp gly ala ala asp gly leu ser arg trp pro his
402、1 5 10 15
403、gly leu gly leu leu leu leu leu gln leu leu pro pro ser thr leu
404、 20 25 30
405、ser gln asp arg leu asp ala pro pro pro pro ala ala pro leu pro
406、 35 40 45
407、arg trp ser gly pro ile gly val ser trp gly leu arg ala ala ala
408、 50 55 60
409、ala gly gly ala phe pro arg gly gly arg trp arg arg ser ala pro
410、65 70 75 80
411、gly glu asp glu glu cys gly arg val arg asp phe val ala lys leu
412、 85 90 95
413、ala asn asn thr his gln his val phe asp asp leu arg gly ser val
414、 100 105 110
415、ser leu ser trp val gly asp ser thr gly val ile leu val leu thr
416、 115 120 125
417、thr phe his val pro leu val ile met thr phe gly gln ser lys leu
418、 130 135 140
419、tyr arg ser glu asp tyr gly lys asn phe lys asp ile thr asp leu
420、145 150 155 160
421、ile asn asn thr phe ile arg thr glu phe gly met ala ile gly pro
422、 165 170 175
423、glu asn ser gly lys val val leu thr ala glu val ser gly gly ser
424、 180 185 190
425、arg gly gly arg ile phe arg ser ser asp phe ala lys asn phe val
426、 195 200 205
427、gln thr asp leu pro phe his pro leu thr gln met met tyr ser pro
428、 210 215 220
429、gln asn ser asp tyr leu leu ala leu ser thr glu asn gly leu trp
430、225 230 235 240
431、val ser lys asn phe gly gly lys trp glu glu ile his lys ala val
432、 245 250 255
433、cys leu ala lys trp gly ser asp asn thr ile phe phe thr thr tyr
434、 260 265 270
435、ala asn gly ser cys thr asp leu gly ala leu glu leu trp arg thr
436、 275 280 285
437、ser asp leu gly lys ser phe lys thr ile gly val lys ile tyr ser
438、 290 295 300
439、phe gly leu gly gly arg phe leu phe ala ser val met ala asp lys
440、305 310 315 320
441、asp thr thr arg arg ile his val ser thr asp gln gly asp thr trp
442、 325 330 335
443、ser met ala gln leu pro ser val gly gln glu gln phe tyr ser ile
444、 340 345 350
445、leu ala ala asn asp asp met val phe met his val asp glu pro gly
446、 355 360 365
447、asp thr gly phe gly thr ile phe thr ser asp asp arg gly ile val
448、 370 375 380
449、tyr ser lys ser leu asp arg his leu tyr thr thr thr gly gly glu
450、385 390 395 400
451、thr asp phe thr asn val thr ser leu arg gly val tyr ile thr ser
452、 405 410 415
453、val leu ser glu asp asn ser ile gln thr met ile thr phe asp gln
454、 420 425 430
455、gly gly arg trp thr his leu arg lys pro glu asn ser glu cys asp
456、 435 440 445
457、ala thr ala lys asn lys asn glu cys ser leu his ile his ala ser
458、 450 455 460
459、tyr ser ile ser gln lys leu asn val pro met ala pro leu ser glu
460、465 470 475 480
461、pro asn ala val gly ile val ile ala his gly ser val gly asp ala
462、 485 490 495
463、ile ser val met val pro asp val tyr ile ser asp asp gly gly tyr
464、 500 505 510
465、ser trp thr lys met leu glu gly pro his tyr tyr thr ile leu asp
466、 515 520 525
467、ser gly gly ile ile val ala ile glu his ser ser arg pro ile asn
468、 530 535 540
469、val ile lys phe ser thr asp glu gly gln cys trp gln thr tyr thr
470、545 550 555 560
471、phe thr arg asp pro ile tyr phe thr gly leu ala ser glu pro gly
472、 565 570 575
473、ala arg ser met asn ile ser ile trp gly phe thr glu ser phe leu
474、 580 585 590
475、thr ser gln trp val ser tyr thr ile asp phe lys asp ile leu glu
476、 595 600 605
477、arg asn cys glu glu lys asp tyr thr ile trp leu ala his ser thr
478、 610 615 620
479、asp pro glu asp tyr glu asp gly cys ile leu gly tyr lys glu gln
480、625 630 635 640
481、phe leu arg leu arg lys ser ser val cys gln asn gly arg asp tyr
482、 645 650 655
483、val val thr lys gln pro ser ile cys leu cys ser leu glu asp phe
484、 660 665 670
485、leu cys asp phe gly tyr tyr arg pro glu asn asp ser lys cys val
486、 675 680 685
487、glu gln pro glu leu lys gly his asp leu glu phe cys leu tyr gly
488、 690 695 700
489、arg glu glu his leu thr thr asn gly tyr arg lys ile pro gly asp
490、705 710 715 720
491、lys cys gln gly gly val asn pro val arg glu val lys asp leu lys
492、 725 730 735
493、lys lys cys thr ser asn phe leu ser pro glu lys gln asn ser lys
494、 740 745 750
495、ser asn ser val pro ile ile leu ala ile val gly leu met leu val
496、 755 760 765
497、thr val val ala gly val leu ile val lys lys tyr val cys gly gly
498、 770 775 780
499、arg phe leu val his arg tyr ser val leu gln gln his ala glu ala
500、785 790 795 800
501、asn gly val asp gly val asp ala leu asp thr ala ser his thr asn
502、 805 810 815
503、lys ser gly tyr his asp asp ser asp glu asp leu leu glu
504、 820 825 830
505、<210> 3
506、<211> 694
507、<212> prt
508、<213> 智人(homo sapiens)
509、<400> 3
510、met thr phe gly gln ser lys leu tyr arg ser glu asp tyr gly lys
511、1 5 10 15
512、asn phe lys asp ile thr asp leu ile asn asn thr phe ile arg thr
513、 20 25 30
514、glu phe gly met ala ile gly pro glu asn ser gly lys val val leu
515、 35 40 45
516、thr ala glu val ser gly gly ser arg gly gly arg ile phe arg ser
517、 50 55 60
518、ser asp phe ala lys asn phe val gln thr asp leu pro phe his pro
519、65 70 75 80
520、leu thr gln met met tyr ser pro gln asn ser asp tyr leu leu ala
521、 85 90 95
522、leu ser thr glu asn gly leu trp val ser lys asn phe gly gly lys
523、 100 105 110
524、trp glu glu ile his lys ala val cys leu ala lys trp gly ser asp
525、 115 120 125
526、asn thr ile phe phe thr thr tyr ala asn gly ser cys thr asp leu
527、 130 135 140
528、gly ala leu glu leu trp arg thr ser asp leu gly lys ser phe lys
529、145 150 155 160
530、thr ile gly val lys ile tyr ser phe gly leu gly gly arg phe leu
531、 165 170 175
532、phe ala ser val met ala asp lys asp thr thr arg arg ile his val
533、 180 185 190
534、ser thr asp gln gly asp thr trp ser met ala gln leu pro ser val
535、 195 200 205
536、gly gln glu gln phe tyr ser ile leu ala ala asn asp asp met val
537、 210 215 220
538、phe met his val asp glu pro gly asp thr gly phe gly thr ile phe
539、225 230 235 240
540、thr ser asp asp arg gly ile val tyr ser lys ser leu asp arg his
541、 245 250 255
542、leu tyr thr thr thr gly gly glu thr asp phe thr asn val thr ser
543、 260 265 270
544、leu arg gly val tyr ile thr ser val leu ser glu asp asn ser ile
545、 275 280 285
546、gln thr met ile thr phe asp gln gly gly arg trp thr his leu arg
547、 290 295 300
548、lys pro glu asn ser glu cys asp ala thr ala lys asn lys asn glu
549、305 310 315 320
550、cys ser leu his ile his ala ser tyr ser ile ser gln lys leu asn
551、 325 330 335
552、val pro met ala pro leu ser glu pro asn ala val gly ile val ile
553、 340 345 350
554、ala his gly ser val gly asp ala ile ser val met val pro asp val
555、 355 360 365
556、tyr ile ser asp asp gly gly tyr ser trp thr lys met leu glu gly
557、 370 375 380
558、pro his tyr tyr thr ile leu asp ser gly gly ile ile val ala ile
559、385 390 395 400
560、glu his ser ser arg pro ile asn val ile lys phe ser thr asp glu
561、 405 410 415
562、gly gln cys trp gln thr tyr thr phe thr arg asp pro ile tyr phe
563、 420 425 430
564、thr gly leu ala ser glu pro gly ala arg ser met asn ile ser ile
565、 435 440 445
566、trp gly phe thr glu ser phe leu thr ser gln trp val ser tyr thr
567、 450 455 460
568、ile asp phe lys asp ile leu glu arg asn cys glu glu lys asp tyr
569、465 470 475 480
570、thr ile trp leu ala his ser thr asp pro glu asp tyr glu asp gly
571、 485 490 495
572、cys ile leu gly tyr lys glu gln phe leu arg leu arg lys ser ser
573、 500 505 510
574、val cys gln asn gly arg asp tyr val val thr lys gln pro ser ile
575、 515 520 525
576、cys leu cys ser leu glu asp phe leu cys asp phe gly tyr tyr arg
577、 530 535 540
578、pro glu asn asp ser lys cys val glu gln pro glu leu lys gly his
579、545 550 555 560
580、asp leu glu phe cys leu tyr gly arg glu glu his leu thr thr asn
581、 565 570 575
582、gly tyr arg lys ile pro gly asp lys cys gln gly gly val asn pro
583、 580 585 590
584、val arg glu val lys asp leu lys lys lys cys thr ser asn phe leu
585、 595 600 605
586、ser pro glu lys gln asn ser lys ser asn ser val pro ile ile leu
587、 610 615 620
588、ala ile val gly leu met leu val thr val val ala gly val leu ile
589、625 630 635 640
590、val lys lys tyr val cys gly gly arg phe leu val his arg tyr ser
591、 645 650 655
592、val leu gln gln his ala glu ala asn gly val asp gly val asp ala
593、 660 665 670
594、leu asp thr ala ser his thr asn lys ser gly tyr his asp asp ser
595、 675 680 685
596、asp glu asp leu leu glu
597、 690
- 还没有人留言评论。精彩留言会获得点赞!