一种用于系统性红斑狼疮患者无创诊断的口腔微生物基因标志物及其临床应用
本发明属于生物医药,具体涉及一种用于系统性红斑狼疮患者无创诊断的口腔微生物基因标志物及其临床应用。
背景技术:
1、系统性红斑狼疮(systemic lupus erythematosus,sle)是一种以血清中出现多种自身抗体、临床上出现多器官多系统受累为主要表现的自身免疫性疾病,是自身免疫病的原型。sle的发病机制尚不清楚,可能与遗传、表观遗传、免疫紊乱、种族、激素和环境等多种因素有关。该病主要累及育龄期女性,女性发病率约为男性的9-11倍。近年来,其发病率较前有所上升,这可能与诊断手段的提高有关系。sle可累皮肤黏膜、关节肌肉等器官,也可累及呼吸系统、心血管系统、肾脏、中枢神经系统及血液系统等内脏器官,其临床表现呈个体化特点。sle的治疗主要为糖皮质激素及免疫抑制剂,近年来越来越多的生物制剂应用于sle的治疗。
2、正常人体寄居的细菌种类超过1000种,数量高达100万亿。这些数量庞大的微生物和人体内环境相互作用,共同构成了人体微生态系统。近年来,越来越多的研究显示肠道微生态紊乱与sle的发生发展密切相关。sle的肠道微生物多样性减少,且肠道微生物的变化与sle疾病活动度相关。此外,肠道微生态系统可通过分子模拟、调节t细胞、以及调节i型干扰素的表达等多种途径参与sle的发生发展。口腔微生态系统作为消化系统的起始端,是人体微生态系统的重要组成部分,与人体健康和疾病密切相关。目前从口腔中分离和鉴定出来的细菌种类已经达到700余种。口腔菌群和宿主共生并共进化过程中,在调节宿主的消化吸收、免疫反应、代谢、炎症等方面发挥重要作用。口腔微生态失调促进慢性疾病、系统性疾病的发生发展,包括龋齿、类风湿关节炎、心血管疾病、结肠癌、颈部鳞状细胞癌等。
3、口腔微生物中关健功能菌可成为人类疾病的新型生物标志物。越来越多的研究发现口腔微生态的特征或者基于口腔微生物建立的区别模型可作为某些特定疾病的区分工具。burkhardt f等通过宏基因组学报道了口腔微生态与结直肠癌的相关性,指出16个菌种可能成为区分结直肠癌的口腔微生物标志物。zhang x等通过宏基因组测序技术解析了中国人群类风湿关节炎患者的口腔微生态结果,在微生物基因和功能水平上,鉴定了类风湿关节炎特异性的6个牙齿微生物标志物和2个唾液微生物标志物,创建了两个高准确度的类风湿关节炎区分模型。yang l等指出,口腔微生态的改变与艾滋病毒感染者的肺部功能损害及系统炎症密切相关。口腔微生物可以作为预测艾滋病感染者肺功能的标志物,并且口腔微环境稳态的破坏有助于慢性阻塞性肺疾病的病理发展。farrell j等(gut,2012)揭示了胰腺癌患者的口腔微生态特征,并鉴定出胰腺癌患者的2个口腔微生物标志物,建立了一个高准确度的胰腺癌患者区分模型。我们通过分析新型冠状病毒感染感染者和非感染者的口腔微生物特征,鉴定了新型冠状病毒感染特异性的8个口腔微生物标志物,并构建了一个用于区别新型冠状病毒感染和非感染者的口腔微生物模型。因而,口腔微生物是不同疾病诊断的有力工具。然而,目前用于区别系统性红斑狼疮患者和健康人群的口腔微生物模型还未曾报道过。
技术实现思路
1、本发明提供了一种用于区别系统性红斑狼疮患者和健康人群的口腔微生物基因标志物(微生物模型),由seq id no:1-2所示的2种微生物基因组成,所述微生物基因在人体口腔中富集。
2、>otu49
3、cctacgggtggctgcagtgaggaatattggtcaatgggcgagagcctgaaccagccaagtcgcgtgaaggatgacggccctatgggttgtaaacttcttttgcaggggaataaagatattcacgtgtggatagttgtatgtaccctgcgaataagcatcggctaactccgtgccagcagccgcggtaatacggaggatgcgagcgttatccggatttattgggtttaaagggtgcgtaggtggactgttaagtcagtggtgaaagtttgtcgctcaacgataaaattgccgttgaaactggtggtcttgagtatggatgaagtaggcggaatgcgtggtgtagcggtgaaatgcatagagatcacgcagaactccgattgcgaaggcagcttactaaggcataactgacactgaagcacgaaagcgtgggtatcaaacaggattagataccctagtagtc
4、>otu71
5、cctacgggtggctgcagtggggaatcttccgcaatgggcgaaagcctgacggagcaacgccgcgtgagtgatgacggccttcgggttgtaaaactctgtgatccgggacgaaaaggcagagtgcgaagaacaaactgcattgacggtaccggaaaagcaagccacggctaactacgtgccagcagccgcggtaatacgtaggtggcaagcgttgtccggaattattgggcgtaaagcgcgcgcaggcggcttcccaagtccctcttaaaagtgcggggcttaaccccgtgatgggaaggaaactgggaagctggagtatcggagaggaaagtggaattcctagtgtagcggtgaaatgcgtagagattaggaagaacaccggtggcgaaggcgactttctggacgaaaactgacgctgaggcgcgaaagcgtggggagcaaacaggattagataccctagtagtc
6、另外本发明还提供了一种用于检测试剂,包括用于检测seq id no:1-2所示的2种微生物基因的引物,序列如下:
7、所述引物序列为seq id no:3-4。
8、引物primers
9、测序区域v3+v4:341f-805r
10、上游引物:5’-cctacgggnggcwgcag-3’
11、下游引物:5’-gactachvgggtatctaatcc-3
12、本发明还提供了检测试剂在建立一种区别系统性红斑狼疮和健康人群的口腔微生物模型中的应用,所述检测试剂适用于检测seq id no:1-2所示的2种微生物基因。
13、所述微生物区别模型适用于区别系统性红斑狼疮和健康人群,系统性红斑狼疮者指符合1997年美国风湿病学院关于系统性红斑狼疮的分类标准,且未使用过糖皮质激素和免疫抑制剂的患者。
14、对所述对象的舌苔进行检测,以便确定该样本是否包含所述的微生物基因,是否可以建立区别系统性红斑狼疮和健康人群的微生物基因模型。
15、通过收集入组对象的舌苔样本,抽提微生物总dna,完成微生物dna的16s rdnamiseq测序,检测是否存在seq id no:1-2所示的2种微生物基因。
16、进一步的,通过收集入组对象的舌苔样本,抽提微生物总dna,进行口腔菌群的16srdna miseq测序。基于高通量测序数据,在训练集中建立系统性红斑狼疮和健康人群的微生物区别模型,建立系统性红斑狼疮患病率(probability of disease,pod)指数;pod指数在验证集中计算其区别能力,进行验证;进一步在来自不同地域的独立诊断集中进行独立验证,实现微生物基因区别模型在中国系统性红斑狼疮人群中的普适性。
17、具体包括:
18、(1)收集入组对象(系统性红斑狼疮和健康人群)的舌苔样本,按照dna的标准抽提方法完成舌苔样本中微生物总dna的抽提,在illumina miseq平台完成口腔菌群的16srdna高通量测序工作;
19、(2)基于高通量测序数据,在微生物区别模型的训练集中,在100例系统性红斑狼疮患者和200例健康对照之间,基于一个随机森林模型,通过一个五倍交叉验证的算法,鉴定了用于该模型的最佳的2个微生物基因标志物。
20、(3)基于2个微生物基因标志物,通过使用随机生成的决策树的比率来计算系统性红斑狼疮的患病率(probability of disease,pod)指数。
21、(4)该微生物区别模型在100例系统性红斑狼疮患者和200例健康对照之间的区别能力达到91.66%,pod指数在系统性红斑狼疮患者中明显升高,两组之间有显著性差异(p<0.0001)。(5)在验证集中,该微生物区别模型在40例系统性红斑狼疮患者和80例健康对照之间的区别能力达到84.22%;pod指数在确诊患者中明显升高,两组之间有显著性差异(p<0.0001)。(6)在独立诊断集中,该微生物区别模型在42例来自海南的系统性红斑狼疮患者和80例健康对照之间的区别能力达到84.06%;pod指数在海南地区系统性红斑狼疮患者中明显升高,两组之间有显著性差异(p<0.0001)。
22、因此,本发明的微生物基因区别模型在系统性红斑狼疮患者和健康对照中实现了良好的区别能力。
23、另外,还提供了一种用于区别系统性红斑狼疮患者和健康对照的口腔微生物模型的试剂盒,包括用于检测权利要求1所述的seq id no:1-2所示的2种微生物基因的引物。
24、本发明的具体操作步骤如下:
25、(1)按照前瞻性临床试验的设计原则,本发明的研究设计如图1所示。该研究方案得到了郑州大学第一附属医院和海南省人民医院伦理委员会的批准。所有入组的患者签署研究方案知情同意书和临床样本收集知情同意书。
26、(2)每一个入组的系统性红斑狼疮患者和健康对照的提供一份新鲜的舌苔样本,研究实验人员将样本在70℃灭活1小时,然后立即冻存于-80℃冰箱。舌苔细菌总dna的抽提方法按照试剂盒的说明书进行。
27、(3)完成舌苔细菌总dna样本的扩增和dna文库构建,在illuminamiseq测序平台完成16s rdna测序。所有的输出序列完成基本的预处理和基本的生物信息学分析。
28、(4)从所有样本中随机抽选等量的序列数,按照uparse传递途径拼接成对应的16srdna基因序列分类单元(operational taxonomy units,otus)。按照微生物基因标志物训练集、微生物基因标志物验证集和微生物基因标志物独立诊断集,将产生的所有样本的otus基因序列收集整理。基于微生物基因序列,使用rdp分类器2.6版本注释。
29、(5)基于高通量测序数据产生的代表性序列,计算出微生物基因标志物发现集的otus频率文件、验证集的otus频率文件和独立诊断集的otus频率文件。这些otus用于一个相关性研究来鉴定在系统性红斑狼疮患者和健康对照之间差异明显的otus丰度。使用wilcoxon检验方法统计分析系统性红斑狼疮患者和健康对照之间差异的微生物基因标志物。选择出的2个otus微生物基因标志物做进一步的分析。
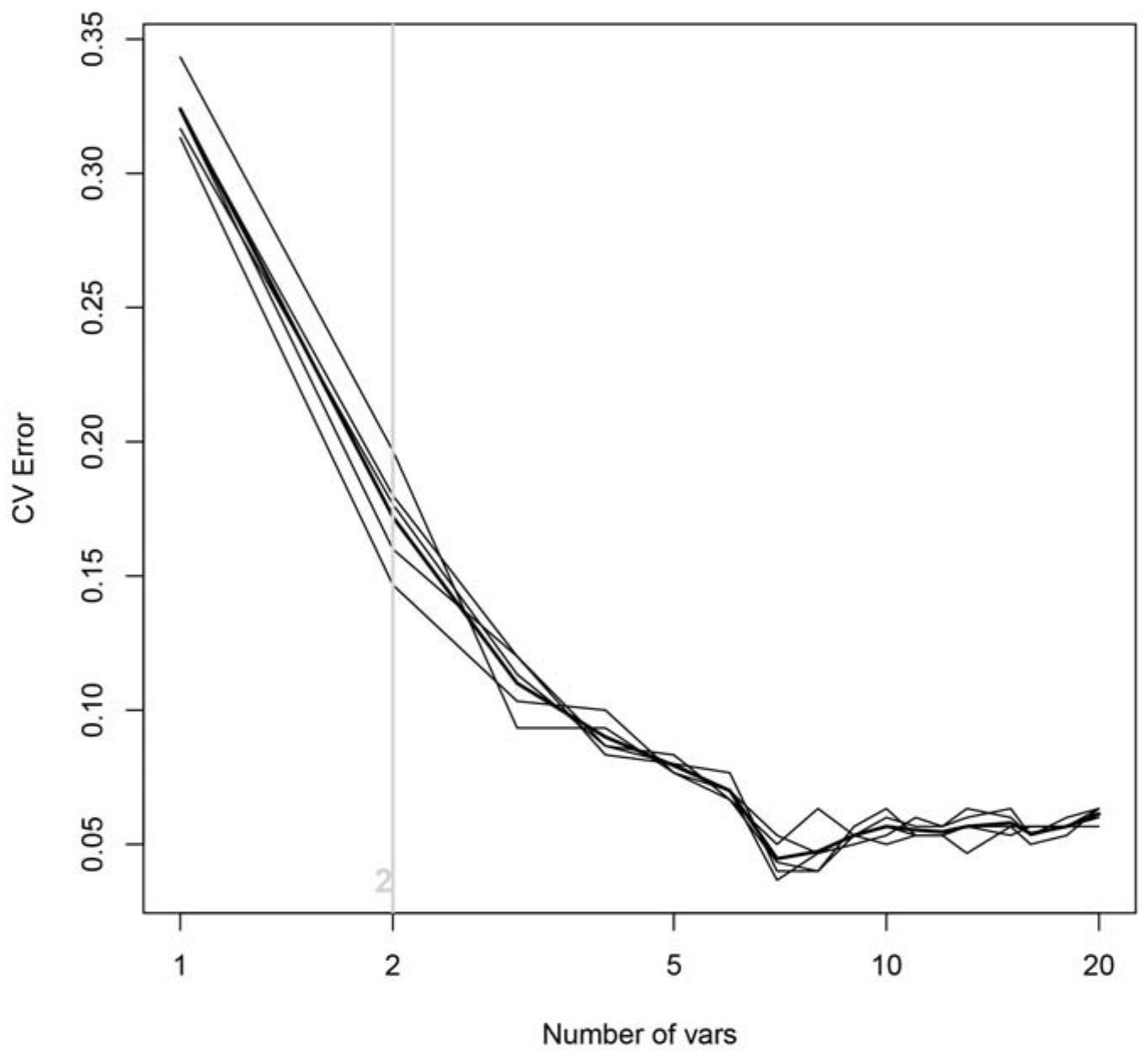
30、(6)在微生物区别模型的训练集中,包括100例系统性红斑狼疮患者和200例健康对照,使用筛选出的otus丰度文件,在一个随机森林模型(r软件3.4.1和随机森林软件包4.6–12)中采用五倍交叉验证的算法(除了设置“importance=true”之外,软件参数默认)进行微生物基因标志物的筛选。采用五倍交叉验证的5次试验,获得了交叉验证错误曲线,其中最小的交叉验证错误点作为cut-off值使用。最小的交叉验证错误值加上对应值的标准差为cut-off值。筛选出小于cut-off值的错误率的2个以下的otus标志物的集合,选择最小数目otus的集合作为最佳的微生物基因标志物的集合,最终鉴定了用于该模型的最佳的2个微生物基因标志物(图2)。选择出的2个微生物otus标志物的基因序列见seq id no:1-2。
31、(7)通过使用随机生成的决策树的比率来计算患病率(probability of disease,pod)指数。决策树预测样本为“cp”,设置的参数预测为:proximity=t,norm.votes=t,predict.all=true。在loo模式中构建的随机森林模型用于预测验证集中每一个样本的pod指数,最终计算每一个样本的平均预测的pod指数。
32、(8)使用r 3.3.0程序包中的proc工具计算受试者工作曲线(roc),用来评估微生物区别模型,曲线下面积(auc)用于指定roc的效应值。
33、(9)该微生物区别模型在100例系统性红斑狼疮患者和200例健康对照之间的区别能力达到91.66%(图4),pod指数在系统性红斑狼疮患者中明显升高,两组之间有显著性差异(p<0.0001)(图3)。
34、(10)在验证集中,pod指数在40例系统性红斑狼疮患者中明显升高,两组之间有显著性差异(p<0.0001)(图5),该微生物区别模型在40例系统性红斑狼疮患者和80例健康对照之间的区别能力达到84.22%(图6)。
35、(11)在独立诊断集中,pod指数在来自海南地区的42例系统性红斑狼疮患者中明显升高,两组之间有显著性差异(p<0.0001)(图7),该微生物区别模型在42例海南地区系统性红斑狼疮患者和80例健康对照之间的区别能力达到84.06%(图8)。
36、因此,本发明的微生物基因标志物(微生物区别模型)在系统性红斑狼疮和健康对照人群中实现了良好的区别能力,也验证了该区别模型在中国不同地域中的可行性、适用性和普适性。
- 还没有人留言评论。精彩留言会获得点赞!