一种通过两步层析法获得三种血液制品的制备工艺的制作方法
1.本发明涉及血液制品技术领域,特别涉及一种通过两步层析法获得三种血液制品的制备工艺。
背景技术:
2.凝血因子是参与血液凝固过程的各种蛋白质组分。它的生理作用是,在血管出血时被激活,和血小板粘连在一起并且补塞血管上的漏口。这个过程被称为凝血。整个凝血过程大致上可分为两个阶段,凝血酶原的激活及凝胶状纤维蛋白的形成。它们部分由肝生成,可以为香豆素所抑制。为统一命名,世界卫生组织按凝血因子被发现的先后次序用罗马数字编号,有凝血因子ⅱ、
ⅴ
、ⅶ、
ⅷ
、
ⅸ
、
ⅹ
、
ⅺ
、xlll等,因子xiii以后被发现的凝血因子经过多年验证,认为对于凝血功能,无决定性的影响,不再列入凝血因子的编号。
3.凝血因子
ⅷ
不仅由肝细胞产生,而且由窦内皮细胞与库普弗细胞产生,其它组织如肾脏也可产生。当肝细胞合成功能减退时,窦内皮细胞及库普弗细胞仍维持凝血因子
ⅷ
的合成;肝脏清除功能减退,内毒素及免疫因素刺激使它的合成与释放增加。
4.血管性血友病因子(von willebrand factor,vwf)主要由肝外合成,肝硬化患者可能由于内毒素血症,血管内皮细胞功能异常,使其释放增加。vwf可同时与胶原纤维和血小板结合,当血管破裂时大量血小板以vwf为中介,粘附在胶原纤维上,形成血栓,得以止血。
5.纤维粘连蛋白(fn)属非胶原糖蛋白的一种,称为冷不溶球蛋白,广泛存在于动物界,包括海绵、海胆及哺乳动物类。在脊椎动物中,fn以可溶的形式存在于血浆和各种体液中,称为血浆纤维粘连蛋白;以不溶的纤维存在于细胞外基质、细胞之间及某些细胞表面,称为细胞纤粘连蛋白。
6.目前国内并无vwf产品上市,人凝血因子
ⅷ
国内也仅有少数几家具有生产批文,供应严重不足,无法满足患者基本的用药需求。面对国内市场紧缺现状,获得产量及纯度较高的
ⅷ
、vwf和fn具有积极意义。
技术实现要素:
7.有鉴于此,本发明旨在提出一种通过两步层析法获得三种血液制品的制备工艺,可同时分离并获得纯度较高的
ⅷ
、vwf和fn,且原料利用率高、操作简单、耗时较短。
8.为达到上述目的,本发明的技术方案是这样实现的:
9.一种通过两步层析法获得三种血液制品的制备工艺,所述制备工艺用于分离并获得凝血因子
ⅷ
、vwf和fn,所述制备工艺包括如下步骤:
10.s1.将血浆原料经过预处理后泵入到平衡好的第一阴离子交换层析柱中;
11.s2.用1~3倍体积的第一平衡液冲洗第一阴离子交换层析柱,并用1~3倍体积的第一洗涤液洗涤,当洗涤流出液的absod280吸收值>20mau时,收集主要成分为vwf和fn的混合液;然后用1~3倍体积的第一洗脱液洗脱,当洗脱流出液的absod280吸收值>20mau
时,收集主要成分为
ⅷ
的收集液;
12.s3.将收集到的主要成分为vwf和fn的混合液泵入到平衡好的第二阴离子交换层析柱中,根据流出液的od280吸收值收集上样流穿液至上样结束;用1~3倍体积的第二平衡液冲洗第二阴离子交换层析柱,并用1~3倍体积的第二洗涤液洗涤,当洗涤流出液的absod280吸收值>20mau时,收集主要成分为fn的收集液;然后用1~3倍体积的第二洗脱液洗脱,当洗脱流出液的absod280吸收值>20mau时,收集主要成分为vwf的收集液;
13.s4.将收集到的
ⅷ
收集液、vwf收集液和fn收集液分别用10kd、30kd和100kd分子量的超滤膜进行浓缩,然后恒体积透析,分别得到凝血因子
ⅷ
、vwf和fn的浓缩液,最后冷冻干燥保存。
14.进一步的,步骤s1中,所述第一阴离子交换层析柱的装填介质为toyopearl deae 650m。
15.进一步的,步骤s1中,所述血浆原料预处理的步骤如下:
16.s11.冷沉淀制备:将血浆原料融化后在0~4℃下离心制备冷沉淀;
17.s12.冷沉淀溶解:用3~5倍冷沉淀体积的氨丁三醇将冷沉淀在室温下溶解;
18.s13.peg沉淀:加入聚乙二醇使聚乙二醇的浓度达到3~5%,离心分别收集上清液和peg沉淀;
19.s14.s/d灭活:将所述上清液搅拌,并加入s/d溶液,使最终制品中s/d溶液终含量为10.0
±
3.0g/l聚山梨酯80和3.0士0.3g/l磷酸三丁酯,调节最终制品的ph为7.0
±
0.5,并保持在温度24.0~26.0℃条件下搅拌灭活至少6h。
20.进一步的,步骤s2中,所述第一平衡液包括80~120mm氯化钠、16~24mm氨丁三醇、100~140mm甘氨酸、35~45mm氯化钙,ph值为7.0
±
0.2。
21.进一步的,步骤s2中,所述第一洗涤液包括140~180mm氯化钠、16~24mm氨丁三醇、100~140mm甘氨酸、35~45mm氯化钙、40~80mm聚山梨酯80,ph值7.0
±
0.2。
22.进一步的,步骤s2中,所述第一洗脱液包括20~30mm组氨酸、140~180mm氯化钠、20mm氨丁三醇、100~140mm甘氨酸、180~220mm氯化钙,ph值7.0
±
0.2。
23.进一步的,步骤s3中,所述第二阴离子交换层析柱的装填介质为nanogel-50sp。
24.进一步的,步骤s3中,所述第二平衡液包括80~110mm氯化钠、10mm枸橼酸、120mm甘氨酸,ph值7.0
±
0.2。
25.进一步的,步骤s3中,所述第二洗涤液包括180~210mm氯化钠、10mm枸橼酸、120mm甘氨酸,ph值7.0
±
0.2。
26.进一步的,步骤s3中,所述第二洗脱液包括300~330mm氯化钠、10mm枸橼酸、120mm甘氨酸,ph值7.0
±
0.2。
27.相对于现有技术,本发明所述的一种通过两步层析法获得三种血液制品的制备工艺具有以下优势:通过第一次阴离子交换层析介质与层析条件,实现凝血因子
ⅷ
的分离,同时通过第二次阴离子层析介质与层析条件,实现对凝血因子vwf和fn的分离,且操作简单、耗时短。通过两次阴离子交换层析组成的工艺,可同时对3种血液制品
ⅷ
、vwf和fn进行分离、制备,以实现对血浆原料的充分利用,提高经济效益。
附图说明
28.构成本发明的一部分的附图用来提供对本发明的进一步理解,本发明的示意性实施例及其说明用于解释本发明,并不构成对本发明的不当限定。在附图中:
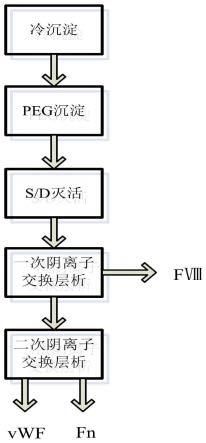
29.图1为本发明所述的一种通过两步层析法获得三种血液制品的制备工艺流程图;
30.图2为本发明一次阴离子交换层析分离提取凝血因子
ⅷ
收集液及vwf和fn的混合物的层析图谱;
31.图3为本发明二次阴离子交换层析分离提取vwf、fn的层析图谱;
32.图4为本发明所述的一种通过两步层析法获得三种血液制品的sds-page电泳检测图谱。
具体实施方式
33.下面结合具体实施方式,进一步阐述本发明。首先应说明的是,下述实验例中的数据是由发明人通过大量实验获得,限于篇幅,在说明书中只展示其中的一部分,且本领域普通技术人员可以在此数据下理解并实施本发明。这些实施例仅用于说明本发明而不用于限制本发明的范围。此外应理解,在阅读了本发明的内容之后,本领域技术人员可以对本发明作各种改动或修改,这些改动或修改同样落于本技术所保护的范围。
34.需要说明的是,在不冲突的情况下,本发明中的实施例及实施例中的特征可以相互组合。
35.下面将参考附图并结合实施例来详细说明本发明。
36.如图1所示,本发明提出一种通过两步层析法获得三种血液制品的制备工艺,用于分离并获得凝血因子
ⅷ
、vwf和fn。所述制备工艺包括如下步骤:
37.s1.将血浆原料经过预处理后泵入到平衡好的第一阴离子交换层析柱中;
38.具体的,步骤s1中,所述第一阴离子交换层析柱的装填介质为toyopearl deae 650m。
39.具体的,所述血浆原料预处理的步骤如下:
40.s11.冷沉淀制备:将血浆原料融化后在0~4℃下离心制备冷沉淀;
41.s12.冷沉淀溶解:用3~5倍冷沉淀体积的氨丁三醇将冷沉淀在室温下溶解;
42.s13.peg沉淀:加入聚乙二醇使聚乙二醇的浓度达到3~5%,离心分别收集上清液和peg沉淀;
43.s14.s/d灭活:将所述上清液搅拌,并加入s/d溶液,使最终制品中s/d溶液终含量为10.0
±
3.0g/l聚山梨酯80和3.0士0.3g/l磷酸三丁酯,调节最终制品的ph为7.0
±
0.5,并保持在温度24.0~26.0℃条件下搅拌灭活至少6h。
44.s2.用1~3倍体积的第一平衡液冲洗第一阴离子交换层析柱,并用1~3倍体积的第一洗涤液洗涤,当洗涤流出液的absod280吸收值>20mau时,收集主要成分为vwf和fn的混合液;然后用1~3倍体积的第一洗脱液洗脱,当洗脱流出液的absod280吸收值>20mau时,收集主要成分为
ⅷ
的收集液;
45.具体的,步骤s2中,所述第一平衡液包括80~120mm氯化钠、16~24mm氨丁三醇、100~140mm甘氨酸、35~45mm氯化钙,ph值为7.0
±
0.2;所述第一洗涤液包括140~180mm氯化钠、16~24mm氨丁三醇、100~140mm甘氨酸、35~45mm氯化钙、40~80mm聚山梨酯80,ph值
7.0
±
0.2;所述第一洗脱液包括20~30mm组氨酸、140~180mm氯化钠、20mm氨丁三醇、100~140mm甘氨酸、180~220mm氯化钙,ph值7.0
±
0.2。
46.s3.将收集到的主要成分为vwf和fn的混合液泵入到平衡好的第二阴离子交换层析柱中,根据流出液的od280吸收值收集上样流穿液至上样结束;用1~3倍体积的第二平衡液冲洗第二阴离子交换层析柱,并用1~3倍体积的第二洗涤液洗涤,当洗涤流出液的absod280吸收值>20mau时,收集主要成分为fn的收集液;然后用1~3倍体积的第二洗脱液洗脱,当洗脱流出液的absod280吸收值>20mau时,收集主要成分为vwf的收集液;
47.具体的,所述第二阴离子交换层析柱的装填介质为nanogel-50sp。所述第二平衡液包括80~110mm氯化钠、10mm枸橼酸、120mm甘氨酸,ph值7.0
±
0.2;所述第二洗涤液包括180~210mm氯化钠、10mm枸橼酸、120mm甘氨酸,ph值7.0
±
0.2;所述第二洗脱液包括300~330mm氯化钠、10mm枸橼酸、120mm甘氨酸,ph值7.0
±
0.2。
48.s4.将收集到的
ⅷ
收集液、vwf收集液和fn收集液分别用10kd、30kd和100kd分子量的超滤膜进行浓缩,然后恒体积透析,分别得到凝血因子
ⅷ
、vwf和fn的浓缩液,最后冷冻干燥保存。
49.本发明的一种同时获得三种血液制品的制备工艺具有如下优势:
50.(1)基于血浆原料中凝血因子
ⅷ
、vwf和fn在特定缓冲溶液中,蛋白表面电荷密度或糖基化修饰的差异,研发了一种基于层析技术手段可同时纯化制备凝血因子
ⅷ
、vwf和fn制剂的工艺技术方法。
51.(2)通过第一次阴离子交换层析介质与层析条件,实现凝血因子
ⅷ
的分离,同时通过第二次阴离子层析介质与层析条件,实现对凝血因子vwf和fn的分离,且操作简单、耗时短。通过两次阴离子交换层析组成的工艺,可同时对3种血液制品
ⅷ
、vwf和fn进行分离、制备,以实现对血浆原料的充分利用,提高经济效益。
52.(3)在层析过程中,通过对紫外吸收强度的监测,可准确收集相应的血液制品,有效提高血液制品的纯度。
53.实施例1
54.在本实施例中,第一阴离子交换层析柱装填介质toyopearl deae 650m购自东曹(上海)生物科技有限公司商业化产品。第二阴离子交换层析柱装填介质nanogel-50sp购自苏州纳微科技股份有限公司。
55.血浆原料预处理
56.s11.将血浆原料融化后在0~4℃下离心,待上清液为澄清透明时收集冷沉淀备用;
57.s12.将冷沉淀置于25℃环境中化冻4~8h,经粉碎机粉碎后,用3~5倍冷沉淀体积的0.01mol/l氨丁三醇溶解液,ph6.50~6.80,搅拌溶解30~50min,
58.s13.溶解后以不超过350ml/min的速度加入25%聚乙二醇使聚乙二醇的终浓度达到3.5%
±
0.5%,搅拌反应0.5~1.0小时,静置0.5~1.5小时后,离心去除沉淀,将上清液进行澄清过滤;
59.s14.将步骤s13获得的上清液搅拌,并加入s/d溶液,所述s/d溶液内含110.0士10g/l聚山梨酯80和33.0士3g/l的磷酸三丁酯,使制品中含有10.0
±
3.0g/l聚山梨酯80和3.0士0.3g/l磷酸三丁酯,水浴升温制品至24.0℃时开始计时灭活,保持制品温度在24.0~
26.0℃条件下,搅拌灭活至少6小时,获得经预处理后的血浆样品。
60.一次阴离子交换层析分离提取凝血因子
ⅷ
收集液及vwf和fn的混合物
61.将经s/d灭活后的血浆样品使用纯化水或枸橼酸钠缓冲液稀释,所述纯化水或枸橼酸钠缓冲液的ph为7.0
±
0.2,使稀释后的溶液电导率为10ms/cm,然后加入盐酸或氢氧化钠溶液调节溶液ph值为7.0
±
0.2获得待上样样品。
62.第一阴离子交换层析柱平衡:利用第一平衡液平衡第一阴离子交换层析柱,所述第一平衡液包括80~120mm氯化钠、16~24mm氨丁三醇、100~140mm甘氨酸、35~45mm氯化钙,ph值为7.0
±
0.2。将所述第一平衡液泵入到第一阴离子交换层析柱中,监测第一阴离子交换层析柱流出液,当流出液ph值和第一平衡液ph值相同时,第一阴离子交换层析柱平衡结束。
63.第一阴离子交换层析柱上样:将所述待上样样品泵入到平衡好的第一阴离子交换层析柱中,通过紫外检测器于280nm波长下,监测第一阴离子交换层析柱流出液,至上样结束。
64.第一阴离子交换层析柱冲洗:待上样结束后,采用1~3倍体积的第一平衡液泵入第一阴离子交换层析柱中,以冲洗第一阴离子交换层析柱中残留的样品,期间继续监控od280吸收值,直至od280吸收值趋近基线。
65.第一阴离子交换层析柱洗涤:第一阴离子交换层析柱冲洗完毕后,在第一阴离子交换层析柱中泵入第一洗涤液对第一阴离子交换层析柱进行洗涤,所述第一洗涤液包括140~180mm氯化钠、16~24mm氨丁三醇、100~140mm甘氨酸、35~45mm氯化钙、40~80mm聚山梨酯80,ph值7.0
±
0.2。通过紫外检测器于280nm波长下,监测第一阴离子交换层析柱的流出液,当od280吸收值大于20mau时开始收集洗涤液,获得主要成分为vwf和fn的混合液。
66.第一阴离子交换层析柱洗脱:第一阴离子交换层析柱洗涤完毕后,在第一阴离子交换层析柱中泵入第一洗脱液对第一阴离子交换层析柱进行洗脱,所述第一洗脱液包括20~30mm组氨酸、140~180mm氯化钠、20mm氨丁三醇、100~140mm甘氨酸、180~220mm氯化钙,ph值7.0
±
0.2。通过紫外检测器于280nm波长下,监测第一阴离子交换层析柱的流出液,当od280吸收值大于20mau时开始收集洗脱液,洗脱产物的主要成分为凝血因子
ⅷ
。待od280吸收值吸收值趋近基线时,洗脱结束。具体层析图谱如图2所示。
67.第一阴离子交换层析柱再生:当第一阴离子交换层析柱洗脱完毕后,在第一阴离子交换层析柱泵入3倍柱体积的再生缓冲液,对第一阴离子交换层析柱进行再生。所述再生缓冲液为1m氯化钠。
68.二次阴离子交换层析分离提取vwf和fn
69.第二阴离子交换层析柱平衡:利用第二平衡液平衡第二阴离子交换层析柱,所述第二平衡液包括80~110mm氯化钠、10mm枸橼酸、120mm甘氨酸,ph值7.0
±
0.2。将第二平衡液泵入到第二阴离子交换层析柱中,监测第二阴离子交换层析柱流出液,当流出液ph值和第二平衡液ph值相同时,第二阴离子交换层析柱平衡结束。
70.第二阴离子交换层析柱上样:将上述获得的主要成分为vwf和fn的混合液泵入到平衡好的第二阴离子交换层析柱中,通过紫外检测器于280nm波长下,监测第二阴离子交换层析柱流出液,至上样结束。
71.第二阴离子交换层析柱冲洗:待上样结束后,采用1~3倍体积的第二平衡液泵入
第二阴离子交换层析柱中,以冲洗第二阴离子交换层析柱中残留的样品,期间继续监控od280吸收值,直至od280吸收值趋近基线。
72.第二阴离子交换层析柱洗涤:第二阴离子交换层析柱冲洗完毕后,在第二阴离子交换层析柱中泵入第二洗涤液对第二阴离子交换层析柱进行洗涤,所述第二洗涤液包括180~210mm氯化钠、10mm枸橼酸、120mm甘氨酸,ph值7.0
±
0.2。通过紫外检测器于280nm波长下,监测第二阴离子交换层析柱的流出液,当od280吸收值大于20mau时开始收集洗涤液,获得主要成分为fn的洗涤产物。待od280吸收值趋近基线时,洗涤结束。
73.第二阴离子交换层析柱洗脱:第二阴离子交换层析柱洗涤完毕后,在第二阴离子交换层析柱中泵入第二洗脱液对第二阴离子交换层析柱进行洗脱,所述第二洗脱液包括300~330mm氯化钠、10mm枸橼酸、120mm甘氨酸,ph值7.0
±
0.2。通过紫外检测器于280nm波长下,监测第二阴离子交换层析柱的流出液,当od280吸收值大于20mau时开始收集洗脱液,洗脱产物的主要成分为凝血因子vwf。待od280吸收值吸收值趋近基线时,洗脱结束,具体层析图谱如图3所示。
74.第二阴离子交换层析柱再生:当第二阴离子交换层析柱洗脱完毕后,在第二阴离子交换层析柱泵入3倍柱体积的再生缓冲液,对第二阴离子交换层析柱进行再生。所述再生缓冲液为1m氯化钠。
75.使用电泳测定分离得到的
ⅷ
、vwf和fn的纯度,使用sds-page鉴定电泳条带,用酶底物法检测viii、vwf和fn的活力,电泳检测图谱如图4所示。
76.将凝血因子
ⅷ
、vwf和fn的收集液分别用10kd、30kd和100kd分子量的超滤膜进行浓缩,然后恒体积透析,分别得到凝血因子
ⅷ
、vwf和fn的浓缩液,最后冷冻干燥保存。
77.本发明的一种同时获得三种血液制品的制备工艺,在各阶段vwf比活、
ⅷ
比活和fn含量如表1所示。
78.表1
[0079][0080]
通过表1可知,经过一次阴离子交换层析后,能从洗脱液中获得比活较高的凝血因子
ⅷ
,比活达到58iu/mg。经过二次阴离子交换层析后,能从洗涤液中获得含量较高的fn,从洗脱液中获得比活较高的vwf。通过较为简单的方法,从血浆原料中同时分离得到
ⅷ
、vwf和fn三种血液制品,且这三种血液制品符合使用需求。
[0081]
以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1