一种合成γ-叔醇-(S)-α-氨基酸的酶催化方法
本发明涉及生物催化化学反应领域,特别是涉及一种合成γ-叔醇-(s)-α-氨基酸的酶催化方法。
背景技术:
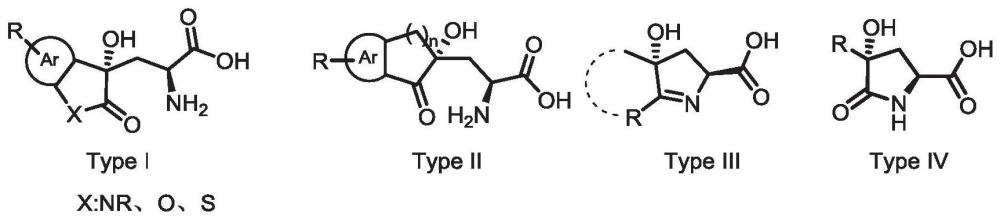
1、type i、type ii、type iii、type iv类非天然氨基酸的结构如下。
2、
3、type i类非天然氨基酸是一种非常重要的手性砌块,应用于很多生物活性化合物的合成中,例如γ-羟基氧代吲哚基-l-丙氨酸是具有潜在蛋白酶抑制活性化合物tmc-95类似物的重要结构片段。
4、文献(j.med.chem.2018,145,570-587.)报道的制备type i类化合物的方法如下所示,其以取代的色氨酸为原料,通过双氧水氧化等多步骤,得到γ位选择性不好的γ-叔醇-(s)-α-氨基酸。此方法立体选择性差,步骤繁琐,收率低,从经济学角度考虑,不适合工业化大规模生产。
5、
6、i.dmso,t-bubr,45℃,24h ii.h2o2,catalytic ki(11%),ch3cn,rt,18h.iii.r1nh2,thf,rt,1.5 to 18h;
7、iv.h2,pd/c,meoh,rt,ovemight,then 1 eq.anhydrous hcl or tfa
8、此外,目前还没有合适的合成方法可以高选择性地制备type ii、type iii、typeiv类非天然氨基酸。
9、生物酶法因为具有立体选择性好、反应条件温和、环境友好等优点,受到越来越广泛的关注和越来越深入的研究。但目前关于高选择性地制备高光学纯度的γ-叔醇-(s)-α-氨基酸的方法仍然没有相关报道。
技术实现思路
1、本发明针对现有γ-叔醇-(s)-α-氨基酸制备方法中,反应步骤多、操作繁琐、方法立体选择性差等问题,提供一种选择性高、反应步骤少、反应条件温和的酶催化方法。
2、具体地,本发明提供一种合成γ-叔醇-(s)-α-氨基酸的酶催化方法,包括:在磷酸吡哆醛(plp)存在下,ustd酶催化l-天冬氨酸脱羧并和邻位双酮化合物1发生羰基加成反应,生成γ-叔醇-(s)-α-氨基酸2,如反应式i所示:
3、
4、其中,x、y各自独立地选自c1-c10烃基、c1-c10烃基氧基、c1-c10烃基胺基、c1-c10烃基巯基、c3-c10脂环烃基、c3-c10脂环烃基氧基、c3-c10脂环烃基胺基、c3-c10脂环烃基巯基、c6-c12芳基、5-12元杂芳基、c6-c12芳基c1-c10烃基或5-12元杂芳基c1-c10烃基;优选选自c1-c10烷基、c1-c10烷氧基、c1-c10烷基胺基、c1-c10烷基巯基、c3-c10环烷基、c3-c10环烷氧基、c3-c10环烷胺基、c3-c10环烷巯基、c6-c12芳基、5-12元杂芳基、c6-c12芳基c1-c10烷基或5-12元杂芳基c1-c10烷基;优选选自c1-c6烷基、c1-c6烷氧基、c3-c7环烷基、c6-c12芳基、c6-c12芳基c1-c6烷基;更优选地,x、y各自独立地选自c1-c4烷基(特别是甲基、乙基、正丙基、异丙基、正丁基、异丁基)、c1-c4烷氧基(特别是甲氧基、乙氧基)、c3-c7环烷基、c6-c12芳基、c6-c12芳基c1-c4烷基(特别是苯乙基);所述c1-c10烃基、c1-c10烃基氧基、c1-c10烃基胺基、c1-c10烃基巯基、c1-c10烷基、c1-c10烷氧基、c1-c10烷基胺基、c1-c10烷基巯基、c1-c6烷基、c1-c6烷氧基、c1-c4烷基、c1-c4烷氧基可选地被一个或多个选自卤素、硝基、羟基、胺基、巯基、c1-c10烃基氧基、c1-c10烃基胺基、c1-c10烃基巯基、c1-c10酰基、c3-c10脂环烃基、c3-c10脂环烃基氧基、c3-c10脂环烃基胺基、c3-c10脂环烃基巯基中的取代基所取代,所述c3-c10脂环烃基、c3-c10脂环烃基氧基、c3-c10脂环烃基胺基、c3-c10脂环烃基巯基、c6-c12芳基、5-12元杂芳基、c6-c12芳基c1-c10烃基、5-12元杂芳基c1-c10烃基、c3-c10环烷基、c3-c10环烷氧基、c3-c10环烷胺基、c3-c10环烷巯基、c6-c12芳基c1-c10烷基、5-12元杂芳基c1-c10烷基、c3-c7环烷基、c6-c12芳基c1-c6烷基、c6-c12芳基c1-c4烷基可选地被一个或多个选自卤素、硝基、羟基、胺基、巯基、c1-c10烃基、c1-c10烃基氧基、c1-c10烃基胺基、c1-c10烃基巯基、c1-c10酰基、c3-c10脂环烃基氧基、c3-c10脂环烃基胺基、c3-c10脂环烃基巯基、c6-c12芳基、5-12元杂芳基、c6-c12芳基c1-c10烃基或5-12元杂芳基c1-c10烃基中的取代基所取代;
5、或,x和y与连接的邻位双酮构成4-10元脂环烃基二酮、5-10元杂环二酮、c6-c12芳基并4-10元脂环烃基二酮、5-12元杂芳基并4-10元脂环烃基二酮、c6-c12芳基并5-10元杂环二酮、5-12元杂芳基并5-10元杂环二酮;所述c6-c12芳基并4-10元脂环烃基二酮、5-12元杂芳基并4-10元脂环烃基二酮、c6-c12芳基并5-10元杂环二酮、5-12元杂芳基并5-10元杂环二酮可由1、2或3个c6-c12芳基或5-12元杂芳基与4-10元脂环烃基二酮或5-10元杂环二酮形成并环结构;所述5-10元杂环二酮是指环中含有选自n、o或s中的1、2、3或4个杂原子,且环碳被两个氧代基团取代的饱和或部分不饱和的单环或多环非芳香性杂环化合物;优选地,所述4-10元脂环烃基二酮选自邻位环丁二酮、邻位环戊二酮、邻位环己二酮、邻位环庚二酮或邻位环辛二酮,所述5-10元杂环二酮选自吡咯-2,3-二酮、呋喃-2,3-二酮、噻吩-2,3-二酮;更优选地,x和y与连接的邻位双酮构成4-10元环烷二酮、二氢吲哚-2,3-二酮、1,2-茚满二酮或菲-9,10-二酮;所述4-10元脂环烃基二酮、5-10元杂环二酮、c6-c12芳基并4-10元脂环烃基二酮、5-12元杂芳基并4-10元脂环烃基二酮、c6-c12芳基并5-10元杂环二酮、5-12元杂芳基并5-10元杂环二酮、4-10元环烷二酮、二氢吲哚-2,3-二酮、1,2-茚满二酮或菲-9,10-二酮可选地被一个或者多个选自卤素、硝基、羟基、胺基、巯基、c1-c10烃基、c1-c10烃基氧基、c1-c10烃基胺基、c1-c10烃基巯基、c1-c10酰基、c3-c10脂环烃基、c3-c10脂环烃基氧基、c3-c10脂环烃基胺基、c3-c10脂环烃基巯基、c6-c12芳基、5-12元杂芳基、c6-c12芳基c1-c10烃基或5-12元杂芳基c1-c10烃基中的取代基所取代;优选地被一个或多个选自卤素、硝基、羟基、胺基、巯基、c1-c10烷基、c1-c10烷氧基、c1-c10烷基胺基、c1-c10烷基巯基、c1-c10烷基c1-c10烷基氧基、c1-c10烷基c1-c10烷基胺基、c1-c10烷基c1-c10烷基巯基、c1-c8酰基、c3-c10环烷基、c3-c10环烷氧基、c3-c10环烷胺基、c3-c10环烷巯基、c6-c12芳基、5-12元杂芳基、c6-c12芳基c1-c10烷基或5-12元杂芳基c1-c10烷基中的取代基所取代;更优选地被一个或多个选自卤素、硝基、羟基、胺基、巯基、c1-c6烷基、c1-c6烷氧基、c1-c6烷基胺基、c1-c6烷基巯基、c1-c6酰基、c3-c7环烷基、c3-c7环烷氧基、c3-c7环烷基胺基、c3-c7环烷基巯基、c6-c12芳基、5-12元杂芳基、c6-c12芳基c1-c6烷基或5-12元杂芳基c1-c6烷基中的取代基所取代;进一步优选地被一个或多个选自卤素(特别是氟、氯、溴)、硝基、羟基、胺基、巯基、c1-c4烷基(特别是甲基、乙基、正丙基、异丙基、正丁基、异丁基)、c1-c4烷氧基(特别是甲氧基、乙氧基)、c1-c4烷胺基、c1-c4烷巯基、c1-c4酰基、c3-c7环烷基、c3-c7环烷氧基、c3-c7环烷胺基、c3-c7环烷巯基、c6-c12芳基、5-12元杂芳基、c6-c12芳基c1-c4烷基或5-12元杂芳基c1-c4烷基中的取代基所取代。
6、在一些实施方式中,所述方法中的γ-叔醇-(s)-α-氨基酸2进一步通过与x相连的羰基与α-氨基发生自发成环反应而成环。
7、在一些实施方式中,所述酶催化方法选自下列方法一至四之一:(1)方法一:
8、
9、如反应式i-1所示,在磷酸吡哆醛(plp)存在下,ustd酶催化l-天冬氨酸脱羧并和邻位双酮化合物1-1发生羰基加成反应生成γ-叔醇-(s)-α-氨基酸2-1,其为type i类非天然氨基酸;
10、其中,
11、环a为c6-c12的芳基环或5-12元的杂芳基环;
12、z选自nr2、o、s;
13、m为0-12的整数;优选地,m为0-10的整数,例如0,1,2,3,4,5,6,7,8,9,10;
14、各r1独立地选自卤素、硝基、羟基、胺基、巯基、c1-c10烃基、c1-c10烃基氧基、c1-c10烃基胺基、c1-c10烃基巯基、c1-c10酰基、c3-c10脂环烃基、c3-c10脂环烃基氧基、c3-c10脂环烃基胺基、c3-c10脂环烃基巯基、c6-c12芳基、5-12元杂芳基、c6-c12芳基c1-c10烃基或5-12元杂芳基c1-c10烃基;优选地,各r1独立地选自卤素、硝基、羟基、胺基、巯基、c1-c10烷基、c1-c10烷氧基、c1-c10烷基胺基、c1-c10烷基巯基、c1-c8酰基、c3-c10环烷基、c3-c10环烷氧基、c3-c10环烷胺基、c3-c10环烷巯基、c6-c12芳基、5-12元杂芳基、c6-c12芳基c1-c10烷基或5-12元杂芳基c1-c10烷基;更优选地,各r1独立地选自卤素、硝基、羟基、胺基、巯基、c1-c6烷基、c1-c6烷氧基、c1-c6烷基胺基、c1-c6烷基巯基、c1-c6酰基、c3-c7环烷基、c3-c7环烷氧基、c3-c7环烷基胺基、c3-c7环烷基巯基、c6-c12芳基、5-12元杂芳基、c6-c12芳基c1-c6烷基或5-12元杂芳基c1-c6烷基;进一步优选地,各r1独立地选自卤素(特别是氟、氯、溴)、c1-c4烷基(特别是甲基、乙基、正丙基)、c1-c4烷氧基(特别是甲氧基)、c1-c4烷基胺基、c1-c4烷基巯基、c1-c4酰基、c3-c6环烷基、c3-c6环烷氧基、c3-c6环烷胺基、c3-c6环烷巯基、c6-c12芳基、5-12元杂芳基、c6-c12芳基c1-c6烷基或5-12元杂芳基c1-c6烷基;
15、r2选自氢、c1-c10酰基、c1-c10烃基、c3-c10脂环烃基、c6-c12芳基、5-12元杂芳基、c6-c12芳基c1-c10烃基或5-12元杂芳基c1-c10烃基;优选选自氢、c1-c8酰基、c1-c10烷基、c3-c10环烷基、c6-c12芳基、5-12元杂芳基、c6-c12芳基c1-c10烷基或5-12元杂芳基c1-c10烷基;更优选选自氢、c1-c6酰基、c1-c6烷基、c3-c7环烷基、c6-c12芳基、5-12元杂芳基、c6-c12芳基c1-c6烷基或5-12元杂芳基c1-c6烷基;进一步优选为氢、c1-c4酰基、c1-c4烷基(特别是甲基、乙基、正丙基)、c3-c6环烷基、c6-c12芳基、5-12元杂芳基、c6-c12芳基c1-c4烷基或5-12元杂芳基c1-c4烷基;
16、(2)方法二:
17、
18、如反应式i-2所示,在磷酸吡哆醛(plp)存在下,ustd酶催化l-天冬氨酸脱羧并和邻位双酮化合物1-2发生羰基加成反应生成γ-叔醇-(s)-α-氨基酸2-2,其为type ii类非天然氨基酸;
19、其中,
20、环b为c6-c12的芳基环或5-12元的杂芳基环;
21、n为0-12的整数;优选地,n为0-10的整数,例如0,1,2,3,4,5,6,7,8,9,10;
22、p为0-6的整数;优选地,p为0-4的整数,例如0,1,2,3,4;
23、各r3独立地选自卤素、硝基、羟基、胺基、巯基、c1-c10烃基、c1-c10烃基氧基、c1-c10烃基胺基、c1-c10烃基巯基、c1-c10酰基、c3-c10脂环烃基、c3-c10脂环烃基氧基、c3-c10脂环烃基胺基、c3-c10脂环烃基巯基、c6-c12芳基、5-12元杂芳基、c6-c12芳基c1-c10烃基或5-12元杂芳基c1-c10烃基;优选地,各r3独立地选自卤素、硝基、羟基、胺基、巯基、c1-c10烷基、c1-c10烷氧基、c1-c10烷基胺基、c1-c10烷基巯基、c1-c8酰基、c3-c10环烷基、c3-c10环烷氧基、c3-c10环烷胺基、c3-c10环烷巯基、c6-c12芳基、5-12元杂芳基、c6-c12芳基c1-c10烷基或5-12元杂芳基c1-c10烷基;更优选地,各r3独立地选自卤素、硝基、羟基、胺基、巯基、c1-c6烷基、c1-c6烷氧基、c1-c6烷基胺基、c1-c6烷基巯基、c1-c6酰基、c3-c7环烷基、c3-c7环烷氧基、c3-c7环烷基胺基、c3-c7环烷基巯基、c6-c12芳基、5-12元杂芳基、c6-c12芳基c1-c6烷基或5-12元杂芳基c1-c6烷基;进一步优选地,各r3独立地选自卤素(特别是氟、氯、溴)、c1-c4烷基(特别是甲基)、c1-c4烷氧基、c1-c4烷基胺基、c1-c4烷基巯基、c3-c6环烷基、c3-c6环烷氧基、c1-c4酰基、c3-c6环烷胺基、c3-c6环烷巯基、c6-c12芳基、5-12元杂芳基、c6-c12芳基c1-c6烷基或5-12元杂芳基c1-c6烷基;
24、(3)方法三:
25、
26、如反应式i-3所示,在磷酸吡哆醛(plp)存在下,ustd酶催化l-天冬氨酸脱羧并和邻位双酮化合物1-3发生羰基加成反应生成化合物2-a,然后化合物2-a中与x3相连的羰基与α-氨基自发成环生成化合物2-3,其为type iii类非天然氨基酸;
27、其中,
28、x3、y3各自独立地选自c1-c10烃基、c3-c10脂环烃基、c6-c12芳基、5-12元杂芳基、c6-c12芳基c1-c10烃基或5-12元杂芳基c1-c10烃基;优选选自c1-c10烷基、c3-c10环烷基、c6-c12芳基、5-12元杂芳基、c6-c12芳基c1-c10烷基或5-12元杂芳基c1-c10烷基;更优选选自c1-c6烷基、c3-c7环烷基、c6-c12芳基、5-12元杂芳基、c6-c12芳基c1-c6烷基或5-12元杂芳基c1-c6烷基;更进一步优选地,x3、y3各自独立地选自c1-c4烷基(特别是甲基、乙基、正丙基、异丙基、正丁基、异丁基)、c3-c6环烷基、c6-c12芳基、5-12元杂芳基、c6-c12芳基c1-c4烷基或5-12元杂芳基c1-c4烷基;所述c1-c10烃基、c1-c10烷基、c1-c6烷基、c1-c4烷基可选地被一个或者多个选自卤素、硝基、羟基、胺基、巯基、c1-c10烃基氧基、c1-c10烃基胺基、c1-c10烃基巯基、c1-c10酰基、c3-c10脂环烃基、c3-c10脂环烃基氧基、c3-c10脂环烃基胺基、c3-c10脂环烃基巯基的取代基所取代;所述的c3-c10脂环烃基、c6-c12芳基、5-12元杂芳基、c6-c12芳基c1-c10烃基或5-12元杂芳基c1-c10烃基、c3-c10环烷基、c6-c12芳基c1-c10烷基、5-12元杂芳基c1-c10烷基、c3-c7环烷基、c6-c12芳基c1-c6烷基、5-12元杂芳基c1-c6烷基、c3-c6环烷基、c6-c12芳基c1-c4烷基或5-12元杂芳基c1-c4烷基可选地被一个或者多个选自卤素、硝基、羟基、胺基、巯基、c1-c10酰基、c1-c10烃基、c1-c10烃基氧基、c1-c10烃基胺基、c1-c10烃基巯基、c3-c10脂环烃基氧基、c3-c10脂环烃基胺基、c3-c10脂环烃基巯基、c6-c12芳基、5-12元杂芳基、c6-c12芳基c1-c10烃基或5-12元杂芳基c1-c10烃基中的取代基所取代;
29、或,x3、y3与连接的邻位双酮构成4-10元脂环烃基二酮、5-10元杂环二酮、c6-c12芳基并4-10元脂环烃基二酮、5-12元杂芳基并4-10元脂环烃基二酮、c6-c12芳基并5-10元杂环二酮、5-12元杂芳基并5-10元杂环二酮;所述c6-c12芳基并4-10元脂环烃基二酮、5-12元杂芳基并4-10元脂环烃基二酮、c6-c12芳基并5-10元杂环二酮、5-12元杂芳基并5-10元杂环二酮可由1、2或3个c6-c12芳基或5-12元杂芳基与4-10元脂环烃基二酮或5-10元杂环二酮形成并环结构;所述5-10元杂环二酮是指环中含有选自n、o或s中的1、2、3或4个杂原子,且环碳被两个氧代基团取代的饱和或部分不饱和的单环或多环非芳香性杂环化合物;优选地,所述4-10元脂环烃基二酮选自邻位环丁二酮、邻位环戊二酮、邻位环己二酮、邻位环庚二酮或邻位环辛二酮;所述5-10元杂环二酮选自吡咯-2,3-二酮、呋喃-2,3-二酮、噻吩-2,3-二酮;更优选地,x和y与连接的邻位双酮构成4-10元环烷二酮、二氢吲哚-2,3-二酮、1,2-茚满二酮或菲-9,10-二酮;所述4-10元脂环烃基二酮、5-10元杂环二酮、c6-c12芳基并4-10元脂环烃基二酮、5-12元杂芳基并4-10元脂环烃基二酮、c6-c12芳基并5-10元杂环二酮、5-12元杂芳基并5-10元杂环二酮、4-10元环烷二酮、二氢吲哚-2,3-二酮、1,2-茚满二酮或菲-9,10-二酮可选地被一个或多个选自卤素、硝基、羟基、胺基、巯基、c1-c10烃基、c1-c10烃基氧基、c1-c10烃基胺基、c1-c10烃基巯基、c1-c10酰基、c3-c10脂环烃基、c3-c10脂环烃基氧基、c3-c10脂环烃基胺基、c3-c10脂环烃基巯基、c6-c12芳基、5-12元杂芳基、c6-c12芳基c1-c10烃基或5-12元杂芳基c1-c10烃基的取代基所取代;优选地被一个或多个选自卤素、硝基、羟基、胺基、巯基、c1-c10烷基、c1-c10烷氧基、c1-c10烷基胺基、c1-c10烷基巯基、c1-c10烷基c1-c10烷基氧基、c1-c10烷基c1-c10烷基胺基、c1-c10烷基c1-c10烷基巯基、c1-c8酰基、c3-c10环烷基、c3-c10环烷氧基、c3-c10环烷胺基、c3-c10环烷巯基、c6-c12芳基、5-12元杂芳基、c6-c12芳基c1-c10烷基或5-12元杂芳基c1-c10烷基中的取代基所取代;更优选地被一个或多个选自卤素、硝基、羟基、胺基、巯基、c1-c6烷基、c1-c6烷氧基、c1-c6烷基胺基、c1-c6烷基巯基、c1-c6酰基、c3-c7环烷基、c3-c7环烷氧基、c3-c7环烷基胺基、c3-c7环烷基巯基、c6-c12芳基、5-12元杂芳基、c6-c12芳基c1-c6烷基或5-12元杂芳基c1-c6烷基中的取代基所取代;进一步优选地被一个或多个选自卤素(特别是氟、氯、溴)、硝基、羟基、胺基、巯基、c1-c4烷基(特别是甲基、乙基、正丙基、异丙基、正丁基、异丁基)、c1-c4烷氧基(特别是甲氧基、乙氧基)、c1-c4烷胺基、c1-c4烷巯基、c1-c4酰基、c3-c7环烷基、c3-c7环烷氧基、c3-c7环烷胺基、c3-c7环烷巯基、c6-c12芳基、5-12元杂芳基、c6-c12芳基c1-c4烷基或5-12元杂芳基c1-c4烷基中的取代基所取代。
30、(4)方法四:
31、
32、如反应式i-4所示,在磷酸吡哆醛(plp)存在下,ustd酶催化l-天冬氨酸脱羧并和邻位酮酸酯化合物1-4发生羰基加成反应生成化合物2-b,然后化合物2-b中与x4相连的酯羰基与α-氨基自发成环,并脱去x4基团,生成化合物2-4,其为type iv类非天然氨基酸;
33、其中,
34、x4为c1-c10烃基氧基,优选为c1-c10烷氧基,更优选为c1-c6烷氧基,进一步优选为c1-c4烷氧基(特别是乙氧基);
35、y4选自c1-c10烃基、c3-c10脂环烃基、c6-c12芳基、5-12元杂芳基、c6-c12芳基c1-c10烃基或5-12元杂芳基c1-c10烃基;优选选自c1-c10烷基、c3-c10环烷基、c6-c12芳基、5-12元杂芳基、c6-c12芳基c1-c8烷基或5-12元杂芳基c1-c8烷基;优选选自c1-c6烷基、c3-c7环烷基、c6-c12芳基、5-12元杂芳基、c6-c12芳基c1-c6烷基或5-12元杂芳基c1-c6烷基;更优选地,y4选自c1-c4烷基(特别是甲基、乙基、正丙基、异丙基、正丁基、异丁基)、c3-c7环烷基、c6-c12芳基、5-12元杂芳基、c6-c12芳基c1-c4烷基或5-12元杂芳基c1-c4烷基(特别是苯乙基);所述c1-c10烃基、c1-c10烷基、c1-c6烷基、c1-c4烷基可选地被一个或者多个选自卤素、硝基、羟基、胺基、巯基、c1-c10烃基氧基、c1-c10烃基胺基、c1-c10烃基巯基、c1-c10酰基、c3-c10脂环烃基、c3-c10脂环烃基氧基、c3-c10脂环烃基胺基、c3-c10脂环烃基巯基的取代基所取代;所述c3-c10脂环烃基、c6-c12芳基、5-12元杂芳基、c6-c12芳基c1-c10烃基或5-12元杂芳基c1-c10烃基、c3-c10环烷基、c6-c12芳基c1-c8烷基、5-12元杂芳基c1-c8烷基、c3-c7环烷基、c6-c12芳基c1-c6烷基、5-12元杂芳基c1-c6烷基、c6-c12芳基c1-c4烷基或5-12元杂芳基c1-c4烷基可选地被一个或者多个选自卤素、硝基、羟基、胺基、巯基、c1-c10烃基、c1-c10烃基氧基、c1-c10烃基胺基、c1-c10烃基巯基、c1-c10酰基、c3-c10脂环烃基、c3-c10脂环烃基氧基、c3-c10脂环烃基胺基、c3-c10脂环烃基巯基、c6-c12芳基、5-12元杂芳基、c6-c12芳基c1-c10烃基或5-12元杂芳基c1-c10烃基中的取代基所取代;
36、在具体的实施方式中:邻位双酮化合物1-1选自以下结构:
37、
38、其中r1、r2定义如前所述;
39、优选地,邻位双酮化合物1-1选自以下结构:
40、
41、在具体的实施方式中,邻位双酮化合物1-2选自以下结构:
42、
43、r3定义如前所述;
44、优选地,邻位双酮化合物1-2选自以下结构:
45、
46、在具体的实施方式中,邻位双酮化合物1-3选自以下结构:
47、
48、在具体的实施方式中,邻位酮酸酯化合物1-4选自以下结构:
49、
50、在具体的实施方式中,所述ustd酶具有:
51、(a)如seq id no:1或seq id no:3所示氨基酸序列;
52、
53、
54、或者
55、(b)对seq id no:1和seq id no:3所示的氨基酸序列在保持酶活性范围内,进行一个或者多个氨基酸的替换、缺失、改变、插入或增加所得到的氨基酸序列。
56、在具体的实施方式中,所述ustd酶的编码基因序列选自以下组:
57、(a)如seq id no:2或seq id no:4所述的核苷酸序列;
58、
59、
60、(b)与(a)限定的序列互补的多核苷酸;或
61、(c)与(a)限定的序列具有至少70%(优选至少75%、80%、85%、90%,更优选至少95%、96%、97%、98%、99%)以上的序列一致性的任一多核苷酸或互补序列。
62、在具体的实施方式中,将所述ustd酶的编码基因通过分子克隆技术引入到表达载体中,从而利用大肠杆菌作为宿主异源表达蛋白,所述载体可以选自但不限于petduet、pacycduet、rrsfduet、pet28a(+)或者pet-22b9(+)等大肠杆菌表达载体。
63、在本发明中,所述ustd酶的来源包括但不限于绿核菌、黄曲霉菌,优选ustd来源为黄曲霉菌,或来源于将所述菌种的基因重组表达的大肠杆菌、酵母或者链霉菌等微生物中。
64、在具体的实施方式中,对反应温度没有特别限制,只要使得ustd酶能够具有催化活性即可,例如可以为15℃-50℃,例如,20、25、30、35、40、45℃等,优选为30℃-40℃。
65、在具体的实施方式中,对反应ph没有特别限制,只要使得ustd酶能够具有催化活性即可,例如可以为4-11,例如5、5.5、6、6.5、7、7.5、8、8.5、9、9.5、10、10.5等;优选地,ph为6-9;更优选地ph为7-8。
66、在具体的实施方式中,对反应时间没有特别限制,只要所需的化合物即可,例如为0.1小时以上,0.5小时以上,1小时以上,例如0.1到120小时,例如5、10、12、15、18、24、30、36、48、60、72、80、100小时等;优选为0.5到80小时;更优选为1到72小时,进一步优选为4-72小时。
67、在具体的实施方式中,所述反应体系中,所述邻位二酮化合物1和l-天冬氨酸的摩尔比可以为1∶0.1~10,例如1∶0.2、1∶0.5、1∶1、1∶1.5、1∶2、1∶3、1∶4、1∶5、1∶7等,优选为1∶2~5。优选地,所述反应体系中,所述邻位二酮化合物起始浓度为0.1-200mm,l-天冬氨酸的起始浓度为0.1-200mm,例如0.5、1、1.5、2、3、4、5、6、7、9、10、11、12、15、20、30、40、50、60、70、80、90、100、150、200mm等;更优选地,所述邻位二酮化合物起始浓度为4-12mm,l-天冬氨酸的起始浓度为10-40mm。
68、在具体的实施方式中,所述ustd酶的摩尔浓度是底物(邻位二酮化合物1和l-天冬氨酸)摩尔浓度的0.000001-10倍,例如0.00001、0.0001、0.001、0.01、0.1、0.2、0.3、0.4、0.5、0.6、0.7、0.8、0.9、1、2、3、4、5、10倍等,优选为0.0001-1倍。
69、在具体的实施方式中,所述反应可以在缓冲液(缓冲盐水溶液体系)中进行。通过缓冲液对反应ph进行调节控制,以保持反应稳定进行。常用的缓冲液包括但不限于磷酸盐、tris、醋酸铵缓冲液。
70、在具体的实施方式中,所述反应体系还可以含有助溶剂;所述助溶剂为有机溶剂。
71、在具体的实施方式中,所述助溶剂可以选自:二甲基亚砜、甲醇、乙醇、异丙醇、丙酮,或者其组合。优选地,所述助溶剂选自二甲基亚砜。所使用的助溶剂应当与水可以混溶,以进一步增加底物的溶解性。优选地,所述助溶剂占反应体系总体积的1%-25%。
72、在具体的实施方式中,本发明的酶催化方法还包括分离出γ-叔醇-(s)-α-氨基酸的步骤。
73、具体地,所述分离出γ-叔醇-(s)-α-氨基酸的步骤包括:将反应完成且冷冻干燥后的反应物中加入水,离心取上清后,使用快速制备液相色谱纯化产物,用甲醇/水体系纯化产物,其中水相中加入甲酸。
74、在具体的实施方式中,进行快速制备液相色谱的色谱柱为column;所述甲醇/水体系中,水相中加入0.1%的甲酸,进行梯度洗脱,梯度洗脱程序为:0-30min,1%-70%,50ml/min。
75、有益效果
76、本发明以l-天冬氨酸和邻位二酮化合物为底物,使用特定序列的ustd酶来催化合成制备高光学纯度的多官能团非天然氨基酸,特别是type i-iv四种类型的手性γ-叔醇-(s)-α-氨基酸。该方法在实验操作上简单可行、选择性好、转化率高,对底物的最高转化率可达到99%,所获得产物的d.r.值可大于99∶1,反应条件温和、绿色环保,为工业化生产高光学纯度的非天然氨基酸提供了新的思路与策略,具有工业推广的潜力。
- 还没有人留言评论。精彩留言会获得点赞!