一种水痘-带状疱疹病毒mRNA疫苗及其应用的制作方法
本发明属于生物,具体而言,涉及一种水痘-带状疱疹病毒疫苗及其应用。
背景技术:
1、带状疱疹是由水痘-带状疱疹病毒引起的急性感染性皮肤病。水痘-带状疱疹病毒(varicella-zoster virus,vzv)初次感染引起水痘,愈合后残留的病毒潜伏于脊神经后跟及颅神经的神经节中,当vzv特异性的细胞免疫下降时,病毒重新复活发生带状疱疹;在所有神经系统的疾病中,其发病率最高。带状疱疹的发生风险随年龄增长而增加,高龄之所以成为带状疱疹重要的危险因素,可能是因为随着年龄增长,免疫逐步减弱,vzv特异性细胞免疫(cmi)反应的成分减少所致。带状疱疹患者常伴有较多并发症,如带状疱疹后神经痛(phn)、带状疱疹眼病(hzo)、ramsay hunt综合征,以及其他并发症包括运动神经损伤和其他神经系统并发症如脑膜炎等。据估计,大约三分之一的人在一生中会患带状疱疹,带状疱疹的发病高风险人群为老年人或免疫功能低下者。我国每年有近300万人受带状疱疹影响,50岁及以上人群每年新发带状疱疹病例约156万例。当前,我国正处于老龄化发展阶段,带状疱疹易感人群数量逐年上升,加速研制安全有效的带状疱疹疫苗,将为全面推进中国健康老龄化发展发挥作用。
2、疫苗接种是预防和控制带状疱疹及其并发症最有效的手段。目前批准上市的疫苗有两种,分别是带状疱疹减毒活疫苗和重组带状疱疹佐剂亚单位疫苗。此外,还有一种带状疱疹灭活疫苗处于临床研究阶段。
3、2006年,美国fda批准首个带状疱疹减毒活疫苗(oka/merck strain,merck&co)上市,该疫苗是由merck公司开发的,基于其已上市的水痘减毒活疫苗(varivax,oka/merck),经浓缩制备,病毒含量是水痘减毒活疫苗的14倍,但是该疫苗预防带状疱疹的效力仅为60%-70%。merck公司开发的带状疱疹减毒活疫苗抗原用量大、生产成本高,免疫原性较差,诱导细胞免疫效果差,疫苗保护效力会随着年龄的增长而逐渐降低,并且由于其为减毒活疫苗,限制了其在免疫抑制人群、活动性肺结核患者、孕妇等人群的中使用。因此,2020年7月起,该疫苗已不再使用。
4、2017年,重组带状疱疹佐剂亚单位疫苗(shingrix,gsk)fda批准上市用于50岁以上人群预防带状疱疹和愈后神经痛,该疫苗由重组vzv糖蛋白e和t细胞加强佐剂as01b组成,针对带状疱疹的总体疫苗效力为97.2%。as01b佐剂包含两种免疫刺激剂mpla(3-o-desacyl-4’-monophosphoryl 1ipid a)和qs-21:mpla可激活天然免疫系统,刺激细胞因子的分泌和协同刺激分子的表达;qs-21是一种皂素,可促进抗原特异性抗体反应。但qs-21具有溶血性,需要配合胆固醇和脂质体形式使用以消除副作用。佐剂间接提示该脂质体系统应用于疫苗时稳定性有待进一步提高。此外,采用cho细胞系生产糖蛋白e,具有成本高,发酵、纯化工艺复杂、糖基化产物不稳定、质量控制难度大等缺点。
5、尽管带状疱疹疫苗在全球范围内大多数国家被推广应用,遗憾的是,目前中国仍无带状疱疹疫苗上市。
6、疫苗诱导机体产生体液免疫应答即vzv特异性抗体的能力,是疫苗有效性的一个保障。抗体水平的增长倍数与疫苗的保护性效力密切相关;同时,带状疱疹的发生也与体内vzv特异性细胞介导免疫(cell-mediated immunity,cmi)的下降有着重要的关联。由脂质纳米粒(lnps)包裹的体外转录的mrnas组成的核酸疫苗不仅可有效引发特异性的体液免疫,还激发cd4+t细胞免疫反应。通过lnp递送mrna抗原可提高对疫苗的免疫应答,lnp可以保护mrna不受酶降解,并促进靶细胞对mrna的有效摄取和细胞内释放。
7、因此,尽快研制带状疱疹mrna疫苗,进一步增强细胞免疫应答作用,提高疫苗的有效性,降低成本,是亟需解决的问题。
技术实现思路
1、为解决上述问题,本发明提供了一种新型的水痘-带状疱疹病毒mrna疫苗,通过对mrna核酸序列中的cds序列进行点突变和密码子优化,再选择合适的启动子、5’-utr、3’-utr和3’-端polya组合成完整的编码水痘-带状疱疹病毒的mrna核酸,并改进mrna疫苗的试剂配方,提高lnp载药量,最终获得能呈现强烈且稳定的免疫效果,大幅提升动物体内的抗体滴度,并且不影响动物正常生长的水痘-带状疱疹病毒mrna疫苗,还可显著降低疫苗成本,临床应用前景广阔。
2、一方面,本发明提供了一种编码水痘-带状疱疹病毒的核酸,具有如seq id no.1~seq id no.7任一项所示的序列,或与seq id no.1~seq id no.7任一项具有80%以上同源性的序列,或与seq idno.1~seq id no.7任一项所示的序列中取代、缺失或添加一个或多个核苷酸的序列,或与seq idno.1~seq id no.7任一项部分互补或完全互补的序列,或对seq id no.1~seq id no.7任一项所示的序列进行核苷酸修饰的序列。
3、本发明提供的编码水痘-带状疱疹病毒的核酸,包括编码水痘-带状疱疹病毒糖蛋白ge的核酸,所述核酸为mrna,用于制备mrna疫苗。
4、不同的物种,不同的细胞,选择的候选mrna序列是不同的,这是因为不同的物种,不同的细胞在编码同一种氨基酸时,选择的同义密码子是不同的(也就是密码子使用频率不同),具有各自的偏向性,此种现象称为密码子偏向性。故为了能够在疫苗后续的使用物种比如人或非人灵长类或啮齿类中能够利用其密码子的偏好性稳定且高表达蛋白,必须对ge蛋白翻译区进行密码子优化,才能用于制备mrna疫苗。
5、制备水痘-带状疱疹病毒的mrna疫苗,主要是对ge蛋白翻译区的进行点突变和密码子优化,获得cds序列,其中的点突变采用的是研究团队在前期研究过程中采用的点突变方式:使ge的第569位序列发生y到a的突变,且第593位序列发生s到a的突变,且第595位序列发生s到a的突变,且第596位序列发生t到a的突变,且第598位序列发生t到a的突变;密码子优化包括:针对在小鼠及人体或非人灵长类内表达时的密码子偏好性进行调整、针对在小鼠及人体内表达时的密码子偏好性进行调整,优化并添加个别的稀有密码子和多个终止密码子,得到大量的核苷酸序列;再经过平均gc含量的微调,优化避开因构建质粒时需要的其他酶切位点序列,优化个别连续的短重复碱基结构,优化个别的可能存在co-loop缺陷的二级结构,获得核苷酸序列,使其能顺利在小鼠及人体或非人灵长类内表达,再经筛选获得核苷酸序列如seq id no.1~seq id no.7所示的7条mrna核苷酸。
6、在一些方式中,本发明提供的编码水痘-带状疱疹病毒的核酸,是对水痘-带状疱疹病毒糖蛋白ge双突变株(包括y569a,s593a,s595a,t596a,t598a),其序列如seq idno.15所示)进行密码子优化,其中密码子优化包括:针对在小鼠及人体内表达时的密码子偏好性进行调整、常用密码子的使用频率进行调整得到大量的核苷酸序列;再根据适配质粒构建载体的酶切位点、gc含量、密码子适应指数、稀有密码子使用频率、二级结构等进行筛选,获得核苷酸序列如seq id no.1~seq id no.7所示的7条cds序列。
7、进一步地,还包括启动子、5’-utr、3’-utr或3’-端polya中的至少一种或多种。
8、本发明提供的mrna还包括启动子、5’-utr、3’-utr和3’-端polya等非编码区的序列,非编码区序列的选择也会影响mrna结构的稳定性,以及影响生物体内的目标蛋白翻译效率,因此针对每一个cds序列,还需选择合适的启动子、5’-utr、3’-utr和3’-端polya。
9、在一些方式中,本发明采用t7启动子。
10、在一些方式中,t7启动子优选采用ag结尾的t7promoter,有助于提高mrna结构的稳定性:taatacgactcactataag。
11、在一些方式中,cds序列还包括kozak序列。
12、在一些方式中,kozak序列分别采用ggctagcgccgccacc或gccacc或gccgccacc。
13、在一些方式中,5’utr序列分别采用gagaataaactagtattcttctggtccccacagactcagagagaaccc 或gggaaataagagagaaaagaagagtaagaagaaatataagaccccggcgcc 或gggaaataagagagaaaagaagagtaagaagaaatataagaccccggcgcc 或gagacccaagctggctagcgggagaaagcttacc 或cttgttctttttgcagaagctcagaataaacgctcaactttgg 或ttggaccctcgtacagaagctaatacgactcactatagggaaataagagagaaaagaagagtaagaagaaatataaga或gggaaataagagagaaaagaagagtaagaagaaatataaga。
14、在一些方式中,3’utr序列分别采用ctcgagctggtactgcatgcacgcaatgctagctgcccctttcccgtcctgggtaccccgagtctcccccgacctcgggtcccaggtatgctcccacctccacctgccccactcaccacctctgctagttccagacacctcccaagcacgcagcaatgcagctcaaaacgcttagcctagccacacccccacgggaaacaggattaacctttagcaataaacgaaagtttaactaagctatactaaccccagggttggtcaatttcgtgccagccacaccctggagctagc或gctggagcctcggtggcctagcttcttgccccttgggcctccccccagcccctcctccccttcctgcacccgtacccccgtggtctttgaataaagtctgagtgggcggca或tgataataggctggagcctcggtggcctagcttcttgccccttgggcctccccccagcccctcctccccttcctgcacccgtacccccgtggtctttgaataaagtctgagtgggcggc或gctggagcctcggtagccgttcctcctgcccgctgggcctcccaacgggccctcctcccctccttgcaccggcccttcctggtctttgaataaagtctgagtgggcagc或gctcgctttcttgctgtccaatttctattaaaggttcctttgttccctaagtccaactactaaactgggggatattatgaagggccttgagcatctggattctgcctaataaaaaacatttattttcattgc或
15、gctgccttctgcggggcttgccttctggccatgcccttcttctctcccttgcacctgtacctcttggtctttgaataaagcctgagtaggaagtgagggtctagaactagtgtcgacgc或tgataataggctggagcctcggtggccatgcttcttgccccttgggcctccccccagcccctcctccccttcctgcacccgtacccccgtggtctttgaataaagtctga。
16、进一步地,所述seq id no.1~seq id no.7任一项所示的序列与启动子、5’-utr、3’-utr和3’-端polya组合后的序列分别如seq id no.8~seq id no.14所示。
17、cds序列为seq id no.1时,与优选的启动子、5’-utr、3’-utr和3’-端polya组合后的mrna序列为seq id no.8;cds序列为seq id no.2时,与优选的启动子、5’-utr、3’-utr和3’-端polya组合后的mrna序列为seq id no.9;cds序列为seq id no.3时,与优选的启动子、5’-utr、3’-utr和3’-端polya组合后的mrna序列为seq id no.10;cds序列为seq idno.4时,与优选的启动子、5’-utr、3’-utr和3’-端polya组合后的mrna序列为seq idno.11;cds序列为seq id no.5时,与优选的启动子、5’-utr、3’-utr和3’-端polya组合后的mrna序列为seq id no.12;cds序列为seq id no.6时,与优选的启动子、5’-utr、3’-utr和3’-端polya组合后的mrna序列为seq id no.13;cds序列为seq id no.7时,与优选的启动子、5’-utr、3’-utr和3’-端polya组合后的mrna序列为seq id no.14。
18、进一步地,所述编码水痘-带状疱疹病毒的核酸优选具有如seq id no.4或seq idno.5所示的序列。
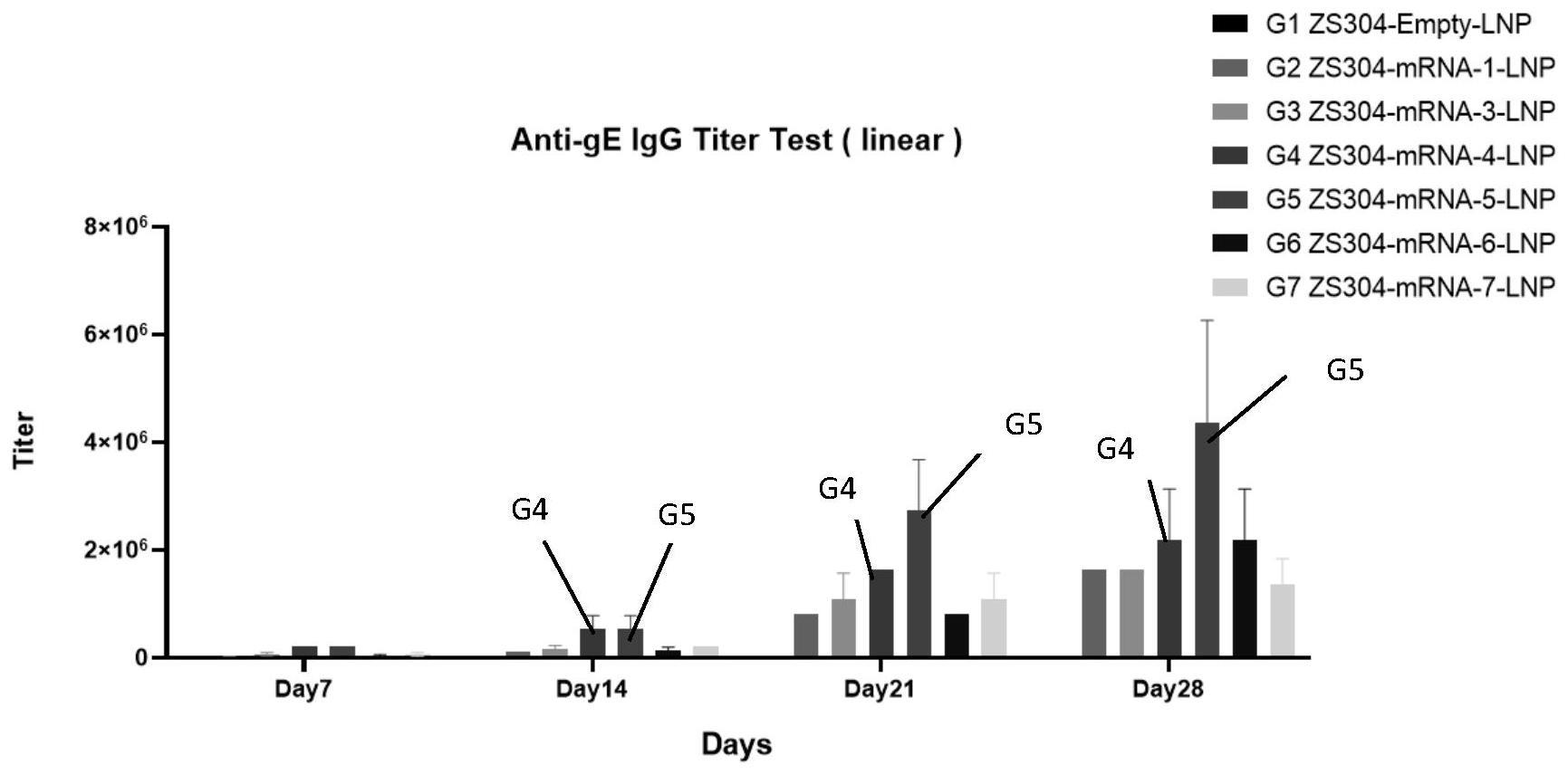
19、研究证明,含有seq id no.4或seq id no.5所示序列的mrna疫苗,能在动物体内产生更高更稳定的抗体滴度。
20、进一步地,具有如seq id no.11或seq id no.12所示的序列。
21、cds序列为seq id no.4或seq id no.5时,与启动子、5’-utr、3’-utr和3’-端polya组合后的mrna序列为seq id no.11或seq id no.12。
22、另一方面,本发明提供了一种核酸-脂质复合物,包括如上所述的核酸和递送核酸的脂质体。
23、进一步地,所述递送核酸的脂质体包括缓冲液和脂质溶液;所述缓冲液与如上所述的核酸共同组成水相溶液,缓冲液ph为4~6;所述脂质溶液用于包裹水相溶液。
24、进一步地,所述缓冲液中包括冰乙酸、三水乙酸钠和depc水;所述脂质溶液中的脂质含量为10~20mg/ml,所述脂质包括可电离阳离子脂质、胆固醇、磷脂和peg化脂质。
25、在一些方式中,缓冲液中还包括氨基丁三醇、三(羟甲基)氨基甲烷盐酸盐,ph为5.5。
26、在一些方式中,所述脂质溶液中的脂质含量为10~20mg/ml,所述脂质包括可电离阳离子脂质、胆固醇、磷脂和peg化脂质。
27、在一些方式中,所述sm-102:胆固醇:dspc:dmg-peg2000的质量比为141.36:59.26:31.44:14.97。
28、现有的mrna疫苗试剂的载药量较低,在生物体内要达到治疗效果所需要的用量较大,存在试剂用量大给患者带来潜在的毒副作用增加的危害隐患。因此需要开发载药量更高、用量和毒副作用更低、免疫效果更好的,既可以预防也可以起到治疗作用的mrna疫苗试剂。本发明所述载药量是指单位体积的药物试剂中mrna的含量。
29、比如,现有水痘-带状疱疹mrna试剂配方的载药量较低,导致同等剂量时所需的给药试剂体积偏大,同时由于载药量低,使较多的大分子辅料带入体内,副作用风险高。
30、本发明通过改进水痘-带状疱疹mrna疫苗试剂的缓冲液配方和ph,使试剂配方中的mrna载药量显著提升,同等辅料物质的量下,提高单位体积mrna载药量,可以有效减少同等剂量下的给药制剂体积,从而获得更加显著的免疫治疗效果,同时相应地减少了进入体内的大分子辅料等的量,在一定程度上降低辅料可能带来的副反应,如有效减少peg等成分在其他脏器或组织等中的免疫刺激作用。
31、在一些方式中,本发明经研究证明,相比于现有的含有三甲胺、盐酸三乙胺等成分的水相溶液配方,采用本发明提供的含有氨基丁三醇和三(羟甲基)氨基甲烷盐酸盐的水相溶液配方能显著提升注射试剂的载药量,同时该试剂具有非常好的稳定性,可长期保存,其中的mrna含量等药物成分含量稳定,有良好的临床应用条件。
32、另外,本发明发现,维持水相溶液合适的ph值,也能显著提升用于微针皮内注射的mrna疫苗的载药量,若将ph调至4~6等偏酸性范围内,能使脂质体中负载的mrna含量显著提升,并在特定ph条件下,即ph5.5时达到最优。其原因可能是,在制备时,在偏酸环境可以使得可电离阳离子脂质带正电荷,同等条件下可以吸附更多核酸分子(如mrna等,本身带负电荷),且这种最优是在水相制备溶液为ph5.5时体现,相比于ph7.4或ph4等条件下的缓冲液,ph5.5时可以更加有效荷载核酸分子,达成相对稳定的可用制剂,因此载药量更高。
33、在一些方式中,所述缓冲液中的氨基丁三醇:三(羟甲基)氨基甲烷盐酸盐:冰乙酸:三水乙酸钠:depc水的质量比为99.2:377.6:13.76:64:40。本发明提供的水相溶液配方必须严格按照特定比例配置,才能维持在较高的载药量。
34、在一些方式中,所述脂质溶液中的脂质含量为10~20mg/ml,所述脂质包括可电离阳离子脂质、胆固醇、磷脂和peg化脂质。
35、本发明经大量研究证明,通过调控试剂中的脂质含量,也可显著提高脂质体的载药量。所述脂质包括胆固醇、可电离阳离子脂质、磷脂和peg化脂质,是一种复合脂质体;提高脂质含量,是指同时提高胆固醇、可电离阳离子脂质、磷脂和peg化脂质四种成分的含量,使脂质溶液中的脂质含量从最初的7.72mg/ml提高到10~20mg/ml,最优选为15.44mg/ml,可使脂质制剂体系的载药量由29.39μg/ml左右至少提高到157.75μg/ml左右。
36、在一些方式中,所述可电离阳离子脂质为sm-102(十七烷-9-基-8-((2-羟乙基)(6-氧代-6-((十一烷氧基)己基)氨基)辛酸酯));磷脂为dspc(1,2-二硬脂酰-sn-甘油-3-磷酸胆碱);peg化脂质为dmg-peg(1,2-二肉豆蔻酰-rac-甘油-3-甲氧基聚乙二醇2000),其peg分子量范围可为1000~5000da;可电离阳离子脂质:胆固醇:磷脂:peg化脂质的质量比为(9~10):(3~4):(2~3):1。
37、在一些方式中,所述peg化脂质为dmg-peg2000;所述sm-102:胆固醇:dspc:dmg-peg2000的质量比为141.36:59.26:31.44:14.97。
38、本发明提供的核酸-脂质复合物通过微流控纳米药物制备系统制得。
39、再一方面,本发明提供了一种水痘-带状疱疹病毒疫苗,所述疫苗包括如上所述的核酸,或包括如上所述的核酸-脂质复合物。
40、再一方面,本发明提供了一种水痘-带状疱疹病毒疫苗在提高动物体内产生的水痘-带状疱疹病毒抗体滴度的用途,所述疫苗包括如seq id no.4或seq id no.5所示的序列,或包括如seq id no.11或seq id no.12所示的序列。
41、再一方面,本发明提供了一种脂质体在制备高载药量的水痘-带状疱疹病毒疫苗的用途,所述脂质体包括缓冲液和脂质溶液;所述缓冲液与如上所述的mrna共同组成水相溶液,缓冲液ph为4~6;所述脂质溶液用于包裹水相溶液;其中,缓冲液中包括氨基丁三醇和三(羟甲基)氨基甲烷盐酸盐;所述脂质溶液中的脂质含量为10~20mg/ml,所述脂质包括可电离阳离子脂质、胆固醇、磷脂和peg化脂质。
42、本发明具有以下有益效果:
43、(1)通过对mrna核酸序列中的cds序列进行点突变和密码子优化,再选择合适的启动子、5’-utr、3’-utr和3’-端polya组合成完整的编码水痘-带状疱疹病毒的mrna核酸,共计筛选获得7组全新的编码水痘-带状疱疹病毒的mrna核酸;
44、(2)改进了lnp的试剂配方,提高lnp载药量;
45、(3)采用编码水痘-带状疱疹病毒的mrna核酸,与lnp组合,制备得到mrna疫苗,最终获得能呈现强烈且稳定的免疫效果,大幅提升动物体内的抗体滴度,并且不影响动物正常生长;
46、(4)降低疫苗成本,临床应用前景广阔。
47、详细说明
48、定义
49、除非另有定义,否则本文中使用的所有技术和科学术语所具有的含义与本发明所属领域的普通技术人员通常理解的相同。以下参考文献为本领域技术人员提供了本发明中使用的许多术语的一般定义:生物化学与分子生物学词典(dictionary of biochemistryand molecular biology),(第2版)j.stenesh(编著),wiley-interscience(1989);微生物学与分子生物学词典(dictionary of microbiology and molecular biology)(第3版),p.singleton和d.sainsbury(编著),wiley-interscience(2007);钱伯斯科技词典(chambers dictionary of science and technology)(第2版),p.walker(编著),chambers(2007);遗传学词汇(glossary of genetics)(第5版),r.rieger等(编著),springer-verlag(1991);以及哈珀柯林斯生物学词典(the harpercollins dictionaryof biology),w.g.hale和j.p.margham,(编著),harpercollins(1991)。
50、尽管与本文所描述的类似或等效的任何方法和组合物可用于本发明的实践或检验,但本文描述了优选的方法和组合物。出于本发明的目的,下面为了清楚和便于参考起见对以下术语加以定义:根据长期以来的专利法惯例,当在本技术包括权利要求书中使用不带数量指示的指称物时,表示“一或多”。术语“约”和“近似”用于本文中时是可互换的,并且一般应理解为是指一个给定数字周围的数字范围,以及所叙述的数字范围内的所有数字。此外,本文中的所有数值范围应理解为包括该范围内的各个整数。
51、mrna
52、mrna可以包括至少两种核苷酸。核苷酸可以是天然存在的核苷酸或修饰核苷酸。在一些实施例中,rna分子包括约5种核苷酸至约5,000种核苷酸。在一些实施例中,rna分子包括至少约5种核苷酸。在一些实施例中,rna分子包括至多约5,000种核苷酸。在一些实施例中,rna分子包括约5种核苷酸至约20种核苷酸、约5种核苷酸至约40种核苷酸、约5种核苷酸至约60种核苷酸、约5种核苷酸至约80种核苷酸、约5种核苷酸至约100种核苷酸。在一些实施例中,rna分子包括约5种核苷酸、约20种核苷酸、约40种核苷酸、约60种核苷酸、约80种核苷酸、约100种核苷酸、约200种核苷酸、约500种核苷酸、约1,000种核苷酸、约2000种核苷酸或约5000种核苷酸。
53、mrna可以包括至少一种本技术所述的修饰核苷酸。在一些实施例中,rna分子包括约1种修饰核苷酸至约100种修饰核苷酸。在一些实施例中,rna分子包括至少约1种修饰核苷酸。在一些实施例中,rna分子包括至多约100种修饰核苷酸。
54、mrna可以包括至少0.1%的修饰核苷酸。修饰核苷酸的分数可以计算为:修饰核苷酸的数量/核苷酸的总数*100%。在一些实施例中,rna分子包括约0.1%修饰核苷酸至约100%修饰核苷酸。在一些实施例中,rna分子包括至少约0.1%的修饰核苷酸。在一些实施例中,rna分子包括至多约100%修饰核苷酸。
55、经过修饰的核苷酸
56、在一些方式中,所述的mrna包括经过修饰的核苷酸,其中修饰的核苷酸选择如下一种或者几种核苷酸:2-氨基腺苷、2-硫代胸苷、肌苷、吡咯并嘧啶、3-甲基腺苷、5-甲基胞苷、c-5丙炔基-胞苷、c-5丙炔基-尿苷、2-氨基腺苷、c5-溴尿苷、c5-氟尿苷、c5-碘尿苷、c5-丙炔基-尿苷、c5-丙炔基-胞苷、c5-甲基胞苷、2-氨基腺苷、7-脱氮腺苷、7-脱氮鸟苷、8-氧代腺苷、8-氧代鸟苷、o(6)-甲基鸟嘌呤、假尿苷、n-1-甲基-假尿苷、2-硫代尿苷以及2-硫代胞苷;甲基化碱基;插入碱基;2'-氟代核糖、核糖、2'-脱氧核糖、阿拉伯糖以及己糖;硫代磷酸基和5'-n-亚磷酰胺键。以及pct/cn2020/074825,pct/cn2020/106696中所描述的改性核苷酸进行修饰。
57、mrna疫苗
58、mrna疫苗是将含有编码抗原蛋白的mrna导入人体,直接进行翻译,形成相应的抗原蛋白,从而诱导机体产生特异性免疫应答,达到预防免疫的作用,是继灭活疫苗、减毒活疫苗、亚单位疫苗和病毒载体疫苗后的第三代疫苗,具有针对病原体变异反应速度快、生产工艺简单、易规模化扩大等特点。mrna疫苗的基本原理是通过特定的递送系统将表达抗原靶标的mrna导入体内,在体内表达出蛋白并刺激机体产生特异性免疫学反应,从而使机体获得免疫保护。
59、由于mrna自身的稳定性差、易被组织内的核酸酶降解、进入细胞的效率较低、翻译效率较低等问题,这些缺陷限制了mrna疫苗的应用,不同的递送载体对mrna疫苗的稳定性和翻译效率也起到非常关键的作用,递送载体可分为病毒载体和非病毒载体(包括脂质体、非脂质体、病毒、纳米颗粒等)。因此需要进行相关的改进措施,以下是mrna制备的药理学改进策略:1、合成帽类似物或使用加帽酶通过与真核翻译起始因子4e(eif4e)结合来稳定mrna并增加蛋白翻译;2、调节5′-非翻译区(utr)和3′-utr中的元件来稳定mrna并增加蛋白翻译;3、添加poly(a)尾可使mrna稳定并增加蛋白质翻译;4、修饰核苷来减少先天免疫激活并增加翻译;5、使用rnase iii处理和快速蛋白质液相色谱(fplc)纯化可降低免疫激活并增加翻译;6、优化序列或密码子来增加翻译;7、翻译起始因子和其他方法的共同递送来改变翻译和免疫原性。本发明主要通过采用突变序列,优化密码子,并调整启动子、5′-utr、3′-utr和poly(a)尾,从而获得能产生更高免疫活性的水痘-带状疱疹mrna疫苗。
60、cds序列
61、cds(coding sequence)是指成熟mrna中可以被翻译为蛋白质的编码序列区域,自起始密码子开始至终止密码子结束。cds必定是一个orf(开放读码框),但也可能包括很多orf。反之,每个orf不一定都是cds。该区域由外显子组成,编码蛋白质的部分,边界范围从靠近5′末端的起始密码子开始,到靠近3′末端的终止密码子为止。mrna的编码区范围位于5′非翻译区和部分同样为外显子的3′非翻译区之间。
62、合成后处理
63、合成后可加入5'帽和/或3'尾。帽的存在可以提供对大多数真核细胞中发现的核酸酶的抗性。“尾”的存在可以用于保护mrna免于核酸外切酶降解和/或调节蛋白质表达水平。
64、可以如下添加5'帽:第一,rna末端磷酸酶从5'核苷酸中去除一个末端磷酸基,留下两个末端磷酸基;然后通过鸟苷酰转移酶将鸟苷三磷酸(gtp)加入到末端磷酸基中,产生5,5,5三磷酸键;然后用甲基转移酶将鸟嘌呤的7-氮甲基化。帽结构的实例包括但不限于m7g(5')ppp(5'(a,g(5')ppp(5')a 和g(5')ppp(5')g。更多帽结构在已公布的美国申请no.us 2016/0032356中进行了描述,阿什奎尔海克(ashiqul haque)等,“化学修饰的hcftrmrna在囊性纤维化小鼠模型中恢复肺功能”(chemicallymodifiedhcftr mrnasrecuperate lung function in a mouse model of cysticfibrosis),科学报告(scientific reports)(2018)8:16776,以及科尔(kore)等,“5'-端帽类似物的最新进展:合成和生物分支”(recent developments in 5’-terminal cap analogs:synthesisandbiological ramifications)有机化学迷你读物(mini-reviews in organic chemistry)2008,5,179-192,其通过引用并入本技术。
65、尾结构可以包括聚(a)和/或聚(c)尾。mrna的3'末端(例如,3'末端的10、20、30、40、50、60、70、80、90或100种核苷酸)上的聚-a尾可以包括至少50%、55%、65%、70%、75%、80%、85%、90%、92%、94%、95%、96%、97%、98%或99%的腺苷核苷酸。mrna的3'末端(例如,3'末端的10、20、30、40、50、60、70、80、90或100种核苷酸)上的聚-a尾可以包括至少50%、55%、65%、70%、75%、80%、85%、90%、92%、94%、95%、96%、97%、98%或99%胞嘧啶核苷酸。
66、如本技术所述,添加5'帽和/或3'尾可以有助于检测体外合成期间产生的无效转录物,因为没有加帽和/或加尾,那些过早中止的mrna转录物的大小可能太小而无法被检测到。因此,在一些实施例中,在测试mrna纯度(例如,mrna中存在的无效转录物的水平)之前,将5'帽和/或3'尾加入合成的mrna中。在一些实施例中,在如本技术所述纯化mrna之前,将5'帽和/或3'尾加入到合成的mrna中。在其他实施例中,在如本技术所述纯化mrna后,将5'帽和/或3'尾加入到合成的mrna中。
67、除了以上方法外,加帽或者加尾的步骤是在从dna体外转录为rna的转录过程总完成的,这些方法都是本领域一般技术人员可以自由选择。
68、根据本发明合成的mrna可以不需进一步纯化而使用。特别地,可以使用根据本发明合成的mrna而无需去除短聚物的步骤。在一些实施例中,根据本发明合成的mrna进一步纯化。根据本发明可以使用各种方法纯化合成的mrna。例如,可以使用离心、过滤和/或色谱方法进行mrna的纯化。在一些实施例中,合成的mrna通过乙醇沉淀或过滤或色谱法、或凝胶纯化或任何其它合适的方法纯化。在一些实施例中,通过hplc纯化mrna。在一些实施例中,在标准酚:氯仿:异戊醇溶液中提取mrna,这是本领域技术人员所熟知的。在一些实施例中,使用切向流过滤纯化mrna。合适的纯化方法包括在us 2016/0040154、us 2015/0376220、于2018年2月27日提交的pct申请pct/us18/19954,名称为“用于纯化信使rna的方法”以及于2018年2月27日提交的题为“纯化信使rna的方法”的pct申请pct/us18/19978中所描述的方法,所有这些都通过引用并入本技术并且可以用于实施本发明。
69、在一些实施例中,mrna在加帽和封尾之前被纯化。在一些实施例中,加帽和封尾之后纯化mrna。在一些实施例中,加帽和封尾之前和之后均纯化mrna。在一些实施例中,通过离心在加帽和封尾之前或之后或之前和之后均纯化mrna。在一些实施例中,通过过滤在加帽和封尾之前或之后或之前和之后均纯化mrna。在一些实施例中,通过切向流过滤(tff)或通过色谱法在加帽和封尾之前或之后或之前和之后均纯化mrna。
70、在一些方式中,加尾是伴随转录同时完成的,因此,也可以在加尾和加帽步骤完成后对核酸进行纯化,纯化的方法如前述的方法。所以,在一些方式中,纯化步骤应该都是在封尾之后。当然,mrna也可以在加帽之前被纯化。当然也可以在转录之后就进行纯化。可以使用本领域可用的任何方法来检测和定量mrna的全长或无效转录物。在一些实施例中,使用印迹、毛细管电泳、色谱、荧光、凝胶电泳、hplc、银染色、光谱、紫外(uv)或uplc或其组合检测合成的mrna分子。本领域已知的其他检测方法包括在本发明中。在一些实施例中,使用uv吸收光谱法通过毛细管电泳分离来检测合成的mrna分子。在一些实施例中,在凝胶电泳之前,mrna被乙二醛染料变性。在一些实施例中,合成的mrna在加帽或封尾前表征。在一些实施例中,合成的mrna在加帽和封尾后表征。
71、在一些实施例中,根据本发明制备的mrna基本上没有短聚物或无效转录物。特别地,通过毛细管电泳或乙二醛凝胶电泳,根据本发明制备的mrna包括不可检测水平的短聚物或无效转录物。如本文所用,术语“短聚物”或“无效转录物”是指任何小于全长的转录物。在一些实施例中,“短聚物”或“无效转录物”的长度小于100核苷酸、小于90、小于80、小于70、小于60、小于50、小于40、小于30、小于20或者长度小于10核苷酸。在一些实施例中,添加5'-帽和/或3'-聚a尾后检测或量化短聚物。
72、utr序列
73、3’-非翻译区(3’-utr):通常,术语“3’-utr”是指人工核酸分子的一部分,其位于可读框的3’(即“下游”),并且其不翻译为蛋白。通常,3’-utr是mrna的蛋白编码区(可读框(orf)或编码序列(cds))和聚腺苷酸序列之间的mrna的一部分。在本发明的情况中,术语3’-utr还可以包含这样的元件,其不在模板中编码,rna由其转录,但在成熟过程中在转录后添加,例如聚腺苷酸序列。mrna的3’-utr不翻译为氨基酸序列。3′utr序列通常由在基因表达过程中被转录为各自的mrna的基因编码。基因组序列首先转录为包含任选内含子的成熟前mrna。成熟前mrna随后在成熟过程中进一步被加工为成熟mrna。该成熟过程包含以下步骤:5′加帽、剪接成熟前mrna以切除任选内含子和3′末端修饰(如成熟前mrna 3′末端的聚腺苷酸化和任选的核酸内切酶/或核酸外切酶切割等)。在本发明范围内,3′-utr对应于位于蛋白编码区终止密码子,优选紧接蛋白编码区终止密码子的3′端和mrna的聚腺苷酸序列之间。术语“对应于”意为3′-utr序列可以是如用于限定3′-utr序列的mrna序列中的rna序列,或对应于此rna序列的dna序列中。在本发明范围内,术语“基因的3′-utr”,为对应于源自该基因的成熟mrna的3′-utr的序列,所述成熟mrna即通过基因转录和成熟前mrna的成熟获得的mrna。术语“基因的3′-utr”包括3′-utr的dna序列和rna序列(正义和反义链二者以及成熟和未成熟的二者)。优选3′utr具有多于20,30,40或50个核苷酸的长度。3′-非翻译区(3′utr):3′utr典型地是mrna的一部分,其位于mrna的蛋白编码区(即可读框)和多聚腺苷酸序列之间。mrna的3′utr不翻译为氨基酸序列。在本发明范围内,3′utr对应于位于蛋白编码区终止密码子的3′端,优选紧接蛋白编码区终止密码子的3′端,并且向多聚腺苷酸序列的5′侧,优选向紧接多聚腺苷酸序列的5′侧的核苷酸延伸的成熟mrna序列。术语“对应于”意为3′utr序列可以是如用于限定3′utr序列的mrna序列中的rna序列,或对应于此rna序列的dna序列中。在本发明范围内,术语“基因的3′utr”,如“白蛋白基因的3′utr”,为对应于源自该基因的成熟mrna的3′utr的序列,所述成熟mrna即通过基因转录和成熟前mrna的成熟获得的mrna。术语“基因的3′utr”包括3′utr的dna序列和rna序列。
74、5’-非翻译区(5’-utr):通常,术语“5’-utr”是指人工核酸分子的一部分,其位于可读框的5’(即“上游”),并且其不翻译为蛋白。5’-utr通常理解为信使rna(mrna)的特定区段,所述信使rna位于mrna的可读框的5’。通常,5’-utr在转录起始位点起始并且在可读框的起始密码子之前的一个核苷酸处终止。优选地,所述5’utr具有多于20,30,40或50个核苷酸的长度。5’-utr可以包含用于控制基因表达的元件,也称为调控元件。所述调控元件可以是例如核糖体结合位点。5’-utr可以被转录后修饰,例如通过加入5’-帽修饰。mrna的5’-utr不翻译为氨基酸序列。5’-utr序列通常由基因表达过程中转录为各个mrna的基因编码。基因组序列首先转录为成熟前mrna,其包含任选的内含子。成熟前mrna然后在成熟过程中进一步加工为成熟mrna。该成熟过程包括以下步骤:5′加帽、剪接成熟前mrna以切除任选内含子和3′末端修饰(如成熟前mrna 3′末端的聚腺苷酸化和任选的核酸内切酶/或核酸外切酶切割等)。在本发明范围内,5′-utr对应于位于起始密码子和例如5’-帽之间的成熟mrna序列。优选地,5′-utr对应于从位于5′帽的3′侧的核苷酸,更优选从紧邻5′帽的3′侧核苷酸,向位于蛋白编码区起始密码子5′侧的核苷酸,优选向紧接蛋白编码区起始密码子5′侧的核苷酸延伸的序列。紧接成熟mrna 5′帽的3′侧的核苷酸典型地对应于转录起始位点。术语“对应于”意为5′-utr序列可以是如用于限定5′-utr序列的mrna序列中的rna序列,或与此rna序列对应的dna序列。在本发明范围内,术语“基因的5′-utr”,是对应于源自该基因的成熟mrna的5′-utr的序列,所述成熟mrna即通过基因转录和成熟前mrna的成熟获得的mrna。术语“基因的5′-utr”包括5′-utr的dna序列和rna序列(正义和反义链以及成熟和未成熟的二者)。
75、作为mrna稳定化的备选方案,已经发现天然存在的真核mrna分子含有特征稳定化元件。例如,它们可以包含在其5'末端(5'-utr)和/或在其3'末端(3'-utr)的所谓非翻译区(utr)以及其它结构特征,如5'帽结构或3'-聚腺苷酸尾。5'-utr和3'-utr二者都典型地从基因组dna转录并且因此是成熟前(premature)mrna元件。在mrna加工过程中,成熟mrna的特有结构特征,如5'帽和3'-聚腺苷酸尾(也称为多聚腺苷酸尾或聚腺苷酸序列)通常被添加于转录的(成熟前)mrna。
76、3'-聚腺苷酸尾典型地是添加在转录的mrna的3'末端的一段单调腺苷核苷酸序列。其可以包含至多约400个腺苷核苷酸。发现此种3'-聚腺苷酸尾的长度对于个体mrna的稳定性是可能的关键要素。此外,已显示α-球蛋白mrna的3'utr可能是对于公知的α-球蛋白mrna稳定性的重要因素(rodgers等人,regulatedα-globin mrna decay is acytoplasmic eventproceeding through 3'-to-5'exosome-dependent decapping,rna,8,第1526-1537页,2002)。α-球蛋白mrna的3'utr明显参与特定核蛋白-复合物(α-复合物)的形成,其存在与mrna体外稳定性相关(wang等人,an mrna stability complexfunctions with poly(a)-binding protein to stabilize mrna in vitro,molecularand cellular biology,第19卷,第7期,1999年7月,第4552-4560页)。对于核糖体蛋白mrna中的utr已经进一步表明有趣的调节功能:在核糖体蛋白mrna的5’-utr控制生长相关的mrna翻译的同时,该调节的严格性由核糖体蛋白mrna中的各个3’-utr赋予(ledda等人,effect of the 3’-utr length on the translationalregulation of 5’-terminaloligopyrimidine mrnas,gene,第344卷,2005,p.213-220)。该机制促进核糖体蛋白的特异表达,所述核糖体蛋白通常以恒定的方式转录从而一些核糖体蛋白mrna如核糖体蛋白s9或核糖体蛋白l32称为看家基因(janovick-guretzky等人,housekeeping gene expressionin bovine liver is affected by physiologicalstate,feed intake,and dietarytreatment,j.dairy sci.,vol.90,2007,p.2246-2252)。核糖体蛋白的生长相关的表达模式因此主要是由于对翻译水平的调节。
77、术语“3’-utr元件”是指包含源自3’-utr或源自3’-utr的变体或片段的核酸序列或由源自3’-utr或源自3’-utr的变体或片段的核酸序列组成的核酸序列。“3’-utr元件”优选是指人工核酸序列,如人工mrna的3’-utr包含的核酸序列。因此,在本发明的意义中,优选地,3’-utr元件可以由mrna,优选人工mrna的3’-utr包含,或3’-utr元件可以由各自的转录模板的3’-utr包含。优选地,3’-utr元件是对应于mrna的3’-utr,优选人工mrna,如通过转录基因改造的载体构建体获得的mrna的3’-utr的核酸序列。优选地,本发明的意义中的3’-utr元件作为3’-utr行使功能或编码执行3’-utr的功能的核苷酸序列。
78、因此,术语“5’-utr元件”是指包含源自5’-utr或5’-utr的变体或片段的核酸序列或由源自5’-utr或5’-utr的变体或片段的核酸序列组成的核酸序列。“5’-utr元件”优选是指人工核酸序列,如人工mrna的5’-utr包含的核酸序列。因此,在本发明的意义中,优选地,5’-utr元件可以由mrna,优选人工mrna的5’-utr包含,或5’-utr元件可以由各自的转录模板的5’-utr包含。优选地,5’-utr元件是对应于mrna的5’-utr,优选人工mrna,如通过转录基因改造的载体构建体获得的mrna的5’-utr的核酸序列。优选地,本发明的意义中的5’-utr元件作为5’-utr行使功能或编码执行5’-utr的功能的核苷酸序列。
79、根据本发明的人工核酸分子中的3’-utr元件和/或5’-utr元件延长和/或增加从所述人工核酸分子的蛋白生产。因此,根据本发明的人工核酸分子可以尤其包含一下一种或者几种功能的3’-utr元件和/或5’-utr元件:增加从所述人工核酸分子的蛋白生产的3’-utr元件,延长从所述人工核酸分子的蛋白生产的3’-utr元件,增加和延长从所述人工核酸分子的蛋白生产的3’-utr元件,增加从所述人工核酸分子的蛋白生产的5’-utr元件,延长从所述人工核酸分子的蛋白生产的5’-utr元件,增加和延长从所述人工核酸分子的蛋白生产的5’-utr元件,增加从所述人工核酸分子的蛋白生产的3’-utr元件和增加从所述人工核酸分子的蛋白生产的5’-utr元件,增加从所述人工核酸分子的蛋白生产的3’-utr元件和延长从所述人工核酸分子的蛋白生产的5’-utr元件,增加从所述人工核酸分子的蛋白生产的3’-utr元件和增加和延长从所述人工核酸分子的蛋白生产的5’-utr元件,延长从所述人工核酸分子的蛋白生产的3’-utr元件和增加从所述人工核酸分子的蛋白生产的5’-utr元件,延长从所述人工核酸分子的蛋白生产的3’-utr元件和延长从所述人工核酸分子的蛋白生产的5’-utr元件,延长从所述人工核酸分子的蛋白生产的3’-utr元件和增加和延长从所述人工核酸分子的蛋白生产的5’-utr元件,增加和延长从所述人工核酸分子的蛋白生产的3’-utr元件和增加从所述人工核酸分子的蛋白生产的5’-utr元件,增加和延长从所述人工核酸分子的蛋白生产的3’-utr元件和延长从所述人工核酸分子的蛋白生产的5’-utr元件,或增加和延长从所述人工核酸分子的蛋白生产的3’-utr元件和增加和延长从所述人工核酸分子的蛋白生产的5’-utr元件。优选地,根据本发明的人工核酸分子包含延长从所述人工核酸分子的蛋白生产的3’-utr元件和/或增加从所述人工核酸分子的蛋白生产的5’-utr元件。优选地,根据本发明的人工核酸分子包含至少一个3’-utr元件和至少一个5’-utr元件,即延长和/或增加从所述人工核酸分子的蛋白生产并且源自稳定mrna的至少一个3’-utr元件和延长和/或增加从所述人工核酸分子的蛋白生产并且源自稳定mrna的至少一个5’-utr元件。“延长和/或增加从所述人工核酸分子的蛋白生产”通常是指与从缺少3’-utr和/或5’-utr或包含参比3’-utr和/或参比5’-utr(如天然与orf组合存在的3’-utr和/或5’-utr)的各个参比核酸产生的蛋白的量相比,从具有各个3’-utr元件和/或5’-utr元件的根据本发明的人工核酸分子产生的蛋白的量。尤其是,与缺少3’-utr和/或5’-utr或包含参比3’-utr和/或5’-utr,如天然与orf组合存在的3’-和/或5’-utr的各个核酸相比,根据本发明的人工核酸分子的至少一个3’-utr元件和/或5’-utr元件延长从根据本发明的人工核酸分子,例如从根据本发明的mrna的蛋白生产。尤其是,与缺少3’-和/或5’-utr或包含参比3’-和/或5’-utr,如天然与orf组合存在的3’-和/或5’-utr的各个核酸相比,根据本发明的人工核酸分子的至少一个3’-utr元件和/或5’-utr元件增加从根据本发明的人工核酸分子,例如从根据本发明的mrna的蛋白生产,尤其是蛋白表达和/或总蛋白生产。优选地,与缺少3’-utr和/或5’-utr或包含参比3’-utr和/或参比5’-utr,如天然与orf组合存在的3’-utr和/或5’-utr的各个核酸的翻译效率相比,根据本发明的人工核酸分子的所述至少一个3’-utr元件和/或所述至少一个5’-utr元件不消极影响核酸的翻译效率。甚至更优选地,与其天然情况下各个orf编码的蛋白的翻译效率相比,翻译效率由3’-utr和/或5’-utr增强。本文中使用的术语“各个核酸分子”或“参比核酸分子”意为-除不同3’-utr和/或5’-utr之外-参比核酸分子是与包含3’-utr元件和/或5’-utr元件的本发明的人工核酸分子相当的,优选相同的。
80、递送载体
81、可使用任何方法配制和递送根据本发明合成的mrna用于体内生产蛋白质,例如抗体,或者抗原,或者抗体片段或者抗原片段等。在一些实施例中,将mrna封装到转移载体中,例如纳米颗粒。除此之外,这种包封的一个目的通常是保护核酸免受可能含有降解核酸和/或引起核酸快速排泄的系统或受体的酶或化学物质的环境的影响,并促进细胞摄取和相应序列的表达。因此在一些实施例中,合适的递送载体能增强其中包括mrna的稳定性和/或促进mrna递送至靶细胞或组织。在一些实施例中,纳米颗粒可以是基于脂质的纳米颗粒,例如包括脂质体或基于聚合物的纳米颗粒。在一些实施例中,用于递送载体的纳米颗粒可具有约1~1000nm之间的颗粒直径。纳米颗粒可包括至少0.001μg、0.01μg、0.1μg、1μg、10μg、100μg、1mg、10mg、100mg、1g或更多mrna。
82、当然,这种纳米粒子也可以是核壳类结构的颗粒,如果核酸与聚合物混合形成了核,然后再在核结构外包裹脂质体,也可以通过本发明的混合器来完成。可以先通过混合器让核酸和聚合物形成微粒结构,然后在通过混合器让微粒与脂质成分形成微粒结构。这种所谓的核壳结构,例如专利申请号201880001680.5中所有核的材料以及壳的材料都可以用本发明的混合器来形成,该专利的所有组成核的材料和形成壳的材料都是本发明的一个具体实施方式。
83、在一些实施例中,转运载体是脂质体囊泡、或促进核酸转移至靶细胞和组织的其他手段。合适的转运载体可以包括但不限于脂质体、纳米脂质体、含神经酰胺的纳米脂质体、蛋白脂质体、纳米颗粒、磷酸钙-硅酸盐纳米颗粒、磷酸钙纳米颗粒、二氧化硅纳米颗粒、纳米晶颗粒、半导体纳米颗粒、聚(d-精氨酸)、纳米树枝状聚合物、淀粉基递送系统、胶束、乳剂、囊泡、质粒、病毒、钙磷酸基核苷酸、适体、肽和其他载体标签。还考虑使用生物离子胶囊和其他病毒衣壳蛋白组装体作为合适的转移载体。(hum.gene ther.2008september;19(9):887-95)。
84、脂质纳米颗粒可以包括一种或以上阳离子脂质、一种或以上非阳离子脂质、一种或以上基于甾醇的脂质、和/或一种或以上peg-改性脂质。脂质体可包括三种或更多种不同的脂质组分,脂质的一种不同组分是基于甾醇的阳离子脂质。在一些实施例中,基于甾醇的阳离子脂质是咪唑胆固醇酯或“ice”脂质(参见wo2011/068810,其通过引用并入本技术)。在一些实施例中,基于甾醇的阳离子脂质可构成脂质纳米颗粒(例如,脂质体)中总脂质的不超过70%(例如,不超过65%和60%)。合适的脂质的实例可包括,例如,磷脂酰化合物(例如,磷脂酰甘油、磷脂酰胆碱、磷脂酰丝氨酸、磷脂酰乙醇胺、鞘脂、脑苷脂和神经节苷脂。
85、阳离子脂质的非限制性实例可包括(但不限于)c12-200、mc3、dlindma、dlin-mc3-dma、dlinkc2dma、ckk-e12、ice(咪唑基)、hgt5000、hgt5001、of-02、dodac、ddab、dmrie、dospa、dogs、dodap、dodma和dmdma、dodac、dlendma、dmrie、clindma、cplindma、dmoba、docarbdap、dlindap、dlincarbdap、dlincdap、klin-k-dma、dlin-k-xtc2-dma、sm-102、alc-0315和hgt4003等,或其组合。
86、非阳离子脂质的非限制性实例可以包括(但不限于)神经酰胺、脑磷脂、脑苷脂、二酰基甘油、1,2-二棕榈酰基-sn-甘油基-3-磷酰基甘油钠盐(dppg)、1,2-二硬脂酰-sn-甘油基-3-磷酸乙醇胺(dspe)、1,2-二硬脂酰-sn-甘油-3-磷酸胆碱(dspc)、1,2-二棕榈酰-sn-甘油-3-磷酸胆碱(dppc)、1,2-二油基-sn-甘油-3-磷酸乙醇胺(dope)、1,2-二油基-sn-甘油-3-磷脂酰胆碱(dopc)、1,2-二棕榈酰-sn-甘油基-3-磷酸乙醇胺(dppe)、1,2-二肉豆蔻酰-sn-甘油-3-磷酸乙醇胺(dmpe)、和1,2-二油酰基-sn-甘油-3-磷酸-(1'-rac-甘油)(dopg),1-棕榈酰-2-油酰基-磷脂酰乙醇胺(pope)、1-棕榈酰-2-油酰基-sn-甘油-3-磷酸胆碱(popc)、1-硬脂酰基-2-油酰基-磷脂酰乙醇胺(sope)、鞘磷脂、或其组合。
87、在一些实施例中,peg改性脂质可以是peg长度可以是1000~5000da的聚(乙烯)二醇链,其共价连接到具有c6-c20长度的烷基链的脂质上。peg改性脂质的非限制性实例可包括(但不限于)dmg-peg1000、dmg-peg1300、dmg-peg1500、dmg-peg1800、dmg-peg2000、dmg-peg2200、dmg-peg2500、dmg-peg2700、dmg-peg3000、dmg-peg3200、dmg-peg3500、dmg-peg3700、dmg-peg4000、dmg-peg4200、dmg-peg4500、dmg-peg4700、dmg-peg5000、alc-0159、c8-peg、dogpeg、神经酰胺peg和dspe-peg、或其组合。
88、还考虑使用聚合物作为转移载体,无论是单独使用还是与其他转移载体组合使用。合适的聚合物可包括,例如,聚丙烯酸酯、聚烷基氰基丙烯酸酯、聚丙交酯、聚丙交酯-聚乙交酯共聚物、聚己内酯、葡聚糖、白蛋白、明胶、藻酸盐、胶原、壳聚糖、环糊精和聚乙烯亚胺。基于聚合物的纳米颗粒可包括聚乙烯亚胺(pei),例如支化的pei。
89、载体的核壳结构也是另外一种具体的实施方式。在一些方式中,所述的疫苗试剂包括前述的核酸,该核酸可以翻译,表达冠状病毒的抗原或者抗原片段,这样的核酸被包含在多个多聚复合物或蛋白质核粒子内,并且其中所述多个多聚复合物或蛋白质核粒子本身被囊封在第一生物相容性脂质双层壳中。在一些方式中,所述多聚复合物或蛋白质核粒子含有至少第一带正电荷的聚合物或蛋白质。其中所述第一生物相容性脂质双层壳促进一种或多种哺乳动物抗原呈递细胞对所述多个多聚复合物或蛋白质核粒子的巨胞饮作用。在一些方式中,该疫苗试剂还包含囊封在所述生物相容性脂质双层内的选自cpg、聚(i:c)、明矾及其任何组合的佐剂。在一些方式中,疫苗试剂还包括含囊封在所述生物相容性脂质双层之间的空间内的免疫调节化合物,例如il-12p70蛋白质、flt3配体、或吲哚胺2,3-双加氧酶(ido-1)抑制剂。在一些方式中,其中所述吲哚胺2,3-双加氧酶(ido-1)抑制剂是gdc-0919、incb24360或其组合。在一些方式中,其中所述带正电荷的聚合物或蛋白质包含鱼精蛋白、聚乙烯亚胺、聚(β-氨基酯)或其任何组合。在一些方式中,所述生物相容性脂质双层包含以下的一种或多种:1,2-二油酰-sn-甘油-3-乙基磷酸胆碱(edopc);1,2-二油酰-sn-甘油-3-磷脂酰乙醇胺(dope);1,2-二硬脂酰-sn-甘油-3-磷酸乙醇胺-n-[氨基(聚乙二醇)-2000](dspe-peg);及其组合。在一些方式中,所述生物相容性脂质双层包含:(a)约30%至约70%的1,2-二油酰-sn-甘油-3-乙基磷酸胆碱(edopc);(b)约70%至约30%的1,2-二油酰-sn-甘油-3-磷脂酰乙醇胺(dope);或(c)约0.5%至约5%的1,2-二硬脂酰-sn-甘油-3-磷酸乙醇胺-n-[氨基(聚乙二醇)-2000](dspe-peg)。在一些方式中,所述生物相容性脂质双层包含:(a)约45%至约55%的1,2-二油酰-sn-甘油-3-乙基磷酸胆碱(edopc);(b)约55%至约45%的1,2-二油酰-sn-甘油-3-磷脂酰乙醇胺(dope);和(c)约1%至约2%的1,2-二硬脂酰-sn-甘油-3-磷酸乙醇胺-n-[氨基(聚乙二醇)-2000](dspe-peg)。
90、尽管与本文描述的那些类似或等同的方法和材料可用于本发明的实践或测试,但下文描述了合适的方法和材料。本文提及的所有出版物、专利申请、专利和其他参考文献都通过引用整体并入。本文引用的参考文献不被认为是要求保护的发明的现有技术。另外,材料、方法和实施例仅是说明性的,而不是限制性的。
- 还没有人留言评论。精彩留言会获得点赞!