一种N-取代咪唑甲酸酯类衍生物及其用途的制作方法
本发明属于药物化学领域,具体涉及一种结构新颖的n-取代咪唑甲酸酯类衍生物,以及该化合物在制备具有镇静、催眠和/或麻醉作用的药物和制备能够控制癫痫持续状态的药物中的应用。
背景技术:
1、一种咪唑类衍生物依托咪酯,化学名称为r-(+)-1-(1-苯乙基)-1-氢-咪唑-5-甲酸乙酯,是一种催眠性静脉全身麻醉药,安全性范围大,曾是麻醉诱导常用的药物之一。该咪唑类衍生物临床应用已有30年的历史(br j anaesth.1976;48(3):213-6.pubmed:1259887;arch int pharmacodyn ther.1975;214(1):92 -132.pubmed:1156027;academerg med.2006;13(4):378-83.pubmed:16531603)。依托咪酯为非巴比妥类静脉镇静药,其作用强度分别为巴比妥钠的4倍和硫喷妥钠的12倍,且全麻诱导快,给药后的苏醒、恢复也快,病人苏醒后不再出现嗜睡、眩晕及其他不良反应,并有一定的抗呕吐的作用,因此得到了广泛的应用。其结构式如下式所示,分子式c14h16n2o2,分子量244.29。该咪唑类衍生物不溶于水,中性溶液中不稳定。
2、
3、杨森制药最早于上世纪70年代开始将依托咪酯推入临床。作为最主要研发人员,janssen pa等在1965年发表的一篇研究报道中记录了合成依托咪酯的主要过程,且描述了如何将依托咪酯从42个类似化合物中筛选而出的经过。在明确有麻醉作用的11种化合物之中,依托咪酯在大鼠体内表现出了最好的安全性(即最高的治疗指数ti)。此外,科研人员还发现了依托咪酯的镇静催眠作用是具有立体选择性的,r构型药物的药效比s构型药物的药效高十倍(j med chem.1965;8:220-3.pubmed:14332665;anesthesiology.1998;88(3):708-17.pubmed:9523815)。该咪唑类衍生物的优点十分突出,比如在现有全身麻醉药中治疗窗比较大、对循环系统的抑制比较小,这种特点尤其适用于老年人、冠心病和高血压病人、危重病人。曾经是麻醉诱导的标准药物、也被用于作为全凭静脉麻醉的药物。
4、但是,自上世纪八十年代以来,随着临床上的长期使用,依托咪酯的一些缺点(如苏醒质量比另一种全身麻醉药物丙泊酚略差)尤其是对肾上腺皮质功能产生抑制这一不良反应逐渐被人们所发现。有文献报道由于依托咪酯具有抑制肾上腺皮质激素的合成,从而降低危重症病人的存活率(lancet.1983;1(8339):1434.pubmed:6134189;critcare.2007;11(3):145.pubmed:17610749;anesthesiology.2011;114(3):695-707.pubmed:21263301)。甚至一些研究表明单次快速顺序诱导中使用依托咪酯会增加住院病人的死亡率(crit care med.2012;40(11):2945-53.pubmed:22971586;anesthanalg.2013;117(6):1329-37.pubmed:24257383);许多研究者推测这种高死亡率的发生和依托咪酯抑制肾上腺皮质激素合成有关(cochrane database syst rev.2015;1:cd010225.pubmed:25568981)。同时,另一种目前临床上常用的静脉全身麻醉药丙泊酚,除了治疗窗比较小之外,麻醉诱导过程中有明显降低血压的不良反应(crit care.2015;19:45.pubmed:25887642),常常会增加心血管不良事件的发生。因此,设计一种新的化合物,使其既可以保留依托咪酯循环稳定性的优良特点,又可以不抑制肾上腺皮质激素的合成则具有非常重要的临床意义和广阔的应用前景。
5、文献提示,依托咪酯抑制肾上腺皮质激素的合成位点主要有11-β羟化酶和胆固醇侧链裂解酶,这些酶是肾上腺皮质合成皮质酮、皮质醇等途径中的关键酶。(n engl jmed.1984;310(22):1415-21.pubmed:6325910)。atucha等(bioorg med chem lett.2009;19(15):4284-7.pubmed:19497738)发现依托咪酯的酯质侧链不仅可以影响gaba受体(依托咪酯起麻醉效应的主要位点)还可以影响肾上腺皮质激素的合成。此外,依托咪酯代谢主要产物依托咪酯酸相较于依托咪酯几乎没有发现其有抑制11-β羟化酶的效应(anesthesiology.2016;125(5):943-951.pubmed:27541316)。如果通过对依托咪酯的结构进行修饰减少或消除化合物本身对肾上腺皮质功能的抑制并且使化合物的代谢产物也没有对肾上腺皮质功能的影响,那么就可以减少或消除药物对肾上腺皮质功能的抑制作用。后续基于依托咪酯结构的研究,则主要集中在保留依托咪酯临床应用上的优点之外,如何降低或没有对肾上腺皮质功能的抑制上。
6、wo 2009/146024a1公开了一种具有提高的药物动力学性能和药效学性能的依托咪酯类似物及其作为麻醉剂的用途,并公开了该化合物可以为moc-(r)-依托咪酯。
7、wo 2011/005969a2公开了一种具有提高的药物动力学性能和药效学性能的依托咪酯类似物及其作为麻醉剂的用途,并公开了该化合物可以为moc-碳依托咪酯。
8、cn201380014062公开了一种能提高的药代动力学和药效学性质的美托咪酯和依托咪酯的类似物,并公开了该化合物可以为环丙基moc-美托咪酯。
9、虽然科学家们后续基于依托咪酯结构的研究,主要集中在保留依托咪酯临床应用上的优点之外,如何降低或没有对肾上腺皮质功能的抑制上。且陆续发现了诸如dimethylmethoxycarbonyl metomidate(dmmm)和cyclopropyl methoxycarbonylmetomidate(cpmm)等的依托咪酯类似物,但仍然还没有寻找到既保留了依托咪酯独特优点(如高效,安全),又消除了其对肾上腺皮质功能的抑制效应的化合物。
10、因此,设计一种新的化合物,使其既可以保留依托咪酯循环稳定性的优良特点,又可以不抑制肾上腺皮质激素的合成则具有非常重要的临床意义和广阔的应用前景。
11、同时,临床上也亟需更安全的咪唑类衍生物用于制备具有镇静、催眠和/或麻醉作用的药物以及控制癫痫持续状态的药物。
技术实现思路
1、为了解决上述问题,本发明提供了一种结构新颖的n-取代咪唑甲酸酯类衍生物。
2、本发明还提供了该n-取代咪唑甲酸酯类衍生物具有中枢神经系统抑制作用,并提供了该n-取代咪唑甲酸酯类衍生物在制备具有镇静、催眠和/或麻醉作用的药物中的应用,以及在制备能够控制癫痫持续状态的药物中的应用。
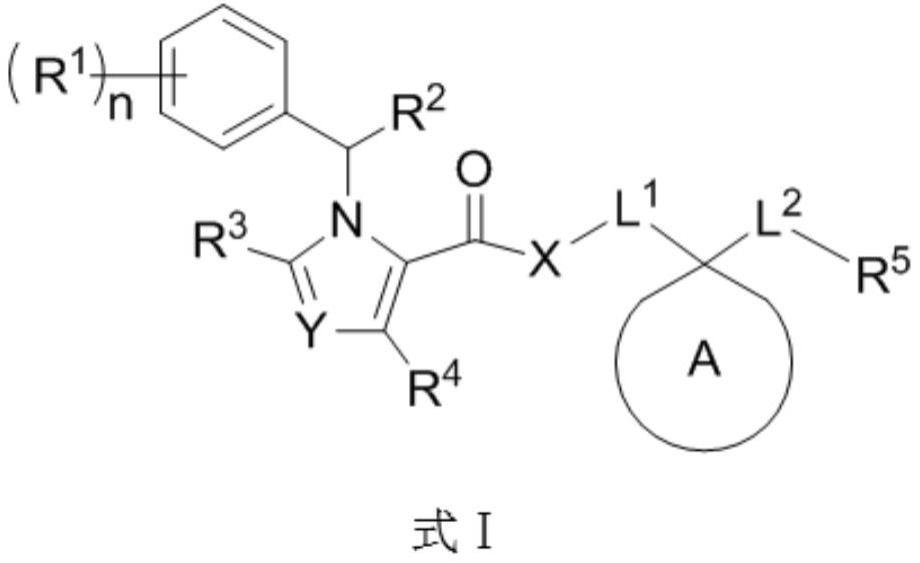
3、本发明提供了式ⅰ所示的化合物、或其立体异构体、或其药学上可接受的盐、或其溶剂
4、合物、或其前体药物、或其代谢产物、或其氘代衍生物:
5、
6、x选自o、s或nr30,其中,r30选自氢、氘或c1-8烷基;
7、y选自n;
8、r1各自独立地选自氘、卤素、-cn、-no2、-or32、-c(o)r32、-co2r32、-con(r32)2、-n(r32)2、-oc(o)r32、-so2r32、取代或未取代的3~8元杂环基、取代或未取代的c1-8烷基、取代或未取代的c2-8烯基、取代或未取代的c2-8炔基;
9、其中,r32各自独立地选自氢、氘、取代或未取代的c1-8烷基、取代或未取代的c2-8烯基、取代或未取代的c2-8炔基、取代或未取代的c3-8环烷基、取代或未取代的3~8元杂环基、取代或未取代的芳基、取代或未取代的杂芳基;所述取代基为氘、氰基、羟基、羧基、卤素、c3-8环烷基或其卤代或氘代物、3~8元杂环基或其卤代或氘代物、芳基或其卤代或氘代物、杂芳基或其卤代或氘代物;
10、n为0~5的整数;
11、r2选自氢、氘、卤素、c1-8烷基或其卤代或氘代物、c1-8烷氧基或其卤代或氘代物、c2-8烯基或其卤代或氘代物、c2-8炔基或其卤代或氘代物、3~8元杂环基或其卤代或氘代物;
12、r3和r4各自独立地选自氢或氘;
13、l1和l2各自独立地选自无、取代或未取代的c1-8亚烷基;所述取代基为氘、氰基、羟基、羧基、卤素、c1-8烷基或其卤代或氘代物、c1-8烷氧基或其卤代或氘代物、c3-8环烷基或其卤代或氘代物、3~8元杂环基或其卤代或氘代物、芳基或其卤代或氘代物、杂芳基或其卤代或氘代物;
14、r5选自取代或未取代的c2-8烯基、取代或未取代的c2-8炔基;
15、所述取代基为氘、氰基、羟基、羧基、卤素、c1-4烷基或其卤代或氘代物、c1-4烷氧基或其卤代或氘代物、c3-8元环烷基或其卤代或氘代物、3~8元杂环基或其卤代或氘代物、芳基或其卤代或氘代物、杂芳基或其卤代或氘代物、-s-c1-4烷基、=r39、c2-8烯基或c2-8炔基、;其中,r39选自o、s、nr40或c(r40)2,r40选自氢、氘、卤素、c1-4烷基或其卤代或氘代物;
16、a环为无,或者,a环选自被0~4个r34取代的3~6元饱和碳环、3~6元不饱和碳环、3~6元饱和杂环或3~6元不饱和杂环;
17、其中,r34各自独立地选自氘、卤素、氰基、硝基、c1-8烷基或其卤代或氘代物、c2-8烯基或其卤代或氘代物、c2-8炔基或其卤代或氘代物、-oc(o)r35、-c(o)r35、-s(o)r35、-c(o)n(r35)2、-l33-r36或=r37;
18、l33选自c1-4亚烷基;
19、r36选自氰基、硝基、-oc(o)r35、-c(o)r35、-s(o)r35、-c(o)n(r35)2;
20、r35各自独立地选自c1-4烷基或其卤代或氘代物;
21、r37选自o、s、n(r38)、c(r38)2;r38选自h或c1-4烷基;
22、当n为0,r2为甲基,y为n,r3、r4为氢,x为o,l1为亚甲基,a环为无,l2为无时,r5不为乙烯基、乙炔基或丙烯基。
23、进一步地,
24、x选自o或s;
25、或,r1各自独立地选自氘、卤素、-cn、-no2、-or32、-c(o)r32、-co2r32、-con(r32)2、-n(r32)2、-oc(o)r32、c1-3烷基、c2-3烯基、c2-3炔基;
26、其中,r32各自独立地选自氢、氘、c1-3烷基、c2-3烯基、c2-3炔基;
27、或,n为0~2的整数;
28、或,r2选自氢、氘、卤素、c1-3烷基或其卤代或氘代物。
29、进一步地,
30、所述化合物如式ⅱ所示:
31、
32、y选自n;
33、x选自o或s;
34、r5选自取代或未取代的c2-8烯基、取代或未取代的c2-8炔基;
35、所述取代基为氘、卤素、c1-4烷基或其卤代或氘代物、c1-4烷氧基或其卤代或氘代物、c3-8元环烷基或其卤代或氘代物、3~8元杂环基或其卤代或氘代物、芳基或其卤代或氘代物、杂芳基或其卤代或氘代物、=r39、c2-6烯基或c2-6炔基;其中,r39选自o、s、nr40或c(r40)2,r40选自氢、氘、卤素、c1-4烷基或其卤代或氘代物;
36、a环为无,或者,a环选自被0~4个r34取代的3~6元饱和碳环、3~6元不饱和碳环、3~6元饱和杂环或3~6元不饱和杂环;
37、其中,r34各自独立地选自氘、卤素、氰基、硝基、c1-8烷基或其卤代或氘代物、c2-8烯基或其卤代或氘代物、c2-8炔基或其卤代或氘代物、-oc(o)r35、-c(o)r35、-s(o)r35、-c(o)n(r35)2、-l33-r36或=r37;
38、l33选自c1-4亚烷基;
39、r36选自氰基、硝基、-oc(o)r35、-c(o)r35、-s(o)r35、-c(o)n(r35)2;
40、r35各自独立地选自c1-4烷基或其卤代或氘代物;
41、r37选自o、s、n(r38);r38选自h或c1-4烷基。
42、进一步地,
43、y选自n;
44、或,r3和r4各自独立地选自氢、氘;
45、或,l1和l2各自独立地选自无、取代或未取代的c1-4亚烷基;所述取代基为氘、氰基、羟基、羧基、卤素、c1-4烷基或其卤代或氘代物、c1-4烷氧基或其卤代或氘代物、c3-5环烷基或其卤代或氘代物、3~5元杂环基或其卤代或氘代物、芳基或其卤代或氘代物、杂芳基或其卤代或氘代物;
46、或,r5选自取代或未取代的c2-6烯基、取代或未取代的c2-6炔基;
47、所述取代基为氘、氰基、羟基、羧基、卤素、c1-4烷基或其卤代或氘代物、c1-4烷氧基或其卤代或氘代物、c3-6元环烷基或其卤代或氘代物、3~6元杂环基或其卤代或氘代物、芳基或其卤代或氘代物、杂芳基或其卤代或氘代物、=r39、c2-4烯基或c2-4炔基;其中,r39选自o、s、nr40或c(r40)2,r40选自氢、氘、卤素、c1-4烷基;
48、或,a环为无,或者,a环选自被0~4个r34取代的3~6元饱和碳环、3~6元不饱和碳环、3~6元饱和杂环或3~6元不饱和杂环;
49、其中,r34各自独立地选自氘、卤素、c1-4烷基或其卤代或氘代物、c2-4烯基或其卤代或氘代物、c2-4炔基或其卤代或氘代物。
50、进一步地,
51、y选自n;
52、或,r3和r4各自独立地选自氢、氘;
53、或,l1和l2各自独立地选自无、取代或未取代的c1-3亚烷基;所述取代基为氘、卤素、c1-3烷基或其卤代或氘代物、c1-3烷氧基或其卤代或氘代物;
54、或,r5选自取代或未取代的c2-6烯基、取代或未取代的c2-6炔基;
55、所述取代基为氘、卤素、羟基、c1-3烷基或其卤代或氘代物、c1-3烷氧基或其卤代或氘代物、=r39、c2-4烯基或c2-4炔基;其中,r39选自o、s、nr40或c(r40)2,r40选自氢、氘、卤素、c1-4烷基;
56、或,a环为无,或者,a环选自被0~2个r34取代的3~6元饱和碳环或3~6元饱和杂环;
57、其中,r34各自独立地选自氘、卤素、c1-3烷基、c2-3烯基、c2-3炔基。
58、进一步地,
59、y选自n;
60、或,r3和r4各自独立地选自氢、氘;
61、或,l1和l2各自独立地选自无、取代或未取代的c1-2亚烷基;所述取代基为氘、卤素、c1-2烷基;
62、或,r5选自取代或未取代的c2-6烯基、取代或未取代的c2-6炔基;
63、所述取代基为氘、羟基、c1-2烷基、c1-2烷氧基、=r39、c2-4烯基或c2-4炔基;其中,r39选自o、s、nr40或c(r40)2,r40选自氢、氘、卤素、c1-3;
64、或,a环为无,或者,a环选自被0~2个r34取代的3~6元饱和碳环或3~6元饱和杂环;
65、其中,r34各自独立地选自氘、c1-2烷基。
66、进一步地,
67、所述化合物如式ⅱda所示:
68、
69、y选自n;
70、l1和l2各自独立地选自无、取代或未取代的c1-2亚烷基;所述取代的取代基为氘、c1-2烷基;
71、r、r’各自独立地选自氢、氘、c1-2烷基、c1-2烷氧基、取代或未取代的c2-4烯基或c2-4炔基,所述取代基选自羟基、c1-2烷基;
72、a环为无,或者,a环选自3~6元饱和碳环或4~6元饱和杂环;
73、或,
74、所述化合物如式ⅱdb所示:
75、
76、x选自o或s;
77、r3和r4各自独立地选自氢、氘;
78、l1和l2各自独立地选自无、取代或未取代的亚甲基;所述取代的取代基为氘、c1-2烷基;
79、r”选自氢、氘、c1-2烷基、c1-2烷氧基、取代或未取代的c2-4烯基或c2-4炔基,所述取代基选自羟基、c1-2烷基;
80、a环为无,或者,a环选自3~6元饱和碳环或4~6元饱和杂环;
81、或,
82、所述化合物如式ⅱdc所示:
83、
84、x选自o或s;
85、r3和r4各自独立地选自氢、氘;
86、l1和l2各自独立地选自无、取代或未取代的亚甲基;所述取代的取代基为氘、c1-2烷基;
87、r5’选自s或ch2;
88、a环为无,或者,a环选自3~6元饱和碳环或4~6元饱和杂环。
89、进一步地,
90、所述化合物为:
91、
92、
93、
94、。
95、本发明还提供了一种药物,它是以上述的化合物、或其立体异构体、或其药学上可接受的盐、或其溶剂合物、或其前体药物、或其代谢产物、或其氘代衍生物、或其组合物,加上药学上可接受的辅料制备而成的制剂。
96、本发明还提供了上述的化合物、或其立体异构体、或其药学上可接受的盐、或其溶剂合物、或其前体药物、或其代谢产物、或其氘代衍生物、或其组合物,在制备具有镇静、催眠、和/或麻醉作用、和/或可用于控制癫痫持续状态的药物中的用途
97、前述化合物、或其立体异构体、或其药学上可接受的盐、或其溶剂合物、或其前体药物、或其代谢产物在制备具有镇静、催眠和/或麻醉作用的药物中的用途。
98、本发明所述“具有镇静的药物”是指一种有效帮助睡眠和有效改善睡眠的药物。即能避免失眠对人体的严重危害,治疗失眠病,提高睡眠质量。
99、本发明所述“具有催眠的药物”是指一种能诱导睡意、促使睡眠的药物。即对中枢神经系统有抑制作用,小剂量引起镇静,过量导致全身麻醉。
100、本发明所述“具有麻醉的药物”是指由药物产生的一种中枢神经和(或)周围神经系统的可逆性功能抑制,这种抑制的特点主要是感觉特别是痛觉的丧失。
101、优选地,所述麻醉为全身麻醉。
102、本发明所述“全身麻醉”简称全麻,是指麻醉药进入体内后对中枢神经系统产生的暂时抑制,临床表现为神志消失、全身痛觉消失、遗忘、反射抑制和骨骼肌松弛。
103、前述化合物、或其立体异构体、或其药学上可接受的盐、或其溶剂合物、或其前体药物、或其代谢产物在制备能够控制癫痫持续状态的药物中的应用。
104、本发明所述的“癫痫持续状态”是指癫痫连续发作之间意识未完全恢复又频繁再发,或发作持续30分钟以上不自行停止。长时间癫痫发作,若不及时治疗,可因高热、循环衰竭或神经元兴奋毒性损伤导致不可逆的脑损伤,致残率和病死率很高,因而癫痫状态是内科常见的急症。
105、本发明提供了一种药物,它是以前述的化合物、或其立体异构体、或其药学上可接受的盐、或其溶剂合物、或其前体药物、或其代谢产物、或其氘代衍生物,加上药学上可接受的辅料制备而成的制剂。
106、本发明中提供的化合物和衍生物可以根据iupac(国际纯粹与应用化学联合会)或cas(化学文摘服务社,columbus,oh)命名系统命名。
107、关于本发明的使用术语的定义:除非另有说明,本文中基团或者术语提供的初始定义适用于整篇说明书的该基团或者术语;对于本文没有具体定义的术语,应该根据公开内容和上下文,给出本领域技术人员能够给予它们的含义。
108、“取代”是指分子中的氢原子被其它不同的原子或分子所替换。
109、本发明中所述化合物的结构均是指能够稳定存在的结构。
110、“氘”是指氢(h)的同位素,也被称为重氢,元素符号一般为d或2h。
111、本发明中取代基“-c(o)r32”的结构式为:
112、本发明中取代基“-co2r32”的结构式为:
113、本发明中取代基“-con(r32)2”的结构式为:
114、本发明中取代基“-n(r32)2”的结构式为:
115、本发明中取代基“-oc(o)r32”的结构式为:
116、本发明中取代基“-so2r32”的结构式为:
117、本发明中取代基“-c(s)r33”的结构式为:
118、本发明中取代基“-s(o)r33”的结构式为:
119、碳氢基团中碳原子含量的最小值和最大值通过前缀表示,例如,前缀(ca~cb)烷基表明任何含“a”至“b”个碳原子的烷基。因此,例如,c1~c8烷基是指包含1~8个碳原子的烷基。c1~c8烷基是指含有一个至八个碳原子的直链或支链的烃链。
120、“烷基”是烷烃分子中少掉一个氢原子而成的烃基,例如甲基-ch3,乙基-ch3ch2等。
121、“亚烷基”是指烷烃分子中少掉两个氢原子而成的烃基,例如亚甲基-ch2-,亚乙基-ch2ch2-等。“c1-8亚烷基”是指含有一个至八个碳原子的直链或支链的烃链。
122、“取代或未取代的c1-8烷基”是指c1-8烷基可以是被取代的,也可以没有取代基的。
123、本发明所述“a环为3~6元饱和碳环”中的“3~6元饱和碳环”是指由3~6个碳原子组成的碳环,其中该碳环中无双键。例如:
124、
125、本发明所述“a环为3~6元不饱和碳环”中的“3~6元不饱和碳环”是指由3~6个碳原子组成的碳环,其中该碳环中含有双键。例如:
126、
127、本发明所述“a环为3~6元饱和杂环”中的“3~6元饱和杂环”是指没有双键的饱和的杂环,其中该杂环中携带至少一个选自o、s或取代的氮原子,其余环原子为碳。例如:
128、等
129、本发明所述“a环为3~6元不饱和杂环”中的“3~6元不饱和碳环”是指含有双键的饱和的杂环,其中该杂环中携带至少一个选自o、s或取代的氮原子,其余环原子为碳。例如:
130、等。
131、“炔基”是指具有至少一个碳-碳三键的脂肪族碳氢基团。所述的炔基可以是直链或支链的。当炔基前具有碳原子数限定(如c2-8炔基)时,例如,术语“c2-8炔基”指具有2-8个碳原子的直链或支链炔基。
132、“烯基”是指具有至少一个碳-碳双键的脂肪族碳氢基团。所述的烯基可以是直链或支链的。当烯基前具有碳原子数限定(如c2-8烯基)时,例如,术语“c2-8烯基”指具有2-8个碳原子的直链或支链烯基。
133、卤素为氟、氯、溴或碘。
134、“芳基”指具有共轭的π电子体系的全碳单环或稠合多环(也就是共享毗邻碳原子对的环)基团,例如苯基和萘基。所述芳基环可以稠合于其它环状基团(包括饱和和不饱和环),但不能含有杂原子如氮,氧,或硫,同时连接母体的点必须在具有共轭的π电子体系的环上的碳原子上。芳基可以是取代的或未取代的。
135、“杂芳基”指包含一个到多个杂原子的杂芳族基团。这里所指的杂原子包括氧、硫和氮。例如呋喃基、噻吩基、吡啶基、吡唑基、吡咯基、n-烷基吡咯基、嘧啶基、吡嗪基、咪唑基、四唑基等。所述杂芳基环可以稠合于芳基、杂环基或环烷基环上,其中与母体结构连接在一起的环为杂芳基环。杂芳基可以是任选取代的或未取代的。
136、“环烷基”指饱和或不饱和的环状烃取代基;环状烃可以是单环也可以是多环。例如,“c3-8环烷基”指碳原子数为3~8的环烷基。
137、“杂环基”指饱和或不饱和的环状烃取代基;环状烃可以是单环也可以是多环,且携带至少一个选自o、s或取代的氮原子的环烷基,其余环原子为碳,例如,“c3-8杂环基”指碳原子数和杂原子数共为3~8的杂环基。
138、本发明化合物中的“a环”上的一个碳原子是与l1和l2直接相连的。例如:
139、等。
140、a环为无或被“0~4个r34取代”的3~6元饱和碳环、3~6元不饱和碳环、3~6元饱和杂环或3~6元不饱和杂环;此处,与“取代基r34”相连的碳原子不是与l1或l2直接相连的碳原子。例如:
141、等。
142、“c1-4烷基或其卤代或氘代物”是指c1-4烷基、被卤素或氘取代的c1-4烷基。其它关于“或其卤代或氘代物”具有类似的定义。
143、本发明的所有化合物之中,各手性碳原子(手性中心)可以任选地为r构型或s构型,或r构型和s构型的混合物。
144、“药学上可以接受的载体”指的是:一种或多种相容性固体或液体填料或凝胶物质,它们适合于人使用,而且必须有足够的纯度和足够低的毒性。“相容性”在此指的是组合物中各组份能和本发明的化合物以及它们之间相互掺和,而不明显降低化合物的药效。药学上可以接受的载体部分例子有纤维素及其衍生物(如羧甲基纤维素钠、乙基纤维素钠、纤维素乙酸酯等)、明胶、滑石、固体润滑剂(如硬脂酸、硬脂酸镁)、硫酸钙、植物油(如豆油、芝麻油、花生油、橄榄油等)、多元醇(如丙二醇、甘油、甘露醇、山梨醇等)、乳化剂(如)、润湿剂(如十二烷基硫酸钠)、着色剂、调味剂、稳定剂、抗氧化剂、防腐剂、无热原水等。
145、术语“药学上可接受的盐”指本发明化合物与药学上可接受的无机酸和有机酸所形成的盐,适合与对象(例如,人)的组织接触,而不会产生不适度的副作用的盐。其中,优选的无机酸包括(但并不限于):盐酸、氢溴酸、磷酸、硝酸、硫酸;优选的有机酸包括(但并不限于):甲酸、乙酸、丙酸、丁二酸、萘二磺酸(1,5)、亚细亚酸、草酸、酒石酸、乳酸、水杨酸、苯甲酸、戊酸、二乙基乙酸、丙二酸、琥珀酸、富马酸、庚二酸、己二酸、马来酸、苹果酸、氨基磺酸、苯丙酸、葡糖酸、抗坏血酸、烟酸、异烟酸、甲磺酸、对甲苯磺酸、柠檬酸,以及氨基酸。
146、术语“药学上可接受的溶剂合物”指本发明化合物与药学上可接受的溶剂形成溶剂合物,其中,所述药学上可接受的溶剂包括(但并不限于):水、乙醇、甲醇、异丙醇、丙二醇、四氢呋喃、二氯甲烷。
147、如本文所用,术语“药学上可接受的立体异构体”指本发明化合物所涉及手性碳原子可以为r构型,也可以为s构型,或其组合。
148、本发明化合物或其组合物及使用方法:
149、本发明化合物及其各种晶型,药学上可接受的无机或有机盐,水合物或溶剂合物,以及含有本发明化合物为主要活性成分的药物组合物可用于实施镇静、催眠和/或全身麻醉。本发明化合物也可用于控制癫痫持续状态等。
150、本发明的药物组合物包含安全有效量范围内的本发明化合物或其药理上可接受的盐及药理上可以接受的赋形剂或载体。
151、本发明化合物或药物组合物的使用方式包括(但并不限于):胃内、肠内、肠胃外(静脉内、肌肉内或皮下)、口服和各种局部给药。
152、用于肠胃外(静脉内、肌肉内、皮下)注射的组合物可包含生理上可接受的无菌含水或无水溶液、分散液、悬浮液或乳液,和用于重新溶解成无菌的可注射溶液或分散液的无菌粉末。适宜的含水和非水载体、稀释剂、溶剂或赋形剂包括水、乙醇、多元醇及其适宜的混合物。
153、用于口服给药的固体剂型包括胶囊剂、片剂、丸剂、散剂和颗粒剂。在这些固体剂型中,活性化合物与至少一种常规惰性赋形剂(或载体)混合,如柠檬酸钠或磷酸二钙,或与下述成分混合:(a)填料或增容剂,例如,淀粉、乳糖、蔗糖、葡萄糖、甘露醇和硅酸;(b)粘合剂,例如,羟甲基纤维素、藻酸盐、明胶、聚乙烯基吡咯烷酮、蔗糖和阿拉伯胶;(c)保湿剂,例如,甘油;(d)崩解剂,例如,琼脂、碳酸钙、马铃薯淀粉或木薯淀粉、藻酸、某些复合硅酸盐、和碳酸钠;(e)缓溶剂,例如石蜡;(f)吸收加速剂,例如,季胺化合物;(g)润湿剂,例如鲸蜡醇和单硬脂酸甘油酯;(h)吸附剂,例如,高岭土;和(i)润滑剂,例如,滑石、硬脂酸钙、硬脂酸镁、固体聚乙二醇、十二烷基硫酸钠,或其混合物。胶囊剂、片剂和丸剂中,剂型也可包含缓冲剂。
154、用于口服给药的液体剂型包括药学上可接受的乳液、溶液、悬浮液、糖浆或酊剂。除了活性化合物外,液体剂型可包含本领域中常规采用的惰性稀释剂,如水或其它溶剂,增溶剂和乳化剂,例知,乙醇、异丙醇、碳酸乙酯、乙酸乙酯、丙二醇、1,3-丁二醇、二甲基甲酰胺以及油,特别是棉籽油、花生油、玉米胚油、橄榄油、蓖麻油和芝麻油或这些物质的混合物等。
155、固体剂型如片剂、糖丸、胶囊剂、丸剂和颗粒剂可采用包衣和壳材制备,如肠衣和其它本领域公知的材料。它们可包含不透明剂,并且,这种组合物中活性化合物或化合物的释放可以延迟的方式在消化道内的某一部分中释放。可采用的包埋组分的实例是聚合物质和蜡类物质。必要时,活性化合物也可与上述赋形剂中的一种或多种形成微胶囊形式。
156、用于局部给药的本发明化合物的剂型包括软膏剂、散剂、贴剂、喷射剂和吸入剂。活性成分在无菌条件下与生理上可接受的载体及任何防腐剂、缓冲剂,或必要时可能需要的推进剂一起混合。
157、除了这些惰性稀释剂外,组合物也可包含助剂,如润湿剂、乳化剂和悬浮剂、甜味剂、矫味剂和香料。
158、除了活性化合物外,悬浮液可包含悬浮剂,例如,乙氧基化异十八烷醇、聚氧乙烯山梨醇和脱水山梨醇酯、微晶纤维素、甲醇铝和琼脂或这些物质的混合物等。
159、本发明化合物可以单独给药,或者与其他药学上可接受的化合物联合给药。
160、使用药物组合物时,是将安全有效量的本发明化合物适用于需要治疗的哺乳动物(如人),其中施用时剂量为药学上认为的安全和有效给药剂量。
161、使用药物组合物时,是将安全有效量的本发明化合物适用于需要治疗的哺乳动物(如人),其中施用时剂量为药学上认为的有效给药剂量,对于60公斤体重的人而言,日给药剂量通常为1~2000毫克,优选5~500毫克。当然,具体剂量还应考虑给药途径、病人健康状况等因素,这些都是熟练医师技能范围之内的。
162、本发明所述“室温”为25±5℃。
163、本发明所述“过夜”为12±1小时。
164、本发明所述“1n的hcl”为1mol/l的hcl。
165、本发明提供了式ⅰ所示的化合物,该化合物是一种结构新颖的n-取代咪唑甲酸酯类衍生物,该化合物对中枢神经系统具有较好的抑制作用,可用于制备具有镇静、催眠和/或麻醉作用的药物,以及用于制备能够控制癫痫持续状态的药物,为临床上筛选和/或制备具有镇静、催眠和/或麻醉作用及控制癫痫持续状态等的药物提供了一种新的选择。
166、显然,根据本发明的上述内容,按照本领域的普通技术知识和惯用手段,在不脱离本发明上述基本技术思想前提下,还可以做出其它多种形式的修改、替换或变更。
167、以下通过实施例形式的具体实施方式,对本发明的上述内容再作进一步的详细说明。但不应将此理解为本发明上述主题的范围仅限于以下的实例。凡基于本发明上述内容所实现的技术均属于本发明的范围。
- 还没有人留言评论。精彩留言会获得点赞!