一种组氨酸酶及尿刊酸还原酶活性检测方法
本发明属于生物分析化学领域,涉及一种组氨酸酶及尿刊酸还原酶活性检测方法,具体涉及生物样本中组氨酸酶及尿刊酸还原酶提取、相应产物的定性定量分析及活性检测。
背景技术:
1、氨基酸是构成蛋白质分子的基本单位。蛋白质作为生命活动的基础,在维持机体的生理动态平衡中发挥重要作用,氨基酸代谢稳态的维持是蛋白质正常合成的前提,是机体生命活动正常调节的基础;此外,氨基酸代谢过程中生成的代谢产物可通过多种途径发挥如免疫调节、促进细胞增殖等多种生理调节作用。
2、氨基酸代谢稳态失衡与多种疾病的发生相关。如苯丙酮酸尿症,由于苯丙氨酸代谢途径中的酶缺陷,导致苯丙氨酸无法正常转换为酪氨酸,使苯丙氨酸在体内蓄积并随尿排出,患者多出现精神神经症状;在肿瘤微环境中,异常的氨基酸代谢为肿瘤细胞的生长提供坚实后盾,为维持肿瘤细胞的快速增殖,肿瘤细胞自身上调多种转运体及氨基酸代谢酶表达和活性,如在丝氨酸饥饿环境中,肿瘤细胞参与丝氨酸生物合成途径的磷酸甘油脱氢酶(phosphoglycerate dehydrogenase,phgdh)表达及活性上调。除对肿瘤细胞的调节作用,异常氨基酸代谢所生成的代谢产物可维持肿瘤的免疫抑制微环境。
3、氨基酸代谢异常与多种疾病发病机制的关联成为研究者关注的焦点。精氨酸、谷氨酰胺、天冬酰胺、丝氨酸、色氨酸、甲硫氨酸以及组氨酸代谢等的靶向调控在疾病防控中均能够发挥一定的作用,在小分子化合物调控氨基酸代谢的研究中,相关酶活性检测可作为研究者初步评判小分子化合物调控作用强弱的指标。因此,准确高通量的酶活检测技术对于研究者高效开展实验至关重要。
4、组氨酸(l-histidine,l-his)代谢异常可导致高组氨酸血症,患者可出现语言障碍、肌肉痉挛、贫血等症状。组氨酸下游代谢产物尿刊酸(urocanic acid,uca),又名4-咪唑丙烯酸(4-imidazoleacrylic acid),尿刊酸的异常增高可引起患儿神经系统性疾病。尿刊酸下游代谢产物咪唑丙酸(imidazole propionate,imp)的异常增高与ii型糖尿病的发病密切相关。对组氨酸相关代谢酶的活性检测是研究其代谢的基础技术手段。在组氨酸代谢过程中,组氨酸酶可催化组氨酸脱氨形成尿刊酸,而尿刊酸可在尿刊酸还原酶的催化下进一步形成咪唑丙酸。目前,主要通过分光光度法检测组氨酸催化生成的尿刊酸的吸光度值实现对组氨酸酶活性的检测,此方法无法实现其催化产物的精准定量,并且容易受到所用器材、实验反应条件等多种因素的影响,导致实验结果的灵敏度以及准确度下降。而对于尿刊酸还原酶活性的检测,目前尚无相应检测技术手段。
技术实现思路
1、为了实现对生物样本中组氨酸酶及尿刊酸还原酶活性检测以及检测的准确度和灵敏度,本发明提供了一种组氨酸酶及尿刊酸还原酶活性的检测方法,基于lc-ms/ms技术手段,通过体外孵育体系,能够同时检测组氨酸酶及尿刊酸还原酶活性,并实现对组氨酸代谢产物尿刊酸、尿刊酸代谢产物咪唑丙酸的定性定量分析,相对于以往的技术手段而言,本发明方法有较低检测下限,可实现代谢产物检测的较高灵敏度以及准确度;此外,本发明首次实现生物样本中尿刊酸还原酶活性的检测。
2、本发明采用的技术方案为:
3、一种组氨酸酶及尿刊酸还原酶活性检测方法,包括以下步骤:
4、步骤(1)、对生物样本中组氨酸酶和尿刊酸还原酶进行提取:将生物样本和超纯水涡旋混匀,再在低温0~4℃静置2h,静置期间每隔30min涡旋1~2min,获得匀浆液;
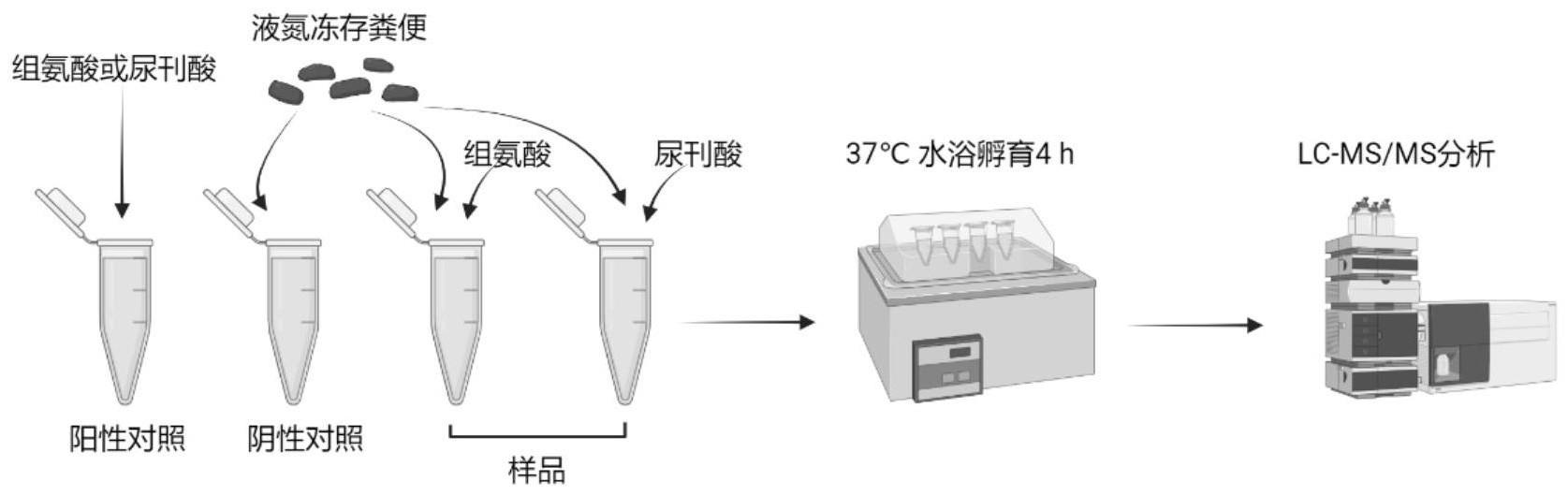
5、步骤(2)、分别构建组氨酸酶孵育体系和尿刊酸还原酶孵育体系,组氨酸酶孵育体系设置四个处理组:组氨酸酶实验组、空白溶剂对照组、生物样本空白匀浆组、组氨酸空白溶剂对照组,尿刊酸还原酶孵育体系设置四个处理组:尿刊酸还原酶实验组、空白溶剂对照组、生物样本空白匀浆组、尿刊酸空白溶剂对照组,其中,组氨酸酶实验组为:往步骤(1)得到的匀浆液中加入组氨酸标准品,尿刊酸还原酶实验组为:往步骤(1)得到的匀浆液中加入尿刊酸标准品,组氨酸酶孵育体系和尿刊酸还原酶孵育体系均在37℃水浴中孵育4h,每隔30min涡旋混匀1min;
6、步骤(3)、孵育结束后,组氨酸酶孵育体系、尿刊酸还原酶孵育体系均进行离心,再采用含内标物1-甲基色氨酸(1-methyl-d-tryptophan,1-met)的有机溶剂沉淀蛋白,挥干上清液,得到进样样品;
7、步骤(4)、步骤(3)得到的进样样品采用体积分数50%的甲醇复溶,离心,取上清液进样,进行lc-ms/ms分析,分别基于尿刊酸标准曲线、咪唑丙酸标准曲线获得尿刊酸、咪唑丙酸的浓度,再根据尿刊酸、咪唑丙酸浓度分别获得生物样品中组氨酸酶、尿刊酸还原酶活性:
8、组氨酸酶酶活性=(实验组尿刊酸浓度-空白溶剂对照组尿刊酸浓度-生物样本空白匀浆组尿刊酸浓度-组氨酸空白溶剂对照组尿刊酸浓度)/孵育时间;
9、尿刊酸还原酶酶活性=(实验组咪唑丙酸浓度-空白溶剂对照组咪唑丙酸浓度-生物样本空白匀浆组咪唑丙酸浓度-尿刊酸空白溶剂对照组咪唑丙酸浓度)/孵育时间。
10、步骤(1)中,所述的生物样本为新鲜粪便或经液氮冻存的粪便。
11、生物样本中酶的提取需在低温操作下进行以保证酶活,同时需要保证生物样本中组氨酸酶和尿刊酸还原酶充分分散到匀浆液中。生物样本中组氨酸酶和尿刊酸还原酶的提取方法为:生物样本和超纯水(ddh2o)按照质量比为1:5~1:20混合,先涡旋3~5min混匀,使粪便均匀分散于超纯水中,再置于冰上0~4℃静置2h,静置期间每隔30min涡旋1~2min,获得含有组氨酸酶和尿刊酸还原酶的匀浆液。
12、为了尽可能增大匀浆液中酶含量,优选的,生物样本和超纯水按照质量比为1:5混合。
13、优选的,生物样本和超纯水混合后,先涡旋混匀5min;再置于冰上静置2h,静置期间每隔30min涡旋1min,获得匀浆液。
14、步骤(2)中,组氨酸酶实验组:往步骤(1)得到的匀浆液中加入组氨酸标准品,组氨酸标准品终浓度为100μg/ml。
15、优选的,组氨酸酶实验组:取步骤(1)得到的500μl匀浆液,加入组氨酸标准品,使孵育体系中组氨酸标准品终浓度为100μg/ml。
16、具体的,组氨酸酶实验组:取500μl匀浆液,加入浓度为50mg/ml组氨酸标准品溶液(超纯水配制),使孵育体系中组氨酸标准品终浓度为100μg/ml。
17、尿刊酸还原酶实验组:往步骤(1)得到的匀浆液中加入尿刊酸标准品,尿刊酸标准品含量为100μg/ml。
18、优选的,尿刊酸还原酶孵育体系:取步骤(1)得到的500μl匀浆液,加入尿刊酸标准品,使孵育体系中尿刊酸标准品终浓度为100μg/ml。
19、具体的,尿刊酸还原酶孵育体系:取500μl匀浆液,加入浓度为50mg/ml尿刊酸标准品溶液(dmso配制),使孵育体系中尿刊酸标准品终浓度为100μg/ml。
20、空白溶剂对照组:与组氨酸酶实验组或尿刊酸还原酶实验组中匀浆液等体积的超纯水,用来排除溶剂中背景杂质的干扰。
21、生物样本空白匀浆组:与组氨酸酶实验组或尿刊酸还原酶实验组中匀浆液等体积的匀浆液,用来扣除粪便匀浆液中本身存在的尿刊酸或咪唑丙酸。
22、组氨酸空白溶剂对照组:与组氨酸酶实验组中匀浆液等体积的、组氨酸标准品含量为100μg/ml的超纯水溶液,用来扣除组氨酸自身分解所生成的尿刊酸。
23、尿刊酸空白溶剂对照组:与尿刊酸还原酶实验组中匀浆液等体积的、尿刊酸标准品含量为100μg/ml的超纯水溶液,用来扣除尿刊酸自身分解所生成的咪唑丙酸。
24、为模拟人体生理环境条件,使体外孵育体系中的组氨酸酶活性与尿刊酸还原酶活性更接近真实生理情况下组氨酸酶与尿刊酸还原酶的活性,本发明组氨酸酶孵育体系和尿刊酸还原酶孵育体系、空白溶剂对照组、生物样本空白匀浆组、组氨酸空白溶剂对照组以及尿刊酸空白溶剂对照组均在37℃进行孵育,并且优选37℃水浴进行孵育,保证孵育体系温度均匀,同时考虑尿刊酸与咪唑丙酸在水中的稳定性,尽量缩短孵育时间,优选孵育时间为4h。
25、步骤(3)中,组氨酸酶孵育体系中,组氨酸酶代谢产物为尿刊酸;尿刊酸还原酶孵育体系中,尿刊酸还原酶代谢产物咪唑丙酸。
26、孵育结束后,组氨酸酶孵育体系4℃离心两次,每次离心的转速为18000rpm,每次离心的时间为10min,保证上清液与沉淀充分分离以去除粪便残渣,得到组氨酸酶孵育体系上清液。
27、孵育结束后,尿刊酸还原酶孵育体系4℃离心两次,每次离心的转速为18000rpm,每次离心的时间为10min,保证上清液与沉淀充分分离以去除粪便残渣,得到尿刊酸还原酶孵育体系上清液。
28、所述的沉淀蛋白的方法为:往组氨酸酶孵育体系上清液、尿刊酸还原酶孵育体系上清液中分别加入有机溶剂,2000rpm涡旋振荡5min保证蛋白充分沉淀。
29、所述的有机溶剂为含500ng/ml内标1-甲基色氨酸的乙腈或甲醇,乙腈提取效率稍低于甲醇,因此,所述的有机溶剂优选为含500ng/ml内标1-甲基色氨酸的甲醇。内标物1-甲基色氨酸用以校正仪器响应不稳,操作条件变化时所带来的待测量物质响应误差。
30、所述的组氨酸酶孵育体系上清液或尿刊酸还原酶孵育体系上清液与有机溶剂的体积比为1:4。
31、为增大进样体系中尿刊酸或咪唑丙酸的浓度,于真空一体式挥干仪中挥干溶剂,分别得到:组氨酸酶孵育体系进样样品、尿刊酸还原酶孵育体系进样样品。
32、步骤(4)中,每0.4g生物样品制得的进样样品,采用100μl50%的甲醇复溶,4℃离心两次,每次离心的转速为18000rpm,每次离心的时间为10min,取上清液进样。利用梯度洗脱程序,分离组氨酸酶及尿刊酸还原酶相应的代谢产物,结合质谱检测,对待测物的特征离子碎片峰进行分析,实现对待测物的定性定量分析以及组氨酸酶及尿刊酸还原酶活性的分析。
33、hplc检测的色谱条件为:eclipse plus c18柱(4.6×150mm,5μm),柱温为40℃,进样量为5μl,流动相a为含0.1%甲酸的超纯水,流动相b为乙腈,流速为0.6ml/min,梯度洗脱条件:梯度洗脱程序:0-2min:1%流动相b,2-6min:40%流动相b,6-9min:90%流动相b,9-14.5min:1%流动相b,14.5min:stop。
34、质谱检测条件为:
35、尿刊酸检测模式为正离子模式;去簇电压(dp)为50v,tof ms scan碎裂电压(ce)为17v;尿刊酸的定性检测离子对为139.0/121.0。
36、咪唑丙酸检测模式为正离子模式;去簇电压(dp)为80v,tof ms scan碎裂电压(ce)为15v;咪唑丙酸的定性检测离子对为141.2/123.0。
37、1-甲基色氨酸检测模式为正离子检测模式,去簇电压(dp)为50v,tof ms scan碎裂电压(ce)为25v;1-甲基色氨酸的定性检测离子对为219.2/160.0。
38、为实现尿刊酸与咪唑丙酸的绝对定量,分别建立尿刊酸标准曲线与咪唑丙酸标准曲线。
39、尿刊酸标准曲线的建立方法为:称取10mg尿刊酸标准品,dmso溶解配制成浓度为10mg/ml尿刊酸储存液;再采用甲醇稀释得到系列浓度的尿刊酸标准曲线工作液;标准曲线工作液和含500ng/ml 1-甲基色氨酸的甲醇(作为蛋白沉淀剂)按照体积比1:4混合,2000rpm涡旋振荡5min,18000rpm离心10min,取400μl上清液,继续18000rpm离心10min,再取350μl上清液,挥干溶剂,100μl50%甲醇复溶,4℃、18000rpm离心10min两次,吸取上清液进样,进行lc-ms/ms分析,测得尿刊酸的浓度,以尿刊酸的浓度为横坐标、以尿刊酸的定性离子对的响应峰面积和1-甲基色氨酸的定性检测离子对的峰面积之比为纵坐标,建立尿刊酸标准曲线。
40、尿刊酸标准曲线工作液浓度为50μg/ml,10μg/ml,5μg/ml,1μg/ml,500ng/ml,100ng/ml,50ng/ml,10ng/ml,5ng/ml,1ng/ml,0.5ng/ml,0.1ng/ml。
41、咪唑丙酸标准曲线的建立方法为:称取10mg咪唑丙酸标准品,dmso溶解配制成浓度为10mg/ml咪唑丙酸储存液;再采用甲醇稀释得到系列浓度的咪唑丙酸标准曲线工作液;标准曲线工作液和含500ng/ml 1-甲基色氨酸的甲醇(作为蛋白沉淀剂)按照体积比1:4混合,2000rpm涡旋振荡5min,18000rpm离心10min,取400μl上清液,继续18000rpm离心10min,取350μl上清液,挥干溶液,100μl 50%甲醇复溶,4℃、18000rpm离心10min两次,吸取上清液进样,进行lc-ms/ms分析,测得咪唑丙酸的浓度,以咪唑丙酸的浓度为横坐标、以咪唑丙酸的定性离子对的响应峰面积和1-甲基色氨酸的定性检测离子对的峰面积之比为纵坐标,建立咪唑丙酸标准曲线。
42、咪唑丙酸标准曲线工作液浓度为500μg/ml,100μg/ml,50μg/ml,10μg/ml,5μg/ml,1μg/ml,500ng/ml,100ng/ml,50ng/ml,10ng/ml,5ng/ml,1ng/ml。
43、和现有技术相比,本发明有益效果:
44、1.利用本发明组氨酸酶活性检测方法,可以对尿刊酸进行绝对的定量分析,实现对尿刊酸纳克级别的灵敏定量,进而提高组氨酸酶活性检测的准确度与灵敏度。
45、2.本发明首次实现了尿刊酸还原酶活性的检测,对尿刊酸还原酶活性检测具备灵敏度与准确度,并且实现尿刊酸代谢产物咪唑丙酸的定量分析。
46、3.本发明通过组氨酸酶及尿刊酸还原酶产物梯度洗脱分离以及质谱检测方法,可实现同时检测组氨酸酶及尿刊酸还原酶产物及酶活性。
47、4.本发明所使用的酶活分析方法,具有极低的检测下限,检测过程中受操作人员主观因素影响小,可实现检测结果的高灵敏度、高准确度、高特异性与客观性。
48、5.本发明所使用的lc-ms/ms分析方法,可实现高通量的检测筛选,大大降低实验检测所需成本。
- 还没有人留言评论。精彩留言会获得点赞!