一种人脂肪来源的间充质干细胞制备方法与流程
本发明涉及生物,具体涉及一种人脂肪来源的间充质干细胞制备方法。
背景技术:
1、间充质干细胞(msc,mesenchymal stem cells)是一类早期未分化细胞,具有自我更新、自我复制、无限增殖及多向分化潜能等特点,可通过分泌细胞因子,减少炎症、减少组织细胞凋亡、促进内源性组织器官的干祖细胞增殖及进行免疫调节,从而作为种子细胞达到修复组织器官的效果,连续传代培养和冷冻保存后仍具有多向分化潜能,医学界称为“万用细胞”;
2、间充质干细胞(msc,mesenchymal stem cells)是干细胞家族的重要成员,来源于发育早期的中胚层,属于多能干细胞,msc最初在骨髓中发现,因其具有多向分化潜能、造血支持和促进干细胞植入、免疫调控和自我复制等特点而日益受到人们的关注;
3、如间充质干细胞在体内或体外特定的诱导条件下,可分化为脂肪、骨、软骨、肌肉、肌腱、韧带、神经、肝、心肌、内皮等多种组织细胞,连续传代培养和冷冻保存后仍具有多向分化潜能,可作为理想的种子细胞用于衰老和病变引起的组织器官损伤修复;
4、从人的脂肪组织中分离出类似于骨髓间充质干细胞(bmscs)的成体多潜能细胞群——脂肪来源干细胞(adipose mesenchymal stem cells,adsc),拥有多向分化潜能。adscs也属于来自中胚层的成体干细胞,其体外扩增和自我更新能力很强,经过诱导培养可分化为脂肪细胞、骨和软骨细胞、肌肉细胞、神经细胞、心肌细胞、神经细胞及血管内皮细胞等多种组织细胞。简而言之,脂肪干细胞(adipose-derived stem cells,adscs)是从脂肪组织中分离得到的一种具有多向分化潜能的干细胞;它能够分化为脂肪、骨、软骨、肌肉、血管内皮、肝、胰、神经等细胞类型。2001年,zuk等通过脂肪抽提术,在吸出的人体脂肪悬液中第一次分离得到;
5、脂肪来源间充质干细胞是近年来从脂肪组织中分离得到的一种具有多向分化潜能的干细胞,可分化为间质类的细胞,如:骨细胞、软骨细胞、神经细胞、胰岛细胞或脂肪细胞等;脂肪干细胞能够在体外稳定增殖且衰亡率低,同时它具有取材容易、体内储备量大、适宜大规模培养,对机体损伤小、适宜自体移植等优点;在再生治疗领域中,脂肪组织是一个实用的、广泛的干细胞来源,脂肪来源间充质干细胞有延缓衰老、组织细胞修复、器官替代等功能,在保持年轻态、提高免疫力、强筋健骨、改善男性功能、推迟女性更年期等临床应用方面有很高的应用价值;
6、以往针对于脂肪来源间充质干细胞的研究多为采用组织块培养法或者胰酶消化法,组织块消化方法消化不均匀,常存在未能完全消化的部分,同时多次吹打对细胞损害很大;同时组织块消化法分离的原代细胞培养时间长,且并非每一块都有细胞萌出,故细胞传代次数和最终获取的细胞数较少,细胞种类不纯,使进一步持续深入的研究受到限制;而胰酶消化法对细胞的损害比较大,尤其是在37℃的条件下,胰酶可以最大程度地发挥其消化效力,故对消化时间和消化次数的掌控较难;过度消化会导致细胞损伤,细胞膜破损,dna溢出;从而导致血管基质组分(svf,stromal vascular fraction,从抽取的脂肪组织中提取有效成分,含有多种具有修复功能的细胞以及细胞因子混合物形成的细胞群)得率低,胰酶消化时间长,严重影响svf细胞群的活性,且多数制备方法中添加有动物源血清,在临床转化应用脂肪来源间充质干细胞作为种子细胞在临床中的应用,存在很大的瓶颈,有许多的问题有待解决:如动物源蛋白成分残留,细胞制备体系中外源病毒的引入,及细胞数量及活性生物学功能方面都存在诸多争议,没有明确的安全应用规范,这使脂肪来源的间充质干细胞在临床应用中受到很大的限制。
技术实现思路
1、本发明要解决的技术问题是对于脂肪来源间充质干细胞的研究多为采用组织块培养法或者胰酶消化法,组织块消化方法消化不均匀,常存在未能完全消化的部分,同时多次吹打对细胞损害很大;同时组织块消化法分离的原代细胞培养时间长,且并非每一块都有细胞萌出,故细胞传代次数和最终获取的细胞数较少,细胞种类不纯,使进一步持续深入的研究受到限制;而胰酶消化法对细胞的损害比较大,尤其是在37℃的条件下,胰酶可以最大程度地发挥其消化效力,故对消化时间和消化次数的掌控较难,本发明提供一种人脂肪来源的间充质干细胞制备方法,能够快速培养出间充质干细胞,且其细胞活率99%以上,采用人的离体脂肪组织诱导培养的间充质干细胞用于治疗病成为可能,从而可以避免异体细胞的免疫排斥反应;本发明方法的诱导过程快速而高效,这将有利于临床治疗方案的及时应用,用以解决现有技术导致的缺陷。
2、为解决上述技术问题本发明提供以下的技术方案:
3、一种人脂肪来源的间充质干细胞制备方法,其中,包含以下步骤:
4、步骤1:取人的离体脂肪组织放入培养皿中,重复加入等体积的平衡盐溶液进行清洗,直至表面无明显血渍,得到脂肪组织块;
5、步骤2:将所述脂肪组织块边清洗边剪碎至绿豆大小,得到脂肪剪碎组织;
6、步骤3:在所述脂肪剪碎组织中加入等体积的消化酶后,放至恒温摇床上进行消化直至无明显结块,加入无血清完全培养基终止消化酶,得到脂肪组织液;
7、步骤4:对所述脂肪组织液采用100um的细胞筛网进行过滤后加入离心管中,定容至40-45ml后,放入离心机,在1200rpm的转速下,升9降3,离心10min后,去除上清液,用适量的完全培养基重悬离心后的细胞沉淀,去不超过0.5ml进行计数,使其最终细胞浓度在0.87*106~1.05*106个/ml的范围内,得到细胞悬液;
8、步骤5:取多个t75cm2培养瓶(优选30个)且每个t75cm2培养瓶中依次加入11ml的无血清完全培养基、1ml的所述细胞悬液,将所述t75cm2培养瓶的瓶盖拧紧后,以3个为一摞将所述t75cm2培养瓶平置,匀速摇晃10sec,使加入的所述细胞悬液能均匀分布整个所述t75cm2培养瓶的底面,随后放置于二氧化碳培养箱中培养6天;
9、步骤6:每2天更换一次完全培养基,当细胞生长到所述t75cm2培养瓶瓶底面积的80%时,使用3ml0.05%胰蛋白酶在37℃下消化1min,使用3ml无血清完全培养基终止消化,收集至50ml离心管中,配平,温度4℃,1200rpm转速下,升9降3,离心10min,得到p0代细胞;
10、步骤7:使用无血清完全培养基将所述p0代细胞按1:3的接种比例接种到新的无菌t75cm2培养瓶中加入12ml无血清完全培养基进行传代培养;
11、步骤8:待所述p0代细胞生长达到80%融合,用dpbs洗液清洗两遍后,每个所述t75cm2培养瓶中加入3ml0.05%胰蛋白酶消化细胞,37℃消化1min,显微镜下观察所述p0代细胞变圆后,将所述p0代细胞从瓶底轻轻拍打下来,加入3ml无血清完全培养基终止消化,将p0代细胞悬液吸入到50ml离心管中,并将每个所述t75cm培养瓶中再加入5mldpbs清洗两次,并将洗液一并加入到已收集的所述p0代细胞细胞悬液中,温度4℃,1200rpm转速,升9降3,离心10min得到p1代细胞;
12、步骤9:按步骤7-8的传代培养依次得到p2代细胞、p3代细胞和p4代细胞,所述p4代细胞为人脂肪来源的间充质干细胞。
13、上述的一种人脂肪来源的间充质干细胞制备方法,其中,步骤1中取10g人的腹部离体脂肪组织;
14、所述培养皿中添加有保护液;
15、所述平衡盐溶液为含有双抗和两性霉素b的d-hanks平衡盐溶液。
16、上述的一种人脂肪来源的间充质干细胞制备方法,其中,步骤3中所述消化酶为0.3%i型胶原酶和0.2%ii胶原酶1:1比例的混合液;
17、所述恒温摇床的温度为37℃,转速为140~150rpm/min,消化时间为30-40min;
18、加入3~5ml的所述无血清完全培养基。
19、上述的一种人脂肪来源的间充质干细胞制备方法,其中,所述无血清完全培养基为每500mldmemf12空白培养基中添加25ml~50ml重组人蛋白、2%~5%血小板裂解液、2mmol/ll-谷氨酰胺、10ng/ml表皮细胞生长因子(egf)、10ng/ml碱性成纤维细胞生长因子(bfgf)的间充质干细胞无血清完全培养基。
20、上述的一种人脂肪来源的间充质干细胞制备方法,其中,所述保护液为:50mldmemf12空白培养基、0.5ml~1mlgibco青链霉素双抗/penstrep(10,000units/mlpenicillin,10,000μg/mlstreptomycin)。
21、上述的一种人脂肪来源的间充质干细胞制备方法,其中,所述二氧化碳培养箱中培养的培养条件为温度37±0.5℃、二氧化碳体积分数5±0.2%。
22、上述的一种人脂肪来源的间充质干细胞制备方法,其中,所述传代培养的培养条件为温度37±0.5℃、二氧化碳体积分数5±0.2%。
23、上述的一种人脂肪来源的间充质干细胞制备方法,其中,还需对所述p4代细胞进行送检,筛选得到约6~8×109个合格所述p4代细胞且细胞活率为99%以上。
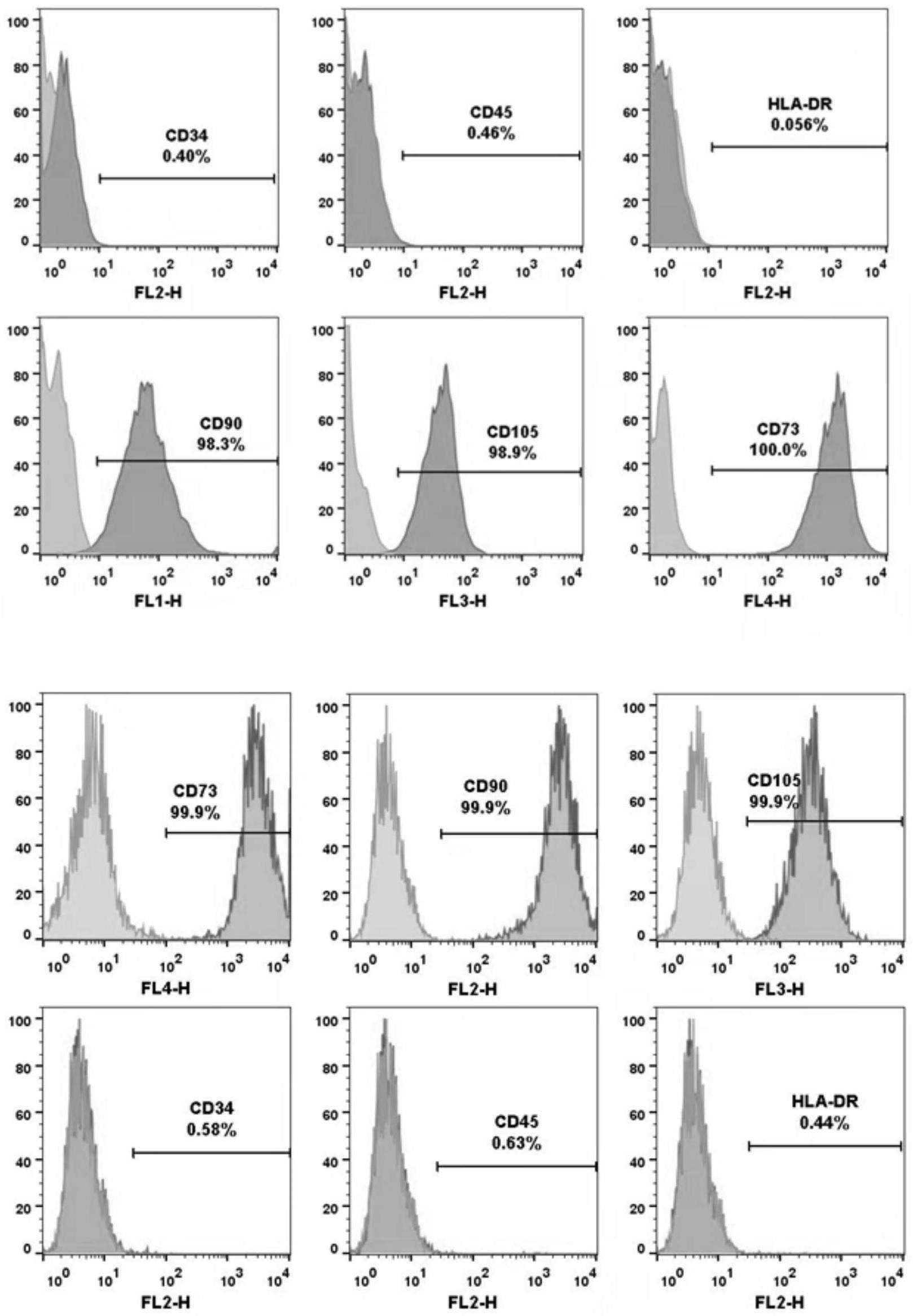
24、上述的一种人脂肪来源的间充质干细胞制备方法,其中,送检包含检测细菌、真菌、支原体、内毒素、传染病、流式鉴定、三系分化试验鉴定、细胞表面抗原鉴定,合格标准为:cd90、cd73、cd105表达均大于95%,cd45、cd34、hla-dr表达均小于2%。
25、依据上述本发明一种人脂肪来源的间充质干细胞制备方法提供的技术方案具有以下技术效果:
26、依据本方法能够快速培养出间充质干细胞,且其细胞活率99%以上,采用人的离体脂肪组织诱导培养的间充质干细胞用于治疗病成为可能,从而可以避免异体细胞的免疫排斥反应;本发明方法的诱导过程快速而高效,这将有利于临床治疗方案的及时应用。
- 还没有人留言评论。精彩留言会获得点赞!