本发明涉及sirna靶向型药物载体,尤其涉及一种ph响应型的肝靶向的药物递送载体及其制备方法和应用。
背景技术:
1、小干扰rna(small interfering rna,sirna)是双链的小分子核酸,在转录后发挥rna干扰作用(rnai),可特异性抑制疾病相关靶基因的rna的表达从而发挥治疗效果,因此,利用rna干扰可以起到与靶向药物相同的作用。随着sirna生物学机制的阐明和sirna合成方法的快速发展,绝大多数的基因可通过sirna技术进行沉默,而sirna则主要作用于rna,其能够特异性抑制靶基因的表达,作用位点专一,通常不影响正常基因表达,因此sirna作为靶向药物应用时,会具有更好的选择性及特异性。目前,国际上已有多个sirna药物获批fda上市许可,国内亦有多款sirna药物处于不同研发阶段。目前sirna体内应用面临的主要难题有:sirna的稳定性较差,半衰期较短,需要提高靶向性,以达到高效递送,以及缺少细胞内涵体的逃逸能力等。
2、脂质纳米粒(lnp)是一种具有均匀脂质核心的脂质囊泡,具有很高的生物相容性和生物可降解性,因此被用来递送多种活性成分。阳离子聚合物可以通过其正电荷属性负载负电荷的药物和基因,递送其进入靶细胞,发挥药物或基因的功能,达到治疗疾病的目的。含有阳离子材料的脂质纳米粒已在世界范围内广泛用于研究sirna递送,因为这些载体可以通过静电相互作用保持带负电荷的sirna;此外,带正电的载体还与带负电的细胞表面相互作用,并将其sirna输送到细胞中。尽管带正电荷的脂质体能够在低浓度的sirna下诱导高细胞溶质sirna递送和高效的基因沉默,但它们的正电荷会引起与生理环境中细胞膜的非特异性相互作用并诱导细胞发生毒性活动,例如产生活性氧物种、能量代谢中断和细胞死亡,因此,开发ph响应型聚合物对于减少非特异性互作及提高sirna递送效率很重要。
3、糖尿病作为非传染性疾病,在自然病程中,胰岛β细胞功能随着病程的延长而逐渐下降,胰岛素分泌量日益减少,因而对降糖药物的需求和依赖程度会逐渐增大,长时间用药机体产生耐药性,加大用药剂量的同时,药物的毒副作用也增加,因此迫切需要开发能提高药效、毒副作用小且药物递送效率高的靶向递送载体。
4、聚集诱导发光(aggregation-induced emission,aie),是指一类有机分子在溶液中溶解状态下发光很弱或者不发光,但当分子聚集时能发出强的荧光的发光现象。aie分子在水中形成聚集体后仍能发射强的荧光,不会因聚集而荧光淬灭,因而在生物领域具有显著的应用优势。材料作为新型的有机荧光材料具有一系列独特的优势,包括灵敏度高、聚集态发射效率高、光稳定性好、斯托克斯(stokes)位移大、背景噪声低、长期无创及生物可视化能力强等,已被成功用于细胞荧光追踪探针,为基于影像指导的疾病临床治疗。
技术实现思路
1、针对现有技术中脂质体的正电荷引起的细胞膜非特异性互作、诱导细胞发生毒性活动以及缺乏高效递送糖尿病药物的载体的问题,本发明提供了一种ph响应型的肝靶向的药物递送载体及其制备方法和应用。
2、为了实现上述发明目的,本发明提供以下技术方案:
3、本发明提供了一种阳离子聚合物,所述阳离子聚合物的结构式如下所示:
4、
5、本发明还提供了上述阳离子聚合物的制备方法,包括如下步骤:
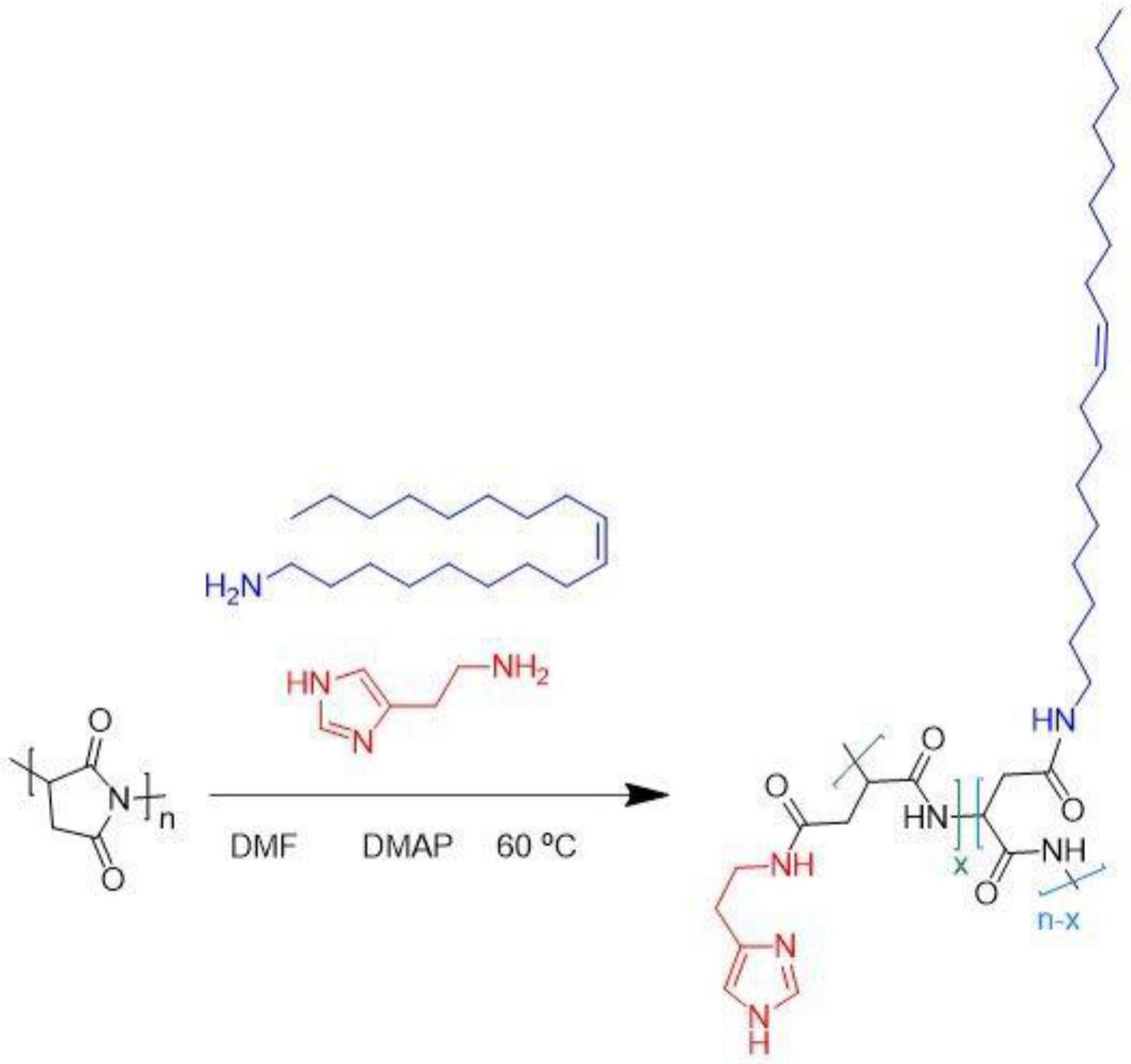
6、(1)将聚琥珀酰亚胺粉末、油胺、组胺二盐酸盐、4-二甲氨基吡啶与n,n二甲基甲酰胺混合,超声助溶,待1/2~3/4的固体溶解后加入磁珠进行磁力搅拌,至固体全部溶解;
7、(2)对上述溶解完成的溶液依次进行透析、离心,然后取上清液进行冻干,得阳离子聚合物。
8、优选的,步骤(1)中所述的聚琥珀酰亚胺粉末、油胺、组胺二盐酸盐、4-二甲氨基吡啶与n,n二甲基甲酰胺的混合比例为1~3g:1~3g:1~2g:0.05~0.15g:28~32ml,所述超声的功率为450~550w,所述磁力搅拌的温度为50~100℃,所述磁力搅拌的转速为250~350rpm;
9、步骤(2)中所述透析的截留分子量为3000~4000d,所述透析的时间为12~24h,所述离心的转速为3500~4500rpm,所述离心的时间为25~35s,所述冻干的温度为-45~-55℃,所述冻干的时间为40~50h。
10、本发明还提供了一种ph响应型的肝靶向的药物递送载体,包括上述的阳离子聚合物,二硬脂酰磷脂酰胆碱,胆固醇和靶向分子。
11、优选的,所述阳离子聚合物,二硬脂酰磷脂酰胆碱,胆固醇和靶向分子的质量比为23~30:5~8:13~15.6:3.2~3.7;
12、所述靶向分子包括胆固醇-聚乙二醇-半乳糖、磷脂酰乙醇胺-聚乙二醇-半乳糖和氨基-聚乙二醇-半乳糖中的一种;
13、所述药物递送载体还包括近红外二区发光染料,所述近红外二区发光染料包括4,8-二取代苯并双噻二唑衍生物,所述4,8-二取代苯并双噻二唑衍生物与所述阳离子聚合物的质量比为0.8~1:23~30。
14、本发明还提供了上述一种ph响应型的肝靶向的药物递送载体的制备方法,包括如下步骤:
15、(1)将上述阳离子聚合物,二硬脂酰磷脂酰胆碱,胆固醇、靶向分子与乙醇溶液混合,得混合液1;
16、(2)将sirna与tris-hclbuffer混合,得混合液2;
17、(3)采用乙醇注射沉淀法将所述混合液1与混合液2混合,得混合液3;
18、(4)对所述混合液3进行透析,得ph响应型的肝靶向的药物递送载体。
19、优选的,步骤(1)中所述乙醇溶液与所述阳离子聚合物的体积质量比为7~9ml:23~30mg,所述乙醇溶液的体积浓度为70~80%;
20、步骤(1)中所述阳离子聚合物中总氮元素的物质的量与步骤(2)中所述sirna中总磷元素的物质的量之比为1:1~10;
21、步骤(2)中所述sirna的核苷酸序列如seq id no.1所示;
22、步骤(2)中所述sirna与tris-hclbuffer的混合比例为100~120μg:20~30ml。
23、优选的,步骤(4)中所述透析的截留分子量为3000~4000d,所述透析的时间为20~25h。
24、本发明还提供了上述一种ph响应型的肝靶向的药物递送载体在制备肝脏靶向药物中的应用。
25、本发明还提供了上述一种ph响应型的肝靶向的药物递送载体在制备治疗糖尿病的药物中的应用。
26、与现有技术相比,本发明的有益效果如下:
27、1、本发明提供的阳离子聚合物,可与带负电荷的sirna通过电荷吸引作用复合后,使得药物递送载体更稳定,粒径分布更集中,有利于药物递送载体在药物输送方面的应用。
28、2、经实验表明,本发明制备的药物递送载体能将sirna包裹递送至人肝癌细胞,并成功进入细胞,实现sirna的内涵体逃逸,实现了良好的递送及释放效果;且活体成像结果表明,小鼠肝脏荧光强度最强,即阳离子脂质体复合物纳米颗粒在对小鼠尾静脉注射24h后富集在肝脏,说明了本发明制备的药物递送载体在活体内的肝脏靶向作用。
