一种转氨酶突变体、编码基因及其应用
本发明涉及生物工程,具体涉及一种针对巨大芽孢杆菌来源转氨酶改造的转氨酶突变体、编码基因及其在制备(s)-1-(3-甲氧苯基)乙胺中的应用。
背景技术:
1、卡巴拉汀(rivastigmine)属于第三代改善胆碱系统功能的药物,通过抑制乙酰胆碱酯酶来增加脑中释放胆碱能的神经元的功能,从而改善阿尔茨海默病患者的认知作用;还可抑制丁酰胆碱酯酶以发挥双重抑制作用,用于治疗轻、中度帕金森型痴呆症。(s)-1-(3-甲氧苯基)乙胺是合成卡巴拉汀的关键手性中间体之一。
2、目前卡巴拉汀手性中间体的制备主要有化学法和生物催化法两种。化学法主要有利用手性催化剂进行不对称诱导合成,如中国专利文献cn111362814a、cn101481335a等中利用(salen)mn(iii)、钛酸四异丙酯等手性催化剂进行不对称诱导合成卡巴拉汀手性中间体;或采用特定的拆分体系进行手性拆分消旋胺或醇中间体,获得关键的手性胺或手性醇中间体,再通过后续转化得到s构型的卡巴拉汀产物,如中国专利文献cn114804989a、cn113461554a、cn104151176a。化学拆分法虽然所用试剂相对比较便宜,但只有一半的消旋体能被利用,另外一个构型被浪费,成本高、废物量大。
3、利用生物催化法可以一步得到对应的高立体选择性产物,减少了不对称诱导合成法中手性诱导剂的使用,简化了操作流程,降低了生产成本,并且可以提高原子经济性。转氨酶(transaminase)可以借由辅因子磷酸吡哆醛将氨基基团从供体转移到受体,有很高的立体选择性,底物谱广泛。中国专利文献cn115807046a利用一种河流弧菌转氨酶vf-ω-ata参与到另一种卡巴拉汀手性中间体3s-(1-氨基乙基)苯基乙基(甲基)氨基甲酸酯的制备中,获得了良好的效果。但是,目前没有天然的能够高效合成(s)-1-(3-甲氧苯基)乙胺的转氨酶。因此,开发催化活力高、立体选择性强的转氨酶用于(s)-1-(3-甲氧苯基)乙胺的合成是本领域技术人员需要解决的问题。
技术实现思路
1、本发明的目的在于提供一种催化活力高、立体选择性强的转氨酶用于制备高光学纯度(s)-1-(3-甲氧苯基)乙胺,满足工业化生产的要求。
2、为实现上述目的,本发明采用如下技术方案:
3、本发明通过对巨大芽孢杆菌来源转氨酶bm-ata的编码基因(seq id no.16)进行定点突变,获得转氨酶突变体。所述转氨酶突变体是氨基酸序列如seq id no.1所示的巨大芽孢杆菌来源转氨酶通过氨基酸突变所得的突变体,其中,所述氨基酸突变的位点为第295位、第387位、第436位中的至少一个,或者第242位与第295位、第387位、第436位中至少一个的组合,且第295位的苏氨酸突变为半胱氨酸,第387位的亮氨酸突变为丙氨酸,第436的缬氨酸突变为丙氨酸,第242位的丙氨酸突变为缬氨酸。
4、具体的,第295位的苏氨酸突变为半胱氨酸bmata-t295c,氨基酸序列如seq idno.2所示;
5、第387位的亮氨酸突变为丙氨酸的突变体bmata-l387a,氨基酸序列如seq idno.3所示;
6、第436位的缬氨酸突变为丙氨酸的突变体bmata-v436a,氨基酸序列如seq idno.4所示;
7、第242位的丙氨酸突变为缬氨酸且第295位的苏氨酸突变为半胱氨酸的突变体bmata-a242v/t295c,氨基酸序列如seq id no.5所示;
8、第242位的丙氨酸突变为缬氨酸且第387位的亮氨酸突变为丙氨酸的突变体bmata-a242v/l387a,氨基酸序列如seq id no.6所示;
9、第242位的丙氨酸突变为缬氨酸且第436位的缬氨酸突变为丙氨酸的突变体bmata-a242v/v436a,氨基酸序列如seq id no.7所示;
10、第295位的苏氨酸突变为半胱氨酸且第387位的亮氨酸突变为丙氨酸的突变体bmata-t295c/l387a,氨基酸序列如seq id no.8所示;
11、第295位的苏氨酸突变为半胱氨酸且第436位的缬氨酸突变为丙氨酸的突变体bmata-t295c/v436a,氨基酸序列如seq id no.9所示;
12、第387位的亮氨酸突变为丙氨酸且第436位的缬氨酸突变为丙氨酸的突变体bmata-l387a/v436a,氨基酸序列如seq id no.10所示;
13、第242位的丙氨酸突变为缬氨酸且第295位的苏氨酸突变为半胱氨酸且第387位的亮氨酸突变为丙氨酸的突变体bmata-a242v/t295c/l387a,氨基酸序列如seq id no.11所示;
14、第242位的丙氨酸突变为缬氨酸且第295位的苏氨酸突变为半胱氨酸且第436位的缬氨酸突变为丙氨酸的突变体bmata-a242v/t295c/v436a,氨基酸序列如seq id no.12所示;
15、第242位的丙氨酸突变为缬氨酸且第387位的亮氨酸突变为丙氨酸且第436位的缬氨酸突变为丙氨酸的突变体bmata-a242v/l387a/v436a,氨基酸序列如seq id no.13所示;
16、第295位的苏氨酸突变为半胱氨酸且第387位的亮氨酸突变为丙氨酸且第436位的缬氨酸突变为丙氨酸的突变体bmata-t295c/l387a/v436a,氨基酸序列如seq id no.14所示;
17、第242位的丙氨酸突变为缬氨酸且第295位的苏氨酸突变为半胱氨酸且第387位的亮氨酸突变为丙氨酸且第436位的缬氨酸突变为丙氨酸的突变体bmata-a242v/t295c/l387a/v436a,氨基酸序列如seq id no.15所示。
18、研究表明,相较于野生型转氨酶,上述转氨酶突变体的催化活力显著提升。
19、对所述转氨酶突变体的其他氨基酸位点的保守取代形式、增加或缺失一个或几个氨基酸的形式、氨基端截断的形式、羧基端截断的形式,这些突变体形式也包括在本发明的范围内。
20、本发明还提供了用于编码所述转氨酶突变体的编码基因,所述编码基因是在seqid no.16所示核苷酸序列的基础上对编码相应氨基酸的密码子进行突变获得。具体的,t295c为编码第295位苏氨酸的密码子acc突变为编码半胱氨酸的密码子tgc,l387a为编码第387位亮氨酸的密码子ctg突变为编码丙氨酸的密码子gcg,v436a为编码第436位缬氨酸的密码子gtt突变为编码丙氨酸的密码子gcg,a242v为编码第242位丙氨酸的密码子gca突变为编码缬氨酸的密码子gtg。
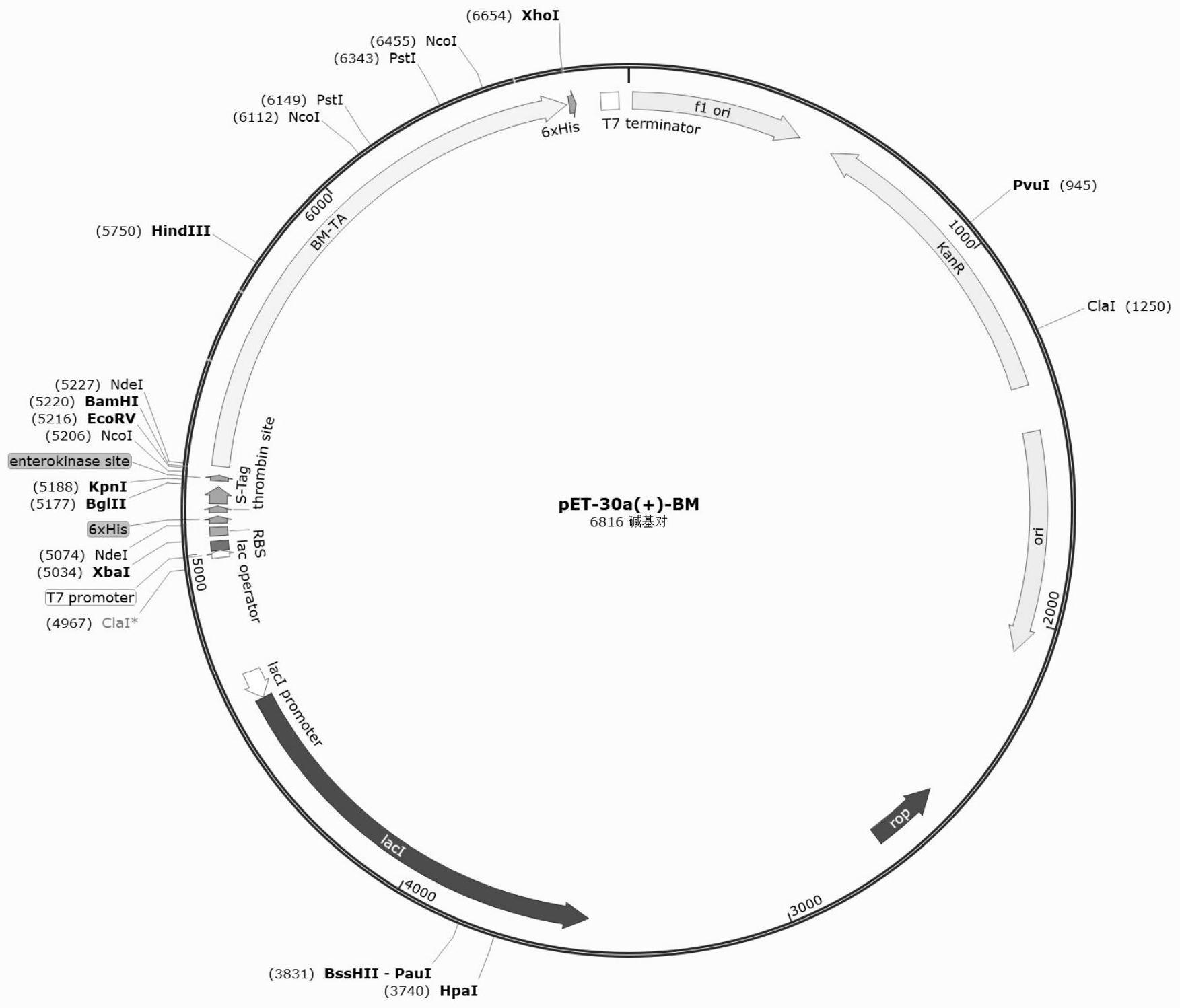
21、本发明还提供了包含编码所述的转氨酶突变体氨基酸序列的编码基因的重组表达载体。优选的,所述重组表达载体以pet30a为载体质粒。
22、本发明还提供了包含所述重组表达载体的基因工程菌,所述基因工程菌用于生产所述的转氨酶突变体。所述重组载体转化宿主细胞获得重组基因工程菌,所述宿主细胞可以为本领域的各种常规宿主细胞,作为优选,基因工程菌的宿主菌采用大肠杆菌e.colibl21。
23、本发明还提供了一种构建所述转氨酶突变体的方法,所述方法包括以下步骤:
24、(1)设计定点突变引物,以携带有巨大芽孢杆菌来源转氨酶编码基因的质粒为模板,进行反向pcr,获得转氨酶中第295位t突变为c或第387位l突变为a或第436位v突变为a的单位点突变产物;
25、(2)以单位点突变产物为模板,利用所述定点突变引物进行反向pcr获得双位点突变产物,或者利用针对第242位a突变为v的引物获得双位点突变产物;以双位点突变产物为模板,利用所述定点突变引物进行反向pcr获得三位点突变产物;以三位点突变产物为模板,利用所述定点突变引物进行反向pcr获得四位点突变产物;
26、(3)将所述单位点突变产物、双位点突变产物、三位点突变产物或四位点突变产物转化至宿主菌,筛选获得转氨酶突变体表达菌株,诱导表达,获得所述的转氨酶突变体。
27、其中第295位t突变为c所需的引物:
28、t295c-f:5’-cagccggatattatttgcatgggtaaaggtctgag-3’;
29、t295c-r:5’-ctcagacctttacccatgcaaataatatccggctg-3’;
30、第387位l突变为a所需的引物:
31、l387a-f:5’-gatggttatggcctggcgtggattgttgatattgtg-3’;
32、l387a-r:5’-cacaatatcaacaatccacgccaggccataaccatc-3’;
33、第436位v突变为a所需的引物:
34、v436a-f:5’-gattggtggtgcgatgccgaataccatgcg-3’;
35、v436a-r:5’-cgcatggtattcggcatcgcaccaccaatc-3’;
36、第242位a突变为v所需的引物:
37、a242v-f:5’-gaagttagccagggtgtgggtagcgcaatg-3’;
38、a242v-r:5’-cattgcgctacccacaccctggctaacttc-3’。
39、优选的,重组质粒的原始载体为pet30a;宿主菌采用大肠杆菌e.coli bl21。
40、本发明的另一个目的是提供所述的转氨酶突变体在制备(s)-1-(3-甲氧苯基)乙胺中的应用,所述应用包括在添加胺供体条件下不对称催化3-甲氧基苯乙酮胺化生成(s)-1-(3-甲氧苯基)乙胺。
41、本发明提供的转氨酶突变体在添加胺供体的形况下不对称催化3-甲氧基苯乙酮胺化,生成高光学纯度(s)-1-(3-甲氧苯基)乙胺,e.e.>99%,具有良好的工业化应用前景。
42、所述应用包括:以含有转氨酶突变体编码基因的工程菌经发酵培养后离心获得的湿菌体、湿菌体固定化细胞、湿菌体超声破碎后提取的酶或者固定化酶为催化剂,在外加(s)-α-甲基苄胺和磷酸吡哆醛条件下以3-甲氧基苯乙酮为底物,以含有机溶剂的ph值≤8的缓冲液为反应介质,在25-37℃、150-300rpm条件下反应,反应结束后,将反应液分离纯化,获得(s)-1-(3-甲氧苯基)乙胺。
43、本发明所述的转氨酶突变体可以以工程菌全细胞形式使用,也可以是未经纯化的粗酶形式使用,也可以是部分纯化的或完全纯化的酶的形式使用。还可以利用本领域已知的固定化技术将本发明的转氨酶突变体制成固定化酶或固定化细胞形式的生物催化剂。
44、优选的,反应体系中,催化剂的用量以湿菌体重量计为20-100g/l,其中湿菌体含水质量为70-90%。更优选为50g/l。
45、优选的,反应体系中,底物的浓度为1-8g/l,更优选为3g/l。
46、优选的,反应体系中,(s)-α-甲基苄胺的浓度为4-35g/l,更优选为12g/l。
47、优选的,反应体系中,磷酸吡哆醛的浓度为0.2-0.4g/l,更优选为0.25g/l。
48、优选的,ph缓冲溶液为磷酸缓冲液,即nah2po4-na2hpo4缓冲液,其缓冲ph值7.0-8.0,进一步优选为7.4-7.6,更优选为7.5。
49、优选的,所述有机溶剂为异丙醇或二甲基亚砜,有机溶剂在ph缓冲溶液中的体积分数为8-12%,更优选为10%。
50、上述各原料的添加浓度,如湿菌体、底物、(s)-α-甲基苄胺、磷酸吡哆醛均以1l ph缓冲液计算。
51、优选的,反应温度为30℃。
52、反应时间为3-6h,优选为4h。
53、优选的,振荡速率为220rpm。
54、优选的,所述的湿菌体为e.coli bl21/pet30a-bmata-t295c/l387a/v436a。该突变体对(s)-1-(3-甲氧苯基)乙胺的产率可以达到75.22%,是同等催化条件下野生型转氨酶的19倍,光学纯度ees为98%。
55、发酵培养方法为:重组工程菌接种至含卡那霉素(终浓度为50μg/ml)的lb液体培养基中,37℃振荡培养18h;种子液以1%体积比接种至新鲜的含有卡那霉素(终浓度为50μg/ml)的lb液体培养基中,37℃、220rpm条件下振荡培养至菌体od600为0.6,加入终浓度为0.1mm的异丙基-β-d-硫代吡喃半乳糖苷(iptg),25℃、220rpm诱导培养16h,于4℃、3500rpm离心10min收集菌体细胞。
56、本发明具备的有益效果:
57、(1)本发明提供的转氨酶突变体相对野生型转氨酶具有更高的酶活力,可以以3-甲氧基苯乙酮为底物制备(s)-1-(3-甲氧苯基)乙胺,产物的收率高,无副产物产生。
58、(2)本发明利用转氨酶突变体作为卡巴拉汀手性中间体生物催化剂,使得高光学纯度手性产物的获得更加经济简便,生产方法具有操作简单、成本低廉等优点,大大降低了生产成本,具有很好的工业化应用前景。
- 还没有人留言评论。精彩留言会获得点赞!