一种激活GRP受体的多肽化合物及其用途的制作方法
本发明属于生物医药多肽,具体涉及一种激活grp受体的多肽化合物及其用途。
背景技术:
1、胃泌素释放肽(gastrin-releasing peptide,grp)是由27个氨基酸构成的哺乳类神经肽,是1971年由anastasi首次从欧洲蛙类皮肤中提取出来的一种与蛙皮素同源的小调节肽,gpr与蛙皮素在结构上相似,在c端部分都是非常保守的,而其c端部分正是其发挥生物活性的重要部位,因此在多种哺乳动物细胞和组织中发挥相似的生物学作用。gpr通过与gpr受体(grp receptor,grpr)高亲和从而发挥生物学作用。grpr也属于g蛋白偶联受体家族,包含典型的7个跨膜结构域[1]。grpr由384个氨基酸构成,在人类、小鼠和大鼠分别定位于染色体xp22.2-p22.13(人类),xf4(小鼠),xq21(大鼠)。在过去的研究中,越来越多的证据表明,grp/grpr系统广泛影响生理功能,包括痒感觉、疼痛感、记忆的形成和表达、应激反应、焦虑、恐惧、细胞增殖和免疫系统中的趋化作用等[2]。
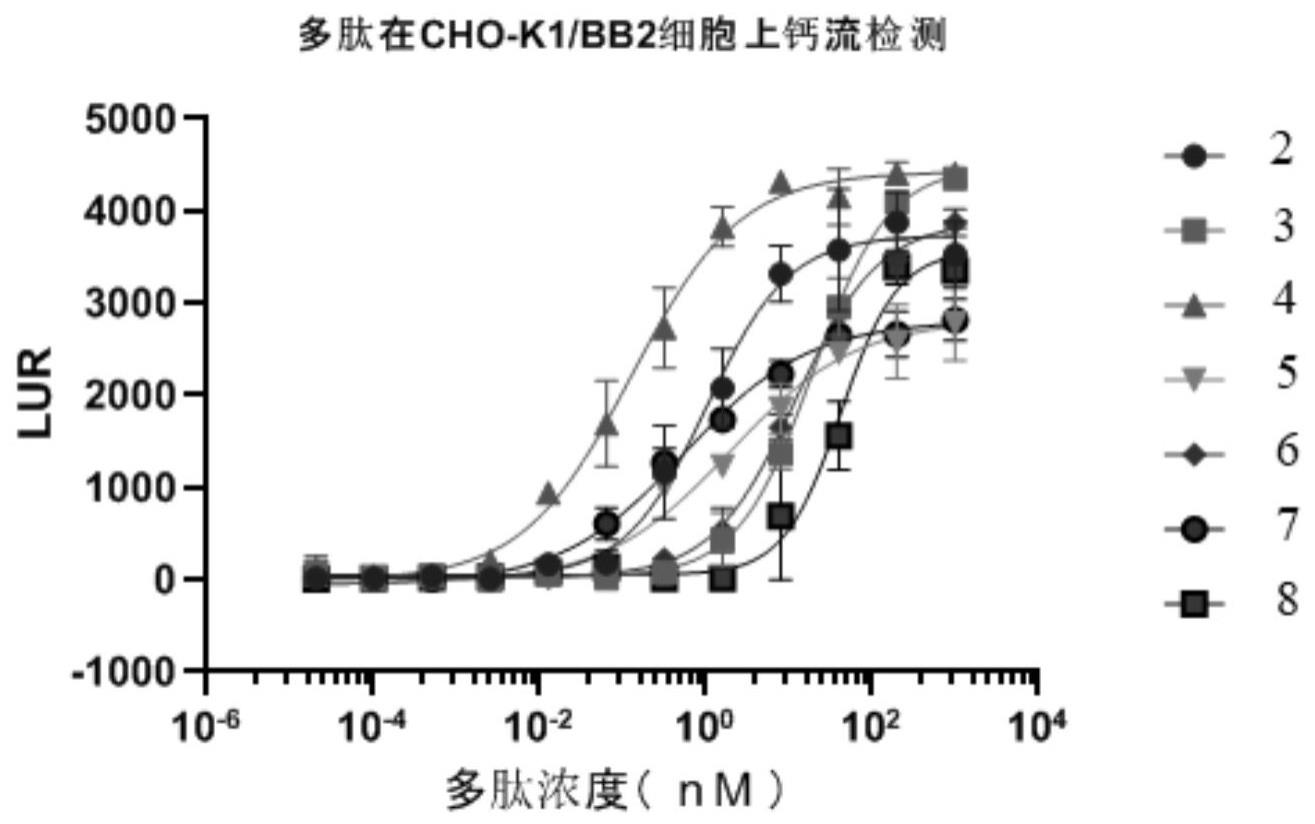
2、grp及其受体广泛地分布于人体胃肠道和中枢神经系统。在胃肠道主要分布于胃窦g细胞、胃黏膜层细胞、胰腺腺泡细胞、平滑肌细胞等[3]。grp及其受体在大脑的分布具有特异性。免疫组化研究表明,在小鼠大脑基底外侧、杏仁核、海马、下丘脑、脑干、孤束核和许多大脑皮质区存在grpr高免疫反应性。重要的是,grpr的表达仅限于神经元的胞体和树突,在轴突和胶质细胞中没有表达[4]。这就表明grpr在大脑内主要参与调节突触传导。大量研究表明,人类和啮齿类动物的正常和肿瘤细胞的grpr与g蛋白中的gq蛋白直接偶联,参与蛋白激酶信号通路,特别是蛋白激酶c(protein kinase c,pkc)/磷脂酶c(phospholipase c,plc)和促分裂原活化蛋白激酶(mitogen-activatedprotein kinase,mapk)/细胞外信号调节蛋白激酶(extracellular signal-regulatedprotein kinase,erk)通路。gpr与grpr结合后激活plc,引起细胞内储存的ca2+释放和细胞外ca2+内流,增加细胞内游离ca2+浓度,激活plc同工酶,引起pkc和mapk的活性增加,最后发挥生物学效应[5]。所以钙流测试是grpr活性检测的重要指标之一。
3、神经退行性疾病(neurodegenerative disease,ndd)是一类发生在神经系统中,造成神经元及其附属树突、轴突和突触,以及遍布神经系统的胶质细胞发生损伤或者功能失常的疾病。世界卫生组织预测,到2040年,神经退行性疾病将会取代癌症,成为人类第二大致死疾病。目前世界范围内还没有任何一种药物能够有效治疗神经退行性疾病。帕金森病(pd)为神经退行性疾病的一种,有关帕金森病的研究发现患者尾状核和苍白球部位的grp同类物,blp(bombesin-like peptides,blp)的浓度显著减少。在阿尔茨海默病患者的成纤维细胞中发现blp密度降低,而且blp引起的ca2+信号有所改变,药理学和基因学方面研究证实grpr还参与调节了其他多种神经和精神疾病的发病机制,比如焦虑症、厌食症和贪食症等。除此之外,grp/grpr系统还参与其他方面的生理作用,比如性功能、痒感觉的调节,更有研究表明grp/grpr对这两种功能的调节来自同一脊柱区域神经元[6]。由此可见,开发活性高并且稳定的grp类肽在治疗神经退行性疾病有着广泛前景。
4、因此,本发明旨在以蛙皮素类似物为基础,通过多肽序列结构改造和性能评估,开发一种具有高亲和力、血浆稳定高和血浆半衰期长的高活性grp激动剂,可以用于开发治疗神经褪变性疾病的新药。
5、引文列表:
6、[1]jensen rt,battey jf,spindel er,et al.international union ofpharmacology.lxviii.mammalian bombesin receptors:nomenclature,distribution,pharmacology,signaling,and functions in normal and disease states[j].pharmacol rev,2008,60(1):1-42.
7、[2]roesler r,schwartsmann g.gastrin-releasing peptide re ceptors inthe central nervous system:role in brain function and as a drug target[j].front endocrinol(lausanne),2012,3:159.
8、[3]fleischmann a,waser b,gebbers jo,et al.gastrin-relea sing peptidereceptors in normal and neoplastic human uterus:involvement of multipletissue compartments[j].j clin endo crinol metab,2005,90(8):4722-4729.
9、[4]roesler r,kent p,luft t,et al.gastrin-releasing peptide receptorsignaling in the integ ration of stress and memory[j].neurobiol learn mem,2014,112:44-52.
10、[5]petronilho f,vuolo f,galant ls,et al.gastrin-releasing peptidereceptor antagonism induces protection from lethal sepsis:involvement oftoll-like receptor 4 signaling[j].mol med,2012,18:1209-1219.
11、[6]roesler r,henriques ja,schwartsmann g.gastrin-releasing peptidereceptor as a molecular target for psychiatric and neurological disorders[j].cns neurol disord drug tar gets,2006,5(2):197-20.
技术实现思路
1、以下仅概况说明本发明的一些方面,并不局限于此。这些方面和其他部分在后面有更完整的说明。本说明书中的所有参考文献通过整体引用与此。当本说明书的公开内容与引用文献有差异时,以本说明书的公开内容为准。
2、本发明的第一方面,提供一种多肽或其药学上可接受的盐,其特征在于,所述多肽的氨基酸序列为任选seq id no:1~seq id no:12氨基酸序列之一或与seq id no:1~seqid no:12具有至少90%序列同一性的氨基酸序列或经修饰的seq id no:1~seq id no:12所示的氨基酸序列的衍生物。
3、在一些实施方式中,所述ser、tyr、x1和x2的构型各自独立的为d型。
4、在一些实施方式中,所述x0为nal或trp;进一步的x1为his或dhis;更进一步的,所述x2为cha、leu、phe或nva。
5、在一些实施方式中,所述经修饰的氨基酸序列的衍生物包括选自以下的一种或更多种修饰:n端和/或c端修饰;以一个或更多个天然和/或非天然氨基酸残基取代一个、二个或更多个氨基酸残基。
6、在一些实施方式中,所述多肽或其药学上可接受的盐,包含与所述多肽seq idno:1~seq id no:13任一的氨基酸序列具有至少60%、65%、70%、75%、80%、85%、90%、93%、94%或95%同一性的氨基酸序列。
7、另一方面,本发明提供了一种多肽,其具有如下之一的结构或所述结构药学上可接受的盐:
8、
9、
10、
11、
12、另一方面,本发明还涉及一种编码所述的多肽分子的一个或多个的多核苷酸分子。
13、在一些实施方案中,所述多核苷酸分子能够编码seq id no.1至seq id no.13的多肽分子的一个或多个的多核苷酸。
14、另一方面,本发明还涉及一种药物组合物,其包含本发明任一所述的多肽或其药学上可接受的盐。
15、在一些实施方案中,本发明所述的药物组合物进一步包含药学上可接受的载体、赋形剂、稀释剂、辅剂和媒介物的至少一种。
16、另一方面,本发明涉及所述的多肽或其药学上可接受的盐或所述的药物组合物在制备用于预防、处理、治疗或减轻神经退行性疾病的药物中的用途。
17、在一些实施方式中,所述所述神经退行性疾病包括脑缺血、脑损伤、癫痫、阿尔茨海默病、帕金森病、亨廷顿病、肌萎缩性侧索硬化、不同类型脊髓小脑共济失调、pick病。
- 还没有人留言评论。精彩留言会获得点赞!