一种检测肿瘤微小核酸标志物的荧光-SERS双模传感器及其制备方法和应用
本发明属于微小核酸类标志物检测,具体涉及一种检测肿瘤微小核酸标志物的荧光-sers双模传感器及其制备方法和应用。
背景技术:
1、肿瘤标志物是指肿瘤细胞发生、增值、转移或复发过程中异常变化的一类物质,可以反映肿瘤的存在和生长情况。微小核酸类标志物(mirna)是常用的一类肿瘤标志物,mirna在正常细胞和肿瘤细胞中存在着广泛的表达差异,其表达水平的分析检测在肿瘤的早期诊断中有着突出的研究价值。因此,准确、快速、灵敏的定量或定性检测核酸标志物对于肿瘤早期的诊断、治疗和发病机制有着非常重要的意义。
2、在检测mirna等生物标志物时,荧光和表面增强拉曼散射(surface-enhancedraman scattering,简称sers)等的光学检测技术由于具有较高的灵敏度和检测效率受到广泛关注。荧光技术具有高分辨率、高选择性以及无创伤等优点,荧光检测工作原理是光谱仪产生一种有特定频率的辐射,称为“激发源”,这种辐射能量传递到被检测的物质,物质中的荧光分子在受到足够的能量吸收之后,发出荧光信号,光谱仪可以检测整个荧光信号的频率和强度,用来检测复杂混合物中的微量成分。sers技术因出色的灵敏度、固有的化学指纹信息等优点,是一种极具潜力的分子检测技术。sers技术是利用金属结构表面的增强效应,分子吸附在金属胶体纳米颗粒或粗糙的金属表面上时会经历更高的散射效率,因此待测分子的拉曼信号会放大百万倍甚至更高,从而实现高灵敏度检测的光学检测技术。目前已有广泛的研究证实了sers技术在mirna检测中的可行性。
3、但是,当前sers技术在mirna检测中通常采用单一检测模式,单一检测模式容易受到复杂的实验条件的干扰,产生假阳性或假阴性信号的机会增加,且灵敏度也会受到影响。
技术实现思路
1、为了克服上述现有技术的缺点,本发明的目的在于提供一种检测肿瘤微小核酸标志物的荧光-sers双模传感器及其制备方法和应用,以解决现有的单一检测模式的检测灵敏度低以及易出现假阳性或假阴性的问题。
2、为了达到上述目的,本发明采用以下技术方案予以实现:
3、本发明公开的一种检测肿瘤微小核酸标志物的荧光-sers双模传感器,所述荧光-sers双模传感器包括sers检测芯片和荧光-sers双功能标签;
4、所述sers检测芯片为表面特异性抗体修饰的金纳米颗粒组装结构sers基底;
5、所述荧光-sers双功能标签为表面修饰有能识别目标核酸的dna单链h1、与dna单链h1互补并标记有荧光探针分子cy5的dna单链h2、拉曼探针分子的金纳米颗粒。
6、优选地,所述特异性抗体修饰采用抗dna-rna杂交单克隆抗体s9.6修饰,能高特异性地识别dna-rna杂合双链结构,不识别单链或dna双链。
7、优选地,所述sers基底为界面自组装方法制备的有序致密排列的金纳米颗粒单层膜结构;
8、优选地,所述dna单链h1和dna单链h2的序列根据目标核酸的序列变化而进行合成设计;
9、进一步优选地,所述单链h1的碱基序列如seq id no:1所示,具体为:
10、5’-tcaacatcagtctgataagctattttttttt-(ch2)6-sh-3’;
11、进一步优选地,所述dna单链h2的碱基序列如seq id no:2所示,具体为:5’-cy5-tag ctt atc aga-3’;
12、进一步优选地,所述目标mirna-21(t)的核酸碱基序列如seq id no:3所示,具体为:5’-uag cuu auc aga cug aug uuga-3’。
13、优选地,所述拉曼探针分子为在拉曼静默区(1800~2800cm-1)处存在特征峰的拉曼分子。
14、进一步优选地,所述拉曼探针分子包括但不限于4-巯基苯甲腈、普鲁士蓝、聚二乙炔等。
15、本发明还公开了上述的检测肿瘤微小核酸标志物的荧光-sers双模传感器的制备方法,包括以下步骤:
16、步骤一:sers检测芯片的制备:
17、1)通过种子介导的生长方法合成十六烷基三甲基溴化铵(ctab)修饰的金纳米颗粒;
18、2)然后在快速搅拌的条件下加入聚乙烯吡咯烷酮(pvp)乙醇溶液混合共培养,乙醇洗一次后浓缩10倍将沉淀分散到乙醇中,从而将金纳米颗粒的配体ctab替换为pvp;
19、3)随后将pvp修饰的金纳米颗粒在二氯甲烷和水混合溶液中剧烈搅拌,转移到疏水的聚四氟乙烯样品槽后添加正己烷,待正己烷挥发后,用硅片捞出组装在界面上的有序致密排列的金纳米颗粒单层膜;
20、4)在金纳米单层膜表面修饰巯基乙酸并用enc/nhs活化其上的羧基,接着在37℃下高湿度孵育s9.6抗体,最后浸泡乙醇胺以阻断非特异性结合,得到sers检测芯片。
21、步骤二:荧光-sers双功能标签的制备
22、1)采用柠檬酸钠还原法制备金纳米颗粒;
23、2)将dna单链h1与dna单链h2退火处理形成h1-h2双链,随后将h1-h2双链与tcep溶液混合以还原巯基被空气氧化形成的二硫键,之后将h1-h2双链与金纳米颗粒混合并共培养,h1-h2双链通过巯基与金形成au-s键修饰在金纳米颗粒表面;
24、3)加入拉曼探针分子共培养,最后得到荧光-sers双功能标签。
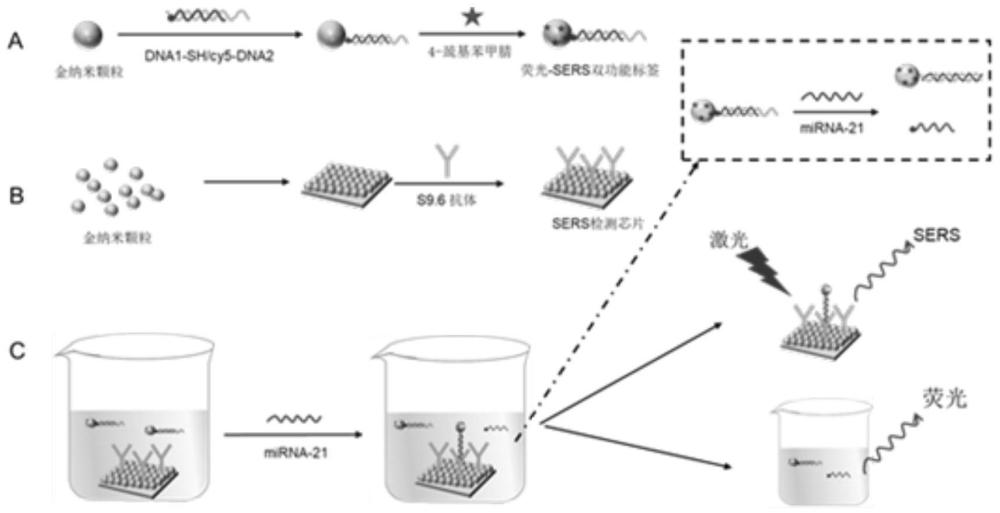
25、步骤三:使用时,在肿瘤微小核酸标志物存在的情况下,先加入荧光-sers双功能标签共同培养,然后加入sers检测芯片,反应后分别进行荧光和sers检测,发挥荧光-sers双模传感器作用。
26、其中,在肿瘤微小核酸标志物存在的情况下,荧光-sers双功能标签上的dna单链h2被该核酸标志物t通过粘性末端介导的链置换反应取代,使得dna单链h1与t形成h1-t双链;将上述溶液加入sers检测芯片后,s9.6抗体高特异性地识别h1-t双链结构,因此将带有拉曼探针分子信号的sers标签结合到sers基底上,形成三明治结构,使得拉曼探针分子的sers信号增强,sers检测可以通过检测拉曼探针分子的sers强度值来实现;将上述溶液离心,其上清液含有被取代下来的dna单链h2,cy5靠近金纳米颗粒被猝灭的荧光信号由于脱离金纳米颗粒而得以恢复,荧光检测可以通过检测cy5的荧光信号来实现。
27、本发明还公开了上述检测肿瘤微小核酸标志物的荧光-sers双模传感器用于检测mirna-21的应用。
28、优选地,使用时:将荧光-sers双功能标签与含有不同浓度的目标mirna-21的样品溶液共培养;得到的混合样品离心浓缩后,将其加入sers检测芯片,清洗后进行sers检测,得到不同浓度目标mirna-21共培养后芯片的sers光谱及相应拉曼探针分子特征峰的sers强度值,以目标mirna-21浓度的对数为横坐标,拉曼探针分子特征峰的sers强度值为纵坐标,做出sers传感的工作曲线,根据工作曲线计算传感器的sers传感检出限。
29、取混合样品离心后的上清液进行荧光检测,得到不同浓度目标mirna-21的荧光光谱,以目标mirna-21浓度的对数为横坐标,cy5的荧光强度为纵坐标,做出荧光传感的工作曲线,根据工作曲线计算传感器的荧光传感检出限。
30、与现有技术相比,本发明具有以下有益效果:
31、本发明公开的检测肿瘤微小核酸标志物的荧光-sers双模传感器,结合自组装结构的sers检测芯片和荧光-sers双功能标签,形成荧光-sers双模式检测,结合了两个信号的优点,可以相互检测形成协同验证的检测策略,因而能够提高传感器的灵敏度和可靠性。具体优势体现在:
32、1、灵敏度高,本发明采用具有高灵敏度的sers方法,通过制备自组装贵金属纳米间隙单层膜结构,获得均匀分布的“热点”区域,同时提高检测的灵敏度和均匀性;
33、2、特异性强,本发明是基于核酸分子之间碱基互补配对原则而构建的生物传感器,待测液中的干扰物质并不能与dna单链h1结合,dna单链h1与dna单链h2的双链结构不能被打开,因此干扰物质无法和信号单元中的dna单链h1杂交,也就不能产生sers信号,dna单链h2没有游离出来,也就不能产生荧光信号;
34、3、抗干扰性强,所选拉曼探针分子在1800~2800cm-1处存在特征信号峰,是生物分子拉曼静默区,也可避免与其他拉曼分子或荧光分子的信号产生干扰;
35、4、准确性高,本发明通过将sers方法与荧光光谱技术结合,形成协同验证的双模态检测策略,提升检测的准确性,因此能够有效解决现有的单一检测模式的检测灵敏度低以及易出现假阳性或假阴性的问题;
36、5、具有普适性,只需针对目标mirna的序列,变更相应的h1、h2序列,即可实现对不同种mirna的检测。
- 还没有人留言评论。精彩留言会获得点赞!