抗-PD-L1抗体及变异体的制作方法
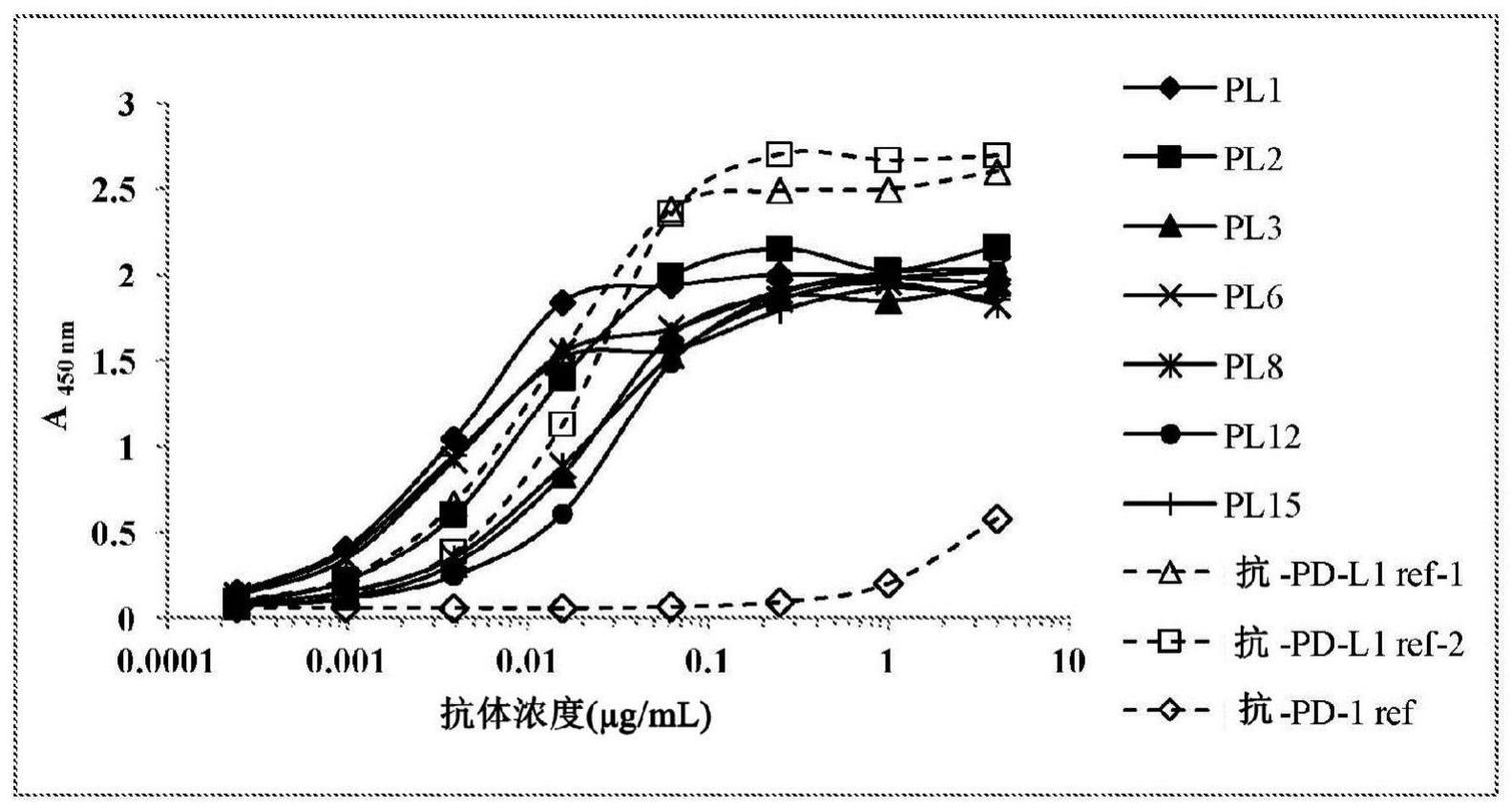
所属熟知的技术可应用于本文所提供的经标记的抗体(或其片段)。这些技术包括,但不限于,双功能性偶联剂的使用(参照,美国专利第5,756,065号;第5,714,631号;第5,696,239号;第5,652,361号;第5,505,931号;第5,489,425号;第5,435,990号;第5,428,139号;第5,342,604号;第5,274,119号;第4,994,560号;及第5,808,003号)。替代地,或额外地,可测量细胞中编码pd-l1多肽的核酸或mrna,例如,经由荧光原位杂交使用相应于编码pd-l1的核酸或其互补物的核酸系探针;(fish;参照世界专利wo98/45479,公开于1998年10月),southern印迹杂交、northern印迹杂交、或聚合酶链式反应(pcr)技术,如实时定量pcr(rt-pcr)。亦可基于抗体的分析通过测量如血清的生物液中的流出抗原而研究pd-l1过度表达(亦参照,例如,于1990年6月12日授权的美国专利第4,933,294号;1991年4月18日公开的世界专利案wo 91/05264;1995年3月28日授权的美国专利第5,401,638号;以及sias et al.,j.immunol.methods 132:73-80(1990))。除上述检测,所述中具有通常知识的人可采用多种活体内及离体的检测。例如,可于哺乳动物体内将细胞暴露于视需要被可检测物标记的抗体,例如,放射活性同位素,以及抗体对细胞的结合予以评估,例如通过外部扫描或分析从预先暴露于抗体的哺乳动物采集的样品(例如,生物切片或其他生物样品)的放射活性。制品及试剂盒本文所提供的另一具体实施例为含有用于治疗癌症的材料的制品,该癌如黑色素瘤、nsclc、头颈癌、泌尿上皮癌、乳腺癌(例如,三阴性乳腺癌,tnbc)、胃癌、典型何杰金氏淋巴瘤(chl)、非何杰金氏淋巴瘤原发性纵膈b细胞淋巴瘤(nhl pmbcl)、间皮瘤、卵巢癌、肺癌(例如,小细胞肺癌)、食道癌、鼻咽癌(npc)、胆管癌、直肠癌、子宫颈癌、甲状腺癌及唾液腺癌。制品可包含容器及容器上或容器内的标签或插页。合适的容器包括,例如,瓶、小瓶、注射器等。容器可由各种材料制成,如玻璃或塑料。一般而言,容器装有有效于治疗症状的组合物且可具有无菌入口部分(例如,容器可为静脉内溶液袋或具有通过皮下注射针可刺穿的瓶塞的小瓶)。组合物中至少一种活性剂为本文所提供的抗-pd-l1抗体及/或其变异体或突变体(或其片段)。标签或插页指示组合物是使用于治疗特定症状。标签或插页将进一步包含用于给药抗体组合物治疗患者的指引。亦涵盖包含本文所揭示的组合疗法的制品和试剂盒。插页意思指包括于治疗产品的商用包装的客制化指引,其含有关于使用所述治疗产品相关的适应症、用法、剂量、投药、限制及/或警语的信息。一具体实施例中,插页指示组合物用于治疗癌(如头颈癌、肺癌或直肠癌)。此外,制品可进一步包含第二容器,其包含医药可接受缓冲剂,如用于注射的抑菌水(bwfi)、磷酸盐缓冲生理盐水、林格氏液及聚葡萄糖溶液。其可进一步包括商业及使用者所需要的其他材料,包括其他缓冲液、稀释剂、滤器、针及注射器。亦可提供实现各种目的的试剂盒,例如,用于患者分离或检测pd-l1,视需要地与制品组合。对于pd-l1的分离及纯化,试剂盒可含有经偶合至珠粒(例如,sepharosetm珠粒)的本发明所提供的抗-pd-l1抗体及/或提变异体或突变体(或其片段)。可提供含有用于活体外检测及定量pd-l1的抗体(或其片段)的试剂盒其,例如于elisa或蛋白质印迹法中。如同制品,试剂盒包含容器及容器上或容器内的标签或插页。例如,容器容纳组合物,其包含本文所提供的至少一种抗-pd-l1抗体及或其变异体或突变体(或其片段)。额外的容器可包括含有,例如,稀释剂及缓冲剂、对照抗体。标签或插页可提供组合物的内容以及意图使用于活体外或诊断用途的指引。【实施例】实施例1人类抗-pd-l1抗体及变异体的开发对于抗-pd-l1抗体的开发,完整的方案总结如下所述:7个阳性先导物(lead)(亦即,pl1、pl2、pl3、pl6、pl8、pl12、pl15)由人类噬菌体展示库利用人类pd-l1_ecd-his筛选而鉴定。一般而言,以生物素化的经偶合至经链霉亲合素包被的磁性m-280(thermo fisher scientific#11205d)的人类pd-l1_ecd-his筛选三次后,经由elisa测量筛选先导物的fab对于hpd-l1_ecd-fc及hpd-l1_ecd-his的结合,然后七个经选择的先导物的fab序列克隆至人类igg1 fc骨架的n297a突变体以成为全长抗体,使用该抗体进行更多试验以测定动力学特征、全细胞pd-l1结合活性、pd-l1阻断活性、活体外及活体内功能。基于所有数据,相较于其他经选择的先导物,发现pl2及pl3具有优异的抗-肿瘤活性,且它们的亲和性进一步通过制造pl2及pl3的噬菌体展示库优化以及对活体外亲和性成熟进行至少三次筛选。然后鉴定出具有增强的亲和性的pl2及pl3所衍生的变异体(亦即,pl2#3及pl3#7),接着以与选择抗体先导物的非常类似的过程证实其活性及功能性。应注意的是于此阶段,同时制备不同的igg同型体的变异体(亦即,igg1、mtigg1(n297a)、igg2、igg4)以及同时比较经与各种fc骨架接合的一组pl2#3及pl3#7的亲和性及活体内与活体外的功效。除了肿瘤/抗原-特异性t细胞异种移植模型(tumor/antigen-specific t cell xenograftmodel),亦使用hpd-1敲入模型(hpd-1 knock-in model)证实pl2#3及pl3#7的功效,以及数据显示该二者皆与抗-pd-l1参照抗体可相比较。为了进一步改良pl3#7的亲和性,如之前方式制备基于pl3#7的另一噬菌体展示库用于亲和性成熟。通过这些过程,三个新颖的变异体(亦即,pl3#7-19、-43、-54)被鉴定且被使用于比较它们与pl2顶级变异体pl2#3的功效。详细的比较数据描述于本文下述实施例。此处,七个经选择的先导物的结合亲和性及动力学(ka、kd及kd)使用表面等离子共振(spr)测量且显示于表4。抗-人类igg fc首先固定至感测芯片,然后捕捉抗-pd-l1参照抗体以及该抗-pd-l1抗体先导物:pl1、pl2、pl3、pl6、pl8、pl12、及pl15,rmax约250ru。试验于25℃进行,以及测量以下述方法进行:以hpd-l1_ecd-his自55.4nm至11.1nm的梯度稀释物,以流速25μl/min通过含有捕捉的抗体且补充有0.1%(w/v)bsa的hbs-p+缓冲液。所有数据利用评估软件分析以及曲线符合1∶1 langmuir结合模型。数据表示二次重复进行的二个独立的试验。表4 ref-1 pl1 pl2 pl3 pl6 pl8 pl12 pl15 ka(1/ms) 1.45e+05 2.91e+05 4.38e+05 3.48e+05 1.05e+06 3.82e+05 4.16e+05 6.45e+05 kd(1/s) 1.29e-03 4.53e-03 3.90e-03 4.10e-03 1.22e-02 3.48e-03 2.67e-03 9.33e-03 <![cdata[k<sub>d</sub>(m)]]> 9.79e-09 1.58e-08 8.72e-09 1.19e-08 1.12e-08 8.85e-09 6.68e-09 1.50e-08 经选择的抗-pd-l1抗体先导物:pl1、pl2、pl3、pl6、pl8、pl12、及pl15的轻链(lc)及重链(hc)的氨基酸序列比对系示于第1a-1b图。该等先导物的lc及hc中的互补决定区(cdr)用粗体及下加底线文字标示。实施例2抗体pl2的抗-pd-l1变异体的结合亲和性与动力学抗体先导物pl22使用活体外噬菌体展示为基础的亲和性成熟试验,以产生具有改良的结合表现的额外的克隆(clone)。首先,cdr-l1/cdr-l3/cdr-h3(着重于3个cdr)核酸库经由pcr产生、克隆至噬菌体展示载体,然后转化为大肠杆菌tg1或ss320细胞以产生噬菌体库。以偶合至链霉亲合素包被的磁性m-280(thermo fisher scientific#11205d)的生物素化hpd-l1-his筛选三次后,经由elisa筛选40个fab克隆,并发现四个fab(亦即,#3、#4、#5、及#39)较亲代pl2具有较佳结合表现。进一步的动力学特征通过表面等离子共振(spr)使用pl2#3、pl2#4、pl2#5、及pl2#39的全长igg进行测量,且发现具有相当于或较佳于pd-l1参照抗体的结合表现。下文表5显示于l1(分别为seq id nos 36,65,94,36与100,依照出现顺序)、l3(分别为seq id nos 45,71,95,98与95,依照出现顺序)及h3区(分别为seq id nos 60,77,96,99与101,依照出现顺序)具有突变的pl2变异体的氨基酸序列。表5使用表面等离子共振(spr)测量结合亲和性及动力学。抗-人类igg fc首先固定于感测芯片,然后捕捉抗-pd-l1参照抗体以及pl2变异体,rmax约250ru。试验于25℃进行,以及测量以hpd-l1-his自19.1nm至0.71nm的梯度稀释物,以流速25μl/min通过补充有0.1%(w/v)bsa的含有捕捉的抗体的hbs-p+缓冲液来做出。所有数据利用评估软件分析以及曲线符合1∶1 langmuir结合模型。所有数据表示重复二次的二个独立的试验。表6显示结合动力学与解离动力学,以及由表面等离子共振(spr)所测量的pl2变异体相较于抗-pd-l1参照抗体的计算亲和性(kd)。此研究中,所有变异体、亲代pl2以及参照抗体克隆至人类igg2骨架。相对于参照抗-pd-1抗体,对于pl2变异体的亲和性的改良显示于表6。表6所呈现的数据显示,pl2变异体中,pl2#3对于人类pd-l1-his具有最佳结合亲和性。表7显示于后续研究中着重于pl2#3的不同人类igg同型体的动力学的比较的结果。此处,pl2#3的不同的同型体对于人类pd-l1-his显示类似的结合亲和性。表6 平均(n=2) ka[1/(m·s)] kd[1/s] <![cdata[k<sub>d</sub>[m]]]> 相对于ref-1的改良 抗-pd-l1 ref-1(igg2) 2.47e+05 2.48e-03 8.41e-09 1.00 抗-pd-l1 ref-2(igg2) 1.24e+06 9.88e-04 9.07e-10 pl2 igg2 7.47e+05 2.17e-03 6.96e-09 1.21 pl2#3igg2 1.32e+06 5.57e-04 5.16e-10 16.30 pl2#4igg2 8.82e+05 9.90e-04 1.27e-09 6.62 pl2#5igg2 8.12e+05 2.21e-03 3.07e-09 2.74 表7 平均(n=2) ka[1/(m·s)] kd[1/s] <![cdata[k<sub>d</sub>[m]]]> 相对于ref-1的改良 抗-pd-l1 ref-1(mtigg1) 7.90e+05 5.05e-04 6.32e-10 1.00 抗-pd-l1 ref-2(igg2) 1.18e+06 2.68e-04 2.37e-10 pl2 igg1 1.25e+06 1.93e-03 1.56e-09 0.41 pl2#3 igg1 1.14e+06 2.76e-04 2.50e-10 2.53 pl2#3 mtigg1(n297a) 1.33e+06 2.86e-04 2.21e-10 2.86 pl2#3 igg2 1.34e+06 1.62e-04 1.18e-10 5.36 pl2#3 igg4 1.26e+06 2.93e-04 2.39e-10 2.64 实施例3抗体pl3的抗-pd-l1变异体的结合亲和性与动力学抗体先导物pl3使用于活体外噬菌体展示为基础的亲和性成熟试验以制造具有改良的结合表现的额外克隆。首先,cdr-l1/cdr-l2/cdr-l3/cdr-h1/cdr-h2/cdr-h3(着重于6个cdr)核酸库由pcr产生、克隆至噬菌体展示载体,然后转化为大肠杆菌tg1或ss320细胞以产生噬菌体库。以偶合至经链霉亲合素包被的磁性m-280(thermo fisherscientific#11205d)的生物素化hpd-l1-his筛选三次后,经由elisa筛选20个fab克隆,并发现二个fab(亦即,#1及#7)较亲代pl3具有较佳结合表现。进一步的动力学特征由表面等离子共振(spr)使用pl3#1及pl3#7的全长igg进行测量,且发现具有相当于或较佳于pd-l1参照抗体的结合表现。下文表8显示于l2、l3及h1、h3区具有突变的pl3变异体的氨基酸序列。表9显示结合动力学与解离动力学,以及由表面电浆共振(spr)所测量的pl3变异体相较于抗-pd-l1参照抗体的计算亲和性(kd)。此结果亦显示p3#1及pl3#7的不同人类igg同型体中的动力学比较。相对于参照抗-pd-l1抗体,对于pl3变异体的亲和性改良显示于表9。所有数据表示重复二次进行的二个独立的试验。这些数据显示,pl3变异体中,pl3#7对于人类pd-l1-his具有稍微较佳的结合亲和性。pl3#7的不同同型体对于人类pd-l1-his显示类似的结合亲和性。l1序列分别为seq idnos 120,120与120,依照出现顺序。l2序列分别为seq id nos 121,122与121依照出现顺序。l3序列分别为seq id nos 123,124与125,依照出现顺序。h1序列分别为seq id nos53,108,与75,依照出现顺序。h2序列分别为seq id nos 126,126与126,依照出现顺序。h3序列分别为seq id nos 61,109与78,依照出现顺序。表8表9克隆pl3#7,其具有远优于亲代pl3的亲和性,进一步使用于活体外噬菌体展示为基础的亲和性成熟试验以制得具有改良的结合表现的额外克隆。首先,cdr-l1/cdr-l2/cdr-l3/cdr-h2/cdr-h3(着重于5个cdr)核酸库由pcr制备、克隆至噬菌体展示载体,然后转化为大肠杆菌tg1或ss320细胞以产生噬菌体库。以偶合至经链霉亲合素包被的磁性m-280(thermo fisher scientific#11205d)的生物素化hpd-l1-his筛选三次后,经由elisa筛选57个fab克隆,以及发现三个fab(亦即,19、43及54)较亲代pl3#7具有较佳结合表现。进一步的动力学特征由生物层干涉技术方案(bio-layer interferometryapproach)(fortebio octet red 96)使用pl3#7-19、pl3#7-43及pl3#7-54的全长igg进行测量,且发现具有相当于或较佳于pd-l1参照抗体的结合表现。下文表10显示于l1(分别为seq id nos 120,127,128与129,依照出现顺序)、l2(分别为seq id nos 121,130,131与132,依照出现顺序)、l3(分别为seq id nos 125,133,134与125,依照出现顺序)及h2(分别为seq id nos 126,126,126与135,依照出现顺序)、h3(分别为seq id nos 78,79,80与80,依照出现顺序)需具有突变的pl3#7变异体的氨基酸序列。h1序列分别揭示为seq id nos 75,75,75与75,依照出现顺序。表10pl3#7变异体的亲和性及动力学由生物层干涉技术方案使用octet red96(fortebio)系统利用链霉亲合素(sa)传感器于25℃且于1000rpm的振荡速度测量。简明地,黑色96-孔盘(plate)以含有200μl/孔的用于亲和性测定所需要的试剂的柱来制备。一般而言,首先将octet sa传感器置于含有1×动力学缓冲液(kinetics buffer)(pbs、0.1%bsa、0.02%tween-20,ph 7.4)的孔180秒以建立基线。然后将传感器转移至含有10μg/ml生物素化pl3#7变异体(抗体:生物素之1∶1比例,利用ez-nhs-peg4-生物素,thermo fisherscientific#21329)的孔300秒以负载sa被覆尖端。然后传感器于再生缓冲液(regeneration buffer)(10mm甘氨酸,ph 1.5)中培养3×5秒,每次于1×动力学缓冲液中培养5秒来再生。再生于每次结合/解离循环的测量前重复。然后将传感器置于新鲜的1×动力学缓冲液持续180秒以建立基线。然后传感器于含有hpd-l1-his的孔中培养5分钟测量结合,接着转移至含有1×动力学缓冲液的孔持续10分钟,以测量解离。动力学(ka、kd及kd)由自hpd-l1_ecd-his从38.28nm至1.42nm(对于一浓度的一结合/解离循环)的1∶3梯度稀释物以1∶1 langmuir结合模型所获得数据的整体拟合(global fitting)四次结合/解离循环所测量。所有数据利用octet数据分析软件版本9.0分析以及表示重复两次进行的二个独立的试验。表11显示结合及解离动力学,与使用生物层干涉技术方案由fortebio octetred96(menlo park,ca,usa)机器所测量的pl3#7变异体相较于参照抗-pd-l1抗体的计算亲和性。相对于参照抗-pd-l1抗体的pl3#7变异体的亲和性的改良显示于表11。所有数据表示重复两次进行的二个独立的试验。显示于表11的数据显示pl3#7-19、pl3#7-43及pl3#7-54相较于亲代pl3#7具有较佳的结合亲和性。表11 平均(n=2) ka[1/(m·s)] kd[1/s] <![cdata[k<sub>d</sub>[m]]]> 相对于ref-1的改良 抗-pd-l1 ref-1(mtigg1) 2.07e+05 5.37e-04 2.46e-09 1.00 抗-pd-l1 ref-2(igg2) 2.91e+05 1.54e-04 5.20e-10 pl2#3 mtigg1 2.21e+05 5.61e-04 2.46e-09 1.00 pl3#7 mtigg1 2.98e+05 3.05e-04 1.09e-09 2.26 pl3#7-19 mtigg1 4.19e+05 2.01e-04 5.38e-10 4.57 pl3#7-43 mtigg1 3.30e+05 1.03e-04 3.13e-10 7.86 pl3#7-54 mtigg1 3.07e+05 2.28e-04 7.72e-10 3.19 因此,具有优异的较高亲和性以及优异功能性活性的pl2顶级变异体(pl2#3)、pl3顶变异体(pl3#7)以及pl3#7顶变异体(pl3#7-19、-43、-54)由活体外噬菌体展示为基础的亲和性成熟试验制备。一般而言,使用经偶合至经链霉亲合素包被的磁性m-280的生物素化hpd-l1-his进行三次筛选。顶级变异体的fab经由elisa筛选且经克隆至人类igg1 fc骨架的n297a突变体以成为全长抗体。该等抗-pd-l1顶变异体的轻链(lc)及重链(hc)的氨基酸序列比对显示于第11a-11b图。所述抗-pd-l1顶变异体的lc及hc中的互补决定区(cdr)标示为粗体及下加底线文字。实施例4抗-pd-l1抗体结合至重组人类pd-l1/fc融合蛋白质与经活化的cd3+t细胞进行elisa检测以评估经选择的抗体对重组人类pd-l1/fc融合蛋白质的结合。每孔15ng的人类pd-l1/fc蛋白质被覆于96-孔eia微孔盘于4℃隔夜。以5%脱脂乳阻断后,添加经梯度稀释的抗体且于室温培养1小时。移除未结合的抗体且以pbst将孔清洗二次。对孔添加hrp--偶联的二次抗体,以及接着培养,洗除过剩的二次抗体。对孔添加tmb,以及接着培养,终止反应,且hrp活性由监测于450nm吸收的增加来测量。人类t细胞系使用magnisorttm人类t细胞富含试剂盒(ebioscience)自pbmc分离。经分离的t细胞由5μg/ml的植物血凝素(phytohemagglutinin,pha)活化3日以刺激pd-l1表达。收集经活化的t细胞且培养于具有人类fc阻断剂(ebioscience)的facs缓冲液(具有2%fbs的pbs)中,于4℃20分钟。通过于facs缓冲液中培养经活化t细胞与经梯度稀释的抗体来评估抗-pd-l1单克隆抗体的结合。细胞以流动缓冲液清洗且结合以经fitc标记的兔抗-人类igg fcγ抗体检测。细胞以针对闸控(gating)cd3-阳性t细胞的小鼠抗-人类cd3pe-cy7(ebioscience)来染色。使用cytomics fc500(beckmen coulter公司)进行流式细胞分析。因此,经选择的抗-pd-l1抗体由elisa测试其对重组人类pd-l1蛋白质的结合以及通过流式细胞仪测试其对活化cd3+t细胞的结合。抗-pd-l1参照及抗-pd-l1参照抗体分别使用作为阳性及阴性对照。第2a及2b图显示所有经选择的抗-pd-l1抗体可结合人类pd-l1重组蛋白质及表达pd-l1的t细胞。实施例5通过抗-pd-l1抗体阻断pd-1结合至pd-l1表达pd-l1的cho-s细胞悬浮于facs缓冲液(具有4%fbs的pbs)。添加各种浓度的测试抗体至细胞悬浮物(3.5e5细胞/孔)且于4℃培养30分钟。洗除未结合抗体且添加经生物素标记的pd-1-fc融合蛋白质,于4℃培养30分钟。清洗细胞后以链霉亲合素-pe于4℃染色30分钟。使用cytomics fc500(beckmen coulter公司)进行流式细胞分析。经选择的抗-pd-l1抗体使用流式细胞术检定测试其阻断pd-1至表达pd-l1的cho-s细胞的结合的能力。抗-pd-l1参照抗体及阿瓦斯汀(avastin)分别使用作为阳性及阴性对照。显示于第3图的数据显示当通过染色的平均荧光强度(mean fluorescent intensity,mfi)测量时,所有经选择的抗-pd-l1单克隆抗体阻断pd-1对经pd-l1转染的cho-s细胞的结合。实施例6抗-pd-l1抗体于混合白细胞反应(mixed leukocyte reaction,mlr)中对于细胞因子产生及t细胞增殖的效果应用混合白细胞反应以显现阻断pd-l1/pd-1途径对于淋巴球效应子细胞的效果。检测中的t细胞测试于抗-pd-l1抗体的存在或不存在下的增殖及ifn-γ或il-23分泌。人类t细胞使用lympho-kwik t(one lamda公司)自pbmc纯化。经分离的t细胞悬浮于pbs且以1μm的cfse于室温标记10分钟。以完全培养基(具有10%fbs的rpmi-1640)清洗细胞后,经cfse标记的t细胞以1e6细胞/ml的浓度悬浮于完全培养基。异体树状细胞自pbmc制备。经分离的pbmc与200u/ml的重组人类il-3(ebioscience)培养过夜,使得单核细胞/巨噬细胞群附在盘上。移除未贴附细胞,盘以完全培养基清洗二次。然后盘上细胞于含有200u/ml的人类il-4(ebioscience)及200u/ml的人类gm/csf(ebioscience)的完全培养基中培养6日。于第6日添加tnf-α(100u/ml)至培养物且培养过夜,测量单核细胞衍生的树状细胞。成熟的dc经胰蛋白处理,收集且以1e5细胞/ml的浓度悬浮于完全培养基。每个反应含有10e5经cfse标记的t细胞及10e4异体树状细胞,总体积为200μl。各培养物中添加不同浓度的抗体。无抗体或抗-vegf抗体(avastin)作为阴性对照。抗-pd-1参照或抗-pd-l1参照抗体作为阳性对照。细胞于37℃培养5日。于第5日,由各培养物取100μl培养基进行细胞因子测量。细胞因子的水平使用人类ifn-γ或il-2elisamaxtm deluxe试剂盒(biolegend)测量。收集细胞并通过流式细胞术分析t细胞增殖。显示于第4a-4b图的数据指示所有经选择的抗-pd-l1抗体于混合白细胞反应检测中,增强ifn-γ分泌以及促进t细胞增殖。抗-pd-l1及抗-pd-1参照抗体作为阳性对照。阿瓦斯汀(抗-vegf)作为阴性对照。第4a图显示tfn-γ分泌的条状图,以及第4b图显示于抗体的指定浓度的cd3+t细胞增殖的条状图。再者,于mlr中通过抗-pd-l1抗体pl2亲代及变异体所诱发的il-2分泌显示于第6a图,以及mlr中于指定浓度的抗-pd-l1抗体pl3亲代抗体及变异体所诱发的il-2分泌显示于第6b图。所述数据指示经选择的pl2变异体pl2-3/3(pl2#3)及pl3变异体(pl3#7)相较于亲代抗体对刺激t细胞活化显示优异的功效。此外,于混合白细胞反应(mlr)中的抗-pd-l1抗体pl2#3、pl3#7及pl3#7变异体的不同igg型的功效显示于第8a-8d图以及第12a-12b图。显示由所述抗-pd-11抗体所诱发的ifn-γ及il-2分泌的条状图呈现于第8a、8b及12a图。第8c图显示于各种浓度的抗-pd-l1抗体pl2#3、pl3#7的cd4+t细胞增殖的条状图,以及第8d及12b图显示于指定浓度的所述三种抗-pd-l1抗体的cd8+t细胞增殖的条状图。第12a及12b图特别指示抗-pd-l1抗体pl3#7变异体,例如,pl3#7-19、-43及-54,于ifn-γ分泌及cd8+t细胞增殖的增强显示优异活性。实施例7pl2及pl3抗-pd-l1抗体于a375/抗原-特异性t细胞异种移植模型中的肿瘤生长抑制抗-人类pd-l1抗体的活体内活性通过免疫受损的nod/scid(非肥胖糖尿病/严重合并免疫缺陷)小鼠于异种移植小鼠模型中研究。小鼠皮下植入表达人类pd-l1及人类pbmc或抗原-特异性t细胞的人类癌细胞株。对小鼠以人类黑色素瘤细胞株a375或人类nsclc细胞株nci-h292给予抗体的腹腔剂量。抗体的效果于肿瘤生长至2000mm3肿瘤体积或显著的肿瘤坏死进行观察。为了制造抗原-特异性t细胞,使用人类t细胞富集试剂盒(ebioscience)由健康捐赠者的pbmc分离t细胞。经分离的t细胞系与经丝裂霉素-c处理的a375细胞与rhil-2(50iu/ml)共培养10至14日以富集抗原-特异性t细胞。人类pbmc使用-0177(sigma-aldrich)自健康捐赠者的全血分离。a375及抗原-特异性t细胞以指定的效应子-对-目标(e∶t)比例于皮下给药前即刻混合。nci-h292细胞以指定的e:t比例与新鲜的人类pbmc混合且皮下接种至小鼠。测试物的第1剂量系于癌/效应子细胞的植入后2小时腹腔给药。小鼠以抗体每周处理二次持续3至5周。每周二次观察各个动物的肿瘤的形成。肿瘤由卡尺测量;肿瘤体积(v)使用下式计算:v(mm3)=0.5(长度(mm)×宽度(mm)×宽度(mm)/2)小鼠(n=4/群)以人类黑色素细胞株a375及抗原-特异性t细胞的混合物(t细胞∶癌细胞=1∶100)皮下植入。测试抗体自第0日每周二次腹腔注射至小鼠。于a375/抗原-特异性t细胞异种移植模型中测试所有抗-pd-l1先导物的活体内功效。经pl2及pl3处理的小鼠的肿瘤生长曲线显示于第5a及5b图。数据显示pl2及pl3于活体内显著地抑制a375肿瘤生长。再者,抗pd-l1抗体pl2及pl3顶级变异体于a375/抗原-特异性t细胞异种移植模型中的肿瘤生长抑制活性显示于第7a及7b图。数据指示pl2#3igg2于剂量30mg/kg及10mg/kg抑制a375肿瘤生长。pl3#7igg2仅于剂量30mg/kg抑制a375生长。此外,各种pl2#3及pl3#7igg同型体于a375/抗原-特异性t细胞异种移植模型中的肿瘤生长抑制活性显示于第9a(pl2#3)及9b(pl3#7)图。数据显示抗-pd-l1抗体pl2#3的突变的igg1及igg4型于剂量20mg/kg显示较佳的抗肿瘤效果。抗-pd-l1抗体pl3#7的野生型igg1、突变的igg1、以及igg2于剂量30mg/kg抑制a375肿瘤生长。基于这些数据,突变体igg(n297a)选择做为fc骨架。抗-pd-l1抗体pl2#3及pl3#7的突变体于a375/抗原-特异性t细胞异种移植模型中的肿瘤生长抑制活性显示于第15a-15b图。小鼠(n=4/群)以人类黑色素细胞株a375及抗原-特异性t细胞的混合物(t细胞:癌细胞=1:100)皮下植入。pl2#3及pl3#7测试抗体突变体自第0日每周二次腹腔注射至小鼠。经单克隆抗体处理的小鼠的肿瘤生长曲线显示于第15a图。第31日的个别肿瘤体积呈现于第15b图。数据显示pl2#3 mtigg1于a375(黑色素瘤)/抗原-特异性t细胞模型中于剂量20mg/kg及1mg/kg显示抗肿瘤活性;以及pl3#7-43于剂量20mg/kg显示优异的抗肿瘤活性。实施例8抗-pd-l1抗体突变体于hpd1 ki小鼠中的肿瘤生长抑制活性抗-人类pd-l1抗体的活体内活性于人类pd-l1敲入c57bl/6小鼠(hpd1 ki小鼠)中研究。小鼠经人类pd-l1转染的小鼠mc38癌细胞皮下接种(每小鼠5e5细胞)。当肿瘤体积接近约86mm3时开始抗体处理。处理前对各试验组分配6只小鼠。动物接受抗-pd-l1抗体每周二次持续3周的剂量。每周二次对各个动物观察肿瘤的形成。肿瘤由卡尺测量以及肿瘤体积(v)使用下式计算:v(mm3)=0.5(长度(mm)×宽度(mm)×宽度(mm)/2)。人类pd-l1敲入(hpd1 ki)小鼠(n=6/群)以mc38-hupd-l1(经人类pd-l1转染的mc38)细胞皮下植入。当肿瘤体积接近约86mm3时开始抗体处理。测试抗体:pl2#3-mtigg1及pl3#7-mtigg1,腹腔注射至小鼠每周二次持续3周。显示于第10图的数据指示pl2#3-mtigg1及pl3#7-mtigg1的抗肿瘤活性可相当于抗-pd-l1参照抗体阿特珠单抗(atezolizumab)类似物的抗肿瘤活性。实施例9抗-pd-l1抗体对pd-l1表达细胞的细胞表面的结合使用人类t细胞富集试剂盒(ebioscience)由pbmc分离人类t细胞。经分离的t细胞由5μg/ml的植物血凝素(pha)活化6日以刺激pd-l1表现。收集经活化的t细胞且于具有人类fc阻断剂(ebioscience)的facs缓冲液(具有2%fbs的pbs)中,于4℃培养20分钟。移除阻断剂后,t细胞悬浮于facs缓冲液以用于染色过程。肿瘤细胞(a375及nci-h292)由胰蛋白酶处理细胞而自培养盘收集且以facs缓冲液清洗二次以用于细胞染色。抗-pd-l1单克隆抗体的结合通过将细胞与经梯度稀释的抗-pd-l1单克隆抗体于facs缓冲液(具有2%fbs的pbs)中培养。细胞以流动缓冲液清洗二次,结合以经生物素标记的兔抗-人类igg fcγ抗体及链霉亲合素-pe检测。使用cytomics fc 500(beckmencoulter公司)进行流式细胞分析。13a-13c图显示pl2#3及pl3#7变异体对pd-l1表达细胞的细胞表面的结合:经活化t细胞(第13a图)、a375人类黑色素瘤细胞株(第13b图)及nci-h292人类nsclc细胞株(第13c图)。抗-pd-l1参照抗体及hlx01(抗-cd20单克隆抗体)分别使用作为阳性及阴性对照。对于经活化t细胞的结合活性的排序为:pl2#3 mtigg1>pl3#7-54 mtigg1>pl3#7-43 mtigg1>pl3#7-19 mtigg1。对于a375人类黑色素瘤细胞的结合活性的排序为:pl3#7-54 mtigg1>pl2#3 mtigg1>pl3#7-43 mtigg1>pl3#7-19 mtigg1。对于nci-h292人类nsclc细胞的结合活性的排序为:pl3#7-54 mtigg1≥pl2#3 mtigg1=pl3#7-43 mtigg1≥pl3#7-19mtigg1。数据结论为所有pl3#7变异体及p2#3结合至pd-l1表达细胞表面。实施例10抗-pd-l1抗体变异体于nci-h292/pbmc异种移植模型的肿瘤生长抑制活性抗-人类pd-l1抗体的活体内活性使用免疫受损nod/scid(非肥胖糖尿病/严重合并免疫缺陷)小鼠于异种移植模型中研究。癌细胞及经分离的人类pbmc以指定的效应子-对-目标(e∶t)比例于皮下给药前即刻混合。各小鼠以癌细胞与人类pbmc的混合物于两侧接种。测试对象的第一剂量于癌/效应子细胞的植入后2小时腹腔给药。动物接受每周二次测试抗体的剂量持续3至4周。每周二次于各个动物观察肿瘤的形成。肿瘤由卡尺测量以及肿瘤体积(v)使用下式计算:v(mm3)=0.5(长度(mm)×宽度(mm)×宽度(mm)/2)。小鼠(n=4/群)以人类nsclc细胞株nci-h292及新鲜经分离的人类pbmc的混合物(癌细胞(t)∶pbmc(e)=3∶1)皮下植入。抗-pd-l1抗体自第0日每周两次腹腔注射至小鼠。肿瘤曲线示于第14a图。于第28日的各肿瘤体积显示于第14b图。这些数据显示当添加效应子细胞(pbmc)时,所有测试的抗pd-l1抗体变异体抑制肿瘤生长。变异体pl2#3、pl3#7-19及pl3#7-43显示类似的活体内肿瘤生长抑制药效,其较优异于pl3#7-54变异体及参照抗-pd-l1抗体。抗-pd-l1单克隆抗体的抗癌效果通过免疫细胞。实施例11抗-人类pd-l1单克隆抗体对小鼠黑色素瘤细胞的交叉结合抗-pd-l1单克隆抗体的结合通过将a375黑色素瘤细胞(1.5e5细胞/测试)与经梯度稀释的抗体于facs缓冲液中培养而予以评估。细胞以流动缓冲液清洗且以fitc-标记的兔抗-人类igg fcγ抗体检测结合。使用cytomics fc 500(beckmen coulter公司)进行流式细胞分析。pl2#3及pl3#7变异体由流式细胞术测试对于小鼠pd-l1表达的黑色素瘤细胞(b16-f10)的结合。抗-pd-l1参照抗体分别使用作为阳性及阴性对照。显示于第16图的数据指示pl3#7-43及pl3#7-54交叉结合至小鼠pd-l1,而pl2#3及pl3#7-19变异体与小鼠黑色素瘤细胞不具有显著的交叉反应性。实施例12抗-pd-l1变异体的食蟹猴pd-l1交叉结合由sino biological公司购入重组食蟹猴pd-l1_ecd fc-融合蛋白质。pd-l1_ecd/fc(每孔9ng)通过于4℃培养过夜固定化至96-孔检测盘。使用pbs中的5%脱脂乳于室温一小时阻断非特异性结合位点。以pbst清洗盘三次后,将指定浓度的抗-pd-l1抗体与hlx01(阴性对照)与固定的蛋白质于室温培养一小时。以pbst清洗盘三次,之后以于pbs稀释1/1000的过氧化酶标记的山羊抗-人类igg f(ab)’2(jackson immunoresearchlaboratories)于室温培养一小时。清洗后,使用tmb(ebioscience)使盘显色。由varioskanlux微孔盘读值仪(thermo scientific)读取于波长450nm的吸收。p2#3及pl3#7变异体通过elisa测试对重组食蟹猴pd-l1_ecd fc-融合蛋白质的结合。hlx01(抗-cd20单克隆抗体)作为阴性对照。显示于第17图的数据指示pl2#3及pl3#7变异体与食蟹猴pd-l1交叉反应。实施例13构筑去糖基化pl3#7-19变异体及pl3#7-43变异体pl3#7-19及pl3#7-43为衍生自pl3#7的二个主要变异体但需要进行进一步的突变以去除非期望的l-cdr2区中的n-糖基化位点。n-糖基化发生于序列段(sequon)n-x-s/t。由于亲代pl3#7-19及pl3#7-43中的n-糖基化位点经编码为n-s-t及n-r-s,所述工程的进行通过将第二s/t由n突变为pl3#7中的相同者或类似氨基酸,亦即,对于pl3#7-19及pl3#-43分别将n-s-t与n-r-s突变为n-s-n/q及n-r-p(亦即,pl3#7-19去糖基1、去糖基3及pl3#7-43去糖基1),或通过将n-x-s/t序列段直接突变n为q,亦即,对于pl3#7-19及pl3#7-43分别突变n-s-t与n-r-s为q-s-t及q-r-s(亦即,pl3#7-19去糖基2及pl3#7-43去糖基2)。之后,以液相色谱-质谱(lc-ms)及sds-page(数据未显示)证实l-cdr2的n糖基化位点的移除。pl3#7-19变异体及pl3#7-43变异体的去糖基化版本的轻链可变区的氨基酸序列比对显示于第18图。列出的这些去糖基化变异体的轻链的序列比对以及cdr(互补决定区)标示为粗体及下加底线文字。所述重链未改变且与其亲代变异体相同(此处未显示序列比对)。所述去糖基化变异体对于人类pd-l1的结合活性以后续试验中的流式细胞术及octet予以测定。实施例14去糖基化pl3#7-19变异体及pl3#7-46变异体的全细胞结合测试的去糖基化变异体的结合通过将pd-l1表达的cho-s细胞(2e5细胞/孔)与经梯度稀释的抗体于facs缓冲液(具有%fbs的pbs)于4℃培养30分钟而予以评估。这些细胞以流动缓冲液清洗且之后以抗-人类igg fc-fitc(1∶500x)于4℃染色30分钟以检测结合于细胞表面的抗体。使用cytoflex(beckmen coulter公司)进行流式细胞分析。pl3#7-19变异体及pl3#7-43变异体的去糖基化版本的全细胞结合显示于第19(a)及(b)图。pl3#7-19及pl3#7-43为两个首要变异体但需要工程化以移除l-cdr2区内的非期望的n-糖基化位点(参照上述实施例13)。所得的对于pl3#7-19的三个去糖基化变异体(亦即,pl3#7-19去糖基1、去糖基2、去糖基3)以及对于pl3#7-13的二个去糖基化变异体(亦即,pl3#7-46去糖基1、去糖基2)对于经pd-l1转染的cho-s细胞的全细胞结合活性以流式细胞术测定。此处所测试的所有去糖基化抗体变异体位于人类igg1 fc骨架的n2978突变体中。使用内部(in-house)抗-pd-1抗体(亦即,hlx1 0)作为阴性对照。显示于第19(a)及(b)图的数据指示去糖基化pl3#7-19及pl3#7-43变异体的全细胞结合活性不受l-cdr2区中n-糖基化位点的去除而影响。实施例15pl3#7-19去糖基1及pl3#7-43去糖基2于混合白细胞反应中的igg同型体pl3#7-19去糖基1及pl3#7-43去糖基2的不同igg同型体的功效使用混合白细胞反应(mlr)检测而予以测定,以及结果示于第20(a)及(b)图。hlx04及hlx20(pl2#3)分别使用作为阴性及阳性对照。条状图显示由测试抗体所诱发的ifn-γ(第20a图)及il-2分泌(第20b图)。如同去糖基化的pl3#7-19mtigg1及pl3#7-43meigg1,去糖基化pl3#7-19及pl3#7-43的mtigg1及igg4同型体显著地增强mlr中的细胞因子分泌。pl3#7-19去糖基1及pl3#7-43去糖基1的野生型igg1显示较低的细胞因子释放的增强,其可能是由于野生型igg1对于t细胞的潜在adcc效果。实施例16去糖基化pl3#7-19及pl3#7-43变异体于a375/抗原特异性t细胞异种移植模型中的肿瘤生长抑制活性小鼠(n=5/群)皮下植入人类黑色素瘤细胞株a375及抗原-特异性t细胞的混合物(t细胞:癌细胞=1:100)。测试抗体自第0日每周二次腹腔注射至小鼠。以去糖基化pl3#7-19及pl3#7-13变异体处理的小鼠的肿瘤生长分别显示于第21a及21c图。第28日的各肿瘤体积呈现于第21b及21d图。所有数据点为平均±sem。显示于所述图的数据指示pl3#7-19去糖基1mtigg1及igg4变异体,以及pl3#7-43去糖基2wtigg1的抗肿瘤功效,于a375/抗原特异性t细胞异种移植模型中可与hlx20(pl2#3)之抗肿瘤功效相比较。实施例17抗-pd-l1单克隆抗体与抗-vegf单克隆抗体于nsclc异种移植小鼠模型中的肿瘤生长抑制活性抗-人类pd-l1抗体活体内活性使用免疫受损nod/scid(非肥胖糖尿病/严重合并免疫缺陷)小鼠于异种移植模型中研究。癌细胞与经分离人类pbmc以指定的效应子-对-目标(e∶t)比例于皮下给药前即刻混合。各小鼠与癌细胞与人类pbmc的混合物于两侧接种。各试验组分派四只动物。测试对象的第一剂量于癌/效应子细胞的植入后于第1日腹腔给药。每周二次于各个动物观察肿瘤形成。肿瘤由卡尺测量以及肿瘤体积(v)使用下式计算:v(mm3)=0.5(长度(mm)×宽度(mm)×宽度(mm)/2)。小鼠(n=5/群)皮下植入人类nsclc细胞nci-h292以及新鲜经分离的人类pbmc的混合物(癌细胞∶pbmc=3∶1)。抗-pd-l1(pl2#3)及抗-vegf(hlx04)抗体自第1日每周二次腹腔注射至小鼠。肿瘤生长曲线示于第22a图。第21日的个别肿瘤体积呈现于第22b图。所有数据点为平均±sem。数据说明组合抗-pd-l1单克隆抗体,pl2#3,与抗-vegf单克隆抗体,hlx04,相较于单独使用试剂,更为有效地抑制nci-h292异种移植(xenograft)的肿瘤生长。实施例18去糖基化pl3#7-19及pl3#7-43变异体的平恒解离常数(kd)的测定n-糖基化发生于序列段n-x-s/t。因此,于亲代pl3#7-19及pl3#7-43中的n-糖基化位点位于l-cdr2。通过序列段库的s/t突变为与pl3#7为相同或类似氨基酸(亦即,pl3#7-19去糖基1、去糖基3以及pl3#7-43去糖基1),或直接突变糖基化的n为q(亦即,pl3#7-19去糖基3及pl3#7-43去糖基2),来进行n-糖基化位点的移除。除了被工程化排除n糖基化的l-cdr2之外,去糖基化变异体的l-cdr1、l-cdr3、及h-cdr1、h-cdr2、h-cdr3区皆保留无变化。于此所测试的所有去糖基化变异体经克隆至人类igg fc骨架的n297a突变体以与亲代pl3#7-19及pl3#7-43变异体并列比较。去糖基化抗-pd-l1变异体(亦即pl3#7-19去糖基1、去糖基2、去糖基3以及pl3#7-43去糖基1、去糖基2)亲和性及动力学由生物层干涉方法测量,使用octet red96(fortebio)系统利用ahc抗-人类-fc捕捉传感器于25℃,1000rpm的振荡速度测量。简明地,黑色96-孔盘以含有200μl/孔的用于亲和性测定所需要的试剂的管柱制备。一般而言,octet抗-人类-fc传感器首先置于含有1×动力学缓冲液(pbs、0.1%bsa、0.02%tween-20,ph 7.4)的孔180秒以建立基线。然后将传感器转移至含有10μg/ml抗-pd-l1变异体的孔600秒以负载抗-人类-fc尖端。然后将传感器置于新鲜的1×动力学缓冲液180秒以建立基线。然后培养传感器于含有hpd-l1-his的孔中3分钟测量结合,接着转移至含有1×动力学缓冲液的孔持续10分钟,以测量解离。然后传感器每次于再生缓冲液(10mm甘氨酸,ph1.5)中培养3×5秒,接着于1×动力学缓冲液培养5秒而再生。测定各结合/解离循环的之前重复再生。动力学(ka、kd及kd)通过对四个结合/解离循环所测量数据的整体拟合测定,所述数据来自从21.3nm至0.79nm(对于一浓度之一缔合/解离循环)的1∶3梯度稀释的具有1∶1langmuir结合模型的hpd-l1-his的。所有数据利用octet数据分析软件版本9.0分析,表示重复两次进行的二个独立的试验。表12显示通过fortebio octet red96机器(menlo park,ca,usa)使用生物层干涉方法所测量的去糖基化变异体的结合、解离动力学及计算的亲和性(kd)。相对于l-cdr2中具有n-糖基化位点的亲代变异体,去糖基化变异体的亲和性倍数差异显示于表12。所有数据表示重复两次进行的二个独立的试验。这些数据显示去糖基化变异体具有非常类似于亲代pl3#7-19及pl3#7-43的结合亲和性。亲和性不受l-cdr2中的n-糖基化位点移除的影响。表12 平均(n=2) ka[1/(m·s)] kd[1/s] <![cdata[k<sub>d</sub>[m]]]> 倍数差异 pl3#7-19亲代mtigg1 3.28e+05 2.07e-04 6.19e-10 1.00 pl3#7-19去糖基1 mtigg1 3.84e+05 1.62e-04 4.17e-10 1.48 pl3#7-19去糖基2 mtigg1 4.15e+05 1.51e-04 3.69e-10 1.68 pl3#7-19去糖基3 mtigg1 5.06e+05 1.76e-04 3.56e-10 1.74 average(n=2) ka[1/(m·s)] kd[1/s] <![cdata[k<sub>d</sub>[m]]]> 倍数差异 pl3#7-43亲代mtigg1 6.28e+05 2.12e-04 3.45e-10 1.00 pl3#7-43去糖基1 mtigg1 6.12e+05 2.71e-04 4.39e-10 0.79 pl3#7-43去糖基2 mtigg1 6.00e+05 2.38e-04 3.95e-10 0.87 前述实施例仅用于说明目的,不以任何方式意图限制本发明的范畴。除了本文所示以及所述以外的本发明的各种修改,为所属中具有通常知识者根据前文叙述明显可知,且落入本技术专利范围的范畴。具体实施例列表本发明所提供的具体例包括,但不限于:1.一种抗-pd-l1抗体(pl1),包含轻链(lc)可变区序列,该轻链可变区序列包含:(1)包含seq id no:35的氨基酸序列的cdr-l1;(2)包含seq id no:41的氨基酸序列的cdr-l2;及(3)包含seq id no:44的氨基酸序列的cdr-l3;以及重链(hc)可变区序列,该重链可变区序列包含:(1)包含seq id no:51的氨基酸序列的cdr-h1;(2)包含seq id no:55的氨基酸序列的cdr-h2;及(3)包含seq id no:59的氨基酸序列的cdr-h3。2.一种抗-pd-l1抗体(pl2),包含轻链(lc)可变区序列,该轻链可变区序列包含:(1)包含seq id no:36的氨基酸序列的cdr-l1;(2)包含seq id no:42的氨基酸序列的cdr-l2;及(3)包含seq id no:45的氨基酸序列的cdr-l3;以及重链(hc)可变区序列,该重链可变区序列包含:(1)包含seq id no:52的氨基酸序列的cdr-h1;(2)包含seq id no:56的氨基酸序列的cdr-h2;及(3)包含seq id no:60的氨基酸序列的cdr-h3。3.一种抗-pd-l1抗体(pl3),包含轻链(lc)可变区序列,该轻链可变区序列包含:(1)包含seq id no:37的氨基酸序列的cdr-l1;(2)包含seq id no:41的氨基酸序列的cdr-l2;及(3)包含seq id no:46的氨基酸序列的cdr-l3;以及重链(hc)可变区序列,该重链可变区序列包含:(1)包含seq id no:53的氨基酸序列的cdr-h1;(2)包含seq id no:55的氨基酸序列的cdr-h2;及(3)包含seq id no:61的氨基酸序列的cdr-h3。4.一种抗-pd-l1抗体(pl6),包含轻链(lc)可变区序列,该轻链可变区序列包含:(1)包含seq id no:37的氨基酸序列的cdr-l1;(2)包含seq id no:41的氨基酸序列的cdr-l2;及(3)包含seq id no:47的氨基酸序列的cdr-l3;以及重链(hc)可变区序列,该重链可变区序列包含:(1)包含seq id no:54的氨基酸序列的cdr-h1;(2)包含seq id no:57的氨基酸序列的cdr-h2;及(3)包含seq id no:62的氨基酸序列的cdr-h3。5.一种抗-pd-l1抗体(pl8),包含轻链(lc)可变区序列,该轻链可变区序列包含:(1)包含seq id no:38的氨基酸序列的cdr-l1;(2)包含seq id no:43的氨基酸序列的cdr-l2;及(3)包含seq id no:48的氨基酸序列的cdr-l3;以及重链(hc)可变区序列,该重链可变区序列包含:(1)包含seq id no:51的氨基酸序列的cdr-h1;(2)包含seq id no:58的氨基酸序列的cdr-h2;及(3)包含seq id no:63的氨基酸序列的cdr-h3。6.一种抗-pd-l1抗体(pl12),包含轻链(lc)可变区序列,该轻链可变区序列包含:(1)包含seq id no:39的氨基酸序列的cdr-l1;(2)包含seq id no:41的氨基酸序列的cdr-l2;及(3)包含seq id no:49的氨基酸序列的cdr-l3;以及重链(hc)可变区序列,该重链可变区序列包含:(1)包含seq id no:51的氨基酸序列的cdr-h1;(2)包含seq id no:55的氨基酸序列的cdr-h2;及(3)包含seq id no:64的氨基酸序列的cdr-h3。7.一种抗-pd-l1抗体(pl15),包含轻链(lc)可变区序列,该轻链可变区序列包含:(1)包含seq id no:40的氨基酸序列的cdr-l1;(2)包含seq id no:41的氨基酸序列的cdr-l2;及(3)包含seq id no:50的氨基酸序列的cdr-l3;以及重链(hc)可变区序列,该重链可变区序列包含:(1)包含seq id no:53的氨基酸序列的cdr-h1;(2)包含seq id no:55的氨基酸序列的cdr-h2;及(3)包含seq id no:61的氨基酸序列的cdr-h3。8.一种抗-pd-l1抗体变异体(pl2#3),包含轻链(lc)可变区序列,该轻链可变区序列包含:(1)包含seq id no:65的氨基酸序列的cdr-l1;(2)包含seq id no:42的氨基酸序列的cdr-l2;及(3)包含seq id no:71的氨基酸序列的cdr-l3;以及重链(hc)可变区序列,该重链可变区序列包含:(1)包含seq id no:52的氨基酸序列的cdr-h1;(2)包含seq id no:56的氨基酸序列的cdr-h2;及(3)包含seq id no:77的氨基酸序列的cdr-h3。9.一种抗-pd-l1抗体变异体(pl3#7),包含轻链(lc)可变区序列,该轻链可变区序列包含:(1)包含seq id no:37的氨基酸序列的cdr-l1;(2)包含seq id no:41的氨基酸序列的cdr-l2;及(3)包含seq id no:72的氨基酸序列的cdr-l3;以及重链(hc)可变区序列,该重链可变区序列包含:(1)包含seq id no:75的氨基酸序列的cdr-h1;(2)包含seq id no:55的氨基酸序列的cdr-h2;及(3)包含seq id no:78的氨基酸序列的cdr-h3。10.一种抗-pd-l1抗体变异体(pl3#7-19),包含轻链(lc)可变区序列,该轻链可变区序列包含:(1)包含seq id no:66的氨基酸序列的cdr-l1;(2)包含seq id no:68的氨基酸序列的cdr-l2;及(3)包含seq id no:73的氨基酸序列的cdr-l3;以及重链(hc)可变区序列,该重链可变区序列包含:(1)包含seq id no:75的氨基酸序列的cdr-h1;(2)包含seq id no:55的氨基酸序列的cdr-h2;及(3)包含seq id no:79的氨基酸序列的cdr-h3。11.一种抗-pd-l1抗体变异体(pl3#7-43),包含轻链(lc)可变区序列,该轻链可变区序列包含:(1)包含seq id no:35的氨基酸序列的cdr-l1;(2)包含seq id no:69的氨基酸序列的cdr-l2;及(3)包含seq id no:74的氨基酸序列的cdr-l3;以及重链(hc)可变区序列,该重链可变区序列包含:(1)包含seq id no:75的氨基酸序列的cdr-h1;(2)包含seq id no:55的氨基酸序列的cdr-h2;及(3)包含seq id no:80的氨基酸序列的cdr-h3。12.一种抗-pd-l1抗体变异体(pl3#7-54),包含轻链(lc)可变区序列,该轻链可变区序列包含:(1)包含seq id no:67的氨基酸序列的cdr-l1;(2)包含seq id no:70的氨基酸序列的cdr-l2;及(3)包含seq id no:72的氨基酸序列的cdr-l3;以及重链(hc)可变区序列,该重链可变区序列包含:(1)包含seq id no:75的氨基酸序列的cdr-h1;(2)包含seq id no:76的氨基酸序列的cdr-h2;及(3)包含seq id no:81的氨基酸序列的cdr-h3。13.一种抗-pd-l1抗体变异体(pl2#4),包含轻链(lc)可变区序列,该轻链可变区序列包含:(1)包含seq id no:94的氨基酸序列的cdr-l1;(2)包含seq id no:42的氨基酸序列的cdr-l2;及(3)包含seq id no:95的氨基酸序列的cdr-l3;以及重链(hc)可变区序列,该重链可变区序列包含:(1)包含seq id no:52的氨基酸序列的cdr-h1;(2)包含seq id no:56的氨基酸序列的cdr-h2;及(3)包含seq id no:96的氨基酸序列的cdr-h3。14.一种抗-pd-l1抗体变异体(pl2#5),包含轻链(lc)可变区序列,该轻链可变区序列包含:(1)包含seq id no:97的氨基酸序列的cdr-l1;(2)包含seq id no:42的氨基酸序列的cdr-l2;及(3)包含seq id no:98的氨基酸序列的cdr-l3;以及重链(hc)可变区序列,该重链可变区序列包含:(1)包含seq id no:52的氨基酸序列的cdr-h1;(2)包含seq id no:56的氨基酸序列的cdr-h2;及(3)包含seq id no:99的氨基酸序列的cdr-h3。15.一种抗-pd-l1抗体变异体(pl2#39),包含轻链(lc)可变区序列,该轻链可变区序列包含:(1)包含seq id no:100的氨基酸序列的cdr-l1;(2)包含seq id no:42的氨基酸序列的cdr-l2;及(3)包含seq id no:95的氨基酸序列的cdr-l3;以及重链(hc)可变区序列,该重链可变区序列包含:(1)包含seq id no:52的氨基酸序列的cdr-h1;(2)包含seq id no:56的氨基酸序列的cdr-h2;及(3)包含seq id no:101的氨基酸序列的cdr-h3。16.一种抗-pd-l1抗体变异体(pl3#1),包含轻链(lc)可变区序列,该轻链可变区序列包含:(1)包含seq id no:37的氨基酸序列的cdr-l1;(2)包含seq id no:106的氨基酸序列的cdr-l2;及(3)包含seq id no:107的氨基酸序列的cdr-l3;以及重链(hc)可变区序列,该重链可变区序列包含:(1)包含seq id no:108的氨基酸序列的cdr-h1;(2)包含seq id no:55的氨基酸序列的cdr-h2;及(3)包含seq id no:109的氨基酸序列的cdr-h3。17.如具体例10的抗-pd-l1抗体变异体,其中,该抗-pd-l1抗体变异体包含cdr-l2,该cdr-l2于n-糖基化位点包含一或多个突变。18.如具体例11的抗-pd-l1抗体变异体,其中,该抗-pd-l1抗体变异体包含cdr-l2,该cdr-l2于n-糖基化位点包含一或多个突变。19.一种具体例1至18中任一者的抗-pd-l1抗体或其变异体或其抗原结合片段,其中,该抗原结合片段选自:fab、fab’、f(ab)’2、单链fv(scfv)、fv片段、双功能抗体、及线性抗体。20.如具体例1至19中任一者的抗-pd-l1抗体、其变异体或其抗原结合片段,其中,该抗体为多特异性抗体。21.如具体例1至20中任一者的抗-pd-l1抗体、其变异体或其抗原结合片段,其接合至治疗剂。22.如具体例1至21中任一者的抗-pd-l1抗体、其变异体或其抗原结合片段,其接合至标记。23.如具体例22的抗-pd-l1抗体、其变异体或其抗原结合片段,其中,该标记选自:放射同位素、荧光染剂及酶。24.一种经分离的核酸分子,其编码具体例1至19中任一者的抗-pd-l1抗体、其变异体、或其抗原结合片段。25.一种表达载体,其编码具体例24的核酸分子。26.一种细胞,其包含具体例25的表达载体。27.一种制造抗-pd-l1抗体、其变异体或其抗原结合片段的方法,该方法包含培养具体例26的细胞,以及自该细胞培养物回收抗体。28.一种组合物,其包含具体例1至23中任一者的抗-pd-l1抗体、其变异体或其抗原结合片段,以及医药可接受载体。29.一种于来自患者的样品中检测pd-l1的方法,该方法通过将具体例1至20中任一者的抗-pd-l1抗体、其变异体或其抗原结合片段,接触该样品,以及检测结合至pd-l1蛋白质的抗-pd-l1抗体。30.如具体例29的方法,其中,该抗-pd-l1抗体、其变异体、或其抗原结合片段使用免疫组织化学检测(ihc)或使用于elisa检测。31.一种于个体治疗癌症的方法,包含对个体投与有效量的具体例28的组合物。32.如具体例31的方法,其中,该癌症选自:黑色素瘤、nsclc、头颈癌、泌尿上皮癌、三阴性乳腺癌(tnbc)、胃癌、典型何杰金氏淋巴瘤(chl)、非何杰金氏淋巴瘤原发性纵膈b细胞淋巴瘤(nhl pmbcl)、间皮瘤、卵巢癌、肺癌、食道癌、鼻咽癌(npc)、胆管癌、直肠癌、乳癌、子宫颈癌、甲状腺癌及唾腺癌。33.如具体例31的方法,其中,该个体进一步投与选自下述的治疗剂:抗肿瘤剂、化疗剂、生长抑制剂及细胞毒性剂。34.如具体例31的方法,其中,该个体系进一步投与放射疗法。序列列表seq id no:1(pli_lc aa序列,参见第1a图)seq id no:2(pl2_lc aa序列,参见第1a图)seq id no:3(pl3_lc aa序列,参见第1a图)seq id no:4(pl6_lc aa序列,参见第1a图)seq id no:5(pl8_lc aa序列,参见第1a图)seq id no:6(pl12_lc aa序列,参见第1a图)seq id no:7(pl15_lc aa序列,参见第1a图)seq id no:8(pl1_hc aa序列,参见第1b图)seq id no:9(pl2_hc aa序列,参见第1b图)seq id no:10(pl3_hc aa序列,参见第1b图)seq id no:11(pl6_hc aa序列,参见第1b图)seq id no:12(pl8_hc aa序列,参见第1b图)seq id no:13(pl12_hc aa序列,参见第1b图)seq id no:14(pl15_hc aa序列,参见第1b图)seq id no:15(pl2#3_vl nt序列)seq id no:16(pl2#3_vlaa序列(下划线:kabat定义的cdrs))seq id no:17(pl2#3_vh nt序列)seq id no:18(pl2#3_vh aa序列(下划线:kabat定义的cdrs))seq id no:19(pl3#7_vl nt序列)seq id no:20(pl3#7_vl aa序列(下划线:kabat定义的cdrs))seq id no:21(pl3#7_vh nt序列)seq id no:22(pl3#7_vh aa序列(下划线:kabat定义的cdrs))seq id no:23(pl3#7-19_vl nt序列)seq id no:24(pl3#7-19_vlaa序列(下划线:kabat定义的cdrs))seq id no:25(pl3#7-19_vh nt序列)seq id no:26(pl3#7-19_vh aa序列(下划线:kabat定义的cdrs))seq id no:27(pl3#7-43_vl nt序列)seq id no:28(pl3#7-43_vl aa序列(下划线:kabat定义的cdrs))seq id no:29(pl3#7-43_vh nt序列)seq id no:30(pl3#7-43_vh aa序列(下划线:kabat定义的cdrs))seq id no:31(pl3#7-54_vl nt序列)seq id no:32(pl3#7-54_vl aa序列(下划线:kabat定义的cdrs))seq id no:33(pl3#7-54_vh nt序列)seq id no:34(pl3#7-54_vh aa序列(下划线:kabat定义的cdrs))seq id no:35(pl1_lc的cdr-l1):tgsssnvgagydvhseq id no:36(pl2_lc的cdr-l1):sgsss.yiessyvsseq id no:37(pl3_lc的cdr-l1):tgsssnigagydvhseq id no:37(pl6_lc的cdr-l1):tgsssnigagydvhseq id no:38(pl8_lc的cdr-l1):qgdslrsyyvsseq id no:39(pl12_lc的cdr-l1):trsssnigaghdvhseq id no:40(pl15_lc的cdr-l1):tgyssnigagydvhseq id no:41(pl1_lc的cdr-l2):gnsnrpsseq id no:42(pl2_lc的cdr-l2):dddmrpsseq id no:41(pl3_lc的cdr-l2):gnsnrpsseq id no:41(pl6_lc的cdr-l2):gnsnrpsseq id no:43(pl8_lc的cdr-l2):gknnrpsseq id no:41(pl12_lc的cdr-l2):gnsnrpsseq id no:41(pl15_lc的cdr-l2):gnsnrpsseq id no:44(pl1_lc的cdr-l3):qsydsslsgwvseq id no:45(pl2_lc的cdr-l3):eiwdsglggvseq id no:46(pl3_lc的cdr-l3):qsydsslsapvvseq id no:47(pl6_lc的cdr-l3):qsydsslsggvseq id no:48(pl8_lc的cdr-l3):nsrdstgnllrvseq id no:49(pl12_lc的cdr-l3):qsydssltgvvseq id no:50(pl15_lc的cdr-l3):qsydnslsvsvseq id no:51(pl1_hc的cdr-h1):syaisseq id no:52(pl2_hc的cdr-h1):sytmnseq id no:53(pl3_hc的cdr-h1):sytisseq id no:54(pl6_hc的cdr-h1):sytinseq id no:51(pl8_hc的cdr-h1):syaisseq id no:51(pl12_hc的cdr-h1):syaisseq id no:53(pl15_hc的cdr-h1):sytisseq id no:55(pl1_hc的cdr-h2):riipilgianyaqkfqgseq id no:56(pl2_hc的cdr-h2):sissgsdylyyadsvkgseq id no:55(pl3_hc的cdr-h2):riipilgianyaqkfqgseq id no:57(pl6_hc的cdr-h2):kiipilgiadyaqmfkgseq id no:58(pl8_hc的cdr-h2):riipifgtanyaqkfqgseq id no:55(pl12_hc的cdr-h2):riipilgianyaqkfqgseq id no:55(pl15_hc的cdr-h2):riipilgianyaqkfqgseq id no:59(pl1_hc的cdr-h3):egssgwlgvldyseq id no:60(pl2_hc的cdr-h3):nelrwypqagafdiseq id no:61(pl3_hc的cdr-h3):srdgysfgafdiseq id no:62(pl6_hc的cdr-h3):ggyvgylnafdiseq id no:63(pl8_hc的cdr-h3):egvldafdiseq id no:64(pl12_hc的cdr-h3):gigsysfgafdiseq id no:61(pl15_hc的cdr-h3):srdgysfgafdiseq id no:65(pl2#3_lc的cdr-l1):sgsssyiessyvgseq id no:37(pl3#7_lc的cdr-l1):tgsssnigagydvhseq id no:66(pl3#7-19_lc的cdr-l1):tgsssnigggydvhseq id no:35(pl3#7-43_lc的cdr-l1):tgsssnvgagydvhseq id no:67(pl3#7-54_lc的cdr-l1):tgsssnigqgydvhseq id no:42(pl2#3_lc的cdr-l2):dddmrpsseq id no:41(pl3#7_lc的cdr-l2):gnsnrpsseq id no:68(pl3#7-19_lc的cdr-l2):gnstrpsseq id no:69(pl3#7-43_lc的cdr-l2):gnsnrssseq id no:70(pl3#7-54_lc的cdr-l2):ansnrpsseq id no:71(pl2#3_lc的cdr-l3):eiwrsglggvseq id no:72(pl3#7_lc的cdr-l3):qtydsslsarvvseq id no:73(pl3#7-19_lc的cdr-l3):qtydsslsatvvseq id no:74(pl3#7-43_lc的cdr-l3):qtydssgsarvvseq id no:72(pl3#7-54_lc的cdr-l3):qtydsslsarvvseq id no:52(pl2#3_hc的cdr-h1):sytmnseq id no:75(pl3#7_hc的cdr-h1):sypisseq id no:75(pl3#7-19_hc的cdr-h1):sypisseq id no:75(pl3#7-43_hc的cdr-h1):sypisseq id no:75(pl3#7-54_hc的cdr-h1):sypisseq id no:56(pl2#3_hc的cdr-h2):sissgsdylyyadsvkgseq id no:55(pl3#7_hc的cdr-h2):riipilgianyaqkfqgseq id no:55(pl3#7-19_hc的cdr-h2):riipilgianyaqkfqgseq id no:55(pl3#7-43_hc的cdr-h2):riipilgianyaqkfqgseq id no:76(pl3#7-54_hc的cdr-h2):riipilgiadyaqkfqgseq id no:77(pl2#3_hc的cdr-h3):nelrwypqagafdrseq id no:78(pl3#7_hc的cdr-h3):srdgyafgafdiseq id no:79(pl3#7-19_hc的cdr-h3):srdgyafgafdvseq id no:80(pl3#7-43_hc的cdr-h3):srpgyafgafdiseq id no:81(pl3#7-54_hc的cdr-h3):srpgyafgafdiseq id no:82(pl2#4_vl nt序列)seq id no:83(pl2#4_vl aa序列(下划线:kabat定义的cdrs))seq id no:84(pl2#4_vh nt序列)seq id no:85(pl2#4_vh aa序列(下划线:kabat定义的cdrs))seq id no:86(pl2#5_vl nt序列)seq id no:87(pl2#5_vl aa序列(下划线:kabat定义的cdrs))seq id no:88(pl2#5_vh nt序列)seq id no:89(pl2#5_vh aa序列(下划线:kabat定义的cdrs))seq id no:90(pl2#39_vl nt序列)seq id no:91(pl2#39_vl aa序列(下划线:kabat定义的cdrs))seq id no:92(pl2#39_vh nt序列)seq id no:93(pl2#39_vh aa序列(下划线:kabat定义的cdrs))seq id no:94(pl2#4_lc的cdr-l1):sgvssyiessyvsseq id no:97(pl2#5_lc的cdr-l1):sgsssyiessyvsseq id no:100(pl2#39_lc的cdr-l1):sgsssyitssyvsseq id no:42(pl2#4_lc的cdr-l2):dddmrpsseq id no:42(pl2#5_lc的cdr-l2):dddmrpsseq id no:42(pl2#39_lc的cdr-l2):dddmrpsseq id no:95(pl2#4_lc的cdr-l3):kiwdsglggvseq id no:98(pl2#5_lc的cdr-l3):eiwdsrlggvseq id no:95(pl2#39_lc的cdr-l3):kiwdsglggvseq id no:52(pl2#4_hc的cdr-h1):sytmnseq id no:52(pl2#5_hc的cdr-h1):sytmnseq id no:52(pl2#39_hc的cdr-h1):sytmnseq id no:56(pl2#4_hc的cdr-h2):sissgsdylyyadsvkgseq id no:56(pl2#5_hc的cdr-h2):sissgsdylyyadsvkgseq id no:56(pl2#39_hc的cdr-h2):sissgsdylyyadsvkgseq id no:96(pl2#4_hc的cdr-h3):nelrwyplagafdiseq id no:99(pl2#5_hc的cdr-h3):nelrwypfagafdiseq id no:101(pl2#39_hc的cdr-h3):nelrwypkagafdiseq id no:102(pl3#1_vl nt序列)seq id no:103(pl3#1_vl aa序列(下划线:kabat定义的cdrs))seq id no:104(pl3#1_vh nt序列)seq id no:105(pl3#1_vh aa序列(下划线:kabat定义的cdrs))seq id no:37(pl3#1_lc的cdr-l1):tgsssnigagydvhseq id no:106(pl3#1_lc的cdr-l2):gnsrrpsseq id no:107(pl3#1_lc的cdr-l3):qtydsslsrpvvseq id no:108(pl3#1_hc的cdr-h1):syrisseq id no:55(pl3#1_hc的cdr-h2):riipilgianyaqkfqgseq id no:109(pl3#1_hc的cdr-h3):srdgysvgafdsseq id no:110(pl3#7-19去糖基1_vl nt序列(下加底线:l-cdr2))seq id no:111(pl3#7-19 deglycol_vl aa序列(下加底线:kabat定义cdrs))seq id no:112(pl3#7-19去糖基2_vl nt序列(下加底线:l-cdr2))seq id no:113(pl3#7-19去糖基2_vl aa序列(下加底线:kabat定义cdrs))seq id no:114(pl3#7-19去糖基3_vl nt序列(下加底线:l-cdr2))seq id no:115(pl3#7-19去糖基3_vl aa序列(下加底线:kabat定义cdrs))seq id no:116(pl3#7-43去糖基lvl nt序列(下加底线:l-cdr2))seq id no:117(pl3#7-43去糖基1_vl aa序列(下加底线:kabat定义cdrs))seq id no:118(pl3#7-43去糖基2_vl nt序列(下加底线:l-cdr2))seq id no:119(pl3#7-43去糖基2_vl aa序列(下加底线:kabat定义cdrs))
背景技术:
1、程序性死亡配体(pd-l1)及程序性死亡配体2(pd-l2)表达于抗原提呈细胞以及许多人类癌症,且已显示在结合至pd-1时下调t细胞活化以及细胞因子分泌(freeman etal.,2000;latchman et al.,2001)。不同于ctla-4,pd-1主要在活化的t-细胞遭遇由肿瘤及/或基质细胞所表达的免疫抑制性pd-l1(b7-h1)及pd-l2(b7-dc)配体的周边组织发挥功能(flies et al.,2011;topalian et al.,2012a)。pd-1/pd-l1相互作用的抑制在临床前模型中表明有效的抗肿瘤活性(美国专利第8,008,449号及第7,943,743号),以及用于治疗癌症的pd-1/pd-l1相互作用的抗体抑制剂的使用已进入临床试验(brahmer et al.,2010;flies et al.,2011;topalian et al.,2012b;brahmer et al.,2012)。
2、pd-l1的上调可使癌症逃避宿主免疫系统。虽然许多pd-l1抑制剂已被发展用于免疫-肿瘤学疗法且于临床试验显示良好结果。仍有需求发展直接对抗-pd-l1的抗癌症疗法。本发明符合此方面及其他的需求。
技术实现思路
1、本发明提供一种抗-pd-l1抗体及/或其抗原结合片段。一些具体实施例中,本发明的抗-pd-l1抗体,亦即pl1抗体,包含轻链(lc)可变区序列,该轻链可变区序列包含:
2、(1)包含seq id no:35的氨基酸序列的cdr-l1;
3、(2)包含seq id no:41的氨基酸序列的cdr-l2;及
4、(3)包含seq id no:44的氨基酸序列的cdr-l3;
5、以及重链(hc)可变区序列,该重链可变区序列包含:
6、(1)包含seq id no:51的氨基酸序列的cdr-h1;
7、(2)包含seq id no:55的氨基酸序列的cdr-h2;及
8、(3)包含seq id no:59的氨基酸序列的cdr-h3。
9、其他具体实施例中,本发明的抗-pd-l1抗体,亦即pl2抗体,包含轻链(lc)可变区序列,该轻链可变区序列包含:
10、(1)包含seq id no:36的氨基酸序列的cdr-l1;
11、(2)包含seq id no:42的氨基酸序列的cdr-l2;及
12、(3)包含seq id no:45的氨基酸序列的cdr-l3;
13、以及重链(hc)可变区序列,该重链可变区序列包含:
14、(1)包含seq id no:52的氨基酸序列的cdr-h1;
15、(2)包含seq id no:56的氨基酸序列的cdr-h2;及
16、(3)包含seq id no:60的氨基酸序列的cdr-h3。
17、其他具体实施例中,本发明的抗-pd-l1抗体,亦即pl3抗体,包含轻链(lc)可变区序列,该轻链可变区序列包含:
18、(1)包含seq id no:37的氨基酸序列的cdr-l1;
19、(2)包含seq id no:41的氨基酸序列的cdr-l2;及
20、(3)包含seq id no:46的氨基酸序列的cdr-l3;
21、以及重链(hc)可变区序列,该重链可变区序列包含:
22、(1)包含seq id no:53的氨基酸序列的cdr-h1;
23、(2)包含seq id no:55的氨基酸序列的cdr-h2;及
24、(3)包含seq id no:61的氨基酸序列的cdr-h3。
25、其他具体实施例中,本发明的抗-pd-l1抗体,亦即pl6抗体,包含轻链(lc)可变区序列,该轻链可变区序列包含:
26、(1)包含seq id no:37的氨基酸序列的cdr-l1;
27、(2)包含seq id no:41的氨基酸序列的cdr-l2;及
28、(3)包含seq id no:47的氨基酸序列的cdr-l3;
29、以及重链(hc)可变区序列,该重链可变区序列包含:
30、(1)包含seq id no:54的氨基酸序列的cdr-h1;
31、(2)包含seq id no:57的氨基酸序列的cdr-h2;及
32、(3)包含seq id no:62的氨基酸序列的cdr-h3。
33、其他具体实施例中,本发明的抗-pd-l1抗体,亦即pl8抗体,包含轻链(lc)可变区序列,该轻链可变区序列包含:
34、(1)包含seq id no:38的氨基酸序列的cdr-l1;
35、(2)包含seq id no:43的氨基酸序列的cdr-l2;及
36、(3)包含seq id no:48的氨基酸序列的cdr-l3;
37、以及重链(hc)可变区序列,该重链可变区序列包含:
38、(1)包含seq id no:51的氨基酸序列的cdr-h1;
39、(2)包含seq id no:58的氨基酸序列的cdr-h2;及
40、(3)包含seq id no:63的氨基酸序列的cdr-h3。
41、其他具体实施例中,本发明的抗-pd-l1抗体,亦即pl12抗体,包含轻链(lc)可变区序列,该轻链可变区序列包含:
42、(1)包含seq id no:39的氨基酸序列的cdr-l1;
43、(2)包含seq id no:41的氨基酸序列的cdr-l2;及
44、(3)包含seq id no:49的氨基酸序列的cdr-l3;
45、以及重链(hc)可变区序列,该重链可变区序列包含:
46、(1)包含seq id no:51的氨基酸序列的cdr-h1;
47、(2)包含seq id no:55的氨基酸序列的cdr-h2;及
48、(3)包含seq id no:64的氨基酸序列的cdr-h3。
49、其他具体实施例中,本发明的抗-pd-l1抗体,亦即pl15抗体,包含轻链(lc)可变区序列,该轻链可变区序列包含:
50、(1)包含seq id no:40的氨基酸序列的cdr-l1;
51、(2)包含seq id no:41的氨基酸序列的cdr-l2;及
52、(3)包含seq id no:50的氨基酸序列的cdr-l3;
53、以及重链(hc)可变区序列,该重链可变区序列包含:
54、(1)包含seq id no:53的氨基酸序列的cdr-h1;
55、(2)包含seq id no:55的氨基酸序列的cdr-h2;及
56、(3)包含于seq id no:61的氨基酸序列的cdr-h3。
57、本发明进一步包含抗-pd-l1抗体变异体及/或突变体,或其抗原结合片段。某些具体实施例中,本发明的抗-pd-l1抗体变异体及/或突变体,亦即pl2#3抗体,包含轻链(lc)可变区序列,该轻链可变区序列包含:
58、(1)包含seq id no:65的氨基酸序列的cdr-l1;
59、(2)包含seq id no:42的氨基酸序列的cdr-l2;及
60、(3)包含seq id no:71的氨基酸序列的cdr-l3;
61、以及重链(hc)可变区序列,该重链可变区序列包含:
62、(1)包含seq id no:52的氨基酸序列的cdr-h1;
63、(2)包含seq id no:56的氨基酸序列的cdr-h2;及
64、(3)包含seq id no:77的氨基酸序列的cdr-h3。
65、其他具体实施例中,本发明的抗-pd-l1抗体变异体及/或突变体,亦即pl3#7抗体,包含轻链(lc)可变区序列,该轻链可变区序列包含:
66、(1)包含seq id no:37的氨基酸序列的cdr-l1;
67、(2)包含seq id no:41的氨基酸序列的cdr-l2;及
68、(3)包含seq id no:72的氨基酸序列的cdr-l3;
69、以及重链(hc)可变区序列,该重链可变区序列包含:
70、(1)包含seq id no:75的氨基酸序列的cdr-h1;
71、(2)包含seq id no:55的氨基酸序列的cdr-h2;及
72、(3)包含seq id no:78的氨基酸序列的cdr-h3。
73、其他具体实施例中,本发明的抗-pd-l1抗体变异体及/或突变体,亦即
74、pl3#7-19抗体,包含轻链(lc)可变区序列,该轻链可变区序列包含:
75、(1)包含seq id no:66的氨基酸序列的cdr-l1;
76、(2)包含seq id no:68的氨基酸序列的cdr-l2;及
77、(3)包含seq id no:73的氨基酸序列的cdr-l3;
78、以及重链(hc)可变区序列,该重链可变区序列包含:
79、(1)包含seq id no:75的氨基酸序列的cdr-h1;
80、(2)包含seq id no:55的氨基酸序列的cdr-h2;及
81、(3)包含seq id no:79的氨基酸序列的cdr-h3;某些具体实施例中,抗-pd-l1抗体的突变体包含cdr-12,该cdr12包含于n-糖基化位点的一个或多个突变。
82、其他具体实施例中,本发明的抗-pd-l1抗体变异体及/或突变体,亦即
83、pl3#7-43抗体,包含轻链(lc)可变区序列,该轻链可变区序列包含:
84、(1)包含seq id no:35的氨基酸序列的cdr-l1;
85、(2)包含seq id no:69的氨基酸序列的cdr-l2;及
86、(3)包含seq id no:74的氨基酸序列的cdr-l3;
87、以及重链(hc)可变区序列,该重链可变区序列包含:
88、(1)包含seq id no:75的氨基酸序列的cdr-h1;
89、(2)包含seq id no:55的氨基酸序列的cdr-h2;及
90、(3)包含seq id no:80的氨基酸序列的cdr-h3;某些具体实施例中,抗-pd-l1抗体的突变体包含cdr-12,该cdr12包含于n-糖基化位点的一个或多个突变。
91、其他具体实施例中,本发明抗-pd-l1抗体变异体及/或突变体,亦即
92、pl3#7-54抗体,包含轻链(lc)可变区序列,该轻链可变区序列包含:
93、(1)包含seq id no:67的氨基酸序列的cdr-l1;
94、(2)包含seq id no:70的氨基酸序列的cdr-l2;及
95、(3)包含seq id no:72的氨基酸序列的cdr-l3;
96、以及重链(hc)可变区序列,该重链可变区序列包含:
97、(1)包含seq id no:75的氨基酸序列的cdr-h1;
98、(2)包含seq id no:76的氨基酸序列的cdr-h2;及
99、(3)包含seq id no:81的氨基酸序列的cdr-h3。
100、其他具体实施例中,本发明的抗-pd-l1抗体变异体及/或突变体,亦即pl2#4抗体,包含轻链(lc)可变区序列,该轻链可变区序列包含:
101、(1)包含seq id no:94的氨基酸序列的cdr-l1;
102、(2)包含seq id no:42的氨基酸序列的cdr-l2;及
103、(3)包含seq id no:95的氨基酸序列的cdr-l3;
104、以及重链(hc)可变区序列,该重链可变区序列包含:
105、(1)包含seq id no:52的氨基酸序列的cdr-h1;
106、(2)包含seq id no:56的氨基酸序列的cdr-h2;及
107、(3)包含seq id no:96的氨基酸序列的cdr-h3。
108、其他具体实施例中,本发明的抗-pd-l1抗体变异体及/或突变体,亦即pl2#5抗体,包含轻链(lc)可变区序列,该轻链可变区序列包含:
109、(1)包含seq id no:97的氨基酸序列的cdr-l1;
110、(2)包含seq id no:42的氨基酸序列的cdr-l2;及
111、(3)包含seq id no:98的氨基酸序列的cdr-l3;
112、以及重链(hc)可变区序列,该重链可变区序列包含:
113、(1)包含seq id no:52的氨基酸序列的cdr-h1;
114、(2)包含seq id no:56的氨基酸序列的cdr-h2;及
115、(3)包含seq id no:99的氨基酸序列的cdr-h3。
116、其他具体实施例中,本发明的抗-pd-l1抗体变异体及/或突变体,亦即pl2#39抗体,包含轻链(lc)可变区序列,该轻链可变区序列包含:
117、(1)包含seq id no:100的氨基酸序列的cdr-l1;
118、(2)包含seq id no:42的氨基酸序列的cdr-l2;及
119、(3)包含seq id no:95的氨基酸序列的cdr-l3
120、以及重链(hc)可变区序列,该重链可变区序列包含:
121、(1)包含seq id no:52的氨基酸序列的cdr-h1;
122、(2)包含seq id no:56的氨基酸序列的cdr-h2:及
123、(3)包含seq id no:101的氨基酸序列的cdr-h3。
124、其他具体实施例中,本发明的抗-pd-l1抗体变异体及/或突变体,亦即pl3#1抗体,包含轻链(lc)可变区序列,该轻链可变区序列包含:
125、(1)包含seq id no:37的氨基酸序列的cdr-l1;
126、(2)包含seq id no:106的氨基酸序列的cdr-l2;及
127、(3)包含seq id no:107的氨基酸序列的cdr-l3
128、以及重链(hc)可变区序列,该重链可变区序列包含:
129、(1)包含seq id no:108的氨基酸序列的cdr-h1;
130、(2)包含seq id no:55的氨基酸序列的cdr-h2;及
131、(3)包含seq id no:109的氨基酸序列的cdr-h3。
132、各抗-pd-l1及其变异体/突变体的上述记载的cdrs(cdr-l1、-l2及-l3;以及cdr-h1、-h2及-h3)的氨基酸序列提供于下表1。
133、表1
134、
135、
136、一些具体实施例中,本发明的抗-pd-l1抗体及其变异体,包含轻链(lc)可变区序列,该轻链可变区序列包含:
137、(1)包含选自seq id no:35-40、65-67、94、97及100的氨基酸序列的cdr-l1;
138、(2)包含选自seq id no:41-43、68-70及106的氨基酸序列的cdr-l2;及
139、(3)包含选自seq id no:44-50、71-74、95、98及107的组中选择的氨基酸序列的cdr-l3;
140、以及重链(hc)可变区序列,该重链可变区序列包含:
141、(1)包含选自seq id no:51-54、75及108的氨基酸序列的cdr-h1;
142、(2)包含选自seq id no:55-58及76的氨基酸序列的cdr-h2;及
143、(3)包含选自seq id no:59-64、77-81、96、99、101及109的氨基酸序列的cdr-h3。
144、本发明亦提供抗-pd-l1抗体、其变异体、或其抗原结合片段,包含轻链(lc)可变区序列,该轻链可变区序列包含选自seq id no:1-7、16、20、24、28、32、83、87、91或103的氨基酸序列;以及重链(hc)可变区序列,该重链可变区序列包含选自seq id no:8-14、18、22、26、30、34、85、89、93或105的氨基酸序列。亦提供编码所述lc及hc区的核酸序列。
145、根据(或应用于)上述任何一个具体实施例,本发明的抗体包含于可变区中的一个或多个cdr的n-糖基化位点的一个或多个突变。所得的去糖基化抗体区保留与亲代未去糖基化抗体相等功能性。
146、根据(或应用于)上述任何一个具体实施例,抗体包含人类igg的fc片段。根据(或应用于)上述任何一个具体实施例,抗原结合片段选自fab、fab’、f(ab)’2、单链fv(scfv)、fv片段、双功能抗体(diabody)及线性抗体。根据(或应用于)上述任何一个具体实施例,抗体为多特异性抗体。
147、根据(或应用于)上述任何一个具体例,抗-pd-l1抗体、其变异体或抗原结合片段,与治疗剂结合。根据(或应用于)上述任何一个具体实施例,抗-pd-l1抗体、其变异体或抗原结合片段,与标记物结合。根据(或应用于)上述任何一个具体实施例,该标记物选自放射性同位素、荧光染剂及酶。
148、根据(或应用于)上述任何一个具体实施例,本发明提供编码抗-pd-l1抗体、其变异体、突变体或抗原结合片段的分离的核酸分子。
149、根据(或应用于)上述任何具体实施例,亦提供编码该核酸分子的表达载体。根据(或应用于)上述任何具体实施例,亦提供包含该表达载体的细胞。
150、本发明亦提供制造抗体、其变异体或抗原结合片段的方法,该方法包括培养根据(或应用于)上述任何具体实施例的细胞以及自细胞培养物回收抗体或其抗原结合片段。
151、根据(或应用于)上述任何具体实施例,细胞为哺乳动物细胞。根据(或应用于)上述任何具体实施例,哺乳动物细胞为cho细胞。根据(或应用于)上述任何具体实施例,细胞为稳定的哺乳动物细胞株。根据(或应用于)上述任何具体实施例,稳定的哺乳动物细胞株为cho细胞株。
152、本发明提供组合物,该组合物包含根据(或应用于)上述任何具体例的抗-pd-l1抗体、其变异体、突变体或抗原结合片段,以及医药上可接受的载体。
153、本发明提供于来自患者的样品中检测pd-l1蛋白质的方法,该方法包含使根据(或应用于)上述任何具体实施例的抗-pd-l1抗体、其变异体、突变体或抗原结合片段与样品接触,以及检测结合至pd-l1蛋白质的抗-pd-l1抗体。根据(或应用于)上述任何具体实施例,抗-pd-l1抗体、其变异体或抗原结合片段,使用免疫组织化学检测(ihc)或使用于elisa检测。
154、本技术还提供对个体治疗癌症的方法,该方法包含(或应用于)对该对象给予治疗有效量的根据上述任何具体实施例的组合物。
155、亦提供组合物,该组合物包含根据(或应用于)上述任何具体实施例的抗-pd-l1抗体、其变异体、突变体或抗原结合片段,用以治疗癌症。
156、提供根据(或应用于)上述任何具体实施例的抗-pd-l1抗体、其变异体、突变体或抗原结合片段的用途,用于制造用以治疗癌症的药物。
157、根据(或应用于)上述任何具体实施例,癌症选自黑色素瘤、头颈癌、泌尿上皮癌、乳腺癌(例如,三阴性乳腺癌,tnbc)、胃癌、典型何杰金氏淋巴瘤(chl)、非何杰金氏淋巴瘤原发性纵膈b细胞淋巴瘤(nhl pmbcl)、间皮瘤、卵巢癌、肺癌(例如,小细胞肺癌及非小细胞肺癌(nsclc))、食道癌、鼻咽癌(npc)、胆管癌、直肠癌、子宫颈癌、甲状腺癌及唾腺癌。
158、根据(或应用于)上述任何具体实施例,对个体进一步给予选治疗剂,抗肿瘤剂、化疗剂、生长抑制剂或细胞毒性剂。根据(或应用于)上述任何具体实施例,对个体进一步给予放射疗法。
- 还没有人留言评论。精彩留言会获得点赞!