抑制RNA解旋酶DHX33活性的氘代化合物、合成方法、药物组合物及用途与流程
本发明属于生物医药领域,涉及抑制rna解旋酶dhx33活性的氘代化合物和其制备方法,还涉及包含该氘代化合物的药物组合物以及该氘代化合物在制备用于预防和/或治疗dhx33相关疾病的药物中的用途。
背景技术:
1、dhx33属于含有dead/h盒的rna解旋酶蛋白家族,其中dead/h代表氨基酸的缩写asp-glu-ala-asp/his,这一序列连同其他多个保守性氨基酸序列,出现在rna解旋酶家族成员的蛋白序列中,高度参与核酸底物结合以及atp水解。虽然这些家族成员共有这些相同的序列,但是每个rna解旋酶都有各自特定的专一性和独特的生物功能。人dhx33蛋白的分子量是72kda,具有解旋核酸的功能,它利用atp水解所释放的生物能来驱动改变rna和蛋白质复合物的构象,进而参与多种rna的代谢活动,具体地,从rna转录、剪切、编辑、翻译到降解等一系列生物过程。dhx33的功能并不仅仅局限于对rna分子的修饰,研究表明,除了解旋rna双链之外,dhx33蛋白也参与到dna的代谢。具体,dhx33蛋白可以解开dna的双链结构,并在基因表达过程中起重要作用。在体外的酶反应体系中,dhx33蛋白还被发现可以解开dna/rna的杂合双链结构。
2、研究表明,dhx33通过结合在多种癌症相关的基因启动子,影响了dna的甲基化状态,进而在基因组水平调控多种癌症基因的表达和肿瘤发展相关的信号通路,对细胞生长、增殖、迁移、凋亡、糖代谢等多种细胞活动有至关重要的作用。此外,发现dhx33可以感受外来双链rna分子的侵入并在细胞的先天免疫中发挥重要作用。dhx33作为十分重要的细胞生长调控基因,在多种癌症中高度表达,比如肺癌、淋巴瘤、神经胶质母细胞瘤、乳腺癌、结肠癌、肝癌等。多种癌症的发生发展依赖于dhx33蛋白的高度表达。dhx33的遗传敲除可以显著抑制ras癌基因驱动的肺癌发生发展;体内和体外实验证实,抑制dhx33蛋白后,多种癌症如乳腺癌、结肠癌、脑胶质瘤、淋巴瘤等癌症的发生发展都受到明显抑制。
3、研究表明,dhx33的蛋白功能依赖于其解旋酶活力。dhx33的解旋酶活力缺失突变体不具有dhx33蛋白的功能,无法替代野生型dhx33基因的功能。目前针对dhx33作为靶点的小分子抑制剂较为稀少,因此迫切需要开发一类活性高、成药性好的dhx33抑制剂药物。
技术实现思路
1、本发明通过大量的研究,发现了抑制dhx33的rna解旋酶活性的氘代化合物,可以用于预防和/或治疗dhx33相关疾病,例如癌症。
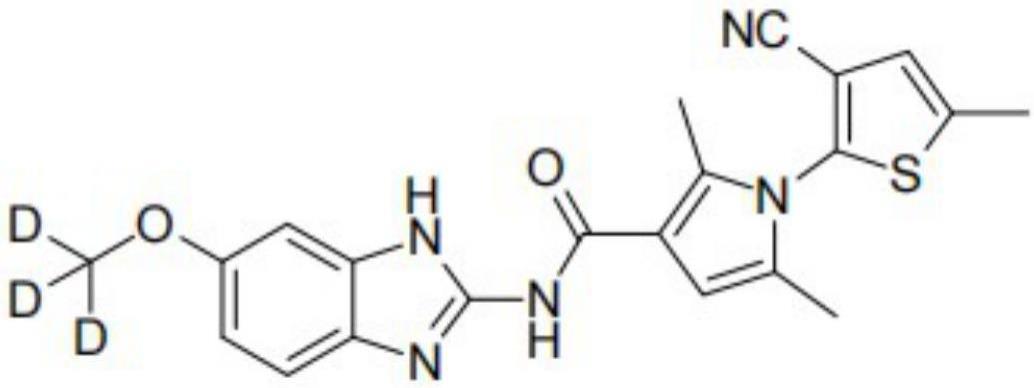
2、一方面,本发明提供了式i所示的抑制dhx33的rna解旋酶活性的氘代化合物:
3、
4、其中,所述氘代化合物的分子式为c21h16d3n5o2s,分子量为408.49。
5、在第二方面,本发明提供了一种药物组合物,包含上述氘代化合物或其药学上可接受的盐或前药,以及一种或多种药学上可接受的载体。
6、在第三方面,本发明提供了上述化合物或其药学上可接受的盐或前药在制备用于预防和/或治疗至少部分由dhx33介导的疾病或病症的药物中的用途。
7、在第三方面的实施方案中,至少部分由dhx33介导的疾病或病症可以是癌症。
8、在第四方面,本发明提供了合成氘代化合物的方法,包括以下步骤:
9、
10、在第四方面的实施方案中,所述化合物4与所述化合物a的摩尔比为2.23:2.35,反应温度为90℃,反应时间为16h。
11、在第四方面的实施方案中,所述化合物4的合成方法包括以下步骤:
12、
13、在第四方面的实施方案中,所述化合物1合成化合物2的方法是向na在cd3od的溶液中加入化合物1,将反应混合物在80℃搅拌16h。
14、与现有技术相比,本发明具有有益的技术效果。具体而言,本发明提供的氘代化合物相比氘代之前的化合物(ab)即如式ⅱ所示,具有更好的代谢稳定性。
15、
16、术语定义
17、除非另有说明,下列术语在本发明中的含义如下。
18、术语“包含”、“包括”、“具有”或“含有”或其任何其它变体旨在涵盖非排他性或开放式的包含内容。例如,包含一系列元素的组合物、方法或装置不一定仅限于已明确列出的元素,而是可能还包含其它未明确列出的元素或上述组合物、方法或装置所固有的元素。
19、术语“药物组合物”是指可以用作药物的组合物,其包含药物活性成分(或治疗剂)以及可选的一种或多种药学上可接受载体。术语“药学上可接受的载体”是指与治疗剂一同给药的辅料,并且其在合理的医学判断的范围内适于接触人类和/或其它动物的组织而没有过度的毒性、刺激性、过敏反应或与合理的益处/风险比相应的其它问题或并发症。在本发明中可使用的药学上可接受的载体包括但不限于:a)稀释剂;b)润滑剂;c)粘合剂;d)崩解剂;e)吸收剂、着色剂、调味剂和/或甜味剂;f)乳化剂或分散剂;和/或g)增强化合物的吸收的物质等。
20、上述药物组合物可以系统地作用和/或局部地作用。为此目的,它们可以通过适合的途径给药,例如通过胃肠外、局部、静脉内、口服、皮下、动脉内、真皮内、经皮、直肠、颅内、腹膜内、鼻内、肌内途径或作为吸入剂给药。
21、上述给药途径可以通过适合的剂型来实现。在本发明中可使用的剂型包括但不限于:片剂、胶囊剂、锭剂、硬糖剂、散剂、喷雾剂、乳膏剂、软膏剂、栓剂、凝胶剂、糊剂、洗剂、软膏剂、水性混悬剂、可注射溶液剂、酏剂、糖浆剂等。
22、当口服给药时,可将上述药物组合物制成任意口服可接受的制剂形式,包括但不限于片剂、胶囊剂、水溶液剂、水混悬剂等。
23、上述药物组合物还可以无菌注射剂的形式给药,包括无菌注射水或油混悬剂,或者无菌注射水或油溶液剂。其中,可使用的载体包括但不限于:水、林格氏溶液和等渗氯化钠溶液。另外,灭菌的非挥发油也可用作溶剂或悬浮介质,如单甘油酯或二甘油酯。
24、上述药物组合物可以包含0.01mg至1000mg的至少一种式i所示的氘代化合物或其药学上可接受盐或其前药。
25、术语“至少部分由dhx33介导的疾病或病症”是指发病机理中至少包含一部分与dhx33有关的因素的疾病,例如癌症,例如前列腺癌或膀胱癌。
26、术语“有效量”是指能够诱发细胞、组织、器官或生物体(例如个体)产生生物或医学反应,并且足以实现所需预防和/或治疗效果的剂量。
27、可调整给药方案以提供最佳所需响应。例如,可单次给药,可随时间分剂量给药,或可根据实际情况按比例减少或增加剂量后给药。可以理解的是,对于任何特定个体,具体的给药方案应根据需要以及给药组合物或监督组合物的给药人员的专业判断而调整。
28、术语“对其有需求”是指医生或其它护理人员对个体需要或者将要从预防和/或治疗过程中获益的判断,该判断的得出基于医生或其它护理人员在其专长领域中的各种因素。
29、术语“个体”(或称受试者)是指人类或非人动物。本发明的个体包括患有疾病和/或病症的个体(患者)和正常的个体。本发明的非人动物包括所有脊椎动物,例如非哺乳动物,例如鸟类、两栖类、爬行类等,和哺乳动物,例如非人灵长类、家畜和/或驯化动物(例如绵羊、犬、猫、奶牛、猪等)。
30、术语“治疗”是指减轻或消除所针对的疾病或病症。如果个体接受了治疗量的本发明的化合物或其药学上可接受的形式或者本发明的药物组合物,该个体的至少一种指标和症状表现出可观察到的和/或可检测出的缓解和/或改善,则表明该个体已被成功地“治疗”。可以理解的是,治疗不仅包括完全地治疗,还包括未达到完全地治疗,但实现了一些生物学或医学相关的结果。具体而言,“治疗”表示本发明的化合物或其药学上可接受的形式或者本发明的药物组合物可以实现下列效果中的至少一种,例如:(1)在可能有疾病倾向,但尚未经历或显示疾病病理学或症状学的动物中防止疾病发生;(2)在正在经历或显示疾病病理学或症状学的动物中抑制疾病(即阻止病理学和/或症状学的进一步发展);(3)在正在经历或显示疾病病理学或症状学的动物中改善疾病(即逆转病理学和/或症状学)。
31、术语“药学上可接受的盐”是指对生物体基本上无毒性的,本发明的化合物的盐。药学上可接受的盐通常包括但不限于本发明的化合物与药学上可接受的无机/有机酸或无机/有机碱反应而形成的盐,此类盐又被称为酸加成盐或碱加成盐。适合的盐的综述参见,例如,jusiak,soczewinski,et al.,remington’s pharmaceutical sciences[m],mackpublishing company,2005和stahl,wermuth,handbook of pharmaceutical salts:properties,selection,anduse[m],wiley-vch,2002。用于制备本发明的化合物的药学上可接受的盐的方法是本领域技术人员已知的。
32、本发明涵盖本发明的化合物的所有可能的代谢物形式,即在施用本发明的化合物的个体体内形成的物质。化合物的代谢物可以通过所属领域的公知技术来鉴定,其活性可以通过试验来表征。
- 还没有人留言评论。精彩留言会获得点赞!