利用CD3254激活RNA外切体驱动体细胞重建多能性
本发明涉及生物医药领域,具体地,本发明涉及利用cd3254激活rna外切体驱动体细胞重建多能性。
背景技术:
1、诱导多能干细胞具备类似于胚胎干细胞的无限自我更新能力和多胚层分化潜能,被广泛应用于疾病建模、药物开发和再生医学。目前,获得诱导多能干细胞主要有2种方式:转录因子重编程和化学重编程。
2、转录因子重编程主要借助转基因方法,外源性转录因子整合到起始细胞基因组中,将会引发安全隐患。相比于转录因子重编程,化学重编程具有独特的优势。
3、化学重编程主要借助小分子组合,小分子不会整合到体细胞基因组,安全性更高。其次,小分子容易穿透细胞膜,处理可逆,处理时间与剂量易控制,小分子可以任意组合,成本更低。
4、最后,一直以来,小分子被用于治疗人类疾病。因此,小分子化学重编程可能更容易被接受应用于临床治疗。目前,细胞化学重编程存在效率低、机制不清晰等问题,严重阻碍了其应用。化学重编程发展至今,仍然是一个缓慢而且低效的过程,分3个阶段,需要将近40天。
5、因此希望找到新的小分子,实现快速有效的化学重编程。
技术实现思路
1、本发明的目的在于提供一种通过小分子调节实现快速有效的化学重编程的方法。
2、在本发明的第一方面,提供了一种活性成分的用途,所述活性成分包含rxra激活剂的试剂,用于制备组合物或制剂,所述组合物或制剂用于:
3、激活rna外切体复合物;
4、促进sall4基因表达;
5、促进细胞重编程;
6、促进诱导多能干细胞的多能标志物表达;和/或
7、治疗或降低炎症反应。
8、在另一优选例中,所述促进细胞重编程为显著提高细胞化学重编程的效率。
9、在另一优选例中,所述rna外切体复合物包括11个亚基:exosc1、exosc2、exosc3、exosc4、exosc5、exosc6、exosc7、exosc8、exosc9、exosc10和dis3。
10、在另一优选例中,所述激活rna外切体复合物包括促进exosc1、exosc2、exosc3、exosc4、exosc5、exosc6、exosc7、exosc8、exosc9、exosc10和dis3的基因或蛋白的表达;较佳地包括促进exosc3,exosc7,exosc8和dis3的基因或蛋白的表达。
11、在另一优选例中,所述激活rna外切体复合物包括:
12、促进exosc3基因或蛋白的表达或活性提高≥2倍,较佳地≥4倍;
13、促进exosc7基因或蛋白的表达或活性提高≥1倍,较佳地≥3倍;
14、促进exosc8基因或蛋白的表达或活性提高≥1倍,较佳地≥3倍;和/或
15、促进exosc8基因或蛋白的表达或活性提高≥1倍,较佳地≥3倍。
16、在另一优选例中,所述激活rna外切体复合物包括:促进转座子rnas(如mmvl30)的降解。
17、在另一优选例中,所述rxra激活剂为cd3254或cd3254样化合物。
18、在另一优选例中,所述活性成分还包括:
19、(i)hdac抑制剂;
20、(ii)gsk-3α/β抑制剂;
21、(iii)tgf-β-ri/alk5抑制剂;
22、(iv)腺苷酸环化酶激活剂;
23、(v)rarα激动剂。
24、在另一优选例中,所述激活剂是指能够在体内或体外提高rxra基因或其蛋白的活性和/或含量的物质;所述物质可以为人工合成的或天然的化合物、蛋白、核苷酸等。
25、在另一优选例中,所述rxra激活剂包括激活rxra表达的物质。
26、在另一优选例中,所述rxra激活剂包括rxra蛋白激活剂和/或rxra基因激活剂。
27、在另一优选例中,所述促进sall4基因表达指将sall4基因或蛋白的表达或活性提高≥1倍,较佳地≥2倍,更佳地≥5倍。
28、在另一优选例中,所述诱导多能干细胞的多能标志物包括oct4、sox2或nanog基因。
29、在另一优选例中,所述促进诱导多能干细胞的多能标志物表达包括:
30、促进oct4基因或蛋白的表达或活性提高≥2倍,较佳地≥4倍;
31、促进sox2基因或蛋白的表达或活性提高≥1倍,较佳地≥2倍;和/或
32、促进nanog基因或蛋白的表达或活性提高≥1倍,较佳地≥3倍。
33、在另一优选例中,所述促进oct4、sox2或nanog基因表达指将sall4基因或蛋白的表达或活性提高≥1倍,较佳地≥2倍,更佳地≥5倍。
34、在另一优选例中,所述hdac抑制剂为vpa(valproic acid)。
35、在另一优选例中,所述gsk-3α/β抑制剂为chir99021。
36、在另一优选例中,所述tgf-β-ri/alk5抑制剂为repsox(616452)。
37、在另一优选例中,所述腺苷酸环化酶激活剂为forskolin。
38、在另一优选例中,所述rarα激动剂为am580。
39、在另一优选例中,所述包含rxra激活剂的试剂组合用于:
40、上调早期多能基因(例如,sall4,lin28a,esrrb,klf4,cmyc)和上皮基因(例如,cdh1,cldn4,tjp3);和/或
41、下调间充质基因(例如,zeb1,twist1,snail1)。
42、在另一优选例中,所述包含rxr激活剂和/或rxr拮抗剂的试剂组合用于:
43、上调干细胞群维持,染色质组织,rna代谢过程和dna复制;
44、下调的胞外基质,上皮到间充质的过渡,tgf-β和mapk信号通路。
45、在另一优选例中,所述细胞为哺乳动物非多能细胞。
46、在另一优选例中,所述哺乳动物包括人或非人哺乳动物。
47、在另一优选例中,所述非人哺乳动物包括啮齿动物(如小鼠、大鼠、兔)、灵长类动物(如猴)。
48、在另一优选例中,所述炎症为ifn-γ-或tnf-α介导的炎症;包括由双链dna引起的ifn-γ的分泌,激活ifngr受体以及下游的jak-stat信号通路,激活炎症反应;以及促进tnf-α的分泌,激活tnfr1受体和下游ikk-nfkb信号通路,激活炎症反应。
49、在本发明的第二方面,提供了一种筛选促进哺乳动物非多能细胞形成诱导多能干细胞(ipsc)的潜在化合物的方法,所述方法包括:
50、(a)提供测试组和空白对照组,将加入测试物的培养体系作为测试组,在测试物存在的情况下,培养非多能细胞;
51、将不加入测试化合物的培养体系作为空白对照组,在不添加该测试物的情况下,培养非多能细胞,空白对照组与测试组其他的条件相同;
52、(b)检测测试组、空白对照组中转座子rna的降解情况,其中测试组的转座子rna的表达量记为c1,空白对照组的转座子rna的表达量记为c0;和
53、(c)比较测试组和空白对照组的转座子rna降解水平,如果测试组的转座子rna的表达量显著低于空白对照组的转座子rna的表达量;则提示所述化合物为能够促进哺乳动物非多能细胞形成诱导多能干细胞(ipsc)的潜在化合物。
54、在另一优选例中,所述哺乳动物包括人或非人哺乳动物。
55、在另一优选例中,所述非人哺乳动物包括啮齿动物(如小鼠、大鼠、兔)、灵长类动物(如猴)。
56、在另一优选例中,所述起始细胞为胚胎成纤维细胞(mefs)。
57、在另一优选例中,所述“显著低于”指在测试组中转座子rna的表达量c1与空白对照组rna的表达量c0之比(c1/c0)≤1/2,较佳地≤1/3,更佳地≤1/4。
58、在另一优选例中,所述转座子rna为vl30 erv1家族;较佳地为mmvl30。
59、在另一优选例中,所述促进哺乳动物非多能细胞向诱导多能干细胞转化的化合物为rxrα特异性激动剂。
60、在另一优选例中,所述rxrα特异性激动剂为cd3452或cd3452样化合物。
61、在另一优选例中,所述cd3452样化合物能够促进转座子mmvl30降解。
62、在另一优选例中,(a)中,还包括阳性对照组,阳性对照组和所述测试组的实验条件相同,其中在阳性对照品cd3452存在下,检测转座子rna的表达量记为c2;
63、如果测试组的转座子rna的表达量c1和表达量c2之比(c1/c2)越小,则提示所述待筛选的物质对转座子rna的降解作用越大。
64、在另一优选例中,所述方法还包括(d),将筛选到的化合物与选自下组的化合物组合进行测试实验,测试所述筛选到的化合物对转座子rna的降解水平:
65、(i)hdac抑制剂;
66、(ii)gsk-3α/β抑制剂;
67、(iii)tgf-β-ri/alk5抑制剂;
68、(iv)腺苷酸环化酶激活剂;和
69、(v)rarα激动剂。
70、在本发明的第三方面,提供了一种筛选促进哺乳动物非多能细胞中sall4基因上调的化合物的方法,所述方法包括:
71、(a)提供测试组和空白对照组,将加入测试物的培养体系作为测试组,在测试物存在的情况下,培养非多能细胞;
72、将不加入测试化合物的培养体系作为空白对照组,在不添加该测试物的情况下,培养非多能细胞,空白对照组与测试组其他的条件相同;
73、(b)检测测试组、空白对照组中转座子rna的降解情况,其中测试组的转座子rna的表达量记为c1,空白对照组的转座子rna的表达量记为c0;和
74、(c)比较测试组和空白对照组的转座子rna降解水平,如果测试组的转座子rna的表达量显著低于空白对照组的转座子rna的表达量;则提示所述化合物为能够促进哺乳动物非多能细胞中sall4基因上调的潜在化合物。
75、在另一优选例中,所述转座子rna为vl30 erv1家族;较佳地为mmvl30。
76、在另一优选例中,所述促进哺乳动物非多能细胞中sall4基因上调的化合物为rxrα特异性激动剂。
77、在另一优选例中,所述rxrα特异性激动剂为cd3452或cd3452样化合物。
78、在本发明的第四方面,提供了用本发明的第二方面的筛选方法获得的具有cd3254活性的化合物。
79、在本发明的第五方面,提供了一种由哺乳动物非多能细胞培养诱导多能干细胞的方法,在细胞适合生长的条件和rxra激活剂存在下,培养哺乳动物非多能细胞,获得诱导的多能干细胞。
80、在另一优选例中,所述培养体系还包括选自下组的一种或多种试剂:
81、(i)hdac抑制剂;
82、(ii)gsk-3α/β抑制剂;
83、(iii)tgf-β-ri/alk5抑制剂;
84、(iv)腺苷酸环化酶激活剂;和
85、(v)rarα激动剂。
86、在另一优选例中,所述方法包括:
87、(s1)提供一起始细胞,使所述细胞与第一培养基接触,培养时间d1;获得第一诱导多能干细胞;
88、所述第一培养基包含第一试剂组合,所述试剂组合包括:rxra激活剂,和选自下述的一种或多种试剂:
89、(i)hdac抑制剂;
90、(ii)gsk-3α/β抑制剂;
91、(iii)tgf-β-ri/alk5抑制剂;
92、(iv)腺苷酸环化酶激活剂;和
93、(v)rarα激动剂。
94、在另一优选例中,所述培养时间d1为10-20天;较佳地为12-15天。
95、在另一优选例中,所述hdac抑制剂为vpa(valproic acid)。
96、在另一优选例中,所述gsk-3α/β抑制剂为chir99021。
97、在另一优选例中,所述tgf-β-ri/alk5抑制剂为repsox(616452)。
98、在另一优选例中,所述腺苷酸环化酶激活剂为forskolin。
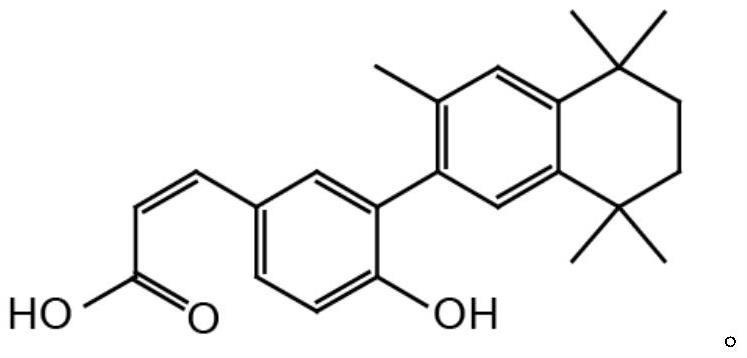
99、在另一优选例中,所述rarα激动剂为am580。
100、在另一优选例中,所述rxra激活剂为cd3254,结构如下所示:
101、
102、在另一优选例中,所述起始细胞的数量为3×105-4×105/plate。
103、在另一优选例中,所述cd3254的浓度为0.1-1mm;较佳地为0.25-0.75mm。
104、在另一优选例中,所述vpa(valproic acid)的浓度为0.1-1mm;较佳地为0.25-0.75mm。
105、在另一优选例中,所述chir99021的浓度为5-30μm;较佳地为10-15μm。
106、在另一优选例中,所述repsox的浓度为5-30μm;较佳地为10-15μm。
107、在另一优选例中,所述forskolin的浓度为1-50μm;较佳地为5-20μm。
108、在另一优选例中,所述am580的浓度为0.1-1mm;较佳地为0.25-0.75mm。
109、在另一优选例中,所述第一诱导多能干细胞诱导的多能干细胞表达选自下组的早期多能基因标志物,包括sall4,cdh1,epcam和lin28a;较佳地为sall4。
110、在另一优选例中,所述第一诱导多能干细胞中:
111、20%-60%的细胞表达早期多能基因标志物sall4。
112、在另一优选例中,所述方法还包括:
113、(s2)将(s1)获得的第一诱导多能干细胞在第二培养基下培养时间d2,获得第二诱导多能干细胞。
114、在另一优选例中,所述第二诱导多能干细胞表达选自下组的早期多能基因标志物,包括sall4,cdh1,epcam和lin28a。
115、在另一优选例中,所述第二诱导的多能干细胞中:
116、40%-80%的细胞表达早期多能基因标志物sall4;
117、40%-80%的细胞表达期多能基因标志物cdh1;
118、40%-80%的细胞表达期多能基因标志物epcam;和
119、40%-80%的细胞表达期多能基因标志物lin28a。
120、在另一优选例中,所述培养时间d2为12-20天;较佳地为12-18天。
121、在另一优选例中,所述第二培养基包含或不包含rxra激活剂。
122、在另一优选例中,所述第二培养基包含选自以下的试剂组合:
123、gsk-3α/β抑制剂,较佳地为chir99021;
124、tgf-β-ri/alk5抑制剂,较佳地为repsox(616452);
125、腺苷酸环化酶激活剂,较佳地为forskolin;
126、单胺氧化酶抑制剂,较佳地为parnatate/tranylcypromine;
127、rarα激活剂,较佳地为am580;
128、组蛋白甲基转移酶ezh2抑制剂,较佳地为dznep。
129、dot1l甲基转移酶抑制剂,较佳地为sgc0946。
130、在另一优选例中,所述方法还包括:
131、(s3)将(s1)获得的第二诱导多能干细胞在第三培养基下培养时间d3,获得胚胎干细胞样细胞。
132、在另一优选例中,所述胚胎干细胞样细胞表达选自下组的多能标志物,包括oct4、sox2和nanog。
133、在另一优选例中,所述胚胎干细胞样细胞中:
134、20%-60%的细胞表达多能标志物oct4;
135、20%-60%的细胞表达多能标志物sox2;和
136、20%-60%的细胞表达多能标志物nanog。
137、在另一优选例中,所述培养时间d3为12-20天;较佳地为12-18天。
138、在另一优选例中,所述第三培养基包含选自以下的试剂组合:
139、gsk-3α/β抑制剂,较佳地为chir99021;
140、mek抑制剂,较佳地为pd0325901。
141、在本发明的第六方面,提供了一种药物组合物,所述的药物组合物含有活性成分,和药学上可接受的载体,其中,所述的活性成分包括rxra激活剂和选自下组的一种或多种试剂:
142、(i)hdac抑制剂;
143、(ii)gsk-3α/β抑制剂;
144、(iii)tgf-β-ri/alk5抑制剂;
145、(iv)腺苷酸环化酶激活剂;
146、(v)rarα激动剂。
147、在另一优选例中,所述药物组合物用于
148、促进sall4基因表达;
149、促进细胞重编程;
150、激活rna外切体复合物;
151、促进诱导多能干细胞的多能标志物表达;和/或
152、治疗或降低炎症反应。
153、在另一优选例中,所述炎症为ifn-γ-或trail介导的炎症。
154、在本发明的第七方面,提供了一种的试剂盒,包括
155、(1)rxra激活剂试剂,和
156、(2)选自下组的一种或多种试剂:
157、(i)hdac抑制剂;
158、(ii)gsk-3α/β抑制剂;
159、(iii)tgf-β-ri/alk5抑制剂;
160、(iv)腺苷酸环化酶激活剂;和
161、(v)rarα激动剂。
162、在另一优选例中,所述试剂盒用于:
163、促进sall4基因表达;
164、促进细胞重编程;
165、激活rna外切体复合物;
166、促进诱导多能干细胞的多能标志物表达;和/或
167、治疗或降低炎症反应。
168、在另一优选例中,所述试剂盒还包括哺乳动物细胞。
169、在另一优选例中,所述rxra激活剂为cd3254或cd3254样化合物。
170、应理解,在本发明范围内中,本发明的上述各技术特征和在下文(如实施例)中具体描述的各技术特征之间都可以互相组合,从而构成新的或优选的技术方案。限于篇幅,在此不再一一累述。
- 还没有人留言评论。精彩留言会获得点赞!