一种泊沙康唑卤环化中间体的合成方法与流程
本发明涉及医药中间体合成领域,具体涉及一种泊沙康唑卤环化中间体的合成方法以及一种泊沙康唑的合成方法。
背景技术:
1、泊沙康唑(posaconazole)是伊曲康唑的衍生物,是2006年fda批准上市的第二代三唑类抗真菌药物,商品名为n0xafil,原研厂家为先灵葆雅。泊沙康唑具有广谱的抗真菌活性,抗菌效力强,对曲霉菌和其他真菌都有良好的杀菌作用,尤其是对多烯类化合物和其他三唑类耐药或侵袭性真菌感染有效。除此之外,泊沙康唑在临床上还用于结合菌感染的治疗,并且也可用于侵袭性曲霉和球孢子菌的挽救性治疗。泊沙康唑自上市以来,其销售额每年呈递增状态,其中2021年泊沙康唑的全球销售额已超过10亿美元,具有很强的经济效应和应用前景。
2、印度msn laboratories limited于2012年在专利us 2014343285a1中公开了泊沙康唑的合成路线:是由间二氟苯为起始原料,通过傅克酰基化、wittig、缩合酰胺、羟甲基化、卤代环合、还原、取代得到目标产物,但是该线路容易产生分子内关环的杂质,虽然能除去,但是严重影响收率。合成路线如下:
3、
4、现有专利与文献公开的合成方法中,对于关键卤环化步骤,存在非对映选择性较差、收率较低且原料用料量大的缺点。考虑到泊沙康唑合成成本高昂,因此开发一种高收率、高非对映选择性的卤环化方法以提升中间体产率从而降低合成成本是十分有必要的。
技术实现思路
1、为弥补现有技术中存在的不足,本发明的一个目的是提供一种泊沙康唑卤环化中间体的合成方法,该合成方法能够明显提高泊沙康唑卤环化中间体的收率和非对映选择性,由此能够显著提高泊沙康唑卤环化中间体的合成效率、降低合成成本。
2、本发明的另一目的是提供一种泊沙康唑的合成方法。
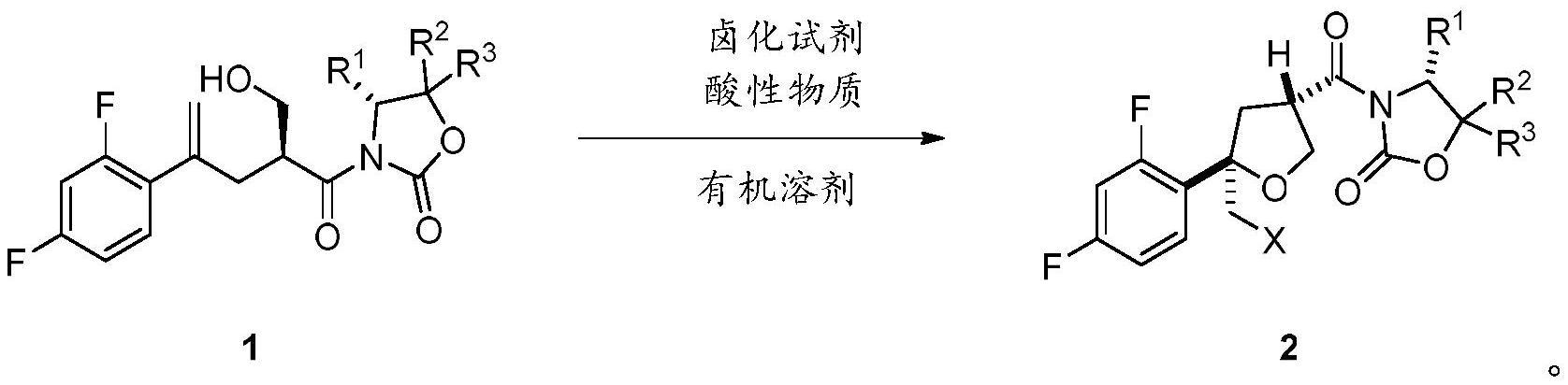
3、本发明的第一个方面提供了一种泊沙康唑卤环化中间体的合成方法,在酸性物质的存在下,如式(1)所示的原料中间体与卤化试剂于有机溶剂中进行卤化反应,制得式(2)所示的泊沙康唑卤环化中间体;
4、
5、其中,r1表示取代或未取代的c1~c6烷基、取代或未取代的c6~c12芳基、或取代或未取代的c7~c18亚烷基芳基;
6、r2和r3各自独立地表示氢、取代或未取代的c1~c6烷基、取代或未取代的c6~c12芳基、或取代或未取代的c7~c18亚烷基芳基;
7、当r1、r2和r3各自独立地表示取代的基团时,取代基选自c1~c4烷基、c1~c4烷氧基或c6~c12芳基;
8、x表示卤素。
9、本发明提供的泊沙康唑卤环化中间体的合成方法在酸性物质的存在下进行反应,卤化试剂在酸性物质的活化下原位生成氢卤酸,氢卤酸再与原料中间体进行反应,卤化试剂的活化和卤化反应“一锅”完成,由此得到目标产物。相对于在中性或碱性条件下的卤化反应,本发明提供的合成方法能够大幅提高目标产物的收率和非对映选择性,继而能够提高目标产物的合成效率、降低合成成本并减轻后续的纯化压力。
10、本发明提供的合成方法中,所述r1可以进一步表示取代或未取代的c1~c4烷基(例如取代或未取代的甲基、乙基、正丙基、异丙基、正丁基、异丁基、仲丁基、叔丁基等)、取代或未取代的苯基、或取代或未取代的苄基;所述r2和r3可以各自独立地进一步表示氢、取代或未取代的c1~c4烷基、取代或未取代的苯基、或取代或未取代的苄基;当r1、r2和r3各自独立地表示取代的基团时,取代基可以选自c1~c4烷基。
11、在一些优选的实施方式中,所述r1可以进一步表示c2~c4烷基(例如异丙基)、苯基或苄基。在另一些优选的实施方式中,所述r2和r3可以各自独立地进一步表示氢或苯基。
12、本发明提供的合成方法中,所述x可以进一步表示br或i。
13、本发明提供的合成方法中,所述酸性物质可以选自常见的无机酸、有机酸或酸式盐(例如碱金属的无机酸式盐),能够活化卤化试剂生成氢卤酸即可。在一些优选的实施方式中,所述酸性物质可以选自盐酸(例如浓度为10~12n的浓盐酸)、硫酸(例如浓度为5~8n的浓硫酸)、硝酸、碳酸、硼酸、正磷酸、对甲苯磺酸(tsoh)、樟脑磺酸、三氟甲磺酸、乙二酸、丙二酸、硫酸氢钾、硫酸氢钠中的一种或多种。在一些更优选的实施方式中,所述酸性物质可以选自盐酸(例如浓度为12n的浓盐酸)。
14、本发明提供的合成方法中,所述酸性物质的用量可以为所述原料中间体的1~50mol%,包括但不限于约1mol%、约5mol%、约8mol%、约10mol%、约12mol%、约15mol%、约18mol%、约20mol%、约25mol%、约30mol%、约35mol%、约40mol%、约45mol%、约50mol%等摩尔百分比或任意的摩尔百分比区间。在一些优选的实施方式中,所述酸性物质的用量可以为所述原料中间体的5~15mol%。
15、本发明提供的合成方法中,所述卤化试剂可以选自常见的卤化试剂,能够被酸性物质活化生成氢卤酸即可。在一些优选的实施方式中,所述卤化试剂可以选自碘(i2)、n-碘代丁二酰亚胺(nis)、n-碘代邻苯二甲酰亚胺、液溴(br2)、二溴海因(dbdmh)、二碘海因、n-溴代丁二酰亚胺(nbs)、n-溴代邻苯二甲酰亚胺中的一种或多种。在一些更优选的实施方式中,所述卤化试剂可以选自i2或nbs。
16、本发明提供的合成方法中,所述卤化试剂的用量可以为所述原料中间体的1.0~5.0当量,包括但不限于约1.0当量、约1.2当量、约1.5当量、约1.8当量、约2.0当量、约2.2当量、约2.5当量、约2.8当量、约3.0当量、约3.5当量、约4.0当量、约4.5当量、约5.0当量等当量值或任意的当量区间。在一些优选的实施方式中,所述卤化试剂的用量可以为所述原料中间体的1.2~2.5当量。
17、本发明提供的合成方法中,所述有机溶剂可以选自常见的乙酸酯类、腈类等有机溶剂。在一些优选的实施方式中,所述有机溶剂可以选自如ch3coor’所示的有机溶剂,其中,r’可以表示c1~c6烷基,优选可以表示c1~c4烷基(例如甲基、乙基、正丙基、异丙基、正丁基、异丁基、仲丁基、叔丁基等)。在一些更优选的实施方式中,所述有机溶剂可以选自乙腈、丁腈、乙酸甲酯、乙酸乙酯、乙酸异丙酯、乙酸正丁酯中的一种或多种。
18、本发明提供的合成方法中,所述卤化反应的反应温度可以为-10~-78℃,包括但不限于约-10℃、约-20℃、约-25℃、约-30℃、约-35℃、约-40℃、约-45℃、约-50℃、约-55℃、约-60℃、约-65℃、约-70℃、约-75℃、约-78℃等温度或任意的温度区间。较低的反应温度有利于提高非对映选择性,基于生产成本等因素综合考虑,在一些优选的实施方式中,所述卤化反应的反应温度可以为-10~-40℃。
19、本发明提供的合成方法中,所述卤化反应的反应时间可以为1~10h。在一些优选的实施方式中,所述卤化反应的反应时间可以为2~5h。
20、本发明的第二个方面提供了一种泊沙康唑的合成方法,包括泊沙康唑卤环化中间体的合成步骤,其中,所述合成步骤采用上述技术方案任一项所述的泊沙康唑卤环化中间体的合成方法。
21、本发明提供的泊沙康唑卤环化中间体的合成方法采用廉价的酸性物质活化卤化试剂并在低温条件下进行卤化反应,制备的目标产物具有高收率、高非对映选择性等优点,工艺简便,便于操作,后处理简单,显著改善了合成效率、降低了合成成本,本发明提供的合成方法还能够实现克级规模反应(如实施例69所示),因而具有工业化规模生产的巨大潜力,工业实用性强,对于扩大泊沙康唑的生产和应用具有重要的意义。
- 还没有人留言评论。精彩留言会获得点赞!