一种紫外可见光可控异构化及催化活性的NHCs-Pd络合物及其制备方法
本发明涉及可用于光敏催化剂及光敏物质的合成技术,进一步涉及可应用于多种催化反应和光控有机材料的合成技术,具体来说涉及一种紫外可见光可控异构化及催化活性的氮杂环卡宾-钯配合物及其制备方法。
背景技术:
1、nhcs(n-heterocyclic carbenes)作为供电子配体可以与诸多种类过渡金属络合生成各式各样不同用途的配合物。相较于传统的金属催化剂,-金属络合物催化剂通常对于酸碱度、空气、温度、湿度等化学环境更加稳定,并且可以展现出更高的催化活性以及化学选择性。但因其催化活性有着不可控性,所以研究者们也希望可以通过修饰络合物结构,并加以“开关”来选择性地促进或抑制络合物的催化活性。相较于磁场、酸碱度、温度、气体氛围等,改变光源有着成本低、清洁、温和、可逆、易引发等特点,因而在诸多“开关”中脱颖而出。
2、2021年hong等人报道了将偶氮苯结构修饰进了caac型的nhcs,随后再与过渡金属钌配位生成目标的光敏催化。作者通过改变光源,调整催化剂分子结构中偶氮苯的构型,从而控制催化剂的反应活性。当在黑暗条件下或白光照射下,其构型为左边的e构型,这样构型的催化剂对于烯烃的复分解反应有着非常高的催化活性;但是在紫外光照射下,偶氮苯结构转变为z构型,其会严重增大催化剂活性中心附近的空间位阻,影响底物分子与金属活性中心的接触,从而极大地抑制了反应活性。作者在这项工作中利用不同光源下催化剂活性中心附近的空间位阻不同来实现光控催化剂的催化活性。请参见下式:
3、
4、同年sasai等人合成了偶氮苯修饰的联萘冠醚化合物(azobenzene binaphtylcrown ether)用于亚胺化合物邻位碳的烷基化反应。与前文不同的是,其在白光下e构型的偶氮苯会让柔性的冠醚呈拉紧状态从而无法让底物分子顺利进入其中参与反应;而在紫外光照射下,z构型的偶氮苯大大减小了空间旋转禁阻性,从而增大了底物分子进入冠醚分子内部的机会。以此达到了光控催化活性的目的。请参见下式:
5、
6、前两篇所讲案例均是将偶氮苯修饰进入催化剂本身结构,利用在不同光源下偶氮苯异构化的现象,从而从空间位阻和空间构型的改变来影响催化剂的催化活性。其主要优点是光的改变对催化活性的影响十分高效,但是缺点在于只利用了空间位阻改变催化剂催化活性。我们更希望通过多元化的方式来控制催化活,比如说通过改变光源直接影响催化剂结构的电子分布、芳香性等因素,从而改变了催化活性。在众多光控分子基团中,将螺吡喃类化合物修饰进催化剂中的研究鲜有问津。而螺吡喃的光致异构前后除了空间结构上的开环与闭环,还会有氮正离子和氧负离子的生成。
技术实现思路
1、本发明所要解决的技术问题是提供一种催化活性可控制的氮杂环卡宾-钯络合物,以解决当下金属配合物催化剂反应活性不可控制的缺点。其目的是合成一系列未被报道过的紫外可见光可控的螺吡喃修饰的氮杂环卡宾-钯配合物,并且希望通过简单的光源改变,即可使其结构发生异构化从而选择性地改变其催化活性。
2、其所要解决的技术问题可以通过以下技术方案来实施。
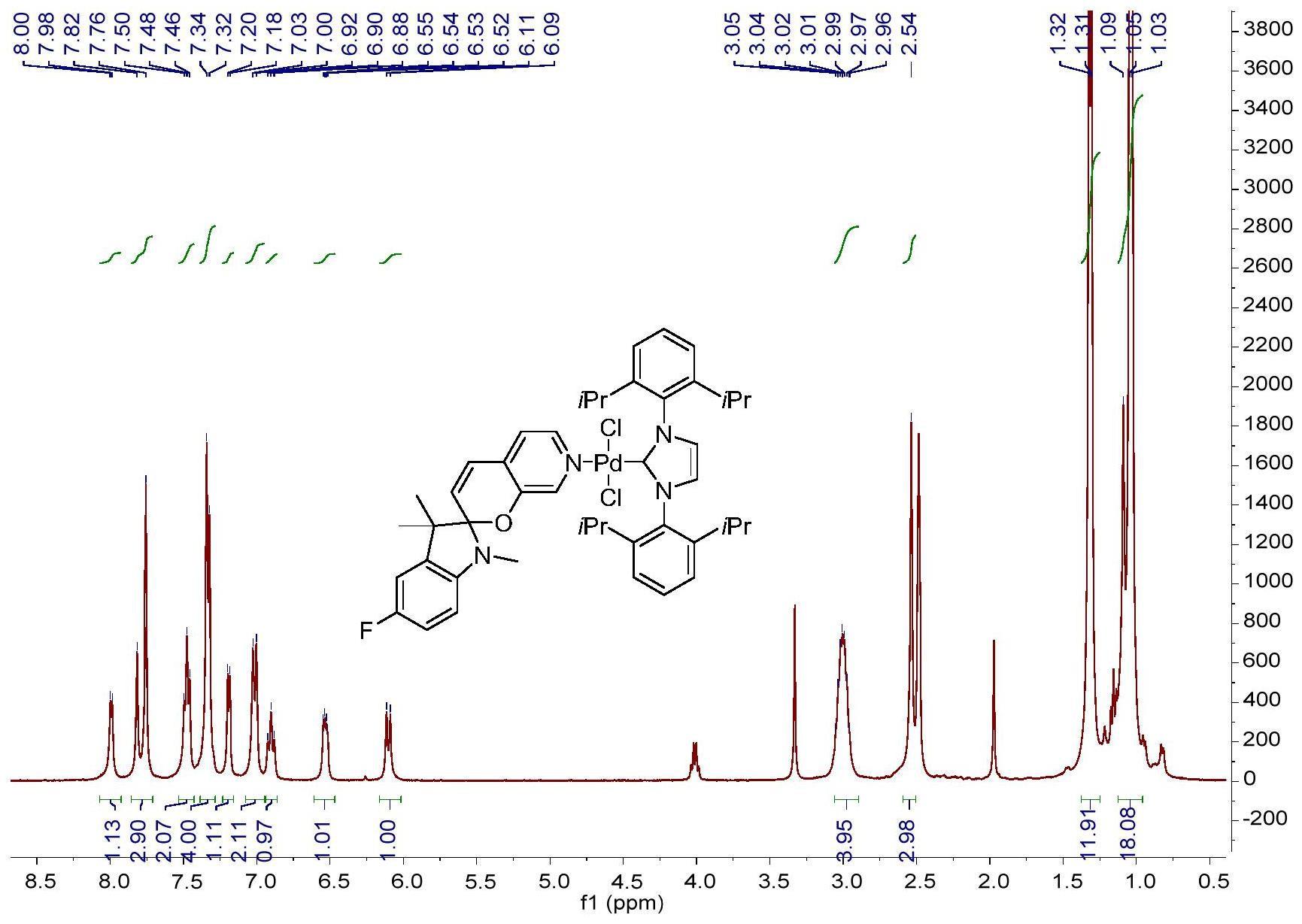
3、一种紫外可见光可控异构化及催化活性的氮杂环卡宾-钯配合物,其结构式如下:
4、
5、其中,r1和r2采用以下7种取代基中的一种:
6、a、r1=f,r2=me;
7、b、r1=f,r2=et;
8、c、r1=cl,r2=me;
9、d、r1=br,r2=me;
10、e、r1=ch3,r2=me;
11、f、r1=h,r2=et;
12、g、r1=obn,r2=me。
13、进一步,该络合物采用如下制备路径:
14、
15、本发明所要解决的另一技术问题在于提供一种上述紫外可见光可控异构化及催化活性的氮杂环卡宾-钯配合物的制备方法,该方法采用如下制备路径:
16、
17、其中,r1和r2采用以下7种取代基中的一种:
18、a、r1=f,r2=me;
19、b、r1=f,r2=et;
20、c、r1=cl,r2=me;
21、d、r1=br,r2=me;
22、e、r1=ch3,r2=me;
23、f、r1=h,r2=et;
24、g、r1=obn,r2=me。
25、进一步,该方法包括吡啶修饰的螺吡喃化合物的合成和螺吡喃修饰的氮杂环卡宾-钯配合物的合成。
26、其中,吡啶修饰的螺吡喃化合物的合成采用如下步骤:
27、(1)、取三口烧瓶,依次加入吲哚碘化物和3-羟基吡啶-4-醛;
28、(2)、架上冷凝回流管后在双排管上抽真空、通氩气;
29、(3)、在抽真空通氩气状态下加入无水甲醇和无水三乙胺;
30、(4)、于65℃-80℃下回流搅拌过夜;
31、(5)、通过tlc监测反应结果,反应结束后在真空下进行浓缩;
32、(6)、使用柱层析分离法提纯目标的吡啶修饰的螺吡喃化合物。
33、进一步,所述吲哚碘化物和3-羟基吡啶-4-醛摩尔比为1:1;所述无水甲醇和无水三乙胺的加入量为每1.98mmol吲哚碘化物对应加入40-60ml无水甲醇和0.1-0.2ml无水三乙胺。
34、优选的,吡啶修饰的螺吡喃化合物的合成采用如下步骤:
35、(1)、取三口烧瓶,依次加入1.98mmol的吲哚碘化物和1.98mmol的3-羟基吡啶-4-醛;
36、(2)、架上冷凝回流管后在双排管上抽真空、通氩气;
37、(3)、在抽真空通氩气状态下加入50ml无水甲醇和0.1ml无水三乙胺;
38、(4)、于70℃下回流搅拌过夜;
39、(5)、通过tlc监测反应结果,反应结束后在真空下进行浓缩;
40、(6)、使用柱层析分离法提纯目标的吡啶修饰的螺吡喃化合物。
41、其中,螺吡喃修饰的氮杂环卡宾-钯配合物的合成采用如下步骤:
42、(1)、取史莱克管,依次加入螺吡喃类化合物、pdcl2、1,3-双(2,6-二异丙基苯)氯化咪唑和k2co3;
43、(2)、使用双排管进行抽真空和通氩气;
44、(3)、在抽真空状态下加入反应溶剂;
45、(4)、于60℃-80℃下搅拌过夜;
46、(5)、通过tlc监测反应结束;使用去离子水和dcm萃取反应液;将收集的有机相使用饱和nacl溶液洗涤;使用无水硫酸钠干燥后将有机相于真空下浓缩;
47、(6)、采用柱层析分离法提纯目标的spp-nhc-pd(spiropyran-containing nhc-pd)配合物。
48、优选的,螺吡喃修饰的氮杂环卡宾-钯配合物的合成采用如下步骤:
49、(1)、取史莱克管,依次加入0.5-1.0mmol的螺吡喃化合物、0.5mmol的pdcl2、0.55mmol的1,3-双(2,6-二异丙基苯)氯化咪唑和2.5mmol的k2co3;
50、(2)、使用双排管进行抽真空和通氩气;
51、(3)、在抽真空通氩气状态下加入2ml反应溶剂;
52、(4)、于60℃-80℃下搅拌过夜;
53、(5)、通过tlc监测反应结束;使用去离子水和dcm萃取反应液;将收集的有机相使用饱和nacl溶液洗涤;使用无水硫酸钠干燥后将有机相于真空下浓缩;
54、(6)、采用柱层析分离法提纯目标的spp-nhc-pd(spiropyran-containing nhc-pd)配合物。
55、采用上述技术方案的紫外可见光可控异构化及催化活性的氮杂环卡宾-钯配合物及其制备方法,通过非常简便的合成方法,首先将光控基团螺吡喃修饰进入吡啶分子结构中,然后根据传统的pd-peppsi络合物的合成方法,将光控基团螺吡喃修饰进入氮杂环卡宾-钯配合物中,并且在后续中通过紫外/可见光的转换来可逆地转变催化剂的结构和催化活性。所合成的光控催化剂和螺吡喃相同有着非常好的光致变色性。
- 还没有人留言评论。精彩留言会获得点赞!