具有中温靶核酸切割活性的PfAgo突变体蛋白及其应用
本发明属于可编程核酸酶,具体涉及具有中温靶核酸切割活性的pfago突变体蛋白及其应用。
背景技术:
1、argonaute(ago)蛋白是一类新型的可编程核酸酶,它广泛分布于真核生物、真细菌和古生菌中。大部分真核ago(eago)蛋白被发现使用5’端磷酸化的向导rna(5’p-grna)去识别靶rna,它在真核生物的rna干扰途径中发挥重要作用。大部分原核ago(pago)蛋白使用5’端磷酸化的向导dna(5’p-gdna)去识别靶dna。原核生物体内缺乏rna干扰途径,尽管近年来的研究表明pago蛋白可以在宿主中防御侵袭性遗传元件,并参与各种细胞内的活动,但目前pago蛋白的生理功能还不是特别清晰。crispr相关蛋白作为一种可编程的核酸酶,已经被报道可应用于不同的领域中。和crispr相关蛋白类似,ago蛋白作为一种新型的可编程核酸酶已经被报道可应用于分子克隆、分子诊断、细胞内rna和基因组编辑、活体成像等。与crispr-cas系统需要在靶标上有特定的基序且只能以rna为向导链相比,pago蛋白在任意靶标序列上都表现出精确的内切酶活性,并且可以同时使用rna和dna作为向导核酸,因此在细胞内rna和基因组编辑等应用方面具有巨大潜力。
2、pfago是一种来源于极端嗜热菌pyrococcusfuriosus的pago蛋白,它能够在5’p-gdna的引导下对靶dna进行切割,其在87~99.99℃的温度范围内活性最高,同时其在37℃下短时间内无法切割靶dna。pfago在高温下具有5’p-gdna介导的高dna靶切割活性,这使其已经应用于分子克隆和分子诊断当中,但其在37℃下几乎没有活性,这限制了其应用于细胞内rna和基因组编辑的可能性。而且,具有热稳定性并在低温下有催化活性的酶不仅易于保存,其应用范围也更加广泛。
3、生物对环境生态位的适应是进化的标志。一个普遍的例子是热适应,其中两个后代在不同的极端温度下进化。这些生物体之间生理差异的基础是催化必要反应的酶的变化,来自每个生物体的同源物经历适应性突变,在各自的生理温度下保持相似的催化速率。然而,导致这些适应性差异的序列变化通常发生在远离底物结合位点的表面暴露位点,使酶的活性位点在结构上不受干扰。这些变化是如何变构传播到活性部位,以调节活性,尚不清楚。2018年,harry g.saavedra等人提出动态变构可以促进酶的冷适应,在保留基态结构的同时,选择可变构的位点进行突变以提高局部展开的概率。2019年,satoshi akanuma等人展示了一种有效的方法去探索氨基酸替代以增强嗜热酶的低温催化活性,该方法基于一组嗜热/中温酶的序列比对。
技术实现思路
1、有鉴于此,本发明旨在对pfago蛋白进行基于结构的突变体筛选以发掘在中温条件下有较好活性的pfago突变体蛋白,不仅可以为细胞内rna靶向和基因编辑及其他应用做铺垫,扩大pago蛋白的使用范围,还能提供一种改造高温ago蛋白的策略。
2、本发明的技术方案具体如下:
3、本发明的目的之一在于提供具有中温靶核酸切割活性的pfago突变体蛋白,这些突变体蛋白相对于野生型pfago蛋白,在结构上距离活性位点和结合底物以外以内的氨基酸发生了突变,使得催化活性温度改变。本发明所述活性位点具体指野生型pfago蛋白的dedh催化四联体。
4、具体的,本发明提供的pfago突变体蛋白的突变位点为seq id no.1所示序列(野生型pfago蛋白的氨基酸序列)的第617位和/或第618位;在seq id no.1所示序列中,第617位的氨基酸为赖氨酸(lys,k),第617位的氨基酸为亮氨酸(leu,l)。
5、在本发明提供的pfago突变体蛋白中,第617位的赖氨酸突变为除赖氨酸以外的其他任意一种氨基酸,第618位的亮氨酸突变为除亮氨酸以外的其他任意一种氨基酸。
6、相对于野生型pfago蛋白,本发明提供的pfago突变体蛋白在30~95℃均具有靶核酸切割活性,扩大了pfago蛋白的适用范围,使其具有了应用于细胞内rna和基因组编辑的潜力。
7、优选地,在本发明提供的pfago突变体蛋白中,第617位的赖氨酸突变为谷氨酸(glu,e)或甘氨酸(gly,g),记为k617e/g;第618位的亮氨酸突变为酪氨酸(tyr,y)、苯丙氨酸(phe,f)、色氨酸(trp,w)或甘氨酸,记为l618y/f/w/g。
8、本发明实施例数据表明:
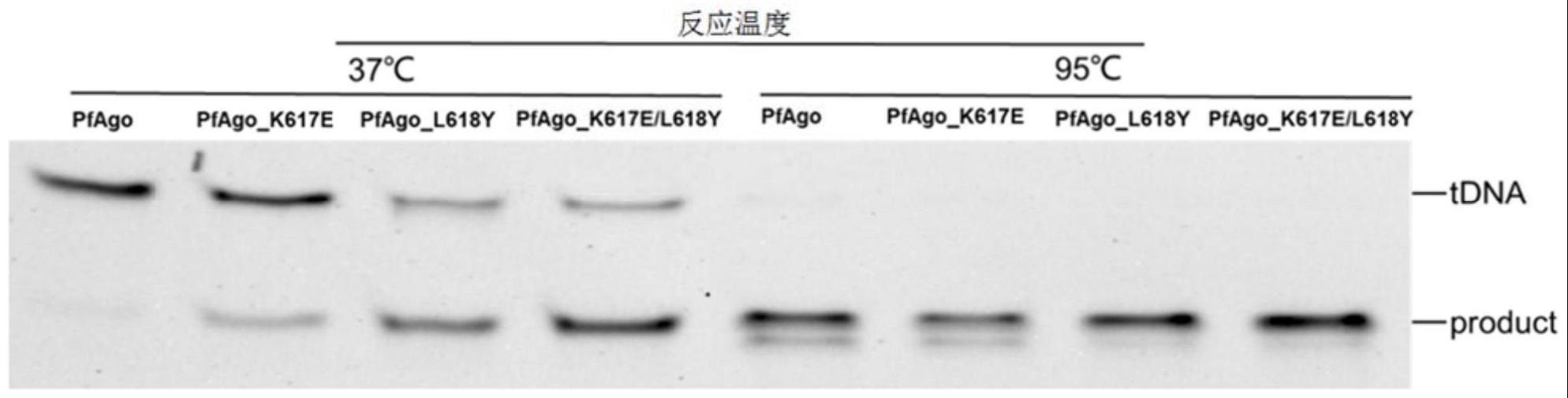
9、(a1)当第617位赖氨酸突变为谷氨酸或甘氨酸后,所得的两个突变体蛋白能够在向导dna的引导下切割靶dna,其中,第617位赖氨酸突变为甘氨酸后所得的突变体蛋白在37℃下的活性更优;
10、(a2)当第618位亮氨酸分别突变为酪氨酸、苯丙氨酸、色氨酸和甘氨酸后,所得的四个突变体能够在向导dna的引导下切割靶dna;其中,第618位亮氨酸突变为酪氨酸或甘氨酸后,所得的突变体蛋白在37℃下的活性更优,且还能在向导dna的引导下切割靶rna;第618位亮氨酸突变为甘氨酸后所得的突变体蛋白还能在5’p-grna的引导下切割靶rna;
11、(a3)当第617位和第618位同时突变时,具体分别突变成甘氨酸和酪氨酸(即k617e和l618y),或同时突变为甘氨酸(即k617g和l618g),所得的两个突变体蛋白在37℃的活性进一步提高,能够在向导dna的引导下切割靶dna和rna;其中,第617位和第618位同时突变为甘氨酸所得的突变体蛋白(记为pfago_k617g/l618g)在37℃下的活性最佳,且还能在5’p-grna的引导下切割靶rna。
12、本发明的目的之二在于提供一些与上述pfago突变体蛋白相关的生物材料,包括:
13、(b1)编码pfago突变体蛋白的核酸分子;
14、(b2)包含(b1)所述核酸分子的表达盒或载体;
15、(b3)包含(b2)所述载体的转化体。
16、对于(b1)所述的核酸分子,本发明一实施例提供了如seq id no.3所示的核苷酸序列,该序列编码的pfago突变体蛋白(即pfago_k617g/l618g)是将第617位赖氨酸、第618位亮氨酸同时突变为甘氨酸,且该突变体蛋白的氨基酸序列如seq id no.2所示。
17、对于(b2)所述的载体,可以为pet质粒,如本发明一实施例将编码pfago突变体蛋白的核酸片段连接至pet-28a中得到重组载体。
18、对于(b3)所述的转化体由重组载体转化至宿主细胞所得,所述宿主细胞可为本领域常规的宿主细胞,但要能满足重组载体稳定的自行复制,且携带的编码pfago突变体蛋白的核酸分子可被有效表达。
19、利用上述生物材料,可以制备pfago突变体蛋白。
20、本发明的目的之三在于提供一种核酸切割体系,该体系包括:
21、(c1)单链向导核酸;
22、(c2)本发明提供的pfago突变体蛋白。
23、在上述核酸切割体系中,单链向导核酸为5’p-grna、5’p-gdna或5’端羟基化的向导dna(5’oh-gdna),且单链向导核酸的长度为12至30个核苷酸。
24、更为优选地,单链向导核酸的长度为15至19个核苷酸;长度为18个核苷酸时为最佳。
25、本发明的目的之四在于提供上述核酸切割体系在特异性切割靶rna或靶dna中的应用,具体的,构建核酸切割体系,并向该体系中添加靶rna或靶dna,若靶rna或靶dna与单链向导核酸序列互补配对,pfago突变体蛋白则在单链向导核酸引导下特异性切割靶rna或靶dna。
26、在上述应用中,靶rna没有高级结构;或有高级结构;或为双链rna;或为体外转录地rna;或为病毒基因组rna;或为mrna;或细胞内的其他rna。靶dna是单链dna或双链dna。
27、在上述应用中,互补配对具体指以下两种情形:
28、靶rna或靶dna具有与单链向导核酸序列完全互补的核苷酸序列;
29、靶rna或靶dna具有与单链向导核酸序列存在单个或多个碱基错配的核苷酸序列,其中,错配的数目可能是1、2、3、4或5,错配通常是分离的,也可能是连续的。
30、在上述应用中,核酸切割体系中含有选自mn2+,mg2+和co2+中至少一种的二价金属阳离子。
31、优选地,二价金属阳离子为mn2+和mg2+,其中最佳的为mn2+。
32、优选地,在核酸切割体系中,二价金属阳离子的终浓度为1~10mm;实施例数据表明:当单链向导核酸为5’p-gdna,靶为dna时,mg2+浓度为3~10mm,mn2+浓度为2~10mm;当单链向导核酸为5’p-gdna,靶为rna时,mg2+浓度为2~10mm,mn2+浓度为1~5mm;当单链向导核酸为5’p-grna,靶为rna时,mn2+浓度为3~10mm。
33、本发明的目的之五在于提供一种检测试剂盒,在该试剂盒中含有本发明提供的pfago突变体蛋白;还可以根据检测目的,包含具有特定序列的单链向导核酸。
34、本发明的目的之六在于提供一种体外基因编辑的方法,具体采用本发明提供的pfago突变体蛋白。
35、与现有技术相比,本发明的有益效果是:
36、(1)通过将野生型pfago蛋白在结构上距离活性位点和结合底物以外以内的氨基酸进行突变,成功筛选到了能够在中低温条件下具有较好活性的pfago突变体蛋白,为高温ago蛋白的改造提供了一种策略。
37、(2)本发明提供的pfago突变体蛋白提高了其在中温下的切割活性,同时保留了其耐热的能力,有利于酶的保存和运输。
38、(3)相对于野生型pfago只能在高温下使用向导dna切割靶dna,本发明提供的最优突变体蛋白pfago_k617g/l618g能够在37℃下使用向导dna切割靶dna和rna,使用5’p-grna切割rna靶,扩大了其使用的温度范围、向导核酸的类型、切割靶标的类型。
39、(4)pfago_k617g/l618g具有特异性切割靶rna和靶dna的活性,本发明还提供了包含编码pfago_k617g/l618g蛋白的核酸表达载体,以及用于以序列特异性方式切割和编辑靶核酸的组合物、试剂盒和方法等,为pfago_k617g/l618g在生物技术的许多领域如核酸检测、分子克隆、rna和基因组编辑等应用奠定了基础。
40、(5)pfago_k617g/l618g可以在37℃下使用向导dna切割靶dna,奠定了其体内基因组编辑的基础;pfago_k617g/l618g可以在37℃下使用向导dna切割靶rna,奠定了其体内rna靶向的基础;pfago_k617g/l618g可以在37℃下使用5’p-grna切割靶rna,奠定了其以蛋白和向导核酸共表达的方式进行体内rna靶向的基础。
41、(6)pfago_k617g/l618g严格依赖于向导和靶标的互补配对发挥切割活性,不存在crispr相关蛋白的非特异性“附带切割”活性,特异性更好。pfago_k617g/l618g所使用的向导核酸的种类具有多样性,可以是dna也可以是rna,一般长度更短,dna较rna的合成成本会相对较低,且dna比rna更加稳定,不易降解。pfago_k617g/l618g和向导核酸形成的pago复合物不用依赖靶位点附近的特殊基序来识别和结合靶,向导核酸设计方便,不用考虑位点限制。
- 还没有人留言评论。精彩留言会获得点赞!