单链接头预连接方法、高通量测序文库的建库方法及试剂盒
本发明涉及高通量测序领域,具体而言,涉及一种单链接头预连接方法、高通量测序文库的建库方法及试剂盒。
背景技术:
1、高通量二代测序技术的快速发展,测序成本的不断降低,已经广泛应用于人类疾病的筛查和诊断、分子育种等领域,产生了巨大的经济和社会效益。测序文库的构建,是高通量测序技术的关键技术环节之一,其中对不同样本建立索引(indexing),即标记一段条形码序列(barcode),可实现多个样本同步测序,是建库测序的重要策略,能够提高建库通量、缩短建库周期、降低建库成本。
2、当前,对样本建立索引主要还是在文库构建的最后一步扩增环节,前期大部分步骤仍需对单个样本分别进行操作,造成建库成本居高不下,且一定时间范围内开展建库的样本数量也会受到很大的限制。因而,样本dna起始阶段标记技术的开发,可实现多个样本混合一起进行后续文库的构建,提高建库效率和通量。由此建立的高通量建库方法,不仅能够降低建库成本,并且一定程度上可以消减每个样本分别建库过程中因试剂、仪器、操作等引起的批次效应。
3、近期,已开发了一些技术对样本进行标记,如(1)通过tn5转座酶把带有标签的寡核苷酸接头插入到基因组dna中,构建了一系列微量、超微量甚至单细胞水平的文库构建技术,这些技术包括scatac-seq、cut&tag、cobatch、cotech等;(2)通过携带有标签的引物对基因组进行扩增,如基于10× genomics的scrna-seq(https://www.10xgenomics.com/)等;(3)对样本进行接头预连接,在建库的起始阶段使用携带有标签的接头进行连接标记样本,标记后的样本混合后即可同步进行建库的后续操作,如ichip、co-chip等。这些方法大大促进了测序建库技术的发展及其在生物学领域的应用,但仍然存在局限性:以双链dna为底物进行文库的构建。在基因组中,除了双链dna还存在大量单链dna、dna-rna杂合链等形态。对于这些形态的dna,现有的上述基于双链dna的建库方法无法进行标记和建库。
技术实现思路
1、本发明的主要目的在于提供一种单链接头预连接方法、高通量测序文库的建库方法及试剂盒,以解决现有技术中对于特殊形态的dna结构基于双链dna的建库方法难以进行标记建库的问题。
2、为了实现上述目的,根据本发明的第一个方面,提供了一种单链接头预连接方法,该单链接头预连接方法包括:a)利用末端转移酶将样本dna的3'端进行延伸形成外延的单链dna结构,获得延伸dna;b)在夹板的作用下,将延伸dna和单链接头进行连接,获得预连接缺刻dna,单链dna结构3'端和单链接头的5'端相邻并存在缺刻;c)利用dna连接酶以磷酸二酯键连接缺刻,获得单链接头预连接dna;其中,单链接头从5'端至3'端依次包括:夹板互补区域、条形码区域和测序接头区域;条形码区域为4-12个碱基组合的序列;夹板包括5'端的单链接头结合区和3'端的目标片段结合区;单链接头结合区与夹板互补区域互补配对;目标片段结合区与外延的单链dna结构互补配对。
3、进一步地,在单链接头的夹板互补区域和条形码区域之间还包括唯一标识符区域;优选地,测序接头区域的3'端含有3'封闭修饰;优选地,目标片段结合区包括(aaaa)n、(cccc)n、(gggg)n、(tttt)n、(rrrr)n、(yyyy)n、(kkkk)n、(mmmm)n、(ssss)n、(wwww)n、(bbbb)n、(dddd)n、(hhhh)n、(vvvv)n或(nnnn)n,其中n表示碱基个数,n为4-8中任意整数;大写字母表示不同脱氧核苷酸碱基类型或组合,其中a:腺嘌呤;t:胸腺嘧啶;c:胞嘧啶;g:鸟嘌呤;y:胞嘧啶或胸腺嘧啶;r:腺嘌呤或鸟嘌呤;m:腺嘌呤或胞嘧啶;k:鸟嘌呤或胸腺嘧啶;w:腺嘌呤或胸腺嘧啶;s:胞嘧啶或鸟嘌呤;v:腺嘌呤、胞嘧啶或鸟嘌呤;h:腺嘌呤、胞嘧啶或胸腺嘧啶;d:腺嘌呤、鸟嘌呤或胸腺嘧啶;b:胞嘧啶、鸟嘌呤或胸腺嘧啶;n:腺嘌呤、鸟嘌呤、胞嘧啶或胸腺嘧啶。优选地,单链接头预连接方法包括:在单链接头连接时,连接体系中含有聚乙二醇;优选地,聚乙二醇包括peg2000、peg4000、peg6000或peg8000中的一种或多种;优选地,聚乙二醇在连接体系中的质量浓度为5%-30%。优选地,a)、b)和c)能够分步或同时进行,获得单链接头预连接dna;优选地,样本dna包括双链dna、单链dna或dna-rna杂合链中的一种或多种。
4、进一步地,将样本dna、夹板、dna连接酶和单链接头混合于t4 rna连接酶缓冲液或t4 dna连接酶缓冲液中,形成连接体系。
5、进一步地,脱氧核糖核苷酸三磷酸包括脱氧腺苷5'-三磷酸、脱氧鸟苷5'-三磷酸、脱氧胞苷5'-三磷酸和脱氧胸腺苷5'-三磷酸其中的一种、两种、三种或四种,在单链接头预连接方法中,末端转移酶催化各脱氧核糖核苷酸三磷酸结合至样本dna的3'端羟基,各脱氧核糖核苷酸三磷酸依次结合形成单链dna结构;优选地,脱氧核糖核苷酸三磷酸为脱氧鸟苷5'-三磷酸。
6、为了实现上述目的,根据本发明的第二个方面,提供了一种高通量二代测序文库的建库方法,该建库方法包括:利用上述单链接头预连接方法获得单链接头预连接dna;利用能够与单链接头特异性结合的引物对单链接头预连接dna进行扩增,得到连接3'端接头的双链dna产物;对连接3'端接头的双链dna产物进行5'端接头连接,得到双端接头产物;对双端接头产物进行扩增,获得高通量二代测序文库。
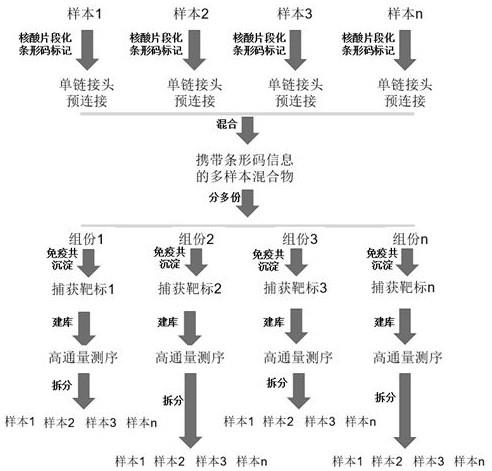
7、进一步地,当样本dna为基因组dna中的r-loop时,建库方法包括:片段化处理不同样本的基因组dna,获得各基因组对应的片段化dna;利用单链接头预连接方法,将携带不同条形码区域的单链接头分别与各基因组对应的片段化dna连接,获得不同的单链接头预连接dna;混合不同的单链接头预连接dna,进行免疫共沉淀,获得单链接头连接r-loop dna,单链接头连接r-loop dna为来源于r-loop的、连接有单链接头的dna-rna杂合链;利用能够与单链接头特异性结合的引物,对单链接头连接r-loop dna进行扩增,获得r-loop的测序文库。
8、进一步地,当样本dna为细胞的染色质中靶向蛋白的dna时,建库方法包括:片段化处理不同的染色质,获得各染色质对应的片段化dna;利用单链接头预连接方法,将携带不同条形码区域的单链接头分别与各染色质对应的片段化dna连接,获得不同的单链接头预连接dna;混合不同的单链接头预连接dna,利用抗体进行免疫共沉淀,获得单链接头连接靶向dna,单链接头连接靶向dna为连接有单链接头的靶向蛋白的dna,利用能够与单链接头特异性结合的引物,对单链接头连接靶向dna进行扩增,获得靶向蛋白的dna的测序文库。
9、进一步地,不同的染色质通过如下方法获得:利用交联剂固定不同的细胞,对固定的细胞进行裂解,获得不同的染色质;交联剂包括甲醛;裂解包括利用化学裂解、机械裂解或酶裂解对细胞进行裂解。
10、为了实现上述目的,根据本发明的第三个方面,提供了一种单链接头试剂盒,该单链接头试剂盒包括单链接头、夹板和末端转移酶;单链接头从5'端至3'端依次包括:夹板互补区域、条形码区域和测序接头区域;条形码区域为4-12个碱基的组合;夹板包括5'端的单链接头结合区和3'端的目标片段结合区;单链接头结合区能够和夹板互补区域进行特异性结合;目标片段结合区能够和待连接的目标片段进行特异性结合,从而将夹板与目标片段连接。
11、进一步地,在单链接头的夹板互补区域和条形码区域之间还包括唯一标识符区域;优选地,测序接头区域的3'端含有3'封闭修饰;优选地,单链接头试剂盒还包括连接缓冲液,连接缓冲液中含有dna连接酶和/或聚乙二醇;优选地,连接缓冲液包括t4 rna连接酶缓冲液或t4 dna连接酶缓冲液;优选地,聚乙二醇包括peg2000、peg4000、peg6000或peg8000中的一种或多种;优选地,聚乙二醇的质量浓度为5%-30%;优选地,目标片段结合区包括(aaaa)n、(cccc)n、(gggg)n、(tttt)n、(rrrr)n、(yyyy)n、(kkkk)n、(mmmm)n、(ssss)n、(wwww)n、(bbbb)n、(dddd)n、(hhhh)n、(vvvv)n或(nnnn)n,其中n表示碱基个数,n为4-8中任意整数;大写字母表示不同脱氧核苷酸碱基类型或组合,其中a:腺嘌呤;t:胸腺嘧啶;c:胞嘧啶;g:鸟嘌呤;y:胞嘧啶或胸腺嘧啶;r:腺嘌呤或鸟嘌呤;m:腺嘌呤或胞嘧啶;k:鸟嘌呤或胸腺嘧啶;w:腺嘌呤或胸腺嘧啶;s:胞嘧啶或鸟嘌呤;v:腺嘌呤、胞嘧啶或鸟嘌呤;h:腺嘌呤、胞嘧啶或胸腺嘧啶;d:腺嘌呤、鸟嘌呤或胸腺嘧啶;b:胞嘧啶、鸟嘌呤或胸腺嘧啶;n:腺嘌呤、鸟嘌呤、胞嘧啶或胸腺嘧啶。
12、应用本发明的技术方案,利用上述单链接头预连接方法、高通量测序文库的建库方法及试剂盒,首先通过末端转移酶将样本dna进行3'端延伸,在夹板的辅助下将单链接头连接在样本dna的3'端,获得单链接头预连接dna。利用此种单链接头预连接dna进行建库,从而实现对于多种形态的dna,尤其是dna-rna杂合链、或基因组水平与蛋白质相互作用的dna等dna的高通量建库,能够实现多样本同步免疫共沉淀处理和建库,具有建库通量高、建库成本低的优点,能够缩短建库周期,也能够消减每个样本分别建库过程中因试剂、仪器、操作等引起的批次效应。
- 还没有人留言评论。精彩留言会获得点赞!