一种非富勒烯受体材料及其制备方法与应用与流程
本发明属于光伏材料,具体涉及一种非富勒烯受体材料及其制备方法与应用。
背景技术:
1、太阳能电池是通过光电效应或者光化学效应直接把光能转化成电能的装置。近年来,有机太阳光伏电池(opv)由于其可溶液加工,且具有制造成本低、柔性、重量轻等优点成为研究热点。随着有机光伏材料的创新,以及器件结构和制备工艺的优化,opv的光电转换效率(pce)得到提高。其中,受体材料的添加可提高光吸收能力,一定程度上提高太阳能电池的光电转换效率(pce)。然而目前,受体材料的种类较为单一,一定程度上限制了太阳能电池的应用和发展。
技术实现思路
1、本发明旨在至少解决上述现有技术中存在的技术问题之一。为此,本发明提出一种新型非富勒烯受体材料,在太阳能电池中有良好的应用前景。
2、本发明还提出一种非富勒烯受体材料的制备方法。
3、本发明还提出一种光伏器件用活性材料。
4、本发明还提出一种光伏电池。
5、本发明还提出了上述非富勒烯受体材料或光伏器件用活性材料的应用。
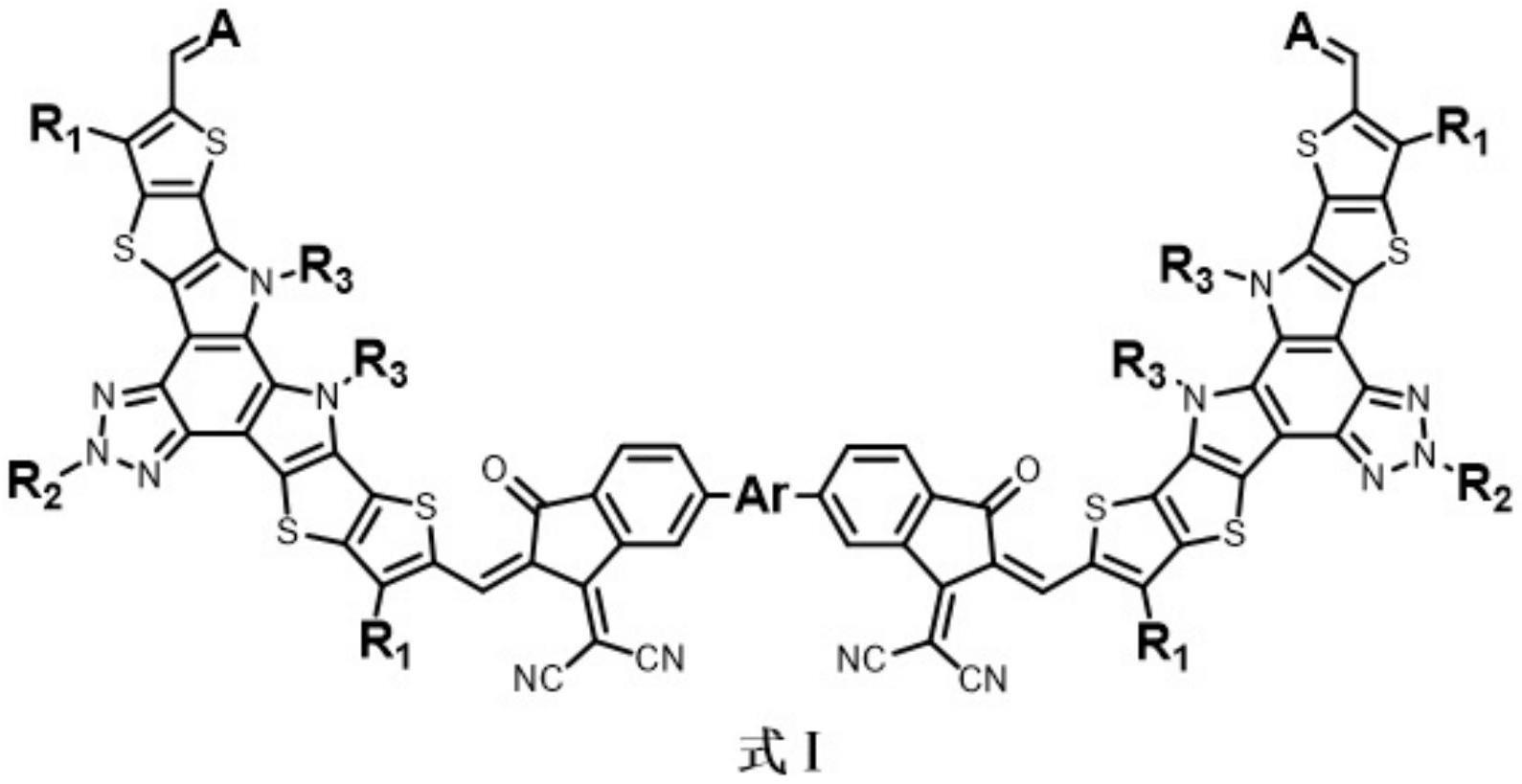
6、本发明的第一方面,提出了一种非富勒烯受体材料,其化学式如式i所示:
7、
8、其中,r1、r2和r3每次出现,均独立地选自取代或未取代的c1~30的烷基、取代或未取代的c1~30的烷氧基、取代或未取代的c2~10的烯基、取代或未取代的c2~30的炔基、取代或未取代的c6~30的芳基;
9、a每次出现,独立地选自取代或未取代的c8~30的稠合芳基的环状基团、取代或未取代的c6~30的稠合杂芳基的环状基团、取代或未取代的c4~30的杂环基;
10、ar选自取代或未取代的c6~30的芳基、取代或未取代的c4~30的杂芳基。
11、根据本发明实施例的非富勒烯受体材料,至少具有以下有益效果:
12、本发明中的非富勒烯受体材料为一种新型的螺旋型的受体材料,在太阳能电池中有良好的应用前景。将其应用于太阳能电池中,所得太阳能电池的短路电流大、光电转换效率高。该螺旋型的受体材料为a-π-a型“准大分子”受体材料,在螺旋型的受体单体与π桥单元之间存在着可旋转的σ单键,优化分子在电池薄膜中的堆积。同时,该螺旋型的受体材料不仅可以保留小分子受体(除ar之外的部分)的优异性能,而且还可以实现更长的器件寿命,可以兼顾“聚合物高稳定性及成膜性和小分子高纯度”的优点,进而有利于大面积印刷制备有机太阳能电池模组。且该螺旋型的受体材料与现有的常见如pm6:l8-bo等二元体系具有更加匹配的能级,可作为第三组分应用于有机光伏电池,得到具有低非辐射复合损失的有机光伏电池三元等多元材料体系。
13、因此该类非富勒烯受体材料不仅可以提高光伏性能,优化相应光伏电池的薄膜形态,而且可以降低器件非辐射重组损失,从而全方面提升光伏性能,可应用于制备高效率、大面积有机光伏电池、有机发光二极管和钙钛矿太阳能电池等,且该类螺旋型非富勒烯受体材料可溶于氯仿、氯苯等常用溶剂,易于加工制备光伏器件,且制备原料易得,成本低,因此,本发明中的非富勒烯受体材料为构筑高效稳定的有机太阳能电池提供了新思路,对制备低成本、大面积有机太阳电池,推动其商业化进程具有重要意义。
14、在本发明的一些实施方式中,r2与r3相同。
15、在本发明的一些实施方式中,所述卤素包括氟、氯、溴或碘中的至少一种。
16、在本发明的一些实施方式中,所述ar选自取代或未取代苯基、取代或未取代联萘基、取代或未取代噻吩基。
17、在本发明的一些实施方式中,所述ar选自如下所示基团中的一种:
18、
19、其中,r4每次出现,独立地选自卤素取代或未取代的c1~15的烷基、卤素取代或未取代的c1~15的烷氧基;x0每次出现,独立地选自卤素、卤素取代或未取代的c1~15的烷基、卤素取代或未取代的c1~15的烷氧基。
20、在本发明的一些实施方式中,所述r4每次出现,独立地选自c4~10的烷基、c4~10的烷氧基。
21、在本发明的一些实施方式中,所述r4每次出现,独立地选自c6~8的烷基、c6~8的烷氧基。
22、在本发明的一些实施方式中,所述r4每次出现,独立地选自2-乙基己基氧基、己基氧基。
23、在本发明的一些实施方式中,x0每次出现,独立地选自氟、氯、溴或碘。
24、在本发明的一些实施方式中,所述a每次出现,独立地选自如下所示基团中的一种:
25、
26、其中,x1和x2每次出现,独立地选自h、卤素、氰基、卤素取代或未取代的c1~30的烷基、卤素取代或未取代的c1~30的烷氧基;r5选自h、卤素取代或未取代的c1~30的烷基、卤素取代或未取代的c1~30的烷氧基。
27、在本发明的一些实施方式中,r5选自c1~5的烷基。
28、在本发明的一些实施方式中,x1和x2每次出现,独立地选自h、卤素、氰基、卤素取代或未取代的c1~5的烷基、卤素取代或未取代的c1~5的烷氧基。
29、在本发明的一些实施方式中,x1和x2每次出现,独立地选自h、卤素、氰基或c1~3的烷基。
30、在本发明的一些实施方式中,所述r1每次出现,独立地选自取代或未取代的c1~15的烷基、取代或未取代的c1~15的烷氧基、取代或未取代的c2~10的烯基、取代或未取代的c2~15的炔基、取代或未取代的c6~15的芳基。
31、在本发明的一些实施方式中,所述r1每次出现,独立地选自c6~15的烷基、c6~15的烷氧基。
32、在本发明的一些实施方式中,所述r1每次出现,独立地选自c8~15的烷基、c8~15的烷氧基。
33、在本发明的一些实施方式中,所述r2每次出现,独立地选自取代或未取代的c5~15的烷基、取代或未取代的c5~15的烷氧基、取代或未取代的c2~10的烯基、取代或未取代的c2~15的炔基、取代或未取代的c6~15的芳基。
34、在本发明的一些实施方式中,所述r2每次出现,独立地选自c5~11的烷基、c5~11的烷氧基。
35、在本发明的一些实施方式中,所述r3每次出现,独立地选自取代或未取代的c5~15的烷基、取代或未取代的c5~15的烷氧基、取代或未取代的c2~10的烯基、取代或未取代的c2~15的炔基、取代或未取代的c6~15的芳基。
36、在本发明的一些实施方式中,所述r3每次出现,独立地选自c5~11的烷基、c5~11的烷氧基。
37、在本发明的一些实施方式中,所述非富勒烯受体材料选自以下化学式中的至少一种:
38、
39、
40、其中,x1和x2每次出现,独立地选自h、卤素、氰基或c1~3的烷基。
41、在本发明的一些实施方式中,所述非富勒烯受体材料选自以下化学式中的至少一种:
42、
43、
44、
45、本发明的第二方面,提出了一种非富勒烯受体材料的制备方法,包括如下步骤:式ⅱ化合物与含ar基团的硼酸酯或含ar基团的硼酸,经suzuki偶联反应,制得所述非富勒烯受体材料,其中,化合物ⅱ、含ar基团的硼酸酯的结构式如下所示:
46、
47、根据本发明实施例的非富勒烯受体材料的制备方法,至少具有以下有益效果:
48、本发明通过选择具有高性能、低能量无序度小分子受体为前驱体,两个受体分子再通过不同螺旋功能化“π桥”相连,制备出具有确定分子量的a-π-a型“准大分子”受体材料,为螺旋型非富勒烯受体材料。该受体材料可以提高光吸收能力,优化薄膜形态和降低器件非辐射复合损失。这种类型的“准大分子”受体材料可以兼顾“聚合物高稳定性及成膜性和小分子高纯度”的优点,进而有利于大面积印刷制备有机太阳能电池模组,应用前景好。
49、在本发明的一些实施方式中,所述制备方法包括如下步骤:
50、取式ⅱ化合物与含ar基团的硼酸酯、有机溶剂ⅰ,加入催化剂ⅰ,经suzuki偶联反应,得到所述非富勒烯受体材料。
51、在本发明的一些实施方式中,所述催化剂ⅰ包括四(三苯基膦)钯、醋酸钯、双(三苯基膦)二氯化钯、三(二亚苄基丙酮)二钯和三(邻甲苯基)膦或碘化亚铜中的至少一种。
52、在本发明的一些实施方式中,所述有机溶剂ⅰ包括甲苯、四氢呋喃、n,n-二甲基甲酰胺、二氯甲烷、1,4-二氧六环或二甲亚砜中的至少一种。
53、在本发明的一些实施方式中,所述suzuki偶联反应的反应时间为15-50h,反应温度为70-130℃。
54、在本发明的一些实施方式中,所述suzuki偶联反应在保护气体氛围下进行。
55、在本发明的一些实施方式中,经suzuki偶联反应后,得到混合物ⅰ,纯化,得到所述非富勒烯受体材料。
56、在本发明的一些实施方式中,所述纯化包括干燥、萃取和层析。
57、在本发明的一些实施方式中,经suzuki偶联反应后,得到混合物ⅰ,除去有机溶剂ⅰ,萃取,硅胶柱层析,得到所述非富勒烯受体材料。
58、在本发明的一些实施方式中,所述萃取采用的萃取剂包括二氯甲烷。
59、在本发明的一些实施方式中,所述制备方法还包括制备式ⅱ化合物,具体包括如下操作:取式ⅲ化合物、含a基团的化合物h-a-h、5-卤-3-(二氰基亚甲基)靛酮,经knoevenagel反应,制得式ⅱ化合物,其中,化合物ⅲ的结构式如下所示:
60、
61、在本发明的一些实施方式中,所述含a基团的化合物h-a-h选自如下化合物中的至少一种:
62、
63、在本发明的一些实施方式中,所述5-卤-3-(二氰基亚甲基)靛酮包括5-氟-3-(二氰基亚甲基)靛酮、5-溴-3-(二氰基亚甲基)靛酮中的至少一种。
64、在本发明的一些实施方式中,所述knoevenagel反应的反应时间为10-36h,和/或,反应温度为60-130℃。
65、在本发明的一些实施方式中,制备式ⅱ化合物具体包括如下操作:
66、取式ⅲ化合物、含a基团的化合物h-a-h、5-卤-3-(二氰基亚甲基)靛酮和有机溶剂ⅱ,加入吡啶,经knoevenagel反应,得到式ⅱ化合物。
67、在本发明的一些实施方式中,所述knoevenagel反应在保护气体氛围下进行。
68、在本发明的一些实施方式中,经knoevenagel反应后,得到混合物ⅱ,纯化,得到式ⅱ化合物。
69、在本发明的一些实施方式中,所述纯化包括将混合物ⅱ和提纯溶剂ⅰ混合,分离得到粗产物,柱层析,得到式ⅱ化合物。
70、在本发明的一些实施方式中,所述提纯溶剂ⅰ包括甲醇、丙酮或乙醚中的至少一种。
71、在本发明的一些实施方式中,所述有机溶剂ⅱ包括氯仿、n,n-二甲基甲酰胺、甲苯、四氢呋喃、二氯甲烷、1,4-二氧六环或二甲亚砜中的至少一种。
72、在本发明的一些实施方式中,所述制备方法还包括制备式ⅲ化合物,具体包括如下操作:取式ⅳ化合物,经vilsmeier-haack反应,制得式ⅲ化合物;
73、其中,式ⅳ化合物的结构式如下所示:
74、
75、在本发明的一些实施方式中,所述vilsmeier-haack反应的反应时间为10-36h,和/或,反应温度为80-130℃。
76、在本发明的一些实施方式中,制备式ⅲ化合物步骤中,包括如下操作:取式ⅳ化合物、n,n-二甲基甲酰胺(dmf)和有机溶剂ⅲ,保护气体氛围下加入pocl3,回流反应,得到所述式ⅲ化合物。
77、在本发明的一些实施方式中,制备式ⅲ化合物步骤中,所述回流反应结束后,萃取,色谱柱纯化,制得式ⅲ化合物。
78、在本发明的一些实施方式中,所述有机溶剂ⅲ包括1,2-二氯乙烷、甲苯、四氢呋喃、n,n-二甲基甲酰胺、二氯甲烷、1,4-二氧六环或二甲亚砜中的至少一种。
79、在本发明的一些实施方式中,所述制备方法还包括制备式ⅳ化合物,具体包括如下操作:取式ⅴ化合物、亚磷酸三乙酯和含r3基团的化合物r3-br,保护气体氛围下反应,得到式ⅳ化合物;
80、其中,式ⅴ化合物的结构式如下所示:
81、
82、在本发明的一些实施方式中,在制备式ⅳ化合物步骤中,包括如下操作:
83、取式ⅴ化合物、亚磷酸三乙酯和二氯苯,反应,得到中间体;
84、取所述中间体、含r3基团的化合物r3-br和有机溶剂ⅳ,保护气体氛围下回流反应,得到式ⅳ化合物。
85、在本发明的一些实施方式中,回流反应的反应时间为10-36h,和/或,反应温度为90-130℃。
86、在本发明的一些实施方式中,所述有机溶剂ⅳ包括氯苯、甲苯、n,n-二甲基甲酰胺、二氯甲烷、1,4-二氧六环或二甲亚砜中的至少一种。
87、在本发明的一些实施方式中,将中间体与k2co3、ki、2-丁基-1-溴辛烷和无水dmf混合,保护气体氛围下搅拌,萃取,色谱柱纯化,得到式ⅳ化合物。
88、在本发明的一些实施方式中所述制备方法还包括制备式ⅴ化合物,具体包括:取式ⅵ化合物和式ⅶ化合物,经stille偶联反应,制得式ⅴ化合物,其中,式ⅵ化合物和式ⅶ化合物的结构式如下所示:
89、
90、在本发明的一些实施方式中,所述stille偶联反应的反应时间为15-36h,反应温度为100-130℃。
91、在本发明的一些实施方式中,制备式ⅴ化合物,具体包括:取式ⅵ化合物、式ⅶ化合物和有机溶剂ⅴ,加入催化剂ⅱ,经stille偶联反应,制得式ⅴ化合物。
92、在本发明的一些实施方式中,所述stille偶联反应在保护气体氛围中进行。
93、在本发明的一些实施方式中,所述催化剂ⅱ包括四(三苯基膦)钯、醋酸钯、双(三苯基膦)二氯化钯、三(二亚苄基丙酮)二钯和三(邻甲苯基)膦或碘化亚铜中的至少一种。
94、在本发明的一些实施方式中,所述有机溶剂ⅴ包括甲苯、四氢呋喃、n,n-二甲基甲酰胺、二氯甲烷、1,4-二氧六环或二甲亚砜中的至少一种。
95、在本发明的一些实施方式中,制备式ⅴ化合物,具体包括:经stille偶联反应后,除去有机溶剂ⅴ,萃取,色谱柱纯化,得到式ⅴ化合物。
96、在本发明的一些实施方式中,所述制备方法包括如下步骤:
97、s1,取式ⅵ化合物和式ⅶ化合物,经stille偶联反应,制得式ⅴ化合物;
98、s2,取式ⅴ化合物、亚磷酸三乙酯和含r3基团的化合物r3-br,保护气体氛围下回流反应,得到式ⅳ化合物;
99、s3,取式ⅳ化合物,经vilsmeier-haack反应,制得式ⅲ化合物;
100、s4,取式ⅲ化合物、含a基团的化合物h-a-h、5-卤-3-(二氰基亚甲基)靛酮,经knoevenagel反应,制得式ⅱ化合物;
101、s5,式ⅱ化合物与含ar基团的硼酸酯或含ar基团的硼酸,经suzuki偶联反应,制得所述非富勒烯受体材料。
102、反应过程如下所示:
103、
104、其中,x3为卤素。
105、本发明的第三方面,提出了一种光伏器件用活性材料,包括受体材料ⅰ,所述受体材料ⅰ为上述非富勒烯受体材料。
106、在本发明的一些实施方式中,所述光伏器件用活性材料还包括给体材料和受体材料ⅱ。
107、在本发明的一些实施方式中,所述给体材料包括pm6、pbtb-t-2f、pbdb-t、d18或ptq-10中的至少一种。
108、在本发明的一些实施方式中,所述受体材料ⅱ包括y6、l8-bo或btp-ec9中的至少一种。
109、通过上述实施方式,光伏器件用活性材料为含上述非富勒烯受体材料、给体材料和受体材料ⅱ的三元体系材料有机光伏电池的活性层。
110、在本发明的一些实施方式中,所述给体材料、所述非富勒烯受体材料和所述受体材料ⅱ的质量比为1:(0.08-0.12):(1-1.3),优选为1:0.1:1.2。
111、本发明的第四方面,提出了一种光伏器件,包括上述非富勒烯受体材料或上述光伏器件用活性材料。
112、在本发明的一些实施方式中,所述光伏器件包括活性层,所述活性层包括所述非富勒烯受体材料或所述光伏器件用活性材料。
113、在本发明的一些实施方式中,所述光伏器件为光伏电池。
114、在本发明的一些实施方式中,所述光伏电池为有机光伏电池。
115、在本发明的一些实施方式中,所述光伏电池包括层叠设置的基底、空穴传输层、活性层、电子传输层和电极层。
116、在本发明的一些实施方式中,所述基底为ito玻璃基底。
117、在本发明的一些实施方式中,所述电极层为金属电极层。
118、在本发明的一些实施方式中,所述基底的厚度为0.01-1mm,比如为0.2mm。
119、在本发明的一些实施方式中,所述空穴传输层的厚度为10-200nm。
120、在本发明的一些实施方式中,所述活性层的厚度为为50-200nm。
121、在本发明的一些实施方式中,所述电子传输层的厚度为2-50nm。
122、在本发明的一些实施方式中,所述电极层的厚度为50-300nm。
123、本发明的第五方面,提出了上述非富勒烯受体材料或光伏器件用活性材料在制备有机光伏电池、有机发光二极管或钙钛矿太阳能电池中的应用。
124、说明和定义
125、在本发明中,除非另有说明,否则本文中所使用的科学和技术名词具有本领域技术人员通常所理解的含义,然而为了更好的理解本发明,下面提供了部分术语的定义。当本发明提供的术语的定义与本领域技术人员所通常理解的含义不相符时,以本发明所提供的术语的定义和解释为准。
126、本文的“保护气体氛围”中的保护气体包括惰性气体或氮气中的至少一种。所述惰性气体可为氩气。
127、本文使用的“取代或未取代的”是指基团可以被或可以不被一个或更多个选自以下的基团进一步取代:烷基、烯基、炔基、芳基、卤素、卤代烷基、卤代烯基、卤代炔基、卤代芳基、羟基、烷氧基、烯氧基、芳氧基、苄氧基、卤代烷氧基、卤代烯氧基、卤代芳氧基、硝基、硝基烷基、硝基烯基、硝基炔基、硝基芳基、硝基杂环基、氨基、烷基氨基、二烷基氨基、烯基氨基、炔基氨基、芳基氨基、二芳基氨基、苯基氨基、二苯基氨基、苄基氨基、二苄基氨基、肼基、酰基、酰氨基、二酰氨基、酰氧基、杂环基、杂环氧基、杂环基氨基、卤代杂环基、羧基酯、羧基、羧基酰胺、巯基、烷硫基、苄硫基、酰硫基和含磷基团。
128、“烷基”是指具有指定碳原子数的支链或直链饱和脂肪族烷烃去掉一个氢衍生的基团。“c1~30的烷基”表示碳原子总数为1~30的烷基,包括c1~30的直链烷基、c1~30的支链烷基和c3~30的环烷基;针对“c1~15的烷基”、“c4~10的烷基”、“c1~5的烷基”等具有与此相似的解释,所不同的是,碳原子数不同。“取代的c1~30的烷基”表示c1~30的任选的烷基中至少有一个h被本文定义的基团所取代,针对“取代的c1~15的烷基”、“取代的c4~10的烷基”、“取代的c1~5的烷基”等具有与此相似的解释,所不同的是,碳原子数不同。
129、“烷氧基”是指本文所定义的烷基通过氧原子与其他基团相连,即“烷基-o-”。“c1~30的烷氧基”表示碳原子总数为1~30的烷氧基,包括c1~30的直链烷氧基、c1~30的支链烷氧基和c2~30的环烷氧基,例如可以为甲氧基、乙氧基、正丙氧基、异丙氧基等。针对“c1~15的烷氧基”、“c4~10的烷氧基”等具有与此相似的解释,所不同的是,碳原子数不同。“取代的c1~30的烷氧基”表示c1~30的任选的烷氧基中至少有一个h被本文定义的基团所取代,针对“取代的c1~15的烷氧基”、“c4~10的烷氧基”等具有与此相似的解释,所不同的是,碳原子数不同。
130、“卤素”包括氟、氯、溴、碘中的任意一个或两个以上。
131、“c2~10的烯基”表示具有一个或多个双键的直链或支链的烃基,且烯基的碳原子总数为2~10,基团中的双键可以在任意位置。“取代的c2~10的烯基”表示c2~10的任选的烯基中至少有一个h被本文定义的基团所取代。
132、“c2~30的炔基”表示具有一个或多个三键的直链或支链的烃基,且炔基的碳原子总数为2~30,基团中的三键可以在任意位置,“c2-15的炔基”等具有与此相似的解释,所不同的是,碳原子数不同。“取代的c2~30的炔基”表示c2~30的任选的炔基中至少有一个h被本文定义的基团所取代,“取代的c2-15的炔基”等具有与此相似的解释,所不同的是,碳原子数不同。
133、“c6~30的芳基”表示全碳单环或稠合多环基团,具有完全共轭的π电子系统。表示6至30个碳原子的全碳单环或稠合多环基团;例如,苯、萘、茚、芴等。c6-15的芳基”等具有与此相似的解释,所不同的是,碳原子数不同。“取代的c6~30的芳基”表示c6~30的任选的芳基中有至少一个h被本文定义的相应基团所取代。“取代的c6-15的芳基”等具有与此相似的解释,所不同的是,碳原子数不同。
134、“c8~30的稠合芳基的环状基团”表示芳基和环状基团通过共用环边形成的基团,且稠合芳基的环状基团的碳原子数为8~30。“取代的c8~30的稠合芳基的环状基团”表示c8~30的任选的稠合芳基的环状基团中至少有一个h被本文定义的基团所取代。
135、“c6~30的稠合杂芳基的环状基团”表示杂芳基和环状基团通过共用环边形成的基团,且稠合杂芳基的环状基团的碳原子数为6~30。“取代的c6~30的稠合杂芳基的环状基团”表示c6~30的任选的稠合杂芳基的环状基团中至少有一个h被本文定义的基团所取代。
136、“杂环基”是指环烷基中的环碳原子被一个或多个杂原子取代所衍生的饱和环状基团,包括单环或多环杂环基;所述的多环杂环基是指由一个单环杂环基与其他杂环基或环烷基通过螺、桥、稠等方式连接形成的多环基团;所述的杂原子一般选自n、o、s;所述杂环基中的碳原子或杂原子可以进一步被氧代,即形成c(o)、n(o)、so、so2。
137、“c4~30的杂环基”表示杂环基的碳原子数为4~30。“取代的c4~30的杂环基”表示c4~30的任选的杂环基中至少有一个h被本文定义的基团所取代。
138、“杂芳基”指环中包含一至多个杂原子的、具有芳香性的单环或多环基团,所述杂原子一般选自n、o、s;优选地,所述的杂原子独立的选自1-3个n和/或o,另外,n原子和s原子可任选被氧化且n原子可任选被季铵化。所述“杂芳基”包括“单环杂芳基”和“稠环杂芳基”,所述的稠环杂芳基是指两个或两个以上环状结构彼此共用两个相邻的原子所形成的包含一至多个杂原子的、整体具有芳香性的基团。
139、“c4~30的杂芳基”中杂芳基的碳原子数为4~30。“取代的c4~30的杂芳基”表示c4~30的任选的杂芳基中至少有一个h被本文定义的基团所取代。
140、本发明的其它特征和优点将在随后的说明书中阐述,并且,部分地从说明书中变得显而易见,或者通过实施本发明而了解。
- 还没有人留言评论。精彩留言会获得点赞!