在分配中使用微粒的多路技术的制作方法
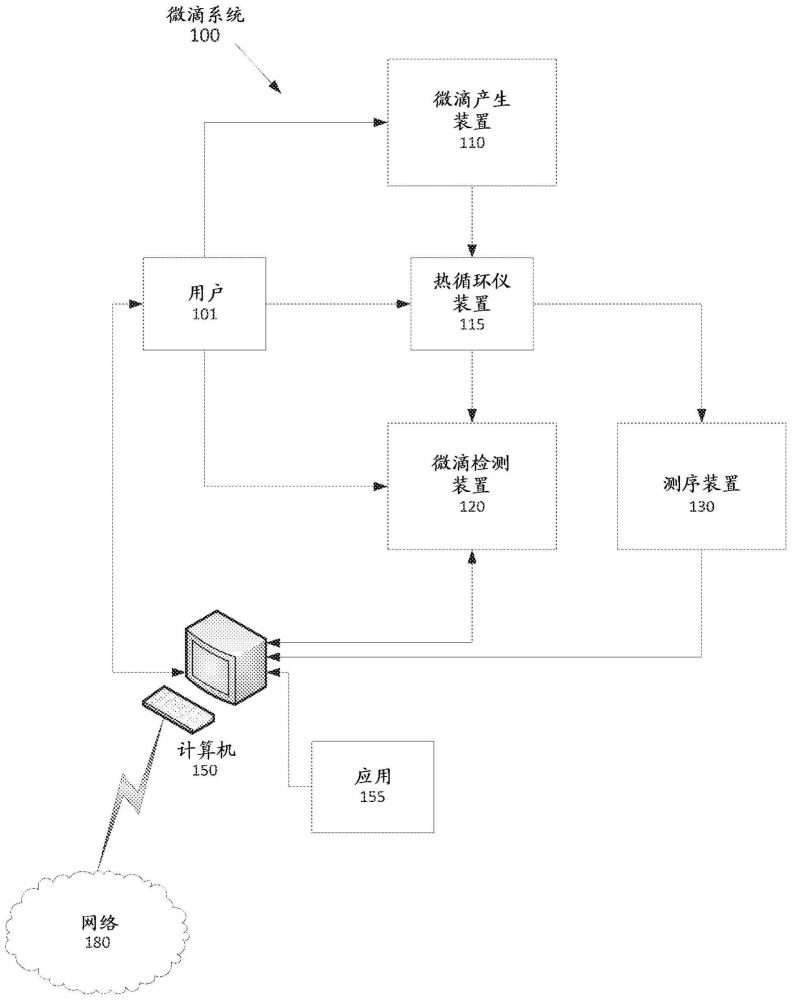
发明领域本发明总体上涉及包含一个或多个引物载体的微滴和其使用方法。背景已经开发在不混溶流体中产生微滴的微流体技术并用于许多目的,包括以大规模平行形式进行各种生物化学反应。微流体技术提供超过之前使用的大量微滴产生方法的重大进步,后者包括以多路方式在微滴中进行pcr反应,其中各自针对不同的靶区域的多个引物种类存在于微滴中。然而,一个困难是如何以可使可用微滴的使用最大化的方式控制引物种类和样品在微滴中的分布。例如,一些实施方案借助于使用将样品和可溶性试剂预合并成水性溶液的方法,所述水溶溶液用于在不混溶流体中形成微滴。除了控制在水性溶液中的初始浓度之外,这些方法不提供对试剂在微滴中的分布的控制。或者,一些实施方案采用以下策略:其提供通过合并第一微滴(例如,含有引物种类)与第二微滴和/或流体流(例如,含有样品)的试剂分布控制以控制试剂递送至微滴中,但这样的方法需要复杂和昂贵的微流体平台。因此,高度需要简化的、成本有效的和可适用的方法来有效产生具有需要的试剂分布的微滴。简述本发明的实施方案涉及核酸扩增和测序的领域。更具体地,本发明的实施方案涉及包含一个或多个引物载体的微滴。在一个方面,本文提供了式(i)的微粒:其中是生物学分子;m是0-100的整数,包括0和100;n是0-100的整数,包括0和100;r1是结合部分,其选自键、任选取代的亚烷基、任选取代的杂亚烷基、任选取代的亚烯基、任选取代的杂亚烯基、任选取代的亚炔基、任选取代的杂亚炔基、任选取代的杂亚环基、任选取代的杂亚芳基,和r2和r3各自独立地是氢、取代或未取代烷基或氮保护基。在某些实施方案中,式(i)的微粒具有式(ii):其中r4是任选取代的亚烷基、任选取代的亚烯基、任选取代的亚炔基、任选取代的杂亚环基或任选取代的杂亚芳基。在某些实施方案中,式(i)的微粒具有式(ii-a):其中p是1-5的整数,包括1和5。在某些实施方案中,式(i)的微粒具有式(ii-b):在某些实施方案中,本文提供了制备式(i)的微粒的方法,包括使式(i)的化合物:与至少一种式(ii)的化合物:或其盐接触。在某些实施方案中,制备式(i)的微粒的方法进一步包括使式(iii)的化合物:与至少一种式(iv)的化合物:或其盐接触。在另一方面,本文提供了包含多个生物学分子的微粒,其中每个生物学分子通过结合部分结合至微粒。在生物学分子和结合部分之间的相互作用可以是一个或多个共价键或氢键。在某些实施方案中,结合部分通过click反应形成。在某些实施方案中,结合部分包含三唑部分。在某些实施方案中,生物学分子是核酸。在某些实施方案中,生物学分子是dna或rna。在某些实施方案中,生物学分子是约3-约30个碱基长度的寡核苷酸序列。在某些实施方案中,生物学分子是约15-约25个碱基长度的寡核苷酸序列。在某些实施方案中,生物学分子是引物成员。在某些实施方案中,生物学分子是约15-约25个碱基长度的dna序列。在另一方面,本文提供了包含多个微滴的微滴库,所述微滴各自包含核酸模板分子和多个引物载体,其中每个引物载体包含通过多个结合部分结合至微粒的多个引物种类,其中每个引物种类对核酸模板分子的不同靶位点是特异性的。在某些实施方案中,引物种类是引物对。在某些实施方案中,引物种类是引物对的成员。在某些实施方案中,引物种类是单个寡核苷酸。在某些实施方案中,单个寡核苷酸进一步包含条码。在某些实施方案中,条码对每个微滴是独特的和在微滴之间不同。在某些实施方案中,引物种类包含条码和随机六聚体。在某些实施方案中,引物种类包含条码和通用序列。在某些实施方案中,引物种类包含条码、通用序列和靶特异性序列。在某些实施方案中,引物种类是三联体,包含通用尾部分(例如,用于测序库构建的寡核苷酸序列),紧接条码序列的5',接着一组能够从基因组的多个位置引发的随机六聚体碱基之一。在另一方面,本文提供了包含本文所述的多个引物载体的引物载体库。本文进一步提供了包含多个微滴的微滴库,每个微滴包含核酸模板分子和多个引物载体,其中每个引物载体包含通过多个结合部分结合至微粒的多个引物对,其中每个引物对对核酸模板分子是特异性的和包含各自对核酸模板分子上的不同靶位点特异性的两个成员。在某些实施方案中,至少一个微滴包含两个或更多个核酸模板分子。在某些实施方案中,至少一个微滴包含单个核酸模板分子。在某些实施方案中,至少一个引物种类对至少一个微滴中的核酸模板分子上的靶位点是特异性的。在某些实施方案中,引物对的至少一个成员对至少一个微滴中的核酸模板分子上的靶位点是特异性的。在某些实施方案中,至少一个引物种类对每个微滴中的核酸模板是特异性的。在某些实施方案中,至少一个引物种类对每个微滴中的核酸模板是特异性的。在某些实施方案中,至少一个引物对对每个微滴中的核酸模板是特异性的。在某些实施方案中,至少两个引物对各自对每个微滴中的核酸模板是特异性的。在某些实施方案中,至少两个引物种类各自对每个微滴中的核酸模板是特异性的。微粒各自可用至少一个结合部分官能化。结合部分可与引物种类形成一个或多个键。在某些实施方案中,引物种类可通过结合部分连接至微粒。在某些实施方案中,引物种类可通过形成例如氢键,与结合部分杂交。在某些实施方案中,微滴中的结合部分是相同的。在某些实施方案中,微滴中的至少一个结合部分是不同的。在某些实施方案中,结合部分包含与引物种类互补的序列。在某些实施方案中,结合部分包含多聚-丙氨酸序列。在某些实施方案中,每个微滴含有至多约200个引物载体。在某些实施方案中,每个微滴含有至多约100个引物载体。在某些实施方案中,每个微滴含有至多约90个引物载体。在某些实施方案中,每个微滴含有至多约80个引物载体。在某些实施方案中,每个微滴含有至多约70个引物载体。在某些实施方案中,每个微滴含有至多约60个引物载体。在某些实施方案中,每个微滴含有至多约50个引物载体。在某些实施方案中,每个微滴含有约10-约50个引物载体。在某些实施方案中,每个微滴含有约10-约30个引物载体。在某些实施方案中,每个微滴含有约25个引物载体。在某些实施方案中,每个微滴含有约5-约10个引物载体。引物载体是包含通过多个结合部分结合至微粒的多个引物种类的复合物。在某些实施方案中,引物载体是包含通过多个结合部分结合至微粒的多个引物对的复合物。在某些实施方案中,引物载体包含至少一个引物种类。在某些实施方案中,引物载体包含至少一个引物对。在某些实施方案中,引物载体具有单个结合的引物种类。在某些实施方案中,引物载体具有单个结合的引物对。在某些实施方案中,引物载体具有单个结合的寡核苷酸。在某些实施方案中,引物载体具有单个结合的引物种类的多个拷贝。在某些实施方案中,引物载体具有不同结合的引物种类。在某些实施方案中,引物载体具有不同结合的引物种类。在某些实施方案中,引物载体具有不同结合的引物对。在某些实施方案中,引物载体具有至少两个不同结合的引物种类。在某些实施方案中,引物载体具有至少三个不同结合的引物种类。在某些实施方案中,引物载体具有至少四个不同结合的引物种类。在某些实施方案中,引物载体具有至少五个不同结合的引物种类。在某些实施方案中,引物载体具有至少两个不同结合的引物对。在某些实施方案中,引物载体具有至少三个不同结合的引物对。在某些实施方案中,引物载体具有至少四个不同结合的引物对。在某些实施方案中,引物载体具有至少五个不同结合的引物对。在某些实施方案中,微滴中的每个引物载体具有单个结合的引物种类。在某些实施方案中,微滴中的每个引物载体具有单个结合的引物对。在某些实施方案中,微滴中的每个引物载体具有单个结合的引物种类的多个拷贝。在某些实施方案中,微滴中的每个引物载体具有单个结合的引物对的多个拷贝。在某些实施方案中,微滴中的每个引物载体具有不同结合的引物种类。在某些实施方案中,微滴中的每个引物载体具有不同结合的引物对。在某些实施方案中,微滴中的每个引物载体具有至少两个不同结合的引物种类。在某些实施方案中,微滴中的每个引物载体具有至少两个不同结合的引物对。在某些实施方案中,微滴中的每个引物载体具有至少三个不同结合的引物种类。在某些实施方案中,微滴中的每个引物载体具有至少三个不同结合的引物对。在某些实施方案中,微滴中的每个引物载体具有至少四个不同结合的引物种类。在某些实施方案中,微滴中的每个引物载体具有至少四个不同结合的引物对。在某些实施方案中,微滴中的每个引物载体具有至少五个不同结合的引物种类。在某些实施方案中,微滴中的每个引物载体具有至少五个不同结合的引物对。在某些实施方案中,每个微滴具有多个相同的引物载体。“相同的引物载体”意思是相同的微粒各自具有相同结合的引物种类。在某些实施方案中,每个微滴具有多个相同的引物载体,各自具有相同的单个结合的引物种类。在某些实施方案中,每个微滴具有多个相同的引物载体,其中每个引物载体包含不同结合的引物种类。在某些实施方案中,每个微滴具有多个不同的引物载体。“不同的引物载体”意思是微粒在引物载体之间是不同的,或者,一个或多个结合的引物种类在引物载体之间是不同的。在某些实施方案中,每个微滴具有多个不同的引物载体,其中每个引物载体包含不同结合的引物种类。在某些实施方案中,多个微滴中的至少一个微滴具有至少一个在微滴之间不同的引物载体。在某些实施方案中,在微滴之间不同的引物载体包含不同的单个结合的引物种类。在某些实施方案中,在微滴之间不同的引物载体包含不同结合的引物种类。在某些实施方案中,在触发事件后引物种类从引物载体释放。例如,在触发事件后,结合部分和引物种类之间的相互作用可完全或部分破坏。示例的触发源(trigger)包括但不限于化学触发源(例如,ph触发源)、生物学触发源(例如,酶触发源)、热触发源、电触发源、照射触发源和/或磁触发源。在某些实施方案中,触发源是升高的温度、uv和/或超声波。在某些实施方案中,触发源是升高的温度。在某些实施方案中,升高的温度低于聚合酶链反应(pcr)的变性温度。在某些实施方案中,升高的温度低于约90℃。在某些实施方案中,升高的温度低于约85℃。在某些实施方案中,升高的温度低于约80℃。在某些实施方案中,多个微滴进一步包含多个探针,其中每个探针杂交至靶位点之一中的特定区域。在某些实施方案中,单个核酸模板是dna或rna分子。在某些实施方案中,多个微滴进一步包含用于进行扩增反应,即聚合酶链反应(pcr)的试剂。在某些实施方案中,探针含有可检测标记。在某些实施方案中,至少一个探针包含不同的可检测标记。在某些实施方案中,微粒是珠。珠可进一步包含聚合物。在某些实施方案中,珠包含自装配dna纳米颗粒。在某些实施方案中,珠是顺磁性的或超-顺磁性的。在某些实施方案中,珠具有官能化的表面。在某些实施方案中珠经官能化以包含结合部分。在某些实施方案中,结合部分是链霉亲和素。在某些实施方案中珠具有二氧化硅外壳。在某些实施方案中,珠的直径是约1-约1000纳米。在某些实施方案中,珠的直径是约1-约500纳米。在某些实施方案中,珠的直径是约1-约100纳米。在某些实施方案中珠的直径是约1-约90微米。在某些实施方案中珠的直径是约1-约80微米。在某些实施方案中珠的直径是约1-约70微米。在某些实施方案中珠的直径是约1-约60微米。在某些实施方案中珠的直径是约1-约50微米。在某些实施方案中珠的直径是约1-约40微米。在某些实施方案中珠的直径是约1-约30微米。在某些实施方案中珠的直径是约1-约20微米。在某些实施方案中珠的直径是约1-约10微米。应理解,当微滴包含单个核酸模板时,微滴可包含超过一个核酸分子。在某些实施方案中,核酸模板分子是dna或rna。在某些实施方案中,本文所述的多个微滴各自进一步包含用于进行聚合酶链反应的试剂。在某些实施方案中,每个微滴进一步包含探针。在某些实施方案中,探针包含可检测标记。本文所述的多个微滴可被不混溶载体围绕。在某些实施方案中,不混溶载体是油。在某些实施方案中,不混溶载体是氟烃油(例如,全氟烃油)。在某些实施方案中,微粒具有引物种类的约102-约1010个成员的负载能力。在某些实施方案中,微粒具有引物种类的约102-约109个成员的负载能力。在某些实施方案中,微粒具有引物种类的约102-约108个成员的负载能力。在某些实施方案中,微粒具有引物种类的约102-约107个成员的负载能力。在某些实施方案中,微粒具有引物种类的约102-约106个成员的负载能力。在某些实施方案中,微粒具有引物种类的约102-约105个成员的负载能力。在某些实施方案中,微粒具有引物种类的约102-约104个成员的负载能力。在某些实施方案中,微粒具有引物种类的约102-约103个成员的负载能力。在某些实施方案中,微粒具有引物种类的约103-约109个成员的负载能力。在某些实施方案中,微粒具有引物种类的约104-约108个成员的负载能力。在某些实施方案中,微粒具有引物种类的约105-约107个成员的负载能力。在某些实施方案中,微粒是具有至少1.0百万个结合的引物种类的珠。在某些实施方案中,微粒是具有至少1千万个结合的引物种类的珠。提供的引物载体库对于贮存可为稳定的。在某些实施方案中,提供的引物载体库在室温下稳定超过3天。在某些实施方案中,提供的引物载体库在室温下稳定超过1周。在某些实施方案中,提供的引物载体库在室温下稳定超过2周。在某些实施方案中,提供的引物载体库在室温下稳定超过3周。在某些实施方案中,提供的引物载体库在室温下稳定超过4周。在某些实施方案中,提供的引物载体库在室温下稳定超过2个月。在某些实施方案中,提供的引物载体库在室温下稳定超过3个月。在某些实施方案中,提供的引物载体库在室温下稳定超过3天。在某些实施方案中,提供的引物载体库在4℃稳定超过1周。在某些实施方案中,提供的引物载体库在4℃稳定超过2周。在某些实施方案中,提供的引物载体库在4℃稳定超过3周。在某些实施方案中,提供的引物载体库在4℃稳定超过4周。在某些实施方案中,提供的引物载体库在4℃稳定超过2个月。在某些实施方案中,提供的引物载体库在4℃稳定超过3个月。在某些实施方案中,提供的引物载体库在低于0℃下稳定超过1周。在某些实施方案中,提供的引物载体库在0℃下稳定超过2周。在某些实施方案中,提供的引物载体库在0℃下稳定超过3周。在某些实施方案中,提供的引物载体库在0℃下稳定超过4周。在某些实施方案中,提供的引物载体库在0℃下稳定超过2个月。在某些实施方案中,提供的引物载体库在0℃下稳定超过3个月。在某些实施方案中,提供的引物载体库在0℃下稳定超过1年。在某些实施方案中,提供的引物载体库在0℃下稳定超过3年。提供的微滴库可对于贮存可为稳定的。在某些实施方案中,提供的微滴库在室温下稳定超过3天。在某些实施方案中,提供的微滴库在室温下稳定超过1周。在某些实施方案中,提供的微滴库在室温下稳定超过2周。在某些实施方案中,提供的微滴库在室温下稳定超过3周。在某些实施方案中,提供的微滴库在室温下稳定超过4周。在某些实施方案中,提供的微滴库在室温下稳定超过2个月。在某些实施方案中,提供的微滴库在室温下稳定超过3个月。在某些实施方案中,提供的微滴库在室温下稳定超过3天。在某些实施方案中,提供的微滴库在4℃下稳定超过1周。在某些实施方案中,提供的微滴库在4℃下稳定超过2周。在某些实施方案中,提供的微滴库在4℃下稳定超过3周。在某些实施方案中,提供的微滴库在4℃下稳定超过4周。在某些实施方案中,提供的微滴库在4℃下稳定超过2个月。在某些实施方案中,提供的微滴库在4℃下稳定超过3个月。在某些实施方案中,提供的微滴库在低于0℃下稳定超过1周。在某些实施方案中,提供的微滴库在0℃下稳定超过2周。在某些实施方案中,提供的微滴库在0℃下稳定超过3周。在某些实施方案中,提供的微滴库在0℃下稳定超过4周。在某些实施方案中,提供的微滴库在0℃下稳定超过2个月。在某些实施方案中,提供的微滴库在0℃下稳定超过3个月。在某些实施方案中,提供的微滴库在0℃下稳定超过1年。在某些实施方案中,提供的微滴库在0℃下稳定超过3年。在另一方面,本文提供了检测生物学样品中的核酸模板分子的方法,包括以下步骤:a)形成任何一个前述权利要求的多个微滴;b)扩增微滴中的至少一个核酸模板分子以得到扩增产物;和c)测序扩增产物。如本文使用的,扩增是指复制核酸模板的一部分或整个序列。在某些实施方案中,复制可以是从dna至dna或从rna至dna(cdna)。可存在核酸模板的单次复制,可存在核酸模板的线性扩增或核酸模板的指数扩增,例如聚合酶链反应(pcr)或多链置换扩增。用于进行扩增的试剂可包括例如聚合酶、反转录酶、核苷酸、缓冲液等。在某些实施方案中,扩增是线性延伸和引物载体进一步包含条码。在某些实施方案中,引物载体上的引物成员进一步包含条码。条码对于每个微滴是独特的,即在一个微滴内相同,但在微滴之间不同。在某些实施方案中,引物载体上的引物成员进一步包含条码和通用或随机序列。引物种类可经设计以靶向特定序列。引物种类可以是随机序列。在一些情况下,引物进一步包含分子标识符(identifier)、条码或具有共同序列将是有利的。在某些实施方案中,引物载体上的引物成员是三联体,含有通用尾部分(例如,用于测序库构建的寡核苷酸序列),紧接条码序列的5',接着一组能够从基因组的多个位置引发的随机六聚体碱基之一。在某些实施方案中,在形成步骤之前,所述方法进一步包括以下步骤:提供包含核酸模板分子的第一溶液;提供包含多个不同的引物种类的第二溶液,所述引物种类各自对核酸模板上的不同靶位点是特异性的;合并第一和第二溶液以形成合并溶液;和在不混溶载体中分配合并溶液。在某些实施方案中,所述方法进一步包括将条码引入微滴。在某些实施方案中,引入包括在测序步骤之前合并所述微滴之一与包含条码的微滴。在某些实施方案中,测序步骤是合成型测序(sequencing-by-synthesis)。在某些实施方案中,扩增步骤通过聚合酶链反应进行。在某些实施方案中,扩增步骤通过延伸一个或多个引物种类进行。在某些实施方案中,核酸模板分子与癌症有关。在某些实施方案中,核酸模板分子与乳腺癌有关。在某些实施方案中,核酸模板分子与brca-1和/或brca-2有关。在某些实施方案中,微粒是固体珠。在某些实施方案中,微粒是磁珠。在某些实施方案中,微粒是链霉亲和素磁珠。在某些实施方案中,微粒是凝胶珠。提供的库和方法具有数个优点:(1)通过在微滴中随机包括微粒,在所有微滴中引物种类的高度均匀分布最可能导致存在对任何靶标具有正扩增反应的微滴;(2)所述方法是方便和高效的,无需微滴合并;(3)生物信息学引物设计的工作可消除或最小化。本文进一步提供了包含本文所述的多个微滴的试剂盒。在另一方面,本文还提供了包含本文所述的一个或多个引物载体的试剂盒。试剂盒还可包括描述微滴和/或微粒的使用的包装信息。上文的实施方案和实施不必然是彼此包括或排斥的,和可以不冲突和另外可能的任何方式组合,无论它们是否结合相同或不同的实施方案或实施呈现。一个实施方案或实施的描述不意图对于其它实施方案和/或实施是限制性的。此外,在可供选择的实施中,本说明书别处描述的任何一项或多项功能、步骤、操作或技术可与在简述中描述的任何一项或多项功能、步骤、操作或技术组合。因此,上文的实施方案和实施是说明性的,而非限制性的。附图简述当结合附图时,根据以下详细描述,将更清楚地理解上述和其它特征。在附图中,同样的参考数字表示同样的结构、要素或方法步骤,和参考数字的最左边一位表示参考要素首次出现的附图编号(例如,要素120首次出现在图1中)。然而,所有这些约定意图是典型的或说明性的,而不是限制性的。图1是用于微滴产生和检测的系统的一个实施方案的功能框图。图2是图1的系统的微流体微滴产生装置的一个实施方案的简化图示。图3a-c显示用于产生引物递送载体和递送至隔室的策略的一个实施方案的简化图示。图4是用于产生水凝胶颗粒以运输引物种类至隔室的策略的一个实施方案的简化图示。图5是用于产生聚合物水凝胶颗粒的化学反应的一个实施方案的简化图示。图6a-c显示用于观察smnc.88扩增子的数字型pcr反应,其进行以评价pcr反应与珠技术的相容性。在对照样品中和当珠以28个珠/微滴和56个珠/微滴加载时,两个群簇wt和nt被鉴定。这证实了珠与pcr扩增反应相容。图7显示来自含结合引物的1和3微米超-顺磁性珠的引物载体的示例性制备。起始总引物(~50bp)浓度6.4um,通过uv/vis分光光度法(nanodrop)测量的浓度为110ng/ul(其等于~6.5um)。野生型(wt)群簇的出现指示存在pcr产物。图8a-c显示用于观察smnc.88扩增子的示例性的数字型pcr反应,其进行以评价pcr反应与超顺磁性引物载体珠技术的相容性。图8a显示不含珠的对照pcr溶液。图8b显示含约28个珠/微滴的pcr溶液。图8c显示含约56个珠/微滴的pcr溶液。对于图8a-8c,100ul被平均分成4个25ul溶液用于四次测试。图9显示具有包含图8的珠溶液的微滴的微通道的图像。图10a和10b显示用于观察smnc.88扩增子的另一个示例性的数字型pcr反应,其进行以评价pcr反应与珠技术的相容性。图11显示在乳液中扩增的人类基因组的2020个严重重叠靶标和序列测序(illumina miseq)。对于2020个靶标的子集的引物对子集(30路(plex)、60路和125路)被直接加入pcr溶液(对照)或通过珠在每个珠类型上作为5路递送。pcr溶液然后制备成5pl微滴乳液用于pcr反应。对于珠-引物递送的样品,因为每个微滴含有有限数量的珠(6、12或25个珠/微滴),微滴将具有30、60或125个引物对(对应于6、12或25个珠/微滴,其中每个珠递送5个引物对)的随机组。随机分布减少引物-引物相互作用和靶标重叠问题。尽管在illumina测序仪上用不结合至任何珠的引物的对照实验对所有2020个靶标没有得到绘图,但珠引物递送的样品对于超过90%的靶标得到令人满意的绘图数。表格显示被超过1、15、30、100和200的绘图数覆盖的靶标的百分比。图12显示本文提供的引物载体的示例性设计。图13显示用两种引物:引物–f和引物-b,来自两种微粒:聚合物a和聚合物b的引物载体的示例性合成。聚合物可以是天然的或合成的。在某些实施方案中,聚合物可以是天然或合成的寡聚物。图14显示与brca-1和brca-2有关的多路引物载体的示例性产生。图15显示示例性引物载体的结合能力。图16显示示例性引物载体库的稳定性。如图16所示的在珠贮存期间引物交换预期对引物载体的性能具有有害影响。当珠在4℃下贮存3周时测量引物释放至溶液的浓度发现很低(0.3ng/ul)。这表明珠的集合可在4℃下长期贮存。贮存后,当它们加热至90℃时,20ng/ul的高浓度从珠释放。图17a-d显示示例性引物载体库的图像。图18显示通过改变引物对类型、引物载体类型和微滴类型,引物载体库的示例性设计。图19显示对于一组122个引物对的测序结果,所述引物对覆盖brca1和brca2基因的基因组连续区域;所有外显子被覆盖。对于“引物的珠递送”和“无珠”的情况,结果表格分为两个部分。“引物的珠递送”情况利用示例性的引物载体,如使用本专利的方法所教导的。在该情况下,给定的引物载体携带单个引物对,和存在122个不同类型的引物载体与样品和主混合物(master mix)组合。以使得在每个微滴中平均加载大约25个珠的珠浓度产生微滴(5pl体积)。高度多路技术增加可扩增分子存在于给定的反应中的可能性。为容易在样品之间比较,对于所有样品,平均覆盖深度下降取样至2500。以500x,大于99%的高覆盖度表明对于用随机多路技术的珠递送,测序覆盖度的格外均匀性。在其中所有引物存在和不使用珠和微滴的样品的情况下,覆盖度均匀性受到影响和以500x的深度,仅50-60%的靶区域被覆盖。详细描述如下文更详细描述的,所述发明的实施方案包括使用高效和廉价的方法控制微滴中的试剂分布的系统、方法和试剂盒。a.概要除非另外定义,本文使用的所有技术和科学术语具有本发明所属领域的普通技术人员通常理解的相同含义。类似或等同于本文所述的那些的方法和材料可用于本发明的实施,并且示例性的合适方法和材料在下文描述。例如,可描述包括超过两个步骤的方法。在这样的方法中,并非所有步骤可能是实现规定的目标所必需的,和本发明预期使用单独步骤以实现这些分立的目标。此外,材料、方法和实施例仅是说明性的和不意图是限制性的。具体官能团和化学术语的定义在下文更详细地描述。化学元素根据元素周期表,cas版本,handbook of chemistry and physics,第75版,内封面确定,和具体官能团如本文所述一般性定义。此外,有机化学的一般原理以及具体的官能部分和反应性描述于organic chemistry,thomas sorrell,university science books,sausalito,1999;smith和march,march’sadvanced organic chemistry,5th edition,john wiley&sons,inc.,new york,2001;larock,comprehensive organic transformations,vchpublishers,inc.,new york,1989;和carruthers,some modern methods oforganicsynthesis,3rd edition,cambridge university press,cambridge,1987。术语“烷基”是指具有1-10个碳原子的直链或支链饱和烃基的基团(“c1-10烷基”)。在一些实施方案中,烷基具有1-9个碳原子(“c1-9烷基”)。在一些实施方案中,烷基具有1-8个碳原子(“c1-8烷基”)。在一些实施方案中,烷基具有1-7个碳原子(“c1-7烷基”)。在一些实施方案中,烷基具有1-6个碳原子(“c1-6烷基”)。在一些实施方案中,烷基具有1-5个碳原子(“c1-5烷基”)。在一些实施方案中,烷基具有1-4个碳原子(“c1-4烷基”)。在一些实施方案中,烷基具有1-3个碳原子(“c1-3烷基”)。在一些实施方案中,烷基具有1-2个碳原子(“c1-2烷基”)。在一些实施方案中,烷基具有1个碳原子(“c1烷基”)。在一些实施方案中,烷基具有2-6个碳原子(“c2-6烷基”)。c1-6烷基的实例包括甲基(c1)、乙基(c2)、丙基(c3)(例如,正丙基、异丙基)、丁基(c4)(例如,正丁基、叔丁基、仲丁基、异丁基)、戊基(c5)(例如,正戊基、3-戊基、戊基(amyl)、新戊基、3-甲基-2-丁基、叔戊基)和己基(c6)(例如,正己基)。烷基的其它实例包括正庚基(c7)、正辛基(c8)等。除非另外规定,烷基的每个实例独立地是未取代的(“未取代的烷基”)或被一个或多个取代基(例如,卤素,例如f)取代(“取代的烷基”)。在某些实施方案中,烷基是未取代的c1-10烷基(例如未取代的c1-6烷基,例如,-ch3(me)、未取代的乙基(et)、未取代的丙基(pr,例如,未取代的正丙基(n-pr)、未取代的异丙基(i-pr))、未取代的丁基(bu,例如,未取代的正丁基(n-bu)、未取代的叔丁基(tert-bu或t-bu)、未取代的仲丁基(sec-bu)、未取代的异丁基(i-bu))。在某些实施方案中,烷基是取代的c1-10烷基(例如取代的c1-6烷基,例如,-cf3、bn)。术语“烯基”是指具有2-10个碳原子和一个或多个碳-碳双键(例如,1、2、3或4个双键)的直链或支链烃基的基团。在一些实施方案中,烯基具有2-9个碳原子(“c2-9烯基”)。在一些实施方案中,烯基具有2-8个碳原子(“c2-8烯基”)。在一些实施方案中,烯基具有2-7个碳原子(“c2-7烯基”)。在一些实施方案中,烯基具有2-6个碳原子(“c2-6烯基”)。在一些实施方案中,烯基具有2-5个碳原子(“c2-5烯基”)。在一些实施方案中,烯基具有2-4个碳原子(“c2-4烯基”)。在一些实施方案中,烯基具有2-3个碳原子(“c2-3烯基”)。在一些实施方案中,烯基具有2个碳原子(“c2烯基”)。所述一个或多个碳-碳双键可以在内部(例如2-丁烯基)或末端(例如1-丁烯基)。c2-4烯基的实例包括乙烯基(c2)、1-丙烯基(c3)、2-丙烯基(c3)、1-丁烯基(c4)、2-丁烯基(c4)、丁二烯基(c4)等。c2-6烯基的实例包括前述c2-4烯基以及戊烯基(c5)、戊二烯基(c5)、己烯基(c6)等。烯基的其它实例包括庚烯基(c7)、辛烯基(c8)、辛三烯基(c8)等。除非另外规定,烯基的每个实例独立地是未取代的(“未取代的烯基”)或被一个或多个取代基取代(“取代的烯基”)。在某些实施方案中,烯基是未取代的c2-10烯基。在某些实施方案中,烯基是取代的c2-10烯基。在烯基中,未规定立体化学的c=c双键(例如,-ch=chch3或)可以是(e)-或(z)-双键。术语“炔基”是指具有2-10个碳原子和一个或多个碳-碳三键(例如,1、2、3或4个三键)的直链或支链烃基的基团(“c2-10炔基”)。在一些实施方案中,炔基具有2-9个碳原子(“c2-9炔基”)。在一些实施方案中,炔基具有2-8个碳原子(“c2-8炔基”)。在一些实施方案中,炔基具有2-7个碳原子(“c2-7炔基”)。在一些实施方案中,炔基具有2-6个碳原子(“c2-6炔基”)。在一些实施方案中,炔基具有2-5个碳原子(“c2-5炔基”)。在一些实施方案中,炔基具有2-4个碳原子(“c2-4炔基”)。在一些实施方案中,炔基具有2-3个碳原子(“c2-3炔基”)。在一些实施方案中,炔基具有2个碳原子(“c2炔基”)。所述一个或多个碳-碳三键可以在内部(例如2-丁炔基)或末端(例如1-丁炔基)。c2-4炔基的实例包括但不限于乙炔基(c2)、1-丙炔基(c3)、2-丙炔基(c3)、1-丁炔基(c4)、2-丁炔基(c4)等。c2-6烯基的实例包括前述c2-4炔基以及戊炔基(c5)、己炔基(c6)等。炔基的其它实例包括庚炔基(c7)、辛炔基(c8)等。除非另外规定,炔基的每个实例独立地是未取代的(“未取代的炔基”)或被一个或多个取代基取代(“取代的炔基”)。在某些实施方案中,炔基是未取代的c2-10炔基。在某些实施方案中,炔基是取代的c2-10炔基。术语“杂环基”或“杂环”是指具有环碳原子和1-4个环杂原子的3-14元非芳族环系统的基团,其中每个杂原子独立地选自氮、氧和硫(“3-14元杂环基”)。在包含一个或多个氮原子的杂环基中,连接点可以是碳或氮原子,只要化合价允许。杂环基可以是单环的(“单环杂环基”)或多环的(例如,稠环、桥环或螺环系统,例如双环系统(“双环杂环基”)或三环系统(“三环杂环基”)),并且可以是饱和的,或可包含一个或多个碳-碳双键或三键。杂环基多环环系统可在一个或两个环中包括一个或多个杂原子。“杂环基”还包括环系统,其中如上定义的杂环基环与一个或多个碳环基稠合,其中连接点在碳环基或杂环基环上;或者环系统,其中如上定义的杂环基环与一个或多个芳基或杂芳基稠合,其中连接点在杂环基环上,并且在这样的情况下,环成员的数量依旧是指杂环基环系统中的环成员的数量。除非另外规定,杂环基的每个实例独立地是未取代的(“未取代的杂环基”)或被一个或多个取代基取代(“取代的杂环基”)。在某些实施方案中,杂环基是未取代的3-14元杂环基。在某些实施方案中,杂环基是取代的3-14元杂环基。术语“芳基”是指具有在芳族环系统中提供的6-14个环碳原子和零个杂原子的单环或多环(例如,双环或三环)的4n+2芳族环系统的基团(例如,具有在环阵列中共享的6、10或14个π电子)(“c6-14芳基”)。在一些实施方案中,芳基具有6个环碳原子(“c6芳基”;例如,苯基)。在一些实施方案中,芳基具有10个环碳原子(“c10芳基”;例如,萘基,例如1-萘基和2-萘基)。在一些实施方案中,芳基具有14个环碳原子(“c14芳基”;例如,蒽基)。“芳基”还包括环系统,其中如上定义的芳基环与一个或多个碳环基或杂环基稠合,其中连接基团或连接点在芳基环上,并且在这样的情况下,碳原子的数量依旧是指芳基环系统中的碳原子的数量。除非另外规定,芳基的每个实例独立地是未取代的(“未取代的芳基”)或被一个或多个取代基取代(“取代的芳基”)。在某些实施方案中,芳基是未取代的c6-14芳基。在某些实施方案中,芳基是取代的c6-14芳基。术语“杂芳基”是指具有在芳族环系统中提供的环碳原子和1-4个环杂原子的5-14元单环或多环(例如,双环、三环)的4n+2芳族环系统的基团(例如,具有在环阵列中共享的6、10或14个π电子),其中每个杂原子独立地选自氮、氧和硫(“5-14元杂芳基”)。在包含一个或多个氮原子的杂芳基中,连接点可以是碳或氮原子,只要化合价允许。杂芳基多环环系统可在一个或两个环中包括一个或多个杂原子。“杂芳基”包括环系统,其中如上定义的杂芳基环与一个或多个碳环基或杂环基稠合,其中连接点在杂芳基环上,并且在这样的情况下,环成员的数量依旧是指杂芳基环系统中的环成员的数量。“杂芳基”还包括环系统,其中如上定义的杂芳基环与一个或多个芳基稠合,其中连接点在芳基或杂芳基环上,并且在这样的情况下,环成员的数量是指稠合多环(芳基/杂芳基)环系统的环成员的数量。其中一个环不包含杂原子的多环杂芳基(例如,吲哚基、喹啉基、咔唑基等)的连接点可在任一环上,即,带有杂原子的环(例如,2-吲哚基)或不包含杂原子的环(例如,5-吲哚基)。将前缀“亚”附着至基团表明该基团是二价部分,例如,亚烷基是烷基的二价部分,亚烯基是烯基的二价部分,亚炔基是炔基的二价部分,杂亚烷基是杂烷基的二价部分,杂亚烯基是杂烯基的二价部分,杂亚炔基是杂炔基的二价部分,碳亚环基是碳环基的二价部分,杂亚环基是杂环基的二价部分,亚芳基是芳基的二价部分,和杂亚芳基是杂芳基的二价部分。在某些实施方案中,氮原子上存在的取代基是氮保护基(在本文亦称为“氨基保护基”)。氮保护基包括但不限于-oh、-oraa、-n(rcc)2、-c(=o)raa、-c(=o)n(rcc)2、-co2raa、-so2raa、-c(=nrcc)raa、-c(=nrcc)oraa、-c(=nrcc)n(rcc)2、-so2n(rcc)2、-so2rcc、-so2orcc、-soraa、-c(=s)n(rcc)2、-c(=o)srcc、-c(=s)srcc、c1-10烷基(例如,芳烷基、杂芳烷基)、c2-10烯基、c2-10炔基、杂c1-10烷基、杂c2-10烯基、杂c2-10炔基、c3-10碳环基、3-14元杂环基、c6-14芳基和5-14元杂芳基,其中每个烷基、烯基、炔基、杂烷基、杂烯基、杂炔基、碳环基、杂环基、芳烷基、芳基和杂芳基独立地被0、1、2、3、4或5个rdd基团取代,并且其中raa、rbb、rcc和rdd如本文所定义。氮保护基是本领域众所周知的和包括在protecting groups in organicsynthesis,t.w.greene和p.g.m.wuts,3rd edition,john wiley&sons,1999(通过引用并入本文)中详细描述的那些。例如,氮保护基例如酰胺基(例如,-c(=o)raa)包括但不限于甲酰胺、乙酰胺、氯乙酰胺、三氯乙酰胺、三氟乙酰胺、苯基乙酰胺、3-苯基丙酰胺、吡啶酰胺、3-吡啶基甲酰胺、n-苯甲酰基苯基丙氨酰基衍生物、苯甲酰胺、p-苯基苯甲酰胺、o-硝基苯基乙酰胺、o-硝基苯氧基乙酰胺、乙酰基乙酰胺、(n’-二硫代苄基氧基酰基氨基)乙酰胺、3-(p-羟基苯基)丙酰胺、3-(o-硝基苯基)丙酰胺、2-甲基-2-(o-硝基苯氧基)丙酰胺、2-甲基-2-(o-苯基偶氮苯氧基)丙酰胺、4-氯丁酰胺、3-甲基-3-硝基丁酰胺、o-硝基肉桂酰胺、n-乙酰基甲硫氨酸衍生物、o-硝基苯甲酰胺和o-(苯甲酰基氧基甲基)苯甲酰胺。氮保护基例如氨基甲酸酯基团(例如,-c(=o)oraa)包括但不限于甲基氨基甲酸酯、乙基氨基甲酸酯、9-芴基甲基氨基甲酸酯(fmoc)、9-(2-硫)芴基甲基氨基甲酸酯、9-(2,7-二溴)芴基甲基氨基甲酸酯、2,7-二-t-丁基-[9-(10,10-二氧代-10,10,10,10-四氢噻吨基)]甲基氨基甲酸酯(dbd-tmoc)、4-甲氧基苯甲酰甲基氨基甲酸酯(phenoc)、2,2,2-三氯乙基氨基甲酸酯(troc)、2-三甲基甲硅烷基乙基氨基甲酸酯(teoc)、2-苯基乙基氨基甲酸酯(hz)、1-(1-金刚烷基)-1-甲基乙基氨基甲酸酯(adpoc)、1,1-二甲基-2-卤代乙基氨基甲酸酯、1,1-二甲基-2,2-二溴乙基氨基甲酸酯(db-t-boc)、1,1-二甲基-2,2,2-三氯乙基氨基甲酸酯(tcboc)、1-甲基-1-(4-联苯基)乙基氨基甲酸酯(bpoc)、1-(3,5-二-t-丁基苯基)-1-甲基乙基氨基甲酸酯(t-bumeoc)、2-(2’-和4’-吡啶基)乙基氨基甲酸酯(pyoc)、2-(n,n-二环己基甲酰胺基)乙基氨基甲酸酯、t-丁基氨基甲酸酯(boc或boc)、1-金刚烷基氨基甲酸酯(adoc)、乙烯基氨基甲酸酯(voc)、烯丙基氨基甲酸酯(alloc)、1-异丙基烯丙基氨基甲酸酯(ipaoc)、肉桂酰基氨基甲酸酯(coc)、4-硝基肉桂酰基氨基甲酸酯(noc)、8-喹啉基氨基甲酸酯、n-羟基哌啶基氨基甲酸酯、烷基二硫代氨基甲酸酯、苄基氨基甲酸酯(cbz)、p-甲氧基苄基氨基甲酸酯(moz)、p-硝基苄基氨基甲酸酯、p-溴苄基氨基甲酸酯、p-氯苄基氨基甲酸酯、2,4-二氯苄基氨基甲酸酯、4-甲基亚磺酰基苄基氨基甲酸酯(msz)、9-蒽基甲基氨基甲酸酯、二苯基甲基氨基甲酸酯、2-甲基硫代乙基氨基甲酸酯、2-甲基磺酰基乙基氨基甲酸酯、2-(p-甲苯磺酰基)乙基氨基甲酸酯、[2-(1,3-二噻烷基)]甲基氨基甲酸酯(dmoc)、4-甲基硫代苯基氨基甲酸酯(mtpc)、2,4-二甲基硫代苯基氨基甲酸酯(bmpc)、2-磷鎓基乙基氨基甲酸酯(peoc)、2-三苯基磷鎓基异丙基氨基甲酸酯(ppoc)、1,1-二甲基-2-氰基乙基氨基甲酸酯、m-氯-p-酰基氧基苄基氨基甲酸酯、p-(二羟基硼基)苄基氨基甲酸酯、5-苯并异噁唑基甲基氨基甲酸酯、2-(三氟甲基)-6-色酮基甲基氨基甲酸酯(tcroc)、m-硝基苯基氨基甲酸酯、3,5-二甲氧基苄基氨基甲酸酯、o-硝基苄基氨基甲酸酯、3,4-二甲氧基-6-硝基苄基氨基甲酸酯、苯基(o-硝基苯基)甲基氨基甲酸酯、t-戊基氨基甲酸酯、s-苄基硫代氨基甲酸酯、p-氰基苄基氨基甲酸酯、环丁基氨基甲酸酯、环己基氨基甲酸酯、环戊基氨基甲酸酯、环丙基甲基氨基甲酸酯、p-癸基氧基苄基氨基甲酸酯、2,2-二甲氧基酰基乙烯基氨基甲酸酯、o-(n,n-二甲基甲酰胺基)苄基氨基甲酸酯、1,1-二甲基-3-(n,n-二甲基甲酰胺基)丙基氨基甲酸酯、1,1-二甲基丙炔基氨基甲酸酯、二(2-吡啶基)甲基氨基甲酸酯、2-呋喃基甲基氨基甲酸酯、2-碘乙基氨基甲酸酯、异硼基氨基甲酸酯、异丁基氨基甲酸酯、异烟碱基氨基甲酸酯、p-(p’-甲氧基苯基偶氮)苄基氨基甲酸酯、1-甲基环丁基氨基甲酸酯、1-甲基环己基氨基甲酸酯、1-甲基-1-环丙基甲基氨基甲酸酯、1-甲基-1-(3,5-二甲氧基苯基)乙基氨基甲酸酯、1-甲基-1-(p-苯基偶氮苯基)乙基氨基甲酸酯、1-甲基-1-苯基乙基氨基甲酸酯、1-甲基-1-(4-吡啶基)乙基氨基甲酸酯、苯基氨基甲酸酯、p-(苯基偶氮)苄基氨基甲酸酯、2,4,6-三-t-丁基苯基氨基甲酸酯、4-(三甲基铵)苄基氨基甲酸酯和2,4,6-三甲基苄基氨基甲酸酯。氮保护基例如磺酰胺基团(例如,-s(=o)2raa)包括但不限于p-甲苯磺酰胺(ts)、苯磺酰胺、2,3,6-三甲基-4-甲氧基苯磺酰胺(mtr)、2,4,6-三甲氧基苯磺酰胺(mtb)、2,6-二甲基-4-甲氧基苯磺酰胺(pme)、2,3,5,6-四甲基-4-甲氧基苯磺酰胺(mte)、4-甲氧基苯磺酰胺(mbs)、2,4,6-三甲基苯磺酰胺(mts)、2,6-二甲氧基-4-甲基苯磺酰胺(imds)、2,2,5,7,8-五甲基色烷-6-磺酰胺(pmc)、甲烷磺酰胺(ms)、β-三甲基甲硅烷基乙烷磺酰胺(ses)、9-蒽磺酰胺、4-(4’,8’-二甲氧基萘基甲基)苯磺酰胺(dnmbs)、苄基磺酰胺、三氟甲基磺酰胺和苯甲酰甲基磺酰胺。其它氮保护基包括但不限于吩噻嗪基-(10)-酰基衍生物、n’-p-甲苯磺酰基氨基酰基衍生物、n’-苯基氨基硫代酰基衍生物、n-苯甲酰基苯基丙氨酰基衍生物、n-乙酰基甲硫氨酸衍生物、4,5-二苯基-3-噁唑啉-2-酮、n-酞酰亚胺、n-二硫代琥珀酰亚胺(dts)、n-2,3-二苯基马来酰亚胺、n-2,5-二甲基吡咯、n-1,1,4,4-四甲基二甲硅烷基氮杂环戊烷加合物(stabase)、5-取代的1,3-二甲基-1,3,5-三氮杂环己烷-2-酮、5-取代的1,3-二苄基-1,3,5-三氮杂环己烷-2-酮、1-取代的3,5-二硝基-4-吡啶酮、n-甲基胺、n-烯丙基胺、n-[2-(三甲基甲硅烷基)乙氧基]甲基胺(sem)、n-3-乙酰氧基丙基胺、n-(1-异丙基-4-硝基-2-氧代-3-吡咯啉-3-基)胺、季铵盐、n-苄基胺、n-二(4-甲氧基苯基)甲基胺、n-5-二苯并环庚基胺、n-三苯基甲基胺(tr)、n-[(4-甲氧基苯基)二苯基甲基]胺(mmtr)、n-9-苯基芴基胺(phf)、n-2,7-二氯-9-芴基亚甲基胺、n-二茂铁基甲基氨基(fcm)、n-2-吡啶甲基氨基n’-氧化物、n-1,1-二甲基硫代亚甲基胺、n-苯亚甲基胺、n-p-甲氧基苯亚甲基胺、n-二苯基亚甲基胺、n-[(2-吡啶基)三甲苯基]亚甲基胺、n-(n’,n’-二甲基氨基亚甲基)胺、n,n’-亚异丙基二胺、n-p-硝基苯亚甲基胺、n-亚水杨基胺、n-5-氯亚水杨基胺、n-(5-氯-2-羟基苯基)苯基亚甲基胺、n-亚环己基胺、n-(5,5-二甲基-3-氧代-1-环己烯基)胺、n-硼烷衍生物、n-二苯基硼酸衍生物、n-[苯基(戊酰基铬或钨)酰基]胺、n-铜螯合物、n-锌螯合物、n-硝基胺、n-亚硝基胺、胺n-氧化物、二苯基膦酰胺(dpp)、二甲基硫代膦酰胺(mpt)、二苯基硫代膦酰胺(ppt)、二烷基氨基磷酸酯、二苄基氨基磷酸酯、二苯基氨基磷酸酯、苯亚磺酰胺、o-硝基苯亚磺酰胺(nps)、2,4-二硝基苯亚磺酰胺、五氯苯亚磺酰胺、2-硝基-4-甲氧基苯亚磺酰胺、三苯基甲基亚磺酰胺和3-硝基吡啶亚磺酰胺(npys)。微滴可使用微流体系统或装置产生。如本文使用的,“微”前缀(例如,“微通道”或“微流体”)通常是指具有小于约1mm、并且在一些情况下小于约100微米的宽度或直径的元件或物品。在一些情况下,所述元件或物品包括流体可流通的通道。另外,如本文使用的“微流体”是指包括至少一个微尺度通道的装置、设备或系统。根据本发明的“微滴”通常包括包在第二载体流体或固体容器或表面中的一定量的第一样品流体。本领域已知用于形成微滴的任何技术可用于本发明的方法。示例性的方法包括使含有目标材料(例如,核酸模板)的样品流体流流动,使得其和两个相反的流动载体流体流交叉。载体流体与样品流体不混溶。样品流体与两个相反的流动载体流体流交叉导致分配样品流体至含有目标材料的单个样品微滴。在一些情况下,微滴可以是球形或基本上球形的;然而,在其它情况下微滴可以是非球形的,例如,微滴可具有“水滴形”或其它不规则形状的外观,例如,取决于外部环境。在一些实施方案中,微滴是被第二流体完全包围的第一流体。如本文使用的,如果仅通过第二实体可围绕第一实体绘制或理想化闭合环路,则第一实体被第二实体“围绕”(在适用时,对于可能与壁或其它边界接触的第一流体的部分有时例外)。术语“生物学分子”是指活的生物体中存在的任何分子,包括大分子例如蛋白、碳水化合物、脂质和核酸,以及小分子例如初级代谢物、次级代谢物和天然产物。在某些实施方案中,生物学分子是蛋白。在某些实施方案中,生物学分子是核酸。在某些实施方案中,生物学分子是dna。在某些实施方案中,生物学分子是rna。如本文使用的术语“结合部分”是指共价连接至分子例如核酸的化学基团或分子,和化学基团或部分例如,click化学把柄。在一些实施方案中,结合部分位于两个基团、分子或部分之间或侧翼,并通过共价键与每个基团、分子或部分连接,从而连接二者。在一些实施方案中,结合部分是一个或多个氨基酸。在一些实施方案中,结合部分包含1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20或超过20个氨基酸。在一些实施方案中,结合部分包含多聚-丙氨酸序列。在一些实施方案中,结合部分包含非蛋白结构。在一些实施方案中,结合部分是有机分子、基团、聚合物或化学部分。在一些实施方案中,结合部分包含寡核苷酸。在某些实施方案中,寡核苷酸与引物种类互补。在一些实施方案中,结合部分包含多聚(t)序列。如本文使用的术语“核苷酸种类”通常是指通常掺入新生核酸分子的核酸单体的身份,包括嘌呤(腺嘌呤、鸟嘌呤)和嘧啶(胞嘧啶、尿嘧啶、胸腺嘧啶)。“天然”核苷酸种类包括例如,腺嘌呤、鸟嘌呤、胞嘧啶、尿嘧啶和胸腺嘧啶。修饰形式的上述天然核苷酸种类包括但不限于α-硫代-三磷酸衍生物(例如datpαs)、次黄嘌呤、黄嘌呤、7-甲基鸟嘌呤、5,6-二氢尿嘧啶和5-甲基胞嘧啶。术语“引物”、“引物种类”和“引物成员”在本文可互换使用,和是指在合适的温度下在合适的缓冲液中诱导与核酸链互补的引物延伸产物的合成的条件下用作dna或rna合成的起始点的寡核苷酸。在某些实施方案中,引物种类是寡核苷酸。在某些实施方案中,引物种类是单链寡脱氧核糖核苷酸。在某些实施方案中,引物种类包含随机序列。在某些实施方案中,引物种类包含条码。在某些实施方案中,引物种类包含通用序列。在某些实施方案中,引物种类包含条码和随机序列(例如,随机六聚体)。在某些实施方案中,引物种类包含条码和通用序列。通用序列可用于随后测序。在某些实施方案中,引物可掺有一个或多个合成或修饰的碱基。如本文使用的术语“变体”或“等位基因”通常是指多个种类之一,各自编码类似序列组成,但彼此具有一定程度的区别。区别可包括相关领域的普通技术人员已知的任何类型的变化,包括但不限于多态性例如单核苷酸多态性(snp)、插入或缺失(插入/缺失事件的组合亦称为"indel")、重复序列(亦称为串联重复序列)的数量差异和结构变化。如本文使用的术语“核酸模板”、“核酸模板分子”、“靶核酸模板分子”、“模板核酸”、“模板分子”、“靶核酸”或“靶分子”可互换和通常是指包含作为扩增和检测过程的对象的目的序列的核酸序列。通常,聚合物核酸,例如,包含三个或更多个核苷酸的核酸分子是线性分子,其中邻近的核苷酸通过磷酸二酯键彼此连接。在一些实施方案中,“核酸模板分子”是指单个核酸残基(例如,核苷酸和/或核苷)。在一些实施方案中,“核酸模板分子”是指包含三个或更多个单个核苷酸残基的寡核苷酸链。在一些实施方案中,“核酸模板分子”包括rna以及单链和/或双链dna。核酸模板分子可以是天然存在的,例如,在基因组、转录物、mrna、trna、rrna、sirna、snrna、质粒、粘粒、染色体、染色单体或其它天然存在的核酸分子的情况下。另一方面,核酸模板分子可以是非天然存在的分子,例如,重组dna或rna、人工染色体、改造的基因组或其片段、或合成的dna、rna、dna/rna杂合体,或包括非天然存在的核苷酸或核苷。此外,术语“核酸”、“dna”、“rna”和/或类似术语包括核酸类似物,即,具有并非磷酸二酯骨架的类似物。核酸模板分子可从天然来源纯化,使用重组表达系统产生,化合合成,和任选地纯化。合适时,例如,在化学合成的分子的情况下,核酸可包含核苷类似物,例如具有化学修饰的碱基或糖以及骨架修饰的类似物。在一些实施方案中,核酸是或包含天然核苷(例如,腺苷、胸苷、鸟苷、胞苷、尿苷、脱氧腺苷、脱氧胸苷、脱氧鸟苷和脱氧胞苷);核苷类似物(例如,2-氨基腺苷、2-硫代胸苷、肌苷、吡咯并-嘧啶、3-甲基腺苷、5-甲基胞苷、2-氨基腺苷、c5-溴尿苷、c5-氟尿苷、c5-碘尿苷、c5-丙炔基-尿苷、c5-丙炔基-胞苷、c5-甲基胞苷、2-氨基腺苷、7-去氮杂腺苷、7-去氮杂鸟苷、8-氧代腺苷、8-氧代鸟苷、o(6)-甲基鸟嘌呤和2-硫代胞苷);化学修饰的碱基;生物学修饰的碱基(例如,甲基化的碱基);嵌入的碱基;修饰的糖(例如,2′-氟核糖、核糖、2′-脱氧核糖、阿拉伯糖和己糖);和/或修饰的磷酸基团(例如,硫代磷酸酯和5′-n-亚氨基磷酸酯键)。核酸分子可获自动物、植物、细菌、真菌、病毒颗粒或制备物或任何其它生物体。在某些实施方案中,核酸分子从单细胞、包含许多细胞的组织或无细胞样品分离。核酸分子可获自生物体或从生物体获得的生物学样品,例如,血液、尿液、脑脊液、精液、唾液、痰、粪便和组织。核酸分子也可从培养的细胞分离,例如原代细胞培养物或细胞系。从中获得模板核酸的细胞或组织可用病毒或其它细胞内病原体感染。通常,核酸可通过多种技术从生物学样品提取,例如描述于maniatis等,molecular cloning:a laboratory manual,cold spring harbor,n.y.,pp.280-281(1982)中的那些技术。核酸分子可以是单链、双链或具有单链区域的双链(例如,茎结构和环结构)。如本文使用的术语“寡核苷酸”、“寡聚物”和“多核苷酸”可互换使用,是指核苷酸的聚合物(例如,一串至少三个核苷酸)。如本文使用的术语“数字型聚合酶链反应”、“数字型pcr”或“dpcr”通常是指通过分配靶核酸至大量单独隔室,克隆扩增和定量核酸(包括dna、cdna或rna)的精确方法,所述靶核酸在隔室内部扩增和检测。如本文使用的术语“读出”或“序列读出”通常是指包含获自单个核酸模板分子或一群多个基本上相同拷贝的模板核酸分子的整个序列组成的数据。如本文使用的术语“读出长度”通常是指可以可靠测序的模板分子的长度的上限。存在有助于系统和/或方法的读出长度的许多因素,包括但不限于模板核酸分子中的gc含量程度。与样品制备和处理、数据产生和数据分析有关的系统和方法的一些示例性的实施方案在下文一般性描述,其一些或所有适合用于本发明的实施方案。特别地,用于制备核酸模板分子、扩增模板分子、检测模板分子和/或其基本上相同的拷贝的系统和方法的示例性的实施方案。描述了利用示例性的仪器和计算机系统执行检测方法例如数字型pcr和/或测序方法的实施方案。“乳液”的典型实施方案包括产生两种不混溶物质的稳定乳液,和在本文所述的实施方案中通常是指在连续油相中水性微滴的乳液,在其中可发生反应。特别地,适合用于与生物学样品进行反应和检测产物的方法的乳液的水性微滴可包括作为微滴(亦称为不连续相)悬浮或分散在另一流体(例如疏水流体(亦称为连续相),通常包括一些类型的油)内的第一流体,例如基于水的流体(通常称为“水性”流体)。可使用的油的实例包括但不限于矿物油、基于硅酮的油、氟化油、部分氟化油或全氟化油。术语“微粒”是指小的离散颗粒。在某些实施方案中,微粒是珠。在某些实施方案中,微粒是水凝胶。珠的组成可改变,取决于寡核苷酸的类型和合成方法。合适的珠包括用于肽、核酸和有机部分合成的那些,包括但不限于塑料、陶瓷、玻璃、聚苯乙烯、甲基苯乙烯、丙烯酸聚合物、顺磁性材料、氧化钍盐、碳石墨、二氧化钛、胶乳或交联葡聚糖例如sepharose、纤维素、尼龙、交联胶束和特氟纶。来自bangs laboratories,fishers ind.的“microsphere detection guide”是一种有用指南。应理解,微粒不需要是球形的;可使用不规则微粒。此外,珠可以是多孔的,因此增加可用于捕获探针连接或标签连接的珠表面积。珠大小范围为从纳米即100nm至毫米即1mm,其中约0.2微米至约200微米的珠是优选的,并且约0.5至约5微米是特别优选的,但在一些实施方案中可使用更小的珠。引物种类可通过以下方法结合至微粒:包括但不限于化学或亲和捕获(例如,包括掺入衍生的核苷酸例如aminolink或生物素化的核苷酸,其然后可用于将引物种类附接至表面,以及通过杂交的亲和捕获)、交联和静电附着等。在优选的实施方案中,亲和捕获通过结合部分用于将引物种类结合至微粒。此外,引物种类可被生物素化(例如使用酶掺入生物素化的核苷酸,或者通过生物素的光激活交联)。生物素化的引物种类然后可在链霉亲和素-涂覆的基质或珠上捕获,如本领域已知的。或者,化学基团可引入引物种类,其然后可用于将引物种类添加至微粒。在某些实施方案中,微粒具有包含寡聚-dt的结合部分。术语“click反应”意思是在2001年由sharpless介绍的化学方法,和描述了为通过将小单元连接在一起迅速和可靠地产生物质而定制的化学。参见例如,kolb,finn和sharpless angewandte chemie international edition(2001)40:2004–2021;evans,australian journal of chemistry(2007)60:384–395)。示例性的偶联反应(其一些可分类为“click化学”)包括但不限于从活化的酸或酰基卤形成酯、硫酯、酰胺(例如肽偶联);亲核置换反应(例如卤素的亲核置换或张力环系统的开环);叠氮化物–炔烃huisgon环加成;硫醇–炔加成;亚胺形成;和michael加成(例如,马来酰亚胺加成)。与本发明的实施方案相容的水性流体的一个实例可包括水性缓冲溶液,例如超纯水(例如,18mega-ohm电阻率,通过例如柱色谱获得)、10mm tris hcl和1mm edta(te)缓冲液、磷酸盐缓冲盐水(pbs)或乙酸盐缓冲液。在本文所述的实例中,可使用与核酸分子或包封的生物学实体生理学上相容的任何液体或缓冲液。此外,在相同或可供选择的实例中,与本发明的实施方案相容的载体流体包括非极性溶剂、癸烷(例如,十四烷或十六烷)、氟烃油、硅酮油或其它油(例如,矿物油)。在某些实施方案中,载体流体可包含一种或多种添加剂,例如增加、减少或以其它方式产生非-牛顿表面张力(表面活性剂)和/或稳定微滴免于在接触时自发聚结的试剂。可特别用于包括与生物学样品进行反应例如pcr的实施方案的用于稳定乳液的表面活性剂的实施方案可包括一种或多种硅酮或含氟表面活性剂。例如,在微流体实施方案中,加入一种或多种表面活性剂可有助于控制或优化微滴大小、流动和均匀性,例如通过减少挤出或注射微滴至交叉通道所需的剪切力。这可影响微滴体积和周期性、或者微滴在交叉通道中破坏的速度或频率。此外,表面活性剂可用于稳定在氟化油中的水性乳液和显著减少微滴聚结的可能性。在一些实施方案中,水性微滴可用表面活性剂或表面活性剂的混合物涂覆,其中本领域技术人员理解表面活性剂分子通常位于不混溶流体之间的界面处,和在一些情况下当表面活性剂的浓度大于所谓的临界胶束浓度(有时亦称为cmc)时形成在连续相中的胶束。可加入载体流体的表面活性剂的实例包括但不限于表面活性剂,例如基于脱水山梨糖醇的羧酸酯(例如,"span"表面活性剂,fluka chemika),包括脱水山梨糖醇单月桂酸酯(span 20)、脱水山梨糖醇单棕榈酸酯(span 40)、脱水山梨糖醇单硬脂酸酯(span 60)和脱水山梨糖醇单油酸酯(span 80),以及全氟聚醚(例如,dupont krytox 157fsl、fsm和/或fsh)。可使用的非离子表面活性剂的其它非限制性实例包括聚氧乙烯化烷基酚(例如,壬基、p-十二烷基和二壬基酚)、聚氧乙烯化直链醇、聚氧乙烯化聚氧丙烯二醇、聚氧乙烯化硫醇、长链羧酸酯(例如,天然脂肪酸的甘油酯和聚甘油酯、丙二醇、山梨醇、聚氧乙烯化山梨醇酯、聚氧乙烯二醇酯等)和烷醇胺(例如,二乙醇胺-脂肪酸缩合物和异丙醇胺-脂肪酸缩合物)。在一个实施方案中,含氟表面活性剂可通过使全氟聚醚dupont krytox 157fsl、fsm或fsh与水性氢氧化铵在挥发性氟化溶剂中反应制备。溶剂和残留的水和氨可用旋转蒸发器除去。表面活性剂然后可溶解(例如,2.5wt%)在氟化油(例如,flourinert(3m))中,其然后用作载体流体(例如,连续相)。在本文所述的实施方案中,产生的表面活性剂是离子盐,并且将理解,也可使用非离子表面活性剂组分的其它实施方案。例如,非离子表面活性剂组分可包括通常包含头基和一个或多个尾基的所谓的嵌段共聚物(例如,二嵌段或三嵌段共聚物)。氟化嵌段共聚物的更具体实例包括聚乙二醇(peg)头基和一个或多个全氟聚醚(pfpe)尾基。此外,在一些实施方案中可包括用作微滴稳定剂(亦称为钝化剂)的其它试剂。可用的微滴稳定剂可包括但不限于聚合物、蛋白、bsa、精胺或peg。在一些实施方案中,可通过添加第二表面活性剂或其它试剂,例如聚合物或其它添加剂至水性流体,实现需要的特征。此外,在利用微流体技术的某些实施方案中,可使载体流体流动通过出口通道,使得在载体流体中的表面活性剂涂覆通道壁。在本文所述的实施方案中,乳液的微滴可被称为隔区(partation)、隔室、微囊、微反应器、微环境或相关领域通常使用的其它名称。水性微滴大小范围可取决于乳液组分或组合物的组成、其中包含的内容物和使用的形成技术。所述的乳液是微环境,其中可进行化学反应,所述化学反应可包括结合反应、反转录、pcr或其它过程。例如,进行所需的pcr反应需要的模板核酸和所有试剂可在乳液的微滴中包封和化学隔离。在一些实施方案中可使用其它表面活性剂或其它稳定剂以促进如上所述的微滴的额外稳定性。pcr方法典型的热循环操作可使用微滴执行以扩增包封的核酸模板,导致产生包含许多基本上相同拷贝的模板核酸的群体。在一些实施方案中,微滴内的群体可被称为“克隆分离的”、“隔室化的”、“隔离的”、“包封的”或“局部的”群体。此外在本实施例中,所述微滴的一些或所有可进一步包封微粒例如珠或水凝胶。在一些实施方案中,珠可用于连接模板和模板的扩增拷贝、与模板互补的扩增拷贝、或其组合。此外,基质能够连接其它类型的核酸、试剂、标签或其它目的分子。还将理解,本文所述的实施方案不限于在微滴中包封核酸,而是微滴可经配置以包封各种实体,包括但不限于细胞、抗体、酶、蛋白或其组合。如同核酸一样,微滴可进一步适合在其中包封的实体上进行各种反应和/或检测方法例如,elisa测定。形成乳液的各种方法可用于所述的实施方案。在一些实施方案中,方法包括形成水性微滴,其中一些微滴包含零个靶核酸分子,一些微滴包含一个靶核酸分子,和一些微滴可包含多个靶核酸分子。本领域技术人员将理解,在一些实施方案中单个微滴可能需要包含来自样品的多个核酸分子,然而在某些测定中可存在离散数量的目的靶标,其中在并非目的靶标的其它核酸分子存在的情况下基于在每个微滴中至多存在单个目的靶标的可能性产生微滴。在一些实施方案中微滴中靶核酸分子的数量通过在水性溶液中有限稀释靶核酸分子控制。或者,在一些实施方案中在微滴中靶核酸分子的数量通过分配非常小体积的水性流体(例如,皮升–纳升体积,例如约5皮升的体积)至微滴的方法控制,其中多个靶核酸分子分布在相同微滴中的统计学可能性非常小。在一些或所有所述的实施方案中,分子在微滴内的分布可通过poisson分布进行描述。然而将理解,在一些实施方案中可使用非poisson微滴加载的方法,和包括但不限于微滴的主动分拣,例如通过激光诱导的荧光,或通过被动一对一加载。产生乳液的系统和方法包括所谓的“大批”乳液产生方法,其通常包括施加能量至水性和载体流体的混合物。在大批产生方法的实例中,可通过在合并的混合物中涡旋、摇动、旋转桨叶(产生剪切力)来搅动施加能量,或在一些实施方案中当从不混溶流体分离时可施加水性溶液的搅动,其中搅动产生加到不混溶流体的微滴,例如当使用压电搅动时。或者,一些大批产生方法包括逐滴添加水性流体至旋转的载体流体。大批乳液产生方法通常非常快地产生乳液,和不需要复杂或专门的仪器。对于乳液中微滴的尺寸和体积,使用大批产生技术产生的乳液微滴通常具有低的均匀性。乳液形成方法的其它实施方案包括基于“微流体”的形成方法,其可利用携带水性和载体流体的通道的接合点,导致在流动流中输出微滴。基于微流体的微滴产生方法的一些实施方案可利用一个或多个电场以克服表面张力。或者,一些实施方案不需要添加电场。例如,水流可从一个通道经过狭窄压缩注入;在其经过压缩通过时,相反传送的油流(优选氟化油)在流体动力学上集中水流和稳定其分裂成微滴。为了形成微滴,通过油施加给水流的粘性力必须克服水表面张力。水微滴的产生速率、间隔和大小通过油和水流的相对流速以及喷嘴几何结构控制。尽管这种乳化技术非常稳健,但微滴大小和速度与流体流速和通道尺寸紧密相关。继续本实例,微流体装置的一些实施方案可并有整合的电场,从而产生电学上可寻址的乳化系统。例如,这可通过施加高电压至水性流和充电油水界面实现。水流作为导体起作用,而油是绝缘体;电化学反应充电流体界面,如同电容器。排出时,界面上的电荷保持在微滴上。微滴大小随电场强度增加而减少。在施加低电压时,电场具有可忽略的影响,并且微滴形成受表面张力和粘性流之间的竞争专门驱动。用于在微流体结构中形成被不混溶载体流体包围的水性微滴的系统和方法的其它实例描述于美国专利号7,708,949;和7,041,481(作为re 41,780重新发布)和美国专利申请公布号2006/0163385a1;2008/0014589;2008/0003142;和2010/0137163;和2010/0172803,其各自为所有目的通过引用以其整体并入本文。在一些实施方案中,乳液形成方法还包括合并已经形成的乳液微滴与其它微滴或流体流以产生合并微滴。微滴的合并可使用例如,描述于例如link等(美国专利申请号2008/0014589;2008/0003142;和2010/0137163)和raindance technologies inc的欧洲公布号ep2047910的一种或多种微滴合并技术实现。在某些实施方案中,反转录酶反应(称为“rt”反应)可用于从rna起始材料转换为核酸例如cdna或其它合成的核酸衍生物。反转录酶反应是指本领域已知的方法,例如通过描述于yih-horng shiao,(bmc biotechnology 2003,3:22;doi:10.1186/1472-6750-3-22)的方法。亦参见j biomol tech.2003march;14(1):33–43,其包括rt反应方法的论述,其各自通过引用并入本文。例如,所述方法包括引入反转录酶的第一步骤,其使用靶标特异性引物(有时称为“rt引物”)、随机六聚体或多聚-丙氨酸尾靶向寡核苷酸用于从rna模板产生单链互补dna(cdna)。对于转化小rna为cdna的实施方案,靶标特异性茎环引物可用于增加长度和优化特征,例如解链温度和特异性。在一些实施方案中,单链cdna然后用作模板以转化与单链cdna互补的第二链。单链或双链cdna然后可用作扩增模板,例如通过pcr。用于扩增靶序列的方法可包括引入过量的寡核苷酸引物至含有所需靶序列的dna或cdna混合物,接着在dna聚合酶的存在下进行准确顺序的热循环。引物与双链靶序列的其相应链互补。如本说明书他处所述的,所述的实施方案包括与乳液微滴内的生物实体进行反应。非常有用的一类反应的实例包括核酸扩增方法。如本文使用的术语“扩增”通常是指产生基本上相同拷贝的核酸序列(通常称为“扩增子”)。最众所周知的扩增策略之一是聚合酶链反应(例如,dieffenbach和dveksler,pcr primer,a laboratory manual,cold springharbor press,plainview,n.y.[1995])。扩增反应可包括本领域已知的扩增核酸分子的任何扩增反应,例如环介导的等温扩增(亦称为lamp)、蜗牛酶依赖性扩增(hda)、切口酶扩增反应(near)、聚合酶链反应、巢式聚合酶链反应、连接酶链反应(barany f.(1991)pnas 88:189-193;barany f.(1991)pcr methods and applications 1:5-16)、连接酶检测反应(barany f.(1991)pnas 88:189-193)、链置换扩增(sda)、基于转录的扩增系统、基于核酸序列的扩增、滚环扩增和超支链滚环扩增。在一些实施方案中,通常称为“多路技术”,乳液微滴包含多个引物对种类,各自对于扩增核酸序列的不同区域是特异性的。在管或孔中标准pcr引物的传统多路技术的优化已知是困难的。由于序列或长度或有限试剂的可及性的差异,在同一反应中产生的多个pcr扩增子可导致具有不同效率的扩增子之间的竞争。这导致在竞争的扩增子之间变化的产率,其可导致非均匀的扩增子产率。然而,因为基于微滴的数字型扩增利用仅一个模板分子/微滴,即使在微滴中存在多个pcr引物对,只有一个引物对将是有效的。因为每个微滴仅产生一个扩增子,在扩增子或试剂之间没有竞争,导致在不同的扩增子之间更均匀的扩增子产率。在一些实施方案中,即使每个微滴中pcr引物对的数量大于1,每个微滴仍存在至多仅一个模板分子,因此每个微滴仅存在一个引物对被一次利用。这意味着消除来自等位基因特异性pcr或不同的扩增子之间的竞争的偏好的微滴扩增优点得到保持。描述用于在微滴中进行扩增的系统和方法的其它实例显示于例如,link等(美国专利申请号2008/0014589、2008/0003142和2010/0137163)、anderson等(美国专利号7,041,481和其作为re 41,780再发行)和raindance technologies inc的欧洲公布号ep2047910。其各自的内容通过引用以其整体结合到本文中。在某些情况下,需要释放微滴的内容物用于进一步的处理和/或检测过程。在一些实施方案中,许多微滴的内容物被释放和合并在一起,然而将理解,在一些实施方案中微滴的内容物单独释放和分开保持。可使用各种用于释放微滴的内容物的方法,通常取决于微滴的组成。例如,在其中水性微滴在基于硅酮的油中的情况下,有机溶剂可用于“破坏”在单一溶液中合并的水性流体和硅酮油之间的界面完整性,其可使用各种技术分离。或者,在其中水性微滴在氟化油中的情况下,可使用全氟化醇试剂。在本实例中,全氟化醇提供用作释放剂的优点,因为其与水性流体不能混溶(例如,释放后将不存在于水性相中)和极好起作用以破坏通常与氟化油一起使用的表面活性剂。用于释放应用的全氟化醇的一个具体实例包括全氟癸醇。在一些实施方案中,通常称为数字型pcr,在扩增后乳液微滴被引入仪器用于光学检测扩增产物。在一些实施方案中核酸分子的产生和扩增在也用于检测的单一流体芯片中发生,或者乳液微滴可从用于微滴产生的流体芯片移出或分配,以进行“芯片外”扩增。对于芯片外应用的实施方案,微滴可引入用于检测的第二流体芯片,或引入用于微滴产生的初始流体芯片。此外,在其中乳液微滴使用大批方法产生的实施方案中,在扩增后微滴可引入用于检测的流体芯片。在相同或可供选择的实施方案中,从pcr热循环产生的反应产物的检测可在每个扩增循环期间或之后进行(例如,有时称为“实时”pcr)。来自反应产物的检测信号可用于产生所谓的“熔解曲线”,有时以已知浓度用作校准标准。在其中探针组合与靶标的特定序列组成有关(例如,作为标识符或分子条码类型)的反应中,熔解曲线也可基于探针的解链温度,其中靶标的存在可从熔解曲线信号(melt curve signature)鉴定。在一些实施方案中,当微滴引入用于检测的流体芯片时,可能高度需要添加额外的载体流体以增加连续微滴之间的间距。增加微滴之间的间距的实例描述于美国专利申请系列号2010-0137163,其为所有目的通过引用以其整体并入本文。乳液微滴可使用本领域已知的任何方法单独分析和检测,例如检测来自报告子的信号的存在和/或量。通常,用于检测的仪器包含一个或多个检测元件。检测元件可以是光、磁、电磁或电检测器、本领域已知的其它检测器、或其组合。合适的检测元件的实例包括光波导管、显微镜、二极管、光刺激装置(例如,激光)、光子倍增管、电荷耦合装置(ccd)和处理器(例如,计算机和软件),以及其组合,其协作检测代表特征、标志或报告子的信号。检测微滴中的扩增产物的检测仪器和方法的更进一步描述显示于link等(美国专利申请号2008/0014589、2008/0003142和2010/0137163)和raindance technologies inc.的欧洲公布号ep2047910,其各自为所有目的通过引用以其整体结合到本文中。在某些实施方案中,扩增的靶核酸分子使用可检测标记的探针、例如杂交探针检测。在一些或所有所述实施方案中,探针类型可包含识别特定核酸序列组成的多个探针。例如,探针类型可包含识别相同的核酸序列组成的一组探针,其中该组的成员具有对探针类型特异性的一个或多个可检测标记,和/或不包括可检测标记的成员(其可被包括以调节报告子信号的强度)。此外,探针成员可以彼此相对不同的浓度存在于微滴内。因此,可检测标记的组合和从探针浓度检测的相对强度对探针类型是特异性的,和能够鉴定探针类型。相关领域的普通技术人员理解,本文所述的实施方案与任何类型的荧光dna杂交探针或水解探针相容,例如taqman探针、分子信标、solaris探针、scorpion探针和通过杂交而序列特异性识别靶dna起作用和在靶序列扩增时导致荧光增加的任何其它探针。此外在本文所述的实施方案中,以与他处关于多路引物种类所述相同的方式,探针类型在乳液微滴中也可以是多路的。如他处所述,微滴可包含多个可检测探针,其与微滴中产生的扩增子杂交。所述多个探针的成员可各自包括相同的可检测标记或不同的可检测标记。多个探针也可包括一组或多组不同浓度的探针。这些组不同浓度的探针可包括由于不同的探针浓度导致强度不同的相同可检测标记。在本文所述的实施方案中,可检测从每个融合微滴发出的荧光和在散布图上基于其波长和强度作图。使用波长和强度的探针检测和分析的实例描述于美国专利申请系列号2011/0250597,其为所有目的通过引用以其整体结合到本文中。适合用于对引物的桥接区特异性的探针和用于本发明的方法的其它探针的可检测标记类型在下文描述。在一些实施方案中,可检测标记的探针是光学标记的探针、例如荧光标记的探针。荧光标记的实例包括但不限于atto染料,4-乙酰胺基-4'-异硫氰酸合芪-2,2'二磺酸;吖啶和衍生物:吖啶、吖啶异硫氰酸酯;5-(2'-氨基乙基)氨基萘-1-磺酸(edans);4-氨基-n-[3-乙烯基磺酰基)苯基]萘酰亚胺-3,5二磺酸酯;n-(4-苯胺基-1-萘基)马来酰亚胺;氨茴酰胺;bodipy;亮黄;香豆素和衍生物:香豆素、7-氨基-4-甲基香豆素(amc、香豆素120)、7-氨基-4-三氟甲基香豆素(香豆素151);花青染料;焰红染料;4',6-二脒基-2-苯基吲哚(dapi);5'5”-二溴邻苯三酚-磺基萘(溴邻苯三酚红);7-二乙基氨基-3-(4'-异硫氰酸合苯基)-4-甲基香豆素;二亚乙基三胺五乙酸酯;4,4'-二异硫氰酸合二氢-芪-2,2'-二磺酸;4,4'-二异硫氰酸合芪-2,2'-二磺酸;5-[二甲基氨基]萘-1-磺酰基氯(dns、丹酰氯);4-二甲基氨基苯基偶氮苯基-4'-异硫氰酸酯(dabitc);伊红和衍生物;伊红、伊红异硫氰酸酯;藻红和衍生物;藻红b、藻红、异硫氰酸酯;乙啡啶;荧光素和衍生物;5-羧基荧光素(fam)、5-(4,6-二氯三嗪-2-基)氨基荧光素(dtaf)、2',7'-二甲氧基-4'5'-二氯-6-羧基荧光素、荧光素、荧光素异硫氰酸酯、qfitc、(xritc);荧光胺;ir144;ir1446;孔雀绿异硫氰酸酯;4-甲基伞形酮邻甲酚酞;硝基酪氨酸;副蔷薇苯胺;酚红;b-藻红蛋白;o-酞二醛;芘和衍生物;芘、芘丁酸酯、琥珀酰亚胺1-芘;丁酸量子点;活性红4(cibacron.tm.brilliant red 3b-a)罗丹明和衍生物:6-羧基-x-罗丹明(rox)、6-羧基罗丹明(r6g)、丽丝胺罗丹明b、磺酰氯罗丹明(rhod)、罗丹明b、罗丹明123、罗丹明x异硫氰酸酯、磺基罗丹明b、磺基罗丹明101、磺基罗丹明101的磺酰氯衍生物(德克萨斯红);n,n,n',n'四甲基-6-羧基罗丹明(tamra);四甲基罗丹明;四甲基罗丹明异硫氰酸酯(tritc);核黄素;玫红酸;铽螯合物衍生物;cy3;cy5;cy5.5;cy7;ird 700;ird 800;la jolta blue;酞菁;和萘菁。对于某些实施方案优选的荧光标记包括fam和vic,和在相同或可供选择的实施方案中还可包括tet、yakima黄、calcein橙、aby和jun染料(来自thermo fisherscientific)。本发明考虑了荧光标记之外的标记,包括其它光学可检测标记。报告子的数字型扩增和检测的其它实例描述于美国专利号8,535,889,其为所有目的通过引用以其整体结合到本文中。在数字型pcr的实施方案中,数据分析通常包括散布图类型的表示,用于鉴定和表征从独特探针信号(波长和强度)得到的统计学类似的微滴群体,并且用于区别一群微滴与其它微滴。在一些实施方案中,用户和/或计算机应用可在直方图中选择与特定微滴或微滴群相关的数据点,用于计算,或用于如在使用光学标记中的测定法选择,或用于任何其它目的。一些选择方法可包括围绕任何可能的形状和尺寸的一个或多个选择的边界(闭合或未闭合)的应用。本文所述的实施方案不限于使用特定数量的探针种类。在一些实施方案中多个探针种类用于给出关于样品中核酸的性质的另外信息。例如,可使用三个探针种类,其中第一探针种类包含具有特定的激发和发射光谱的荧光团(例如,vic),和第二探针种类包含具有特定的激发和发射光谱的荧光团(例如,fam),其中对于第一和第二探针种类的激发光谱可重叠,但具有彼此明显不同的发射光谱。检测的强度差异可用于区别利用相同的荧光团的不同探针种类,其中发射光的强度是可调的。在一些所述实施方案中,从乳液微滴释放转化或扩增的靶分子的进一步的步骤,以进一步分析。释放的转化或扩增材料也可进行进一步处理和/或扩增。从微滴释放扩增的靶分子的系统和方法的其它实例描述于link等(美国专利申请号2008/0014589、2008/0003142和2010/0137163)和raindance technologies inc的欧洲公布号ep2047910。在某些实施方案中,扩增的靶分子使用本领域已知的任何合适的测序技术测序。在一个实例中,测序是单分子合成型测序。单分子测序显示于例如lapidus等(美国专利号7,169,560)、quake等(美国专利号6,818,395)、harris(美国专利号7,282,337)、quake等(美国专利申请号2002/0164629)和braslavsky等,pnas(usa),100:3960-3964(2003),这些参考文献各自的内容通过引用以其整体结合到本文中。测序核酸的其它实例可包括maxam-gilbert技术、sanger型技术、合成型测序方法(sbs)、杂交型测序(sbh)、连接型测序(sbl)、掺入型测序(sbi)技术、大规模平行签名测序(mpss)、polony测序技术、纳米孔、波导和其它单分子检测技术、可逆终止子技术或现在已知或未来可能开发的其它测序技术。典型的基于流体的微滴数字型扩增平台的实施方案通常包括用于执行一个或多个过程步骤的一个或多个仪器元件。图1提供了微滴系统100的说明性的实例,其经构建和安排以产生含有模板的微滴、扩增模板和检测扩增产物。在一些实施方案中,微滴系统100包括微滴产生仪器110、热循环仪115和微滴检测仪器120,但将理解,根据过程步骤的数量和性质,操作可合并至单一仪器。重要地,用户101可包括任何类型的微滴数字型扩增技术用户。另外在相同或可供选择的实施方案中,微滴系统100包含测序仪器130,其可包括将反应基质可操作连接至特定的数据捕获模式(即光学、温度、ph、电流、电化学等)的子系统,一个或多个数据处理元件和能够在反应基质上执行测序反应的流体子系统。例如,荧光读出的检测器的一些实施方案可包括具有定制显微镜的常规表荧光显微镜方法。在本实例中,20mw 488nm激光源(cyan;picarro,sunnyvale,ca)可扩大2x和被物镜(20x/0.45na;nikon,japan)聚焦到微流体通道。两个带通滤波器区别通过物镜收集的荧光:对于fam和vic荧光团分别为512/25nm和529/28nm(semrock,rochester,ny)。荧光可通过两个h5784-20光电倍增器(hamamatsu,japan)检测和通常以200khz采样率用usb-6259数据采集卡(national instruments,austin,tx)记录。此外,如图1所示,微滴系统100可被可操作连接至一个或多个外部计算机元件,例如计算机150,其可例如,执行系统软件或固件,例如应用155,其可提供一个或多个以下仪器的指令控制,例如微滴产生仪器110、热循环仪115、微滴检测仪器120、测序仪器130和/或信号处理/数据分析功能。计算机150可另外通过网络180可操作连接至其它计算机或服务器,其能够远程操作仪器系统和输出大量数据至能够贮存和处理的系统。此外在一些实施方案中网络180能够使所谓的“云计算”用于信号处理和/或数据分析功能。在本实例中,微滴系统100和/或计算机130可包括本文一般性描述的实施方案的一些或所有元件和特征。图2提供微滴产生器200的说明性的实例。微滴产生仪器110通常包括微滴产生器200的一个或多个实施方案,其中在一些实施方案中高度需要具有微滴产生器200的多个实施方案,其平行操作以显著增加微滴产生速率。在本实例中,微滴产生器200包括进口通道201、出口通道202和两个载体流体通道203和204。通道201、202、203和204在接合点205处汇合。进口通道201使样品流体流向接合点205。载体流体通道203和204使与样品流体不混溶的载体流体流向接合点205。进口通道201在其远端部分缩窄,其中其连接至接合点205。进口通道201定向为垂直于载体流体通道203和204。如他处所述,在样品流体从进口通道201流向接合点205时微滴形成,其中样品流体与通过载体流体通道203和204提供至接合点205的流动的载体流体相互作用。出口通道202接收被载体流体包围的样品流体的微滴。用于本发明的计算机系统的示例性的实施方案可包括任何类型的计算机平台,例如工作站、个人计算机、服务器或任何其它目前或未来的计算机。然而,本领域普通技术人员将理解,本文所述的前述计算机平台特别配置为进行所述发明的专门操作和不考虑通用计算机。计算机通常包括已知的元件,例如处理器、操作系统、系统存储器、存储器装置、输入-输出控制器、输入-输出装置和显示装置。相关领域的普通技术人员还将理解,存在许多可能的计算机配置和元件,和还可能包括高速缓冲存储器、数据备份单元和许多其它装置。显示装置可包括提供视觉信息的显示装置,该信息通常可在逻辑上和/或在物理上组织为像素阵列。还可包括界面控制器,其可包含各种已知或未来的软件程序的任何一种以提供输入和输出界面。例如,界面可包括通常所谓的“图形用户界面”(通常称为gui),其向用户提供一种或多种图形表示。界面通常能够接受用户使用选择工具的输入,或相关领域的普通技术人员已知的输入。在相同或可供选择的实施方案中,计算机上的应用可采用包括所谓的“命令行界面”(通常称为cli)的界面。cli通常在应用和用户之间提供基于文本的相互作用。通常,命令行界面通过显示装置作为文本行提供输出和接收输入。相关领域的普通技术人员将理解,界面可包括一种或多种gui、cli或其组合。处理器可包括市售可得的处理器,或可得或将可得的处理器。处理器的一些实施方案可包括所谓的多核处理器和/或能够以单核或多核配置采用平行处理技术。例如,多核构造通常包含两个或更多个处理器“执行核心”。在本实例中,每个执行核心可作为能够平行执行多线的独立处理器执行任务。此外,相关领域的普通技术人员将理解,处理器可配置为通常所谓的32或64比特构造,或现在已知或可未来开发的其它构造配置。处理器通常执行操作系统,所述操作系统以众所周知的方式与固件和硬件交互,并促进处理器协调和执行可以各种编程语言书写的各种计算机程序的功能。通常与处理器协同的操作系统协调和执行计算机的其它元件的功能。操作系统还提供时序安排、输入-输出控制、文件和数据管理、存储器管理和通信控制和相关服务,全部根据已知的技术。系统存储器可包括各种已知或未来的存储器装置的任何一种。实例包括任何通常可得的随机存取存贮器(ram),磁介质例如驻留硬盘或磁带,光学介质例如读写光盘,或其它存储器装置。存储器装置可包括各种已知或未来的装置的任何一种,包括光盘驱动器、磁带机、可移动硬盘驱动器、usb或闪存驱动器、或磁盘驱动器。这样的类型的存储器装置通常从程序存储介质阅读和/或写至程序存储介质,例如分别为光盘、磁带、可移动硬盘、usb或闪存驱动器或软盘。这些程序存储介质的任何一种,或现在使用或可后来开发的其它存储介质,可视为计算机程序产品。如将理解的,这些程序存储介质通常贮存计算机软件程序和/或数据。计算机软件程序,亦称为计算机控制逻辑,通常贮存在系统存储器和/或与存储器装置结合使用的程序存储装置中。在一些实施方案中,描述了计算机程序产品,其包含其中储存有控制逻辑(计算机软件程序,包括程序码)的计算机可用介质。控制逻辑,当被处理器执行时,引起处理器进行本文所述的功能。在其它实施方案中,一些功能使用例如,硬件状态机,主要在硬件中执行。执行硬件状态机以进行本文所述的功能对相关领域的技术人员而言是显而易见的。输入-输出控制器可包括用于从用户(无论是人还是机器,无论是当地还是远端)接收和处理信息的各种已知装置的任何一种。这样的装置包括例如,调制解调卡、无线卡、网络接口卡、声卡或各种已知输入装置的任何一种的其它类型的控制器。输出控制器可包括各种已知的显示装置的任何一种将信息提供给用户(无论是人还是机器,无论是当地还是远端)的控制器。在本文所述的实施方案中,计算机的功能元件通过系统总线彼此通信。计算机的一些实施方案可使用网络或其它类型的远端通信,与一些功能元件通信。如相关领域的技术人员显然的是,仪器控制和/或数据处理应用,如果以软件执行,可加载至系统存储器和/或存储器装置和从其执行。仪器控制和/或数据处理应用的所有或部分也可位于存储器装置的只读存储器或类似装置,这样的装置不要求仪器控制和/或数据处理应用首先通过输入-输出控制器加载。相关领域的技术人员将理解,仪器控制和/或数据处理应用,或其部分,可通过处理器以已知的方式加载至系统存储器,或高速缓冲存储器,或二者,如对于执行有利的。此外,计算机可包括在系统存储器中储存的一个或多个库文件、实验数据文件和因特网客户机。例如,实验数据可包括涉及一个或多个实验或测定的数据,例如检测的信号值,或与一个或多个实验或方法有关的其它值。另外,因特网客户机可包括能够使用网络在另一个计算机上获得远端服务的应用,和可例如包含通常所谓的“网络浏览器”。此外,在相同或其它实施方案中,因特网客户机可包括或可以是能够通过网络获得远端信息的专门软件应用,例如生物学应用的数据处理应用的元件。网络可包括本领域普通技术人员众所周知的许多各种类型网络的一种或多种。例如,网络可包括可利用通常所谓的tcp/ip协议套来通信的局域或广域网络。网络可包括包含互连计算机网络的世界性系统的网络,通常称为因特网,或者可还包括各种内联网结构。相关领域的普通技术人员还将理解,联网环境的一些用户可优选使用通常所谓的“防火墙”(有时亦称为包滤波器或边界保护装置)来控制信息运输至硬件和/或软件系统,和从硬件和/或软件系统运输。例如,防火墙可包含硬件或软件元件或其一些组合,和通常经设计以通过用户例如网络管理员等使安全策略在适当的位置。b.本发明的实施方案如上所述,本发明的实施方案涉及提供廉价策略和载体以递送试剂至微流体产生的微滴的系统、方法和试剂盒。更具体地,本发明的各种实施方案包括隔室化(compartmentalize)隔区中的(in partitions)多个引物种类与隔区中的进行反应所需的分配的核酸和其它组分的有效机制。在一些实施方案中,所述机制包括使用专门的引物递送载体,其将引物种类内容物隔室化至微滴,无需复杂的微滴合并或聚结步骤,其中引物递送载体不干扰扩增或其它处理步骤。例如,本发明的实施方案包括用于有效产生包括内部隔室化的许多不同的引物种类的单个微滴的策略,而不增加引入经设计以合并微滴与其它微滴或流体的电场或其它微流体结构的费用。在本文所述的实施方案中,引物递送载体可用于运输引物种类的足够数量的成员(例如,拷贝)至隔区或隔室(例如,微滴、孔、室等)以使所需反应成为可能。通常需要隔室包括由多个递送载体递送的所需数量和/或种类(例如,多路)的引物种类,所述各个引物成员可容易以足够浓度与递送载体分离,以支持在反应中使用。在一些实施方案中,高度需要在各微滴中引物种类具有一定的多路程度,其在统计学上提高在微滴内隔室化的单核酸分子包括对于至少一个靶种类的靶区域的可能性。在一些实施方案中,递送载体可各自携带引物种类(例如,种类包括有义和反义引物成员,有时亦称为正向和反向引物),其中多个递送载体分布于每个微滴(例如,平均3-100个递送载体/微滴,或超过100个,其可取决于因素例如微滴体积、递送载体尺寸等)。在一些实施方案中,分布可以是随机的,然而在可供选择的实施方案中可应用一定程度的分布控制。另外,在一些实施方案中,对于减少在一些引物种类之间相互作用的可能性,中等程度的多路技术可能是需要,其中例如,如果引物种类的设计不保证没有相互作用,则较高的多路技术程度越高增加彼此相互作用的一起隔室化的两个引物种类可能性,从而产生不需要的产物。引物递送载体的一个实施方案可包含珠类型元件,具有位于可用表面(例如,外表面和/或多孔表面)上的连接元件。珠元件可包括相关领域的普通技术人员已知的任何类型的珠,例如聚苯乙烯或琼脂糖型珠元件。然而将理解,不同的类型的珠元件具有不同的特征,在某些应用中其可能是需要的或不需要的。例如,可能需要珠元件具有一定的耐热性、解链温度、ph缓冲性、多孔性(例如,足够多孔以允许在孔结构内引物进入/结合)或提供在可包括在微滴内或微滴微环境外发生的步骤的预期应用中的有用功能的其它特征。另一需要的特征可包括珠相对于微滴尺寸的小尺寸,其中对于约20μm的微滴,例如5μm或更小的尺寸可能是需要的。这样的基于珠的引物递送载体实施方案的一个实例在图3a-c中说明,其包括珠305的实施方案,其例如,可由水凝胶peg材料构成,和包括位于表面上的结合元件的涂层。结合元件,如结合部分307所示,可包括本领域已知的任何类型的结合元件,例如使用标准化学结合至表面的寡核苷酸。在其中结合部分307包含寡核苷酸的实施方案中,结合部分307可固定在珠305上和包括与一个或多个引物种类(通常待使用的所有引物种类,如引物种类310’、310”和310”’所示)的区域互补的区域。在一些实施方案中每个引物种类通过互补区域的杂交分别固定在珠305的实施方案上以产生引物载体320的实施方案(在图3a-c中作为引物载体320、320’、320”、320”’和320”’所示,各自与不同的引物种类有关)。还将理解,引物种类310的多个实施方案可固定在珠305的单个实施方案上以产生引物载体320的多路实施方案。还将理解,可能需要通过结合部分307的3’端将结合部分307连接至珠305。在一个实例中,结合部分307可在3’端被生物素化和连接至珠305的链霉亲和素-官能化的实施方案。在一些实施方案中,相对于在珠305的表面上可用的那些,链霉亲和素可提供生物素的额外的结合位点,因此增加可通过珠305运输的引物种类的成员数量。在所述的实施方案中,互补区域包括具有高于典型的环境温度的解链温度(tm),但在可包括与pcr反应有关的解链温度的所需温度下容易释放的序列组成。此外,在一些或所有所述的实施方案中,互补区域对于引物种类310的所有实施方案是相同的,使得容易采用结合部分307的通用实施方案。然而,在可供选择的实施方案中可能有利的是使用各自具有互补区域的不同序列组成的结合部分307的不同实施方案,其可对应于引物种类310的互补区域的一个或多个实施方案和/或对应于引物种类310内的不同成员(例如,在引物种类的正向和反向成员之间不同的序列组成)。使用结合部分307的不同的实施方案可有利地允许更大控制在合并群中引物种类310的特定实施方案的分布和/或在珠305上引物种类310的成员的分布。通常,引物载体320的实施方案合并至容器330以贮存和在微滴产生中使用,其中容器330可包括本领域已知的任何类型的容器,包括但不限于管、小池、板等。包含不同的引物种类的引物载体320的合并实施方案可称为引物种类的“库”。在一些实施方案中,引物载体320实施方案的库可被冻干,以提供改进的特征,例如限制引物与引物载体320的不需要缔合的可能性,延长保存限期等。在一些或所有本文所述的实施方案中,作为引物载体320固定的引物种类的库然后可与核酸分子以及用于进行所需测定例如扩增反应的所有必需试剂混合。在所述的实施方案中可能需要引物载体320基本上是中性活性的,其通常可随珠305的组成和/或修饰而变化。然而还将理解,如果需要的话,在使用混合物产生水性微滴的乳液之前,混合物可经搅拌以产生或维持在混合物中引物载体320的实施方案的基本上均匀的悬浮液(例如,平均分布)。在所述的实施方案中,微滴产生器200的一个或多个实施方案可用于从包含引物载体320的实施方案的混合物产生多个微滴(在图3c中作为微滴350显示),其通常包括数量至少1000、100000、1000000、10000000或更多的微滴。根据poisson分布,微滴350的实施方案通常包含许多引物载体320的实施方案,引物载体320的平均数取决于微滴体积、珠305的尺寸和引物载体320实施方案在混合物中的浓度。例如,微滴可具有在每个微滴中范围3–100的平均数的引物载体320实施方案。在所述的实施方案中,微滴350然后可暴露于大于结合部分307和引物种类310之间的互补区域的解链温度的温度,导致从引物载体320的实施方案释放引物种类310和释放至含微滴的水性环境,在图3c中作为微滴350’显示。接着,在一些实施方案中,微滴350’可进行pcr反应典型的热循环过程,以从引物种类310靶向的核酸分子产生一群基本上相同拷贝的一个或多个区域,在图3c中作为微滴350”显示。回到珠305的组成和特征,珠305的各种实施方案可用于上述多路递送策略。一些实施方案可包括经官能化以通过其3’端固定寡核苷酸结合部分分子使得5’端游离在溶液中的珠。在相同或可供选择的实施方案中,珠305可用链霉亲和素官能化,其提供对生物素化的寡核苷酸结合部分更大数量的结合位点。珠305的另一个实施方案可包括由通过可逆键交联的聚合物链构成的所谓的“水凝胶颗粒”。在某些实施方案中,可逆键可通过触发事件破坏,其中触发事件是选自化学触发源、生物学触发源、热触发源、电触发源、照射触发源和/或磁触发源的一种或多种。此外,在本文所述的实施方案中,聚合物链包含可逆偶联至寡核苷酸分子的部分。换句话说,聚合物链连接形成水凝胶颗粒,其中连接随后在隔室中在响应刺激(例如,温度、ph等)时被破坏,释放引物种类的成员。图4提供一个实施方案的材料和化学组成的说明性的实例以及产生它们的方法。例如,对于含有可逆引物连接和交联基团的可交联聚合物链,存在多种选择。可组合在一起以产生可交联聚合物链的材料化学的可能元件包括可溶性聚合物链,其是直链、支链、树枝状或多臂聚合物(例如,4-臂peg)。通常需要可溶性聚合物是水溶性的,和可包括peg、天然聚合物(例如,明胶)、聚丙烯酰胺、含亲水悬挂基团的聚合物(例如,聚hema)的一种或多种。在所述的实施方案中,连接部分经优化以实现有效的交联密度(规定溶胀微粒凝胶的机械性质和大小、溶解速率)和最大化引物的有效载荷。连接部分在整个聚合物中可以是相同的,或可以是不同类型的部分的合集。例如,多个类型的结合部分可用于连接不同类型的引物和/或控制递送的不同种类的相对浓度。互补的连接部分可包括在相同的聚合物上,这意味着材料将是可自交联的,然而,一些连接基团可参与分子内相互作用。在一些实施方案中,一系列聚合物可用通用连接部分和各个结合部分官能化。这有利于调节聚合物凝胶中连接部分的相对浓度(通过混合不同类型的聚合物在一起),而无需改变聚合物链内不同连接序列的相对浓度。在所述的实施方案中,可能需要引物载体上的结合部分的序列包括以下一项或多项:解链温度,其足够高以防止颗粒在低温度下降解,但足够低以在扩增条件下促进溶解和引物释放和溶解;结合部分序列,其仅对引物尾序列是特异性的,以防止对pcr或下游测序产生不需要的干扰;结合部分可包括酶或热不稳定元件,因此一旦引物种类被递送,其可以被“关闭”(例如,dutp)。此外,结合部分还可包括:非共价交联化学、并非寡核苷酸杂交的可逆相互作用。此外在一些实施方案中引物在凝胶内可能不“连接”。例如,凝胶的交联密度(即,孔径)可经调节,使得在温度促使降解和释放之前,引物有效载荷可被物理捕获在凝胶内。各种方法可用于制备微粒。在一个可能的实例中,可溶性聚合物、一个或多个引物种类的成员、和交联部分(如果需要的话)可混合在一起,和在高于结合部分化学的tm下加热。然后,溶液将分配至微滴和冷却以杂交连键和交联凝胶。在凝胶稳定后,然后不混溶相通过过滤或其它方法除去。在相同或可供选择的实例中,可溶性聚合物可用引物有效载荷官能化。然后,第二步骤可用于从含有引物的聚合物产生各个颗粒。珠305的又一个实施方案可包括共聚(dmaa-mappa)-寡聚物,其是具有乙炔基侧链的水溶性聚合物,使用通过应用cu(i)(例如cubr)而催化的通常所谓的“click化学”,乙炔基与叠氮化物官能化的寡聚dna的叠氮化物基团反应。反应的实例在图5中说明,结果是水溶性聚合物,其可结合引物种类以产生热敏感性水凝胶,通过互补核酸之间的杂交相互作用具有上临界溶解温度(有时称为“ucst”)转变性质。如本文一般性定义的,r1是任选取代的亚烷基、任选取代的杂亚烷基、任选取代的亚烯基、任选取代的杂亚烯基、任选取代的亚炔基、任选取代的杂亚炔基、任选取代的杂亚环基或任选取代的杂亚芳基。在某些实施方案中,r1是任选取代的亚烷基。在某些实施方案中,r1是取代的亚烷基。在某些实施方案中,r1是未取代的亚烷基。在某些实施方案中,r1是直链未取代的亚烷基。在某些实施方案中,r1是任选取代的c1-c8亚烷基。如本文一般性定义的,r2是氢、取代或未取代烷基、或氮保护基。在某些实施方案中,r2是氢。在某些实施方案中,r2是取代或未取代烷基。在某些实施方案中,r2是氮保护基。如本文一般性定义的,r3是氢、取代或未取代烷基、或氮保护基。在某些实施方案中,r3是氢。在某些实施方案中,r3是取代或未取代烷基。在某些实施方案中,r3是氮保护基。如本文一般性定义的,r4是任选取代的亚烷基、任选取代的亚烯基、任选取代的亚炔基、任选取代的杂亚环基或任选取代的杂亚芳基。在某些实施方案中,r4是任选取代的亚烷基。在某些实施方案中,r4是取代的亚烷基。在某些实施方案中,r4是未取代的亚烷基。在某些实施方案中,r4是直链未取代的亚烷基。在某些实施方案中,r4是任选取代的c1-c8亚烷基。在本发明的实例中,以甲醇作为溶剂,产生低得多的分子量产物,和未发生胶凝过程,而不管反应时间多长。因此,dmso和甲醇的混合物作为溶剂可用于获得高分子量产物,没有胶凝风险。通过如此进行,也可采用长反应时间获得高的转化率/收率。实施例考虑以下实施例,本发明的这些和其它方面将得到进一步理解,所述实施例意图说明本发明的某些具体的实施方案,但不意图限制如权利要求书定义的其范围。美国专利号8765485、7129091、7655470、7718578、7901939、8273573、8304193、9448172、9029083、9074242、9273308、9328344、9150852、9399797、9266104、9029083、8528589、9012390、9150852、9176031、8841071、8658430、7708949、8337778、8986628和美国专利申请公开号2010-0022414、2012-0264646、2013-0260447、2014-0295421、2014-0045712、2013-0260447、2013-0295567、2013-0295568、2007-0092914、2009-0005254、2005/0221339、2013-0109575、2012-0122714、2013-0064776、2012-0244043、2012-0219947、2015-0126400、2014-0113300、2014-0303005、2015-0167066、2015-0099754、2015-0184256、2015-0283546、2014-0305799、2011-0190146全都通过引用以其整体结合到本文中。合成前体mappa约150ml的无水二氯甲烷、10ml ppa和20ml三甲基胺在250ml容器中混合在一起和以逐滴方式添加15ml甲基丙烯酰基氯。溶液经2hr反应时间形成盐的沉淀,其然后通过0.2um ptfe膜过滤以除去盐沉淀。溶液然后用50ml di水漂洗三次,将有机相经无水na2so4干燥过夜,然后通过旋转蒸发仪干燥。剩余的液体经过滤以除去任何盐和任选真空蒸馏以进一步纯化终产物。按图5所示合成共聚(dmaa-mappa)在25ml schlenk反应管中将0.9ml的n,n-二甲基乙酰胺、0.1ml mappa和20mgaibn溶于10ml dmso。通过“用氩气真空吹扫”方法将溶液脱氧3次。温度升高至70℃和进行反应3小时。乙醚用于从dmso沉淀聚合物。使用dmso作为溶剂有利于形成极高分子量产物。当聚合时间大于3小时时,可存在交联凝胶的粘性和形成的突然增加,因此聚合时间不应延长超过3小时,其中溶液显示中等增加的粘性。产物可通过乙醚沉淀,并且通过溶于thf和在乙醚中沉淀多次以除去dmso。制备引物载体具有官能化表面的市售微珠与引物溶液混合以在低温度(<70℃)下捕获引物。加载引物的微珠与pcr溶液混合,其然后在微流体装置上分成微滴。在温度增加时(>70℃),引物从珠表面释放至溶液相。使用直径为1um或3um的寡聚体d(t)25磁珠(获自new england biolabs)。珠具有在表面上在聚(t)25的5’端连接的聚(dt)25。引物经设计用于smn c88g测定。聚(a)25在正向和反向引物二者的5’端引入以允许结合珠表面上的聚(t)25。为了测量珠对于引物的结合能力,在室温下与珠混合1.5hr之前和之后测量引物溶液在280nm的uv吸光度。对于1um珠以0.13百万个引物/珠和对于3um珠以0.33百万个引物,分别测量结合能力。在珠上捕获的引物也在珠上在室温下保持稳定。两个靶标小组用于制备引物载体库。一个小组含有122个引物对,另一个含有2020个引物对。在这两个小组中所有引物对在5’具有相同的序列,如图15所示。以0.13百万个寡聚物/珠,即0.065百万个引物对/珠,通过uv吸光度测量珠的捕获能力。对于122小组库产生,将10ul的4um每个引物对溶液/tris缓冲液加入在2个96孔板中的小瓶。向每个小瓶中加入10ul的4mg/ml珠悬浮液/2x hi-fi(life tech)。以退火程序将板加载到pcr热循环仪中,该程序经1小时将板从80℃退火至10℃。收集来自不同小瓶的珠和混合,用hi-fi缓冲液漂洗三次,以除去游离的引物寡聚物,以4mg/ml悬浮于hi-fi缓冲液中,在4℃贮存。在此库中,每个珠具有单个引物对。对于2020小组库产生,将2020个引物对分成两个384孔板的405个小瓶,每个小瓶包含5个不同的引物对,总体积为10ul和总浓度为10um。向每个小瓶中加入10ul的4mg/ml珠悬浮液/2x hi-fi(life tech)。以退火程序将板加载到pcr热循环仪上,该程序经1小时将板从80℃退火至10℃。收集来自不同小瓶的珠和混合,用hi-fi缓冲液漂洗三次,以除去游离的引物寡聚物,以4mg/ml悬浮于hi-fi缓冲液,在4℃贮存。在此库中,每个珠具有5个引物对。扩增在第一个pcr反应中,携带引物的珠与taqman genotype主混合物(thermalfisher)和dna模板混合,制备成乳液用于扩增靶标。对于122小组,对于每40ul pcr溶液将24ul珠悬浮液装入pcr小瓶,以达到平均珠数量为25/微滴(5pl)。在通过磁铁将珠沉降到底部后,将珠悬浮液的上清液除去,之后加入40ul含有50ng剪切的人基因组dna(3k bp)的pcr溶液(taqman genotype主混合物)和与珠混合。在raindance raindrop source系统上将该混合物制成5pl微滴。对于2020小组,将24、12和6ul珠悬浮液加入每40ul反应溶液,导致平均数为25、12和6个珠/微滴(5pl)。因为每个珠具有5个不同的引物对,因此平均引物对数量/微滴分别为125、60和6。dna加载水平控制为100ng或1500ng/40ul pcr溶液。在raindropsource系统上将溶液制成5pl微滴。将乳液加载到热循环仪用于pcr反应。进行不添加珠作为载体的含混合的引物对溶液的对照实验,以与含有珠的样品比较。测序在第一次pcr反应后,将乳液破坏,和取出珠。获自第一次pcr扩增的水性相用作模板进行第二次pcr反应。第二次反应使用hi-fi主混合物(lift tech)以引入illumina测序仪接头,和不使用微滴。样品在illumina miseq测序仪上测序。图19和图11显示122引物小组和2020引物小组的测序结果。两个小组包含大量的重叠扩增子以覆盖连续的基因组区域。这些重叠扩增子通常在同一反应中极具扩增挑战性,因为它们趋于产生主要由重叠区域组成的产物。以超过1、15、30、100、200、300、400和500倍的绘图读出覆盖的靶标百分比显示在图19的表中。为容易比较,对于各条件将读出标准化至2500的相同平均覆盖深度。图19显示含珠的样品的覆盖度比没有珠的对照样品更加均匀,如通过以500x覆盖的显著更大分数的靶区域可见的(>99%,相比之下当未使用引物载体,无珠时为55%-60%)。在图11中,其中在第一次pcr反应中所有2020个引物对混合在一起的对照样品根本未显示序列绘图(数据未显示),表明无可用的靶标扩增。用珠递送的引物种类,样品显示对于超过90%的靶标令人满意的绘图数,证明了以下概念:在微滴中引物种类的随机分布减少引物-引物相互作用和靶标重叠问题,和改进了扩增产物的均匀性。已经描述了各种实施方案和实施,相关领域的技术人员应显而易见的是,前述内容仅是说明性的,而不是限制,仅以实例的方式提供。用于在说明性实施方案的各种功能要素中分配功能的许多其它方案是可能的。任何要素的功能可在可供选择的实施方案中以各种方式进行。通过引用并入参考文献和对其它文献的引用,例如专利、专利申请、专利公布、期刊、书籍、论文、网页内容,已在本公开内容全文中提及。所有这样的文件为所有目的通过引用以其整体结合到本文中。等同方案在权利要求中,冠词例如“a”、“an”和“the”可意指一个或超过一个,除非相反指示或以其它方式从上下文得到证明。如果一个、超过一个或所有组成员存在于、用于或以其它方式涉及给定的产物或方法,在一组的一个或多个成员之间包括“或”的权利要求或描述被视为得到满足,除非相反指示或以其它方式从上下文得到证明。本发明包括其中该组的准确一个成员存在于、用于或以其它方式涉及给定的产物或方法的实施方案。本发明包括其中超过一个或所有组成员存在于、用于或以其它方式涉及给定的产物或方法的实施方案。此外,本发明包括其中来自一个或多个所列权利要求的一个或多个限制、要素、条款和描述性术语被引入另一个权利要求的所有变化、组合和排列。例如,从属于另一个权利要求的任何权利要求可经修改,以包括在从属于相同基础权利要求的任何其它权利要求中存在的一个或多个限制。在要素以列表,例如,markush组格式提供时,也公开了要素的每个亚组,并且任何要素可从该组除去。应该理解,一般而言,在本发明或本发明的方面被称为包含特定要素和/或特征时,本发明或本发明的方面的某些实施方案由这样的要素和/或特征组成,或基本上由这样的要素和/或特征组成。为简单目的,这些实施方案没有在本文用文字明确阐述。还应注意,术语“包含”和“含有”意图是开放式的,和允许包括其它要素或步骤。在给定范围的情况下,包括端点。此外,除非另外指示或以其它方式从上下文和本领域普通技术人员的理解显而易见,表示为范围的值在本发明的不同实施方案中可表现为在所述范围内的任何特定值或子范围,至范围下限的单位的1/10,除非上下文明确另外指示。本技术参考了各种发布的专利、公开的专利申请、期刊文章和其它出版物,其所有通过引用并入本文。如果在任何并入的参考资料和本说明书之间存在冲突,应以本说明书为准。此外,落入现有技术内的本发明的任何具体的实施方案可明确从任何一个或多个权利要求中排除。因为这样的实施方案被视为是对本领域普通技术人员已知的,即使本文未明确阐明排除,它们也可排除。本发明的任何具体的实施方案可为任何理由,从任何权利要求排除,无论是否涉及现有技术的存在。使用不超过常规实验,本领域技术人员将认识到或能够确定本文所述的特定的实施方案的许多等同方案。本文所述的实施方案的范围不意图限于上文的描述,而是如随附权利要求所述。本领域普通技术人员将理解,在不脱离随附权利要求所定义的本发明的精神或范围的情况下,对该描述可进行各种变化和修改。
背景技术:
技术实现思路
- 还没有人留言评论。精彩留言会获得点赞!