双载体系统表达Otof基因的组合物和方法与流程
本发明涉及生物分子领域,尤其涉及一种双载体系统中融合多肽的剪接方法及应用。
背景技术:
1、听力损失是最常见的人类感官缺陷性疾病之一,可能是由环境因素和遗传因素造成的。有些人可能出生时出现听力损失,而其他人可能会随着时间的推移慢慢失去听力。听力损失影响全球超过15亿人,约占全球人数的五分之一,其中有4.7亿人患有致残性听力损失(中度及以上的听力障碍),其中有3400万儿童患有耳聋或听力损失。预计到2050年,可能有超过7亿人患有致残性听力损失。我国听力障碍人数约占人口总数的16%,致残性听力障碍患者约占总人口的5%。耳聋在我国新生儿中的发病率为1%~3.47%,即每1000名新生儿就有1-3名聋儿,每年新生约3万聋儿。听力损失的环境原因主要是与使用耳毒性药物、孕期感染、新生儿缺氧及放射线照射等多种环境因素或某些并发症相关。而遗传因素主要是因为个体耳聋基因缺陷,导致不同程度听力下降,致病基因会通过不同的遗传方式传递给下一代,并且可以在任何年龄发生,由遗传因素导致的耳聋约占60%,目前已发现了200多个基因与耳聋相关,涉及1500多种致病变异,至今临床上尚无任何可用于治疗遗传性耳聋的药物。遗传性耳聋根据是否伴有耳外组织异常或病变分为综合征性耳聋(shl)和非综合征性耳聋(nshi)。综合征性耳聋约占遗传性耳聋的30%,除听力障碍外,还伴有其他许多表现。非综合征性耳聋约占遗传性耳聋的70%~80%,只有听力受损症状,其他器官无遗传性损害。
2、遗传性非综合征型耳聋主要为单基因遗传病,按其遗传方式又分为常染色体显性遗传(autosomal dominant deafness,dfna)、常染色体隐性遗传(autosomal recessivedeafness,dfnb)、x-连锁遗传(x-linked deafness,dfnx)、y-连锁遗传(y-linkeddeafness,dfny)、线粒体遗传以及表观遗传等。dfna约占遗传性耳聋的18%,dfnb约占80%,dfnx约占1%,线粒体遗传<1%,dfny和表观遗传仅见个案报道。据报道已鉴定的非综合征型聋相关基因有110个,其中dfna相关基因45个,dfnb相关基因70个,10个同时与dfna和dfnb相关(clol11a2、gjb2、gjb6、myo3a、myo6、myo7a、ptprq、tcb1d24、tecta、tmc1),dfnx相关基因5个。每种类型按耳聋基因的命名原则描述,例如dfna1是第一个发现的常染色体显性耳聋类型。
3、dfnb9听力障碍是先天性遗传耳聋的常见形式,患有dfnb9耳聋的患者通常都是重度感音性耳聋,由otof基因编码耳畸蛋白otoferlin的基因突变引起的。otof基因编码otoferlin蛋白为跨膜蛋白,属于ferlin蛋白家族,otoerlin蛋白包含6个钙离子结合域和两个fer结构域,在细胞膜离子交换、信号转导和神经递质释放等方面起重要作用。otof基因是最早发现的与非综合征型听神经病谱系障碍(auditory neurophy spectrumdisorder,ands)有关的基因。听神经病谱系障碍也称为听神经病。otoferlin蛋白是一种在内毛细胞突触传递声音信息中起关键作用的蛋白质,超过56%的非综合征ansd是由otof基因突变所导致,全世界大约有20万人受此影响。目前otof基因突变患者只能从传统助听获益且临床治疗效果不佳,目前也尚无获批的药物治疗方案。
4、otof基因变异可引起先天性语前重度遗传性耳聋,遗传方式为常染色体隐形遗传。otof基因突变的患者常常从一出生起就患有严重的双侧耳聋,且听觉脑干反应(abr)缺失或高度异常,是目前我们最常见的听力损失原因。目前解决耳聋的方法大多为使用助听器、振动声桥及人工耳蜗等物理方法,虽然患者可以获得不同程度的听功能改善,但是个体差异较大,也有很大的局限和弱点。例如治疗效果有限、频率敏感性、言语分辨及噪声环境下的感知困难及装置需要小心使用等。全世界大约有30万患者接受了人工耳蜗植入,但这仅占所有耳聋患者的一小部分,对于大部分患者仍迫切需要根本性的有效的药物治疗途径,且至今还没有批准的治疗方法,是一个严重未满足需求的领域。
技术实现思路
1、本发明提供了一种双载体系统,目的在于通过双载体将otof基因转到耳蜗内毛细胞中,表达正常的功能性otoferlin蛋白,以治疗otof介导的听力损失。
2、本发明第一方面提供融合多肽,包含otoferlin蛋白的部分和内含肽系统的部分。
3、在一个或多个实施方案中,所述otoferlin蛋白如seq id no:1或与其具有至少90%相同性的序列所示。
4、在一个或多个实施方案中,所述融合多肽是第一融合多肽或第二融合多肽。
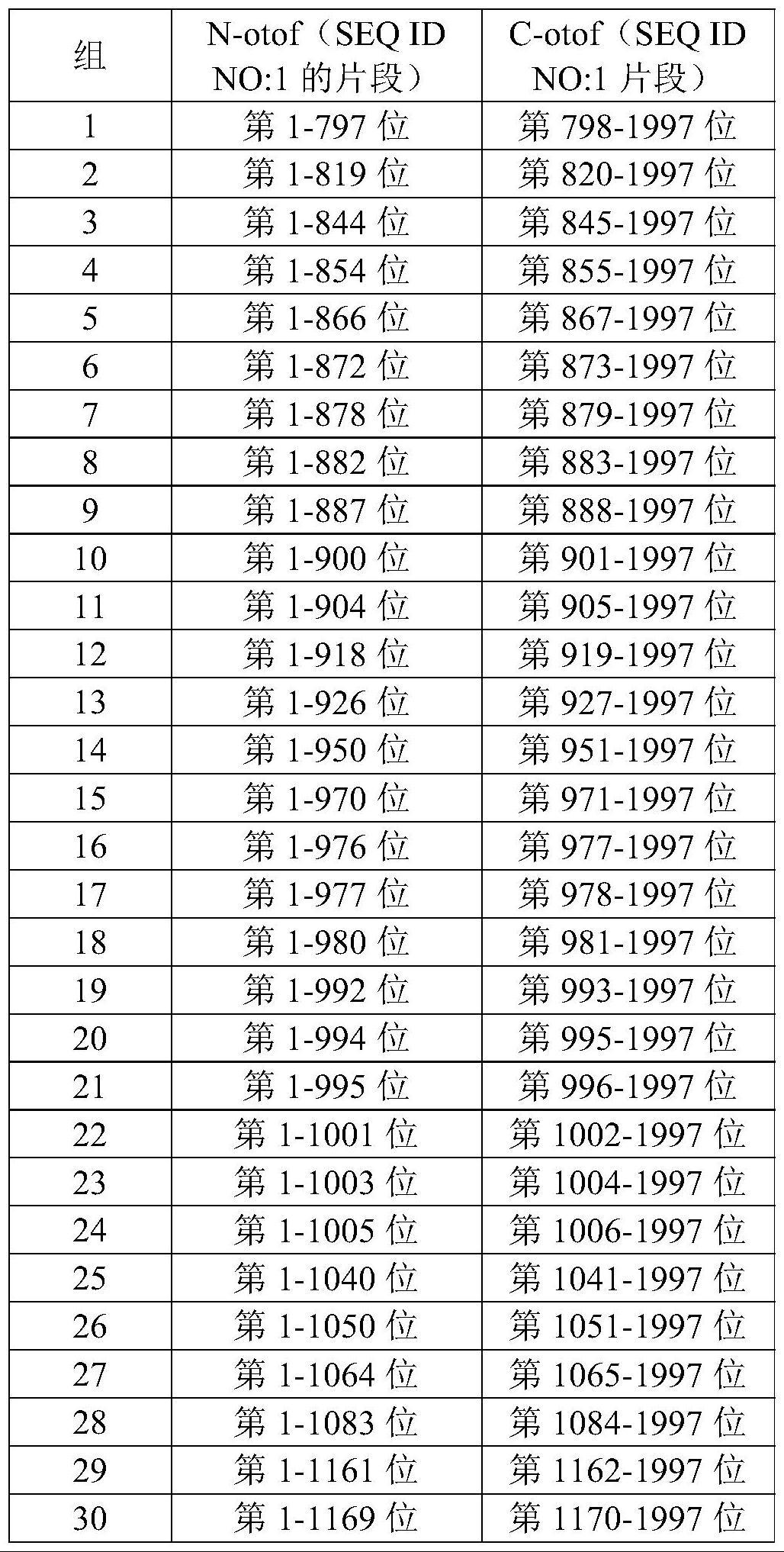
5、在一个或多个实施方案中,所述第一融合多肽包含seq id no:1所示的otoferlin蛋白的第1至第n位氨基酸和内含肽的n端片段(n-intein)或由其组成,其中n是750至1250任意整数,优选n是790至1200的任意整数,更优选n是797至1169的任意整数。
6、在一个或多个实施方案中,所述第二融合多肽包含seq id no:1所示的otoferlin蛋白的第(n+1)至第1997位氨基酸和内含肽的c端片段(c-intein)或由其组成,其中n是750至1250的任意整数,优选n是790至1200的任意整数,更优选n是797至1169的任意整数。
7、在一个或多个实施方案中,n是797、819、844、854、866、872、878、882、887、900、904、918、926、950、970、976、977、980、992、994、995、1001、1003、1005、1040、1050、1064、1083、1161、1169中任一个或多个。
8、在一个或多个实施方案中,所述内含肽的n端片段(n-intein)是分裂内含肽-n,如seq id no:2序列所示。
9、在一个或多个实施方案中,所述内含肽的c端片段(c-intein)是分裂内含肽-c,如seq id no:3序列所示。
10、在一个或多个实施方案中,所述第一融合多肽具有seq id no:5-16中任一项所示的序列或与其具有至少80%序列相同性的变体。
11、在一个或多个实施方案中,所述第二融合多肽具有seq id no:17-28中任一项所示的序列或与其具有至少80%序列相同性的变体。
12、本发明还提供一种多肽组合物,包含本发明第一方面中所记载的第一融合多肽和第二融合多肽。
13、本发明还提供多核苷酸,包含选自以下的序列:
14、(1)编码本文任一实施方案所述的融合多肽或多肽组合物的核酸序列,
15、(2)与(1)具有至少80%、至少90%、至少95%、至少98%或至少99%序列相同性的变体,
16、(3)(1)或(2)的互补序列。
17、在一个或多个实施方案中,编码第一融合多肽的多核苷酸具有seq id no:29-40中任一项所示的序列或与其具有至少80%序列相同性的变体。在一个或多个实施方案中,编码第二融合多肽的多核苷酸具有seq id no:41-52中任一项所示的序列或与其具有至少80%序列相同性的变体。
18、本发明还提供一种核酸构建物,所述核酸构建物:
19、(1)表达本文任一实施方案所述的融合多肽或多肽组合物,和/或
20、(2)包含本文所述的多核苷酸的序列。
21、在一个或多个实施方案中,所述核酸构建物是一表达框,编码第一融合多肽和第二融合多肽的多核苷酸均位于该表达框中。
22、在一个或多个实施方案中,所述核酸构建物是两表达框,分别包含编码第一融合多肽和第二融合多肽的多核苷酸。
23、在一个或多个实施方案中,所述核酸构建物是载体。例如克隆载体、整合载体、表达载体。优选aav载体。
24、在一个或多个实施方案中,所述核酸构建物是两aav载体,分别包含编码第一融合多肽和第二融合多肽的多核苷酸,以及位于所述多核苷酸侧翼的一个或更多个末端反向重复(itr)序列。多核苷酸可以是单链(ss)或自身互补(sc)aav核酸载体的形式,例如是单链或自身互补重组病毒基因组的形式。
25、在一个或多个实施方案中,所述核酸构建物还包括用于表达其上所含多核苷酸的元件。在一个或多个实施方案中,在一个或多个实施方案中,所述多核苷酸与组成型启动子可操作地连接。
26、在一个或多个实施方案中,所述核酸构建物具有seq id no:4所示的序列。
27、本发明还提供一种raav载体系统,包含两aav载体和编码aav病毒所需基因的核酸构建物,所述两aav载体分别包含编码第一融合多肽和第二融合多肽的多核苷酸,所述第一融合多肽和第二融合多肽如本发明第一方面中所记载。
28、在一个或多个实施方案中,aav病毒所需基因包括选自以下的一种或多种:rep、cap、e2a、e4和va基因。
29、在一个或多个实施方案中,所述aav载体系统包含anc80l65质粒、helper质粒和所述aav载体。
30、本发明还提供一种raav病毒颗粒,包含本发明任一实施方案所述的多核苷酸。
31、在一个或多个实施方案中,所述raav病毒颗粒选自raav1、raav2、raav4、raav5、raav6、raav7、raav8、raav9、raav10、raav11、raav12、raav13、raavphp.b或raavrh74中的一种或多种。
32、本发明还提供一种宿主细胞,所述宿主细胞:
33、(1)包含、表达和/或分泌本文所述的融合多肽或多肽组合物,
34、(2)包含本文任一实施方案所述的多核苷酸、核酸构建物或aav载体系统,
35、(3)染色体中整合有本文任一实施方案所述的多核苷酸。
36、在一个或多个实施方案中,所述宿主细胞是hek293细胞。
37、本发明第三方面提供一种制备otoferlin蛋白的方法,包括在适合进行内含肽剪接的条件下使第一融合多肽和第二融合多肽接触,所述第一融合多肽和第二融合多肽如本发明第一方面中所记载。
38、在一个或多个实施方案中,所述方法包括步骤:在适合进行内含肽剪接的条件下孵育本文任一实施方案所述的宿主细胞。
39、在一个或多个实施方案中,所述方法包括以下步骤:将本文任一实施方案所述的aav载体系统导入细胞,在适合第一融合多肽和第二融合多肽表达的条件下孵育所述宿主细胞。
40、在一个或多个实施方案中,所述细胞是动物细胞,优选hek293细胞。
41、在一个或多个实施方案中,所述方法还包括内含肽介导蛋白质的反式剪接的步骤。
42、本发明还提供本文任一实施方案所述的融合多肽、多肽组合物、多核苷酸、核酸构建物、宿主细胞在制备用于治疗由otof基因缺陷引起的疾病的药物中的应用。
43、在一个或多个实施方案中,所述疾病是dfnb9听力障碍。
44、本发明还提供一种药物组合物,包含药学上可接受的辅料,和选自以下的一种或多种:本发明任一实施方案所述的融合多肽、多肽组合物、多核苷酸、核酸构建物、raav载体系统、raav病毒颗粒、宿主细胞。
45、本发明还提供一种治疗遗传性耳聋疾病的方法,所述方法包括给予需要的患者治疗有效量的本发明任一实施方案所述的融合多肽、多肽组合物、多核苷酸、核酸构建物、宿主细胞或药物组合物。优选地,所述遗传性耳聋疾病为dfnb9遗传性耳聋。
46、本发明的有益效果:
47、本发明将otoferlin基因的5'-端和3'-端分别构建进两个不同的raav载体,通过重组aav双载体系统,将编码otof的转基因传递到耳蜗内毛细胞,最终实现毛细胞中otoferlin蛋白的表达,以治疗otof介导的听力损失。这意味着基因替代治疗能够在预防或治疗因otoferlin突变造成的遗传性耳聋中发挥作用。
- 还没有人留言评论。精彩留言会获得点赞!