一种靶向β2AR的纳米抗体及其制备方法和应用
本发明涉及生物,具体涉及一种靶向β2ar的纳米抗体及其制备方法和应用。
背景技术:
1、g蛋白偶联受体(gpcr)是人类基因组中最大的膜蛋白家族。gpcr具有七个跨膜螺旋特征序列,其中n末端位于细胞膜外,c末端位于膜内。依靠这类特征序列,gpcr可响应激素、神经递质、离子、光子、气味剂等刺激并介导其跨膜信号的转导,从而调节细胞内信号级联反应(hilgeretal.2018)。gpcr对信号的响应与转导通常依赖其结构的改变,如视紫红质的激活剂会结合gpcr的跨膜结构域6(tm6),使其向外移动改变其构象激活受体。激活态的受体可与细胞内g蛋白结合,触发鸟苷酸交换(manglik and kobilka2014)。由于gpcr在人体病理生理中起着至关重要的作用,其胞外域成为极具潜力的药物靶点。随着gpcr结构的解析,可以设计药物通过结合gpcr的变构位点,选择性的调节gpcr的结构与功能。从而实现可调控的靶向治疗价值(hauseret al.2017)。β肾上腺素受体(βars),是gpcr超家族成员,其可作为结合受体转导儿茶酚胺对细胞的调控信号。并在心血管的功能控制、心率失常的发生、心室重塑以及心力衰竭的演变中起到关键作用(steinberg2018)。β2ar作为βars家族成员,第一个被克隆并进行结构表征。β2ar是儿茶酚的主要靶标,主要在精神压力的响应,心血管和肺生理学中起重要作用。有研究结果表明β2ar在癌症靶向治疗,疼痛的发生以及自身免疫疾病的进程中也扮演着重要角色。如β2ar拮抗剂可通过抑制erk1/2-jnk-mapk途径和转录因子(nf-κb、ap-1、creb、stat3)来抑制胃癌细胞的增殖,侵袭和转移(zhang etal.2019)。同时β2ar的阻断还可降低人对疼痛的敏感性(nackley et al.2007)。在自身免疫疾病的进展中,β2ar可以通过不同的免疫细胞以及时间节点起到多种调控作用影响疾病进展(wu et al.2018)。综上所述,β2ar可作为多种生理过程和疾病进展的靶点。发掘其特异性的结合蛋白,是精确调控该蛋白的关键步骤。
2、纳米抗体可高效结合并稳定gpcr结构
3、传统的抗体由4条多肽链组成:两条相同且相对分子质量较大的称为重链(heavychain,h链);两条相对分子质量较小的肽链,称为轻链(light chain,l链)。轻链与重链以及重链与重链间由二硫键连接,构成了y字型的抗体结构。除传统的异源四聚体抗体外,骆驼还可产生仅含重链的抗体(hamers-casterman et al.1993)。纳米抗体(nanobody)是重链抗体的重链结构域(vhh),具有与亲本抗体的相同的抗原识别能力。纳米抗体有体积小,穿透性强,高稳定性和溶解性等特点。是由单基因编码的单结构域蛋白。纳米抗体具有稳定且独特的晶体结构,恒定区(fr)与互补决定区(cdr)的相互折叠,使纳米抗体呈现紧凑且含有凸起的长形结构。其互补决定区3(cdr3)长环最为突出,易于识别蛋白构象中的隐蔽表位,并且可以进入传统抗体无法触及的蛋白表面的口袋结构(de genst etal.2006)。这使得纳米抗体具备稳定蛋白中间构象的功能。并已经被应用于捕获淀粉样蛋白纤颤途径中的中间产物(abskharon et al.2014)。
4、如前所述gpcr具有灵活的构象变化以响应细胞外信号,而这种构象异质性是解析其激活态下晶体结构的重要阻碍(kobilka2013)。在之前的研究中,往往依赖具有高亲和力且持续作用的拮抗剂或引入突变维持gpcr的稳定结构。但激活剂非但不能稳定gpcr的构象还会进一步激活其构象异质性。因此限制了gpcr活性构象的解析(cooke et al.2015)。基于上述纳米抗体的独特特征,研究者们开始利用纳米抗体作为天然激活剂的替代物,以稳定gpcr的活性构象。以β2ar为例,目前已开发出其激动剂纳米抗体nb80,可维持其激活构象(rasmussen et al.2011),以及稳定其低活性构象的nb60纳米抗体(staus et al.2014)。血管紧张素受体(at1r)也在纳米抗体nb110i1的稳定作用下,得到了其激活状态下的晶体结构,并且通过亲和力成熟,nb110i1的亲和力达到了18.5nm(wingler et al.2019)。综上所述,纳米抗体可高效结合并稳定gpcr结构,并能以激活剂/拮抗剂类似物的作用调控gpcr的激活/静息构象。
5、膜蛋白抗体筛选的策略
6、目前膜蛋白筛选策略大多是将膜蛋白纯化,结合在固相载体上,此时的膜蛋白结构折叠并不充分可能丧失许多结合靶位。有些研究者为解决该问题,通过双层膜结构保持其活性状态。但这些都基于膜蛋白的纯化上。而gpcr这种具有复杂结构的七次跨膜蛋白不仅结构复杂,分子量也较大。蛋白纯化的质量和成本是有待解决的关键问题。如何较为简单的得到靶向β2ar的纳米抗体是现有技术需要解决的问题。
技术实现思路
1、本发明的目的在于克服上述技术不足,提供一种靶向β2ar的纳米抗体及其制备方法和应用,解决现有技术中如何较为简单地得到靶向β2ar的纳米抗体的技术问题。
2、本发明的筛选基于活细胞展示β2ar受体,这使得β2ar能够呈现天然的构象。再通过酵母文库与展示抗原的细胞共孵育。筛选靶向β2ar胞外段的纳米抗体。并验证其靶向胞外段范围以及对神经元细胞耐受糖氧剥夺模型的影响。
3、为达到上述技术目的,本发明的技术方案提供一种靶向β2ar的纳米抗体,所述纳米抗体的氨基酸序列的互补决定区cdr1、cdr2和cdr3的氨基酸序列分别如seq id no.2、seq id no.3和seq idno.4所示。
4、进一步地,所述纳米抗体的氨基酸序列如seq id no.1所示。
5、进一步地,表达所述纳米抗体的核酸序列如seq id no.5所示。
6、此外,本发明还提出一种分子表达载体,所述载体中含有如seq id no.2、seq idno.3、seq id no.4或者seq id no.1所示的氨基酸序列或者如seq id no.5所示的核酸序列。
7、进一步地,本发明还提出一种含有上述分子表达载体的宿主细胞,所述宿主细胞为原核细胞、酵母细胞或病毒。
8、进一步地,所述宿主细胞为人胚肾细胞或者仓鼠卵巢癌细胞。
9、此外,本发明还提出一种上述纳米抗体的制备方法,包括以下步骤:
10、s1、以过表达β2ar的cho-k1细胞系作为抗原,将酵母与细胞共同孵育,利用酵母表面展示的myc标签将酵母标记上apc647的荧光,通过流式分选出携带gfp与apc647的双荧光复合物,涂布trp缺陷型平板,共进行四轮cho-k1筛选;并用过表达β2ar的hek293t细胞进行第五轮筛;
11、s2、将筛选产物刮下,并提取质粒,利用纳米抗体恒定区序列进行pcr获得筛选文库的dna序列,通过二代测序获得相应dna信息,并按序列富集程度排序,得到排名第一的所述纳米抗体。
12、进一步地,在步骤s1之前还包括:采用pcr技术,将纳米抗体文库序列与aga2的c端融合,实现纳米抗体在酵母细胞表面的展示,构建过表达β2ar细胞系。
13、进一步地,本发明还提出纳米抗体在制备增强增强ht22细胞活性的试剂中的应用。
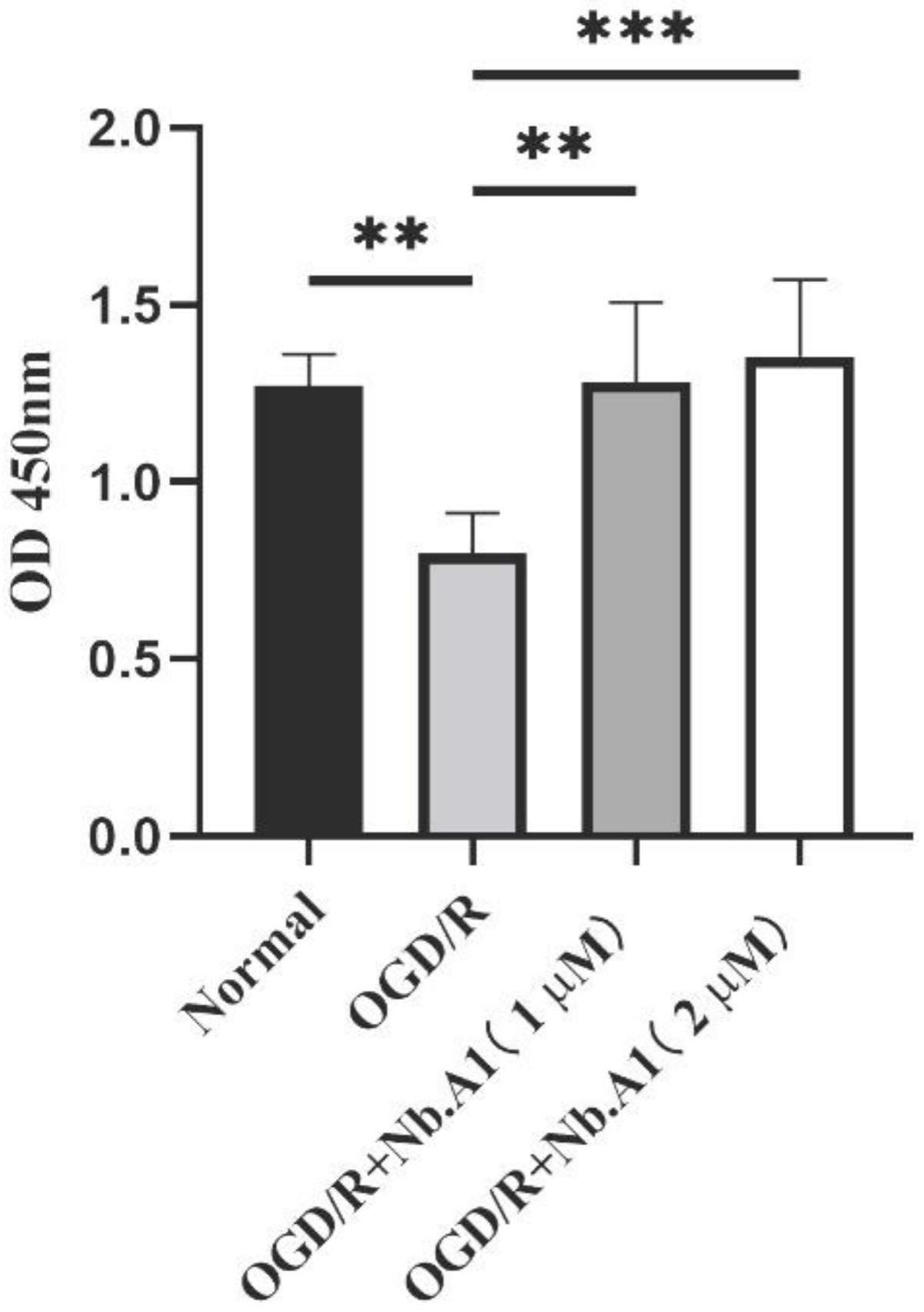
14、进一步地,增强ogd/r处理后的ht22细胞的活性。
15、与现有技术相比,本发明的有益效果包括:本发明提出的纳米抗体,能够靶向β2ar胞外段,具体是靶向前两段,并且能够增强ogd/r处理后的ht22细胞的活性。
- 还没有人留言评论。精彩留言会获得点赞!