一种分子检测方法
本发明属于生物与新医疗,尤其涉及一种分子检测方法。
背景技术:
1、核酸探针是一类由核酸分子或者类核酸分子组成的分子探针,能够通过特定的分子识别机制特异性地感知待测组分中的待测物,并通过特定的信号转导方法将分子识别事件转化为荧光信号或其他电化学信号报告出来。
2、单分子力学操纵技术是一种用于研究蛋白质、核酸等生物分子结构和相互作用的技术,可用于分子检测。与传统方法相比,基于单分子操纵的技术,如光镊、声镊、磁镊、液流操纵等,一方面可借助施加的拉力大小或探针分子的延伸长度作为识别信号,因而无需使用荧光定量等信号转导方法,这既避免了探针设计时信号输出结构域的需求,也大大降低了探针设计的复杂度。另一方面,针对单个分子的测量在理论上可实现单个待测物的检测,是解决经典核酸探针灵敏度不足的终极方案。
3、然而,由于分子扩散速度的限制,待测物与单分子探针的结合速度受到限制,导致对于浓度非常低的待测物,需要耗费相当长的检测时间,极大降低了检测灵敏度。此外,怎样提高检测分辨率、区分多种与核酸探针结合的待测物、同时检测多种待测物、检测待测物的结合速度强度与浓度、在生物或临床样本的背景信号中正确检测待测物、避免假阳性、检测待测物核酸的突变特别是单碱基突变,都是需要解决的技术难题。
技术实现思路
1、为了解决上述技术难题,本发明提供一种分子检测方法,该方法使用多通道单分子力学技术同时操纵多种分子探针以检测待测物,能够同时检测复杂样品中多个待测物。
2、本发明提供的分子检测方法,使用多通道单分子力学技术同时操纵多种分子探针以检测待测物;分子探针的两端通过标记的偶联官能团连接到载体;载体用于对分子探针施加拉力。
3、在上述技术方案的基础上,分子探针为串联核酸探针,串联核酸探针的单体含有靶点序列;在一定范围的拉力下,靶点序列可以形成结合待测物的特异结构;串联核酸探针通过滚环扩增或滚环转录制备而成。该方法可以通过检测有无待测物的分子探针长度差别或长度变化曲线差别为信号强度,检测是否存在待测物、待测物浓度、待测物与特异结构的结合速度与结合强度。串联核酸探针由于增加了特异结构的数量,从而提高了检测灵敏度。
4、在上述技术方案的基础上,滚环扩增包括以下步骤:
5、滚环扩增的起始:需要滚环扩增引物、dna聚合酶和滚环扩增模版;滚环扩增模版含有启动序列和靶点序列互补序列;启动序列可结合滚环扩增引物;
6、滚环扩增的延伸:以所有必需的核苷酸为底物并根据串联核酸探针所需的聚合度持续扩增一段时间。
7、在上述技术方案的基础上,滚环转录包括以下步骤:
8、滚环转录的起始:需要rna聚合酶和滚环转录模版;滚环转录模版含有启动序列和靶点序列互补序列;启动序列是结合rna聚合酶的序列;此步骤中,新生成的rna转录本标记有偶联官能团;
9、滚环转录的延伸:以所有必需的核苷酸为底物并根据串联核酸探针所需的聚合度持续转录一段时间。
10、在上述技术方案的基础上,延伸步骤是固定在载体上进行的。
11、在上述技术方案的基础上,滚环扩增或滚环转录包含暂停后重启的过程。
12、在上述技术方案的基础上,滚环扩增或滚环转录反应试剂中缺少必要核苷酸底物中的至少一种,聚合酶工作到需使用缺少的核苷酸底物时暂停。
13、在上述技术方案的基础上,使用多通道单分子力学技术进行检测的过程包含结合力和检测力:在结合力下,靶点序列形成特异结构,可结合待测物;在检测力下检测待测物;
14、检测力为恒定力时,记录没有待测物时串联核酸探针的长度作为基准长度,从结合力改变到检测力后,计算串联核酸探针的长度与基准长度之间的差别作为信号强度。
15、检测力为渐变力时,记录没有待测物时串联核酸探针的长度变化曲线作为基准曲线。在样品检测过程中,在检测力下计算串联核酸探针的长度变化曲线与基准曲线的差别作为信号强度;
16、根据信号强度来检测样品中是否存在待测物、待测物浓度、待测物与特异结构的结合强度及结合速度。
17、在上述技术方案的基础上,所述多个串联核酸探针的聚合度具有均一性;均一性标准为聚合度的均方差小于平均聚合度的20%。
18、在上述技术方案的基础上,该分子检测包括:同时操纵成组的多种串联核酸探针,组内各种串联核酸探针的靶点序列为鉴别序列多态性的序列。
19、特异结构是由其结合待测物的能力来限定的,包括但不限定于单链dna或单链rna、发夹结构、双链结构、纳米折纸、适配体、g4、i-motif、核酸三链结构等。特异结构可能是在较大拉力下靶点序列形成的去折叠的结构,也可能是在较小拉力下靶点序列折叠成的结构。
20、本发明将串联核酸探针与多通道单分子力学技术结合,同时操纵多个串联核酸探针,利用串联核酸探针在与待测物不同结合条件下的长度差别或长度变化曲线差别获得如下检测结果:(i)是否存在待测物;(ii)待测物的浓度;(iii)待测物与核酸探针的结合强度;(iv)待测物与核酸探针的结合速度;(v)提高待测物的检测分辨率;(vi)区分多种与核酸探针结合的待测物;(vii)同时检测多种待测物;(viii)在生物或临床样本的背景信号中正确检测待测物;(ix)通过多种探针做对照避免假阳性;(x)检测核酸待测物的突变特别是单碱基突变。
21、本发明合成多个串联核酸探针的方法如下:
22、串联核酸探针可以是通过滚环扩增合成,也可以是通过滚环转录合成。探针两端分别偶联到载体上。载体的作用是对探针施加拉力。
23、优选的,所述载体可以是流通池或微球。
24、使用多通道单分子力学技术同时操纵多个探针。
25、优选的,所述多通道单分子力学技术为磁镊。
26、并行测量的多个串联核酸探针的聚合度具有均一性。
27、优选地,所述均一性的标准是聚合度的均方差小于平均聚合度的20%。
28、所述串联核酸探针的聚合度大于500。
29、可以通过起始后,暂停再重启的过程,提高串联核酸探针聚合度的均一性。其中起始后暂停再重启可以采用低温下组装滚环扩增或滚环转录复合体的方法,这时聚合酶的活性极低,从而使得反应体系恢复到反应温度后同时启动。也可以采用聚合酶抑制剂的方法,在滚环扩增或滚环转录起始后抑制扩增或转录活性,从而使得去除抑制剂后同时启动。本发明的实施例方案中,具体采用了在环扩增或滚环转录起始步骤的反应底物中缺少至少一种必要核苷酸的方法来实现暂停再重启的过程。
30、所述串联核酸探针的单体包含形成发夹结构的序列,靶点序列位于发卡结构的茎区。在结合力下发夹结构打开成为单链并暴露靶点序列。单链状态的靶点序列可结合待测物。
31、串联核酸探针的具体制备方法如下:
32、1.通过滚环扩增合成串联核酸探针
33、通过滚环扩增合成串联核酸探针时,其滚环扩增过程可以是在载体上原位进行,也可以是在溶液中进行。相对于在溶液中合成的方法,原位合成优势在于:其一,便于更换反应试剂;其二,由于在合成过程中,滚环扩增复合物之间没有相互干扰,一方面可以防止新合成探针分子间的纠缠,影响探针分子的结构完整性,另一方面有助于合成聚合度更高的探针。
34、滚环扩增原位合成串联核酸探针的技术细节在于:
35、技术细节一,通过偶联反应,将滚环扩增引物通过偶联官能团1偶联到载体上。
36、优选地,所述载体为流通池或微球。
37、滚环扩增引物与流通池或微球的偶联可以是共价结合,也可以是亲和连接。
38、优选地,所述滚环扩增引物修饰的偶联官能团1为巯基,修饰位于引物序列5’末端,可连接到smcc修饰的流通池或微球。
39、优选地,滚环扩增引物连接到smcc修饰的流通池表面上。
40、滚环扩增引物可以根据探针序列进行设计,可结合滚环扩增的模版中的启动序列。
41、优选地,实施例中所使用的滚环扩增引物均为sh_hp。
42、技术细节二,通过酶连反应,制作闭合结构的环状滚环扩增模板。
43、闭合结构的环状扩增模板含有启动序列和靶点序列互补序列。所述启动序列是可以与滚环扩增引物结合的序列;所述靶点序列可以形成结合待测物的特异结构。
44、优选地,所述靶点序列位于探针发卡结构的茎区。
45、闭合结构的环状滚环扩增模板可以是由两条带有粘性末端的发卡结构单链核酸通过连接酶连接而成;也可以是在搭桥dna存在的情况下,由一条单链核酸通过连接酶首尾相连而成。
46、优选地,实施例中的滚环扩增模板都是由两条带有粘性末端的发卡结构单链dna通过连接酶连接而成。
47、优选地,连接酶为商品化的t4dna连接酶。
48、优选地,所述粘性末端长度为6个碱基。
49、优选地,所述粘性末端5’末端都带有磷酸化修饰。5’末端的磷酸化修饰可以在人工合成时添加,也可以使用多核苷酸磷酸化酶添加。
50、优选地,所述5’末端的磷酸化修饰都是在人工合成时添加的。
51、滚环扩增模板的序列可以依据待测物进行设计。
52、优选地,实施例中使用的两条发卡结构分别为t1和t2。发卡结构t1包含启动序列,发卡结构t2包含有靶点序列互补序列。
53、技术细节三,通过滚环扩增,合成串联核酸探针。
54、优选地,所述滚环扩增过程的dna聚合酶为等温聚合酶。
55、优选地,等所述温聚合酶为商品化的phi29dna聚合酶。
56、优选地,所述滚环扩增时的反应温度为30oc。
57、滚环扩增延伸步骤中使用的核苷酸底物可以为带有修饰核苷酸底物,如甲基化修饰的datp或dctp,也可以是不带有修饰的核苷酸底物。
58、优选地,所述滚环扩增延伸步骤中使用的核苷酸底物为不带有修饰的dntp。
59、本发明中,滚环扩增合成的串联核酸探针,其3’端含有偶联官能团2,所述偶联官能团2的标记可以通过dna聚合酶或者末端转移酶来实现。
60、优选的,所述3’端偶联官能团2的标记是在滚环扩增延伸后,通过掺入一定比例的带有偶联官能团2修饰的一种dntp来实现的。
61、优选地,所述带有偶联官能团2修饰的一种dntp为生物素标记的dutp。
62、优选地,所述生物素标记dutp的掺入比例为生物素标记的dutp比上未标记的dttp等于1:9。
63、探针的3’端通过偶联官能团2连接到载体上。
64、优选地,所述载体为流通池或者微球。因此,探针的两端分别连接到流通池或微球。
65、技术细节四,可通过同步化滚环扩增过程,使合成的多个串联核酸探针的聚合度相对均一。
66、滚环扩增时还包括滚环扩增起始后,经过扩增暂停再重启的过程。
67、本发明中,通过在滚环扩增起始步骤的反应试剂中加入缺陷底物来同步化滚环扩增过程。所述缺陷底物中缺少滚环扩增所必需的核苷酸底物中的至少一种,因此,dna聚合酶工作到需使用缺少的核苷酸底物时暂停。
68、优选地,所述缺陷底物中缺少一种dntp核苷酸底物。
69、优选地,所述一种dntp核苷酸底物为dttp。
70、通过滚环扩增合成串联核酸探针时,其滚环扩增过程也可以是在溶液中进行。相较于在载体表面上原位进行的滚环扩增过程,其技术细节的不同点在于:
71、技术细节的不同点之一,滚环扩增延伸不是在载体上进行的。
72、技术细节的不同点之二,在同步化滚环扩增过程时,dna聚合酶暂停扩增后需要对滚环扩增复合物进行回收。
73、2.通过滚环转录合成串联核酸探针
74、通过滚环转录合成串联核酸探针时,其滚环转录过程可以是在载体上原位进行,也可以是在溶液中进行。相对于在溶液中合成的方法,原位合成优势在于:其一,便于更换反应试剂;其二,由于在合成过程中,滚环转录复合物之间没有相互干扰,一方面可以防止新合成探针分子间的纠缠,影响探针分子的结构完整性,另一方面有助于合成聚合度更高的探针。
75、滚环转录原位合成串联核酸探针的技术细节在于:
76、技术细节一,通过酶连反应和退火反应,合成闭合结构的环状滚环转录模板。闭合结构的环状滚环转录模板含有启动序列和靶点序列互补序列。其中,启动序列为双链结构,可以和rna聚合酶结合。
77、所述酶连反应可以是由两条带有粘性末端的发卡结构单链核酸通过连接酶连接而成,也可以是在搭桥dna存在的情况下,由一条单链核酸通过连接酶首尾相连而成。
78、优选地,实施例中,所述滚环转录模板的酶连反应是在搭桥dna存在的情况下,由一条单链核酸通过连接酶首尾相连而成。
79、优选地,所述搭桥dna为bridge1,所述连接酶为商品化的t4dna连接酶。
80、所述退火反应是在酶连后的环状单链模板上退火启动序列互补序列,形成局部双链结构的环状滚环转录模板。
81、优选地,所述启动序列互补序列为t7_c。
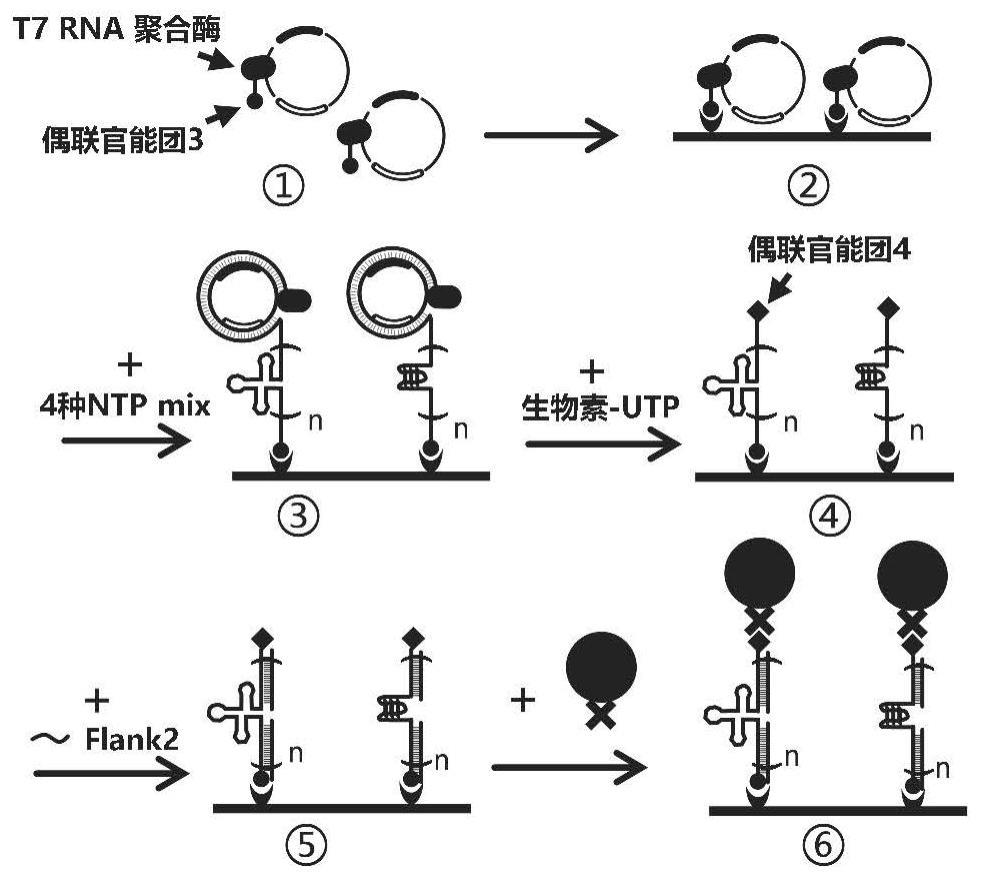
82、闭合结构环状滚环转录模板的序列可以依据rna聚合酶的类型和待测物进行设计。
83、优选地,实施例中,所述滚环转录模板的启动序列为t7启动子序列,rna聚合酶为t7rna聚合酶。
84、闭合结构环状滚环转录模板的靶点序列是可以折叠成为发卡结构的序列,或者是可以折叠成g四联体结构、适配体结构、纳米折纸结构、药物靶点特异结构等的序列。
85、所述单链核酸为t3。
86、优选地,所述t3为t3_g4。所述t3_g4的5’末端带有磷酸化修饰。所述5’末端的磷酸化修饰可以在人工合成时添加或者使用多核苷酸磷酸化酶修饰。
87、优选地,所述5’末端的磷酸化修饰是在人工合成时添加的。
88、技术细节二,通过载体上的原位滚环转录,合成具有一定聚合度的多个串联核酸探针,所述串联核酸探针5’端带有偶联官能团3,3’端带有偶联官能团4。
89、本发明中,通过滚环转录合成的串联核酸探针,所述5’端偶联官能团3是在滚环转录的起始步骤中,通过引入偶联官能团3修饰的底物进行标记的。
90、优选地,所述偶联官能团3为地高辛,所述偶联官能团3修饰的底物为地高辛标记的utp,在滚环转录的起始步骤被引入到新生转录本中,使串联核酸探针的5’端标记上地高辛。
91、滚环转录起始后,纯化标记了地高辛的新生rna转录本和滚环转录复合体形成的复合物。通过偶联反应,将纯化后的复合物偶联到载体上。
92、优选地,所述载体为流通池,所述流通池上修饰了地高辛抗体。
93、加入滚环转录所必需的各种核苷酸底物,使滚环转录反应继续进行,并根据串联核酸探针所需聚合度持续转录一段时间。滚环转录的延伸步骤所必需的各种核苷酸底物可以是带有修饰的核苷酸,如甲基化修饰的atp或者甲基化修饰的ctp,也可以是不带有修饰的核苷酸。
94、优选地,所述滚环转录的延伸步骤所必需的各种核苷酸底物是不带有修饰的核苷酸。
95、本发明中,通过滚环转录合成的串联核酸探针,其3’端偶联官能团4的修饰可以通过rna聚合酶或末端转移酶来实现。
96、优选地,所述3’端偶联官能团4是在滚环转录延伸后,通过掺入一定比例的带有偶联官能团4修饰的一种核苷酸底物来实现的。
97、优选地,所述带有偶联官能团4修饰的一种核苷酸底物为生物素标记的utp。
98、优选地,所述生物素标记utp的掺入比例为生物素标记的utp比上未标记的utp等于1:9。
99、技术细节三,通过同步化滚环转录过程,使合成的多个串联核探针的聚合度相对均一。
100、优选地,聚合度相对均一指的是聚合度的均方差小于平均聚合度的20%。
101、本发明中,通过在滚环转录起始步骤的反应试剂中加入缺陷底物来同步化滚环转录过程。所述缺陷底物中缺少滚环转录所必需的核苷酸底物中的至少一种,因此,rna聚合酶工作到需使用缺少的核苷酸底物时暂停。
102、优选地,所述缺陷底物中缺少一种ntp核苷酸底物。
103、优选地,所述缺少的一种ntp核苷酸底物为gtp。
104、通过滚环转录合成串联核酸探针时,其滚环转录过程的所有步骤也可以都在溶液中进行。相较于在载体上原位进行的滚环转录过程,其技术细节的不同点在于:在滚环转录的延伸步骤之前,新生rna转录本和滚环转录复合体形成的复合物经纯化后,不需要预先偶联到载体上。
105、第二方面,单分子力学检测。
106、本发明使用制备的多个串联核酸探针,结合多通道单分子力学技术,实施分子检测。可使用的多通道单分子力学技术可以是单分子磁镊技术、多通道光镊技术、单分子声镊技术、流体力技术等。
107、优选地,所使用的多通道单分子力学技术为单分子磁镊技术。其技术细节在于:
108、技术细节一,通过偶联反应,将串联核酸探针的两端分别偶联到流通池和微球上。
109、优选地,所述偶联反应是指,经滚环扩增合成的串联核酸探针3’端的偶联官能团2或者经滚环转录合成的串联核酸探针3’端的偶联官能团4偶联到流通池或微球上。
110、优选地,将串联核酸探针的3’端连接到磁性微球。
111、优选地,所述磁性微球为商品化的超顺磁球m-270(dynabeads),直径为2.8微米,磁球的表面修饰为链霉亲和素修饰。采用该种超顺磁球m-270的有益效果在于,该种磁球具有均一的饱和磁矩,因此同时操纵时,能够对连接的探针施加均一的拉力。
112、技术细节二,通过退火与间隔序列互补配对的单链,将串联核酸探针中非功能性间隔序列由单链变成双链。所述非功能性间隔序列为不参与待测物检测的序列。有益效果在于增加探针分子的整体硬度,减小检测过程中的布朗运动噪声。
113、优选的,通过滚环扩增合成的串联核酸探针,其间隔序列互补配对的单链为flank1;通过滚环转录合成的串联核酸探针,其间隔序列互补配对的单链为flank2。
114、技术细节三,设置检测实施过程中的力学拉伸模式。力学拉伸模式中含有检测力和结合力。
115、检测力可以为恒力。在检测力下,记录没有待测物时探针的长度作为基准长度。在样品检测过程中,从结合力改变到检测力后,计算探针的长度与基准长度之间的差别作为信号强度。根据信号强度来检测样品中是否存在待测物、待测物浓度、待测物与特异结构的结合速度与结合强度。
116、优选的,当信号强度大于背景噪声均方差的3倍时,判断为存在待测物。
117、在上述技术方案的基础上,通过预先测量待测物浓度与信号强度的标准曲线,根据检测中的信号强度和标准曲线来计算待测物浓度。
118、在上述技术方案的基础上,使用不同的检测力,可以得到不同的信号强度。当检测力小于结合力时,在信号强度减小到大于背景噪声均方差的3倍时的检测力越小,说明结合越强;当检测力大于结合力时,在信号强度减小到大于背景噪声均方差的3倍时的检测力越大,说明结合越强。
119、检测力可以为渐变力。在检测力下,记录没有待测物时探针的长度变化曲线作为基准曲线。在样品检测过程中,在检测力下计算探针的长度变化曲线与基准曲线的差别作为信号强度。根据信号强度来检测样品中是否存在待测物、待测物浓度、待测物与特异结构的结合速度与结合强度。
120、优选的,当信号强度大于背景噪声均方差的3倍时,判断为存在待测物。
121、在上述技术方案的基础上,通过预先测量待测物浓度与信号强度的标准曲线,根据检测中的信号强度和标准曲线来计算待测物浓度。
122、在上述技术方案的基础上,当检测力小于结合力时,检测力逐渐变小,在信号强度减小到大于背景噪声均方差的3倍时的检测力越小说明结合越强;当检测力大于结合力时,检测力逐渐变大,在信号强度减小到大于背景噪声均方差的3倍时的检测力越大,说明结合越强。
123、在上述技术方案的基础上,可以改变维持结合力的时间,即结合时间。根据信号强度与结合时间的关系,在已知待测物浓度的条件下,测量待测物与特异结构的结合速度。
124、在上述技术方案的基础上,当使用多种探针,所述探针含有不同的特异结构时,可以同时检测待测物与不同特异结构的结合强度和结合速度。
125、在一轮检测完成后,可以增加一个探针重生步骤。在该步骤中,核酸探针可以恢复成没有结合待测物的基准状态,以便进行下一轮检测。
126、优选地,所述重生步骤中探针所受拉力为重生力。
127、实施例中检测过程的施力步骤依次为:检测力,记录没有待测物时探针的长度或长度曲线作为基准长度或基准长度曲线;结合力,探针上的靶点序列形成特异结构,识别并结合待测物,结合力下停留的时间越长,待测物与探针结合的数量就越多,结合信号也越强;检测力,记录待测物结合后探针的长度或长度曲线并计算该长度或长度曲线与基准长度或基准长度曲线之间的差别作为信号强度;重生力,结合在探针上的待测物完全解离,探针回到初始未结合待测物的状态。
128、三、同时测量多个串联核酸探针
129、多个串联核酸探针可以序列相同,用于检测相同的待测物。有益效果是一次测量相当于多次测量,节省了检测时间和试剂,减少了假阳性和假阴性。避免了多次检测之间的平行误差。有益效果还有,增加了特异结构的数量。如聚合度为1000时,同时检测100个探针,那么相当于将特异结构数量增加了100,000倍。
130、多个串联核酸探针可以序列不同。因此可以同时检测多种待测物。
131、优选的,所述多种串联核酸探针可以同时检测引起发热的多种病原体的核酸。
132、多个串联核酸探针可以序列不同。因此可以检测同一种待测物对于不同特异结构的结合强度和结合速度。
133、多个串联核酸探针也可以序列不同。因此,检测过程中可以用不含有靶点序列的探针作为阴性对照。有益效果在于,检测生物或临床样本时,利用阴性对照探针去除样本中无关分子带来的背景噪声。
134、可以同时操纵成组的多种核酸探针。组内的各种核酸探针的靶点序列为鉴别序列多态性的序列,所述靶点序列的长度12-26个碱基。其有益效果在于可以用于核酸类待测物的碱基突变检测。该突变可以是单碱基突变,也可以是多碱基突变,可以是碱基转换或碱基颠换突变,也可以是碱基缺失或者碱基插入突变。
135、优选地,所述待测物的碱基突变数量为1-2个。所述待测物上突变碱基的位置对应于探针靶点序列的中间部位。
- 还没有人留言评论。精彩留言会获得点赞!