α-羰基烯基酯类化合物及其制备方法和应用
本发明涉及有机合成化学,特别涉及α-羰基烯基酯类化合物及其制备方法和应用。
背景技术:
1、多肽在药物开发、生物技术、基因检测等具有非常重要的作用,多肽药物的特异性强、靶向性高、且毒性小等特点,使多肽广泛应用于医疗界,全球已经有近70个多肽药物上市,同时还有几百个新的多肽药物处于临床前和临床开发中。多肽类药物成为当前药物研发领域中最活跃和发展最快的部分。因此,开发一种高效的获取多肽的方法一种是多肽科学家们关注的重点。
2、固相多肽合成技术(solid phase peptide synthesis,spps)是由merrifield在上世纪60年代提出,merrifield也因此获得了1984年诺贝尔化学奖。固相多肽合成是多肽合成中一种非常强大也是一种非常重要的技术,在多肽合成领域发挥着重要的作用。固相多肽合成实际上就是将每一个保护起来的氨基酸作为一个砌块,将树脂看成地基,像建筑师一样不断将砌块连接起来成为所需要的生物大分子。相比于其他的合成方法,固相多肽合成存在许多的优点,如生产效率高,操作简单等。值得一提的是,固相多肽合成技术通过近几十年不断的发展,已经实现从原来的人工操作到全自动固相多肽合成的转变。但是遗憾的是,固相多肽合成技术也并非完美,这主要体现在spps使用的聚合物树脂在常规的反应介质中为非均相的化学反应,在氨基酸氨解的过程中需要过量(3~5倍量)的碱、缩合试剂和氨基酸才能保证每一步反应得到最高效率的偶联产物,使多肽的合成成本大大的提高,因此开发一种高效的固相多肽合成技术依然是多肽化学界一个待解决的问题。
3、炔酰胺作为一种含有特殊官能团的化合物,其能够作为缩合剂来促进氨基酸之间形成肽键。在相关技术中,研究者使用炔酰胺作为缩合试剂合成了一系列的二肽,也完成了脑啡肽的合成,证明了炔酰胺是一种有效的多肽缩合试剂。但是由于其活性低,在氨解过程通常需要24h才能反应完全,因此在固相多肽合成中并没有得到有效的运用。
技术实现思路
1、本发明旨在至少解决现有技术中存在的上述技术问题之一。为此,本发明的目的在于提供活性更高的α-羰基烯基酯类化合物及其制备方法和应用。该类炔酰胺活化酯活性高,无需任何添加剂就能够在固相多肽合成中快速构建酰胺键,并且条件温和、操作简单、收率高,与传统的缩合试剂相比,该类炔酰胺缩合试剂拥有制备简便、稳定性好、分子量小、操作简单、原子经济性高,在活化α-手性羧酸时不发生消旋等优点,是一种高效的酰胺键和肽键缩合试剂。本发明还以该类炔酰胺作为缩合试剂,以羧酸和胺为起始原料,成功发展了一种以炔酰胺作为缩合试剂构建肽键的方法。
2、为了实现上述目的,本发明所采取的技术方案是:
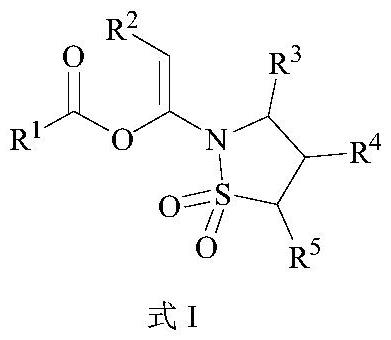
3、本发明的第一个方面,提供了式i化合物或其药学上可接受的盐:
4、
5、其中,r1卤素、硝基、氰基、氨基、烷基、杂烷基、烯基、炔基、环烷基、杂环烷基、芳基、杂芳基、烃氧基、烃硫基、酰基、酰氧基、c端羧基缺失的氨基酸残体、c端羧基缺失的氨基酸类衍生物残体或多肽片段;
6、r2是选自氢、卤素、氰基、烷基、酰基、芳基、杂芳基、烃氧基-羰基;
7、r3、r4、r5是相同或不同的,并且各自独立地选自氢、卤素、氰基、烃基、酰基、烃氧基-羰基;或r4、r5与其相连的原子一起形成选自环烷基、杂环烷基、芳基、杂芳基;
8、其中,所述的烷基、杂烷基、烯基、炔基、环烷基、杂环烷基、芳基、杂芳基、烃氧基、烃硫基任选为非取代,或被一个或多个r11取代;每个r11选自卤素、硝基、氰基、c1~c8烷基、c2~c8烯基、c2~c8炔基、c6~c12芳基、c4~c12杂芳基、c1~c8烃氧基、c1~c8卤代烃氧基、c1~c8烃硫基、c1~c8卤代烃硫基、c1~c8酰基、c1~c8卤代酰基、c1~c8酰氧基、c1~c8卤代酰氧基;
9、所述酰基、酰氧基任选为非取代,或被一个或多个r21取代;每个r21选自卤素、硝基、氰基。
10、在本发明的一些实施方式中,式i化合物选自式i-a化合物式i-b化合物其中,r1、r2、r3的定义如前所述;r8选自h、卤素、硝基、氰基、c1~c8烷基、c2~c8烯基、c2~c8炔基、c6~c12芳基、c4~c12杂芳基、c1~c8烃氧基、c1~c8卤代烃氧基、c1~c8烃硫基、c1~c8卤代烃硫基、c1~c8酰基、c1~c8卤代酰基、c1~c8酰氧基、c1~c8卤代酰氧基;n选自1~4的自然数;m选自1~10的自然数。
11、在本发明的一些实施方式中,r1中所述c端羧基缺失的氨基酸残体或c端羧基缺失的氨基酸类衍生物残体是指氨基酸或氨基酸衍生物中c端羧基缺失后剩余的部分;优选地,所述c端羧基缺失的氨基酸残体包括c端羧基缺失的α-氨基酸残体、c端羧基缺失的β-氨基酸残体或c端羧基缺失的γ-氨基酸残体的至少一种;优选地,所述c端羧基缺失的氨基酸类衍生物残体包括c端氨基保护的c端羧基缺失的氨基酸残体,如c端氨基被n-烷氧羰基和/或n-酰基保护的c端羧基缺失的氨基酸残体;优选地,一般以来表示α-氨基酸,则r1中,所述c端羧基缺失的氨基酸残体为可为r或s构型;具体地,所述c端羧基缺失的氨基酸残体选自
12、优选地,所述c端羧基缺失的氨基酸类衍生物残体选自上述c端羧基缺失的氨基酸残体中c端氨基被n-烷氧羰基和/或n-酰基保护的c端羧基缺失的氨基酸残体。
13、在本发明的一些实施方式中,r1选自卤素、硝基、氰基、氨基、c1~c18烷基、c3~c18环烷基、c3~c18杂环烷基、c2~c18烯基、c2~c18炔基、c6~c18芳基、c4~c18杂芳基、c1~c18烃氧基、c1~c18卤代烃氧基、c1~c18烃硫基、c1~c18卤代烃硫基、c1~c18酰基、c1~c18卤代酰基、c1~c18酰氧基、c1~c18卤代酰氧基、c端羧基缺失的α-氨基酸残体、c端羧基缺失的β-氨基酸残体或c端羧基缺失的γ-氨基酸残体、c端羧基缺失的氨基酸类衍生物残体或多肽片段、保护的氨基c1~c18烷基、保护的氨基c3~c18环烷基、保护的氨基c3~c18杂环烷基、保护的氨基c2~c18烯基、保护的氨基c2~c18炔基、保护的氨基c6~c18芳基、保护的氨基c4~c18杂芳基、保护的氨基c1~c18烃氧基、保护的氨基c1~c18卤代烃氧基、保护的氨基c1~c18烃硫基、保护的氨基c1~c18卤代烃硫基、保护的氨基c1~c18酰基、保护的氨基c1~c18卤代酰基、保护的氨基c1~c18酰氧基、保护的氨基c1~c18卤代酰氧基、保护的氨基c端羧基缺失的α-氨基酸残体、保护的氨基c端羧基缺失的β-氨基酸残体、保护的氨基c端羧基缺失的γ-氨基酸残体、保护的氨基c端羧基缺失的氨基酸类衍生物残体或多肽片段;
14、r2是选自氢、卤素、氰基、c1~c16烷基、c1~c16酰基、c6~c24芳基、c4~c24杂芳基或c1~c16烃氧基-羰基;
15、r3、r4、r5是相同或不同的,并且各自独立地选自氢、卤素、氰基、c1~c16烃基、c1~c16酰基或c1~c16烃氧基-羰基;或r4、r5与其相连的原子一起形成选自c3~c10环烷基、c4~c10杂环烷基、c6~c12芳基、c4~c12杂芳基;
16、其中,所述的烷基、杂烷基、烯基、炔基、环烷基、杂环烷基、芳基、杂芳基、烃氧基、烃硫基、c端羧基缺失的氨基酸残体、c端羧基缺失的氨基酸类衍生物残体或多肽片段任选为非取代,或被一个或多个r11取代;每个r11选自卤素、硝基、氰基、c1~c8烷基、c2~c8烯基、c2~c8炔基、c6~c12芳基、c4~c12杂芳基、c1~c8烃氧基、c1~c8卤代烃氧基、c1~c8烃硫基、c1~c8卤代烃硫基、c1~c8酰基、c1~c8卤代酰基、c1~c8酰氧基、c1~c8卤代酰氧基、保护的氨基;
17、所述酰基、酰氧基任选为非取代,或被一个或多个r21取代;每个r21选自卤素、硝基、氰基。
18、在本发明的一些实施方式中,所述的保护的氨基是指有保护基团保护的氨基;所述保护的氨基包括保护的α-氨基、保护的β-氨基、保护的γ-氨基的至少一种;所述保护基团是本领域中用于保护氨基、氨基酸或多肽链的常用保护基团。例如,保护基团是选自芴甲氧羰基(fmoc),苄氧羰基(cbz),或叔丁氧羰基(boc),烯丙氧羰基(alloc),乙酰基(ac),甲基(me),乙基(et),叔丁基(tbu),三苯甲基(trt)或苄基(bn)中的至少一种。
19、在本发明的一些实施方式中,r1选自卤素、硝基、氰基、氨基、甲基、乙基、丙基、异丙基、丁基、叔丁基、环戊基、环己基、丁烯基、金刚烷基、乙烯基、1-丙烯基、2-丙烯基、1-丁烯基、2-丁烯基、3-丁烯基、乙炔基、1-丙炔基、2-丙炔基、1-丁炔基、2-丁炔基、3-丁炔基、苯乙炔基、苯基、萘基、蒽基、菲基、2-氟苯基、2-氯苯基、2-溴苯基、3-氟苯基、3-氯苯基、3-溴苯基、4-氟苯基、4-氯苯基、4-溴苯基、吡咯基、吲哚基、吲哚甲基、吲唑基、呋喃基、苯并呋喃基、噻吩基、苯并噻吩基、苯乙烯基、苯乙炔基、苄基、11-羟基十一烷基、十五烷基、保护的α-氨基c2~c10烷基、保护的β-氨基c3~c10烷基、保护的γ-氨基c4~c10烷基、保护的氨基c端羧基缺失的α-氨基酸残体、保护的氨基c端羧基缺失的β-氨基酸残体、保护的氨基c端羧基缺失的γ-氨基酸残体、保护的氨基c端羧基缺失的氨基酸类衍生物残体或多肽片段。
20、在本发明的一些实施方式中,r1选自卤素、硝基、氰基、氨基、甲基、乙基、丙基、异丙基、丁基、叔丁基、环戊基、环己基、丁烯基、金刚烷基、乙烯基、1-丙烯基、2-丙烯基、1-丁烯基、2-丁烯基、3-丁烯基、乙炔基、1-丙炔基、2-丙炔基、1-丁炔基、2-丁炔基、3-丁炔基、苯乙炔基、苯基、萘基、蒽基、菲基、2-氟苯基、2-氯苯基、2-溴苯基、3-氟苯基、3-氯苯基、3-溴苯基、4-氟苯基、4-氯苯基、4-溴苯基、吡咯基、吲哚基、吲哚甲基、吲唑基、呋喃基、苯并呋喃基、噻吩基、苯并噻吩基、苯乙烯基、苯乙炔基、苄基、11-羟基十一烷基、十五烷基、保护的甘氨酸、保护的丙氨酸、保护的苯丙氨酸、保护的缬氨酸、保护的半胱氨酸、保护的蛋氨酸、保护的亮氨酸、保护的异亮氨酸、保护的甲硫氨酸、保护的脯氨酸、保护的色氨酸、保护的丝氨酸、保护的酪氨酸、保护的谷氨酰胺、保护的天冬酰胺、保护的精氨酸、保护的苏氨酸、保护的谷氨酸、保护的天冬氨酸、保护的赖氨酸、保护的组氨酸。
21、在本发明的一些实施方式中,r2选自氢、氟、氯、溴、甲基、甲酰基、乙酰基、丙酰基、苯基、4-氟苯基、4-氯苯基、4-溴苯基、4-甲基苯基、4-甲氧基苯基、2-甲基苯基、2-甲氧基苯基、3,5-二甲氧基苯基、3-硝基苯基、4-硝基苯基、2,4-二硝基苯基、3,5-二硝基苯基、五氟苯基、4-三氟甲基苯基、3,5-二氯苯基、1-萘基、2-萘基、呋喃基、噻吩基、吡啶基。
22、在本发明的一些实施方式中,r3、r4、r5各自独立地选自氢、氰基、甲基、甲酰基、乙酰基、丙酰基、丁酰基、甲氧基羰基、乙氧基羰基、叔丁氧羰基、苄氧羰基;或r4、r5与其相连的原子一起形成环丙基、环丁基、环戊基、环己基、降冰片基(双环[2.2.1]庚基)、双环[2.2.2]辛基、金刚烷基、环氧乙烷基、环硫乙烷基、环氮乙烷基、吖丁啶基、噁丁环基、噻丁环基、四氢呋喃基、四氢噻吩基、吡咯烷基、异噁唑烷基、噁唑烷基、异噻唑烷基、噻唑烷基、咪唑烷基、四氢吡唑基、哌啶基、四氢吡喃基、四氢噻喃基、吗啉基、哌嗪基、1,4-噻噁烷基、1,4-二氧六环基、硫代吗啉基、1,3-二噻烷基、1,4-二噻烷基、氮杂环庚烷基、氧杂环庚烷基、硫杂环庚烷基、苯基、邻甲苯基、间甲苯基、对甲苯基、2,4-二甲苯基、对枯烯基、均三甲苯基、1-萘基、2-萘基、1-蒽基、2-蒽基、9-蒽基、1-菲基、9-菲基、1-苊基、2-薁基、1-芘基、2-三亚苯基、邻联苯基、间联苯基、对联苯基、三联苯基、三唑基、3-噁二唑基、2-呋喃基、3-呋喃基、2-噻吩基、3-噻吩基、1-吡咯基、2-吡咯基、3-吡咯基、2-吡啶基、3-吡啶基、4-吡啶基、2-吡嗪基、2-噁唑基、3-异噁唑基、2-噻唑基、3-异噻唑基、2-咪唑基、3-吡唑基、2-喹啉基、3-喹啉基、4-喹啉基、5-喹啉基、6-喹啉基、7-喹啉基、8-喹啉基、1-异喹啉基、2-喹噁啉基、2-苯并呋喃基、2-苯并噻吩基、n-吲哚基、n-咔唑基。
23、在本发明的一些实施方式中,式i化合物选自以下化合物:
24、(e)-n-芴甲氧羰基-l-甘氨酸-1,1-二氧代苯并异噻唑-2-乙烯基-1-酯
25、
26、(e)-n-芴甲氧羰基-l-丙氨酸-1,1-二氧代苯并异噻唑-2-乙烯基-1-酯
27、
28、(e)-n-苄氧羰基-l-丙氨酸-1,1-二氧代苯并异噻唑-2-乙烯基-1-酯
29、
30、(e)-n-苄氧羰基-l-苯丙氨酸-1,1-二氧代苯并异噻唑-2-乙烯基-1-酯
31、
32、(e)-n-苄氧羰基-l-缬氨酸-1,1-二氧代苯并异噻唑-2-乙烯基-1-酯
33、
34、(e)-n-叔丁氧碳基-l-丙氨酸-1,1-二氧代苯并异噻唑-2-乙烯基-1-酯
35、
36、(e)-n-叔丁氧碳基-s-三苯甲基-l-半胱氨酸-1,1-二氧代苯并异噻唑-2-乙烯基-1-酯
37、
38、(e)-n-叔丁氧碳基-l-蛋氨酸-1,1-二氧代苯并异噻唑-2-乙烯基-1-酯
39、
40、(e)-n-芴甲氧羰基-l-苯丙氨酸-1,1-二氧代苯并异噻唑-2-乙烯基-1-酯
41、
42、(e)-n-芴甲氧羰基-l-亮氨酸-1,1-二氧代苯并异噻唑-2-乙烯基-1-酯
43、
44、(e)-n-芴甲氧羰基-l-异亮氨酸-1,1-二氧代苯并异噻唑-2-乙烯基-1-酯
45、
46、(e)-n-芴甲氧羰基-l-甲硫氨酸-1,1-二氧代苯并异噻唑-2-乙烯基-1-酯
47、
48、(e)-n-芴甲氧羰基-l-缬氨酸-1,1-二氧代苯并异噻唑-2-乙烯基-1-酯
49、
50、(e)-n-芴甲氧羰基-l-脯氨酸-1,1-二氧代苯并异噻唑-2-乙烯基-1-酯
51、
52、(e)-n-芴甲氧羰基-l-色氨酸-1,1-二氧代苯并异噻唑-2-乙烯基-1-酯
53、
54、(e)-n-芴甲氧羰基-o-叔丁基-l-丝氨酸-1,1-二氧代苯并异噻唑-2-乙烯基-1-酯
55、
56、(e)-n-芴甲氧羰基-o-叔丁基-l-酪氨酸-1,1-二氧代苯并异噻唑-2-乙烯基-1-酯
57、
58、(e)-n-芴甲氧羰基-s-三苯甲基-l-半胱氨酸-1,1-二氧代苯并异噻唑-2-乙烯基-1-酯
59、
60、(e)-n-芴甲氧羰基-n’-三苯甲基-l-谷氨酰胺-1,1-二氧代苯并异噻唑-2-乙烯基-1-酯
61、
62、(e)-n-芴甲氧羰基-n’-三苯甲基-l-天冬酰胺-1,1-二氧代苯并异噻唑-2-乙烯基-1-酯
63、
64、(e)-n-苄氧羰基-n’,n”-二苄氧羰基-l-精氨酸-1,1-二氧代苯并异噻唑-2-乙烯基-1-酯
65、
66、(e)-n-苄氧羰基-o-叔丁基-l-苏氨酸-1,1-二氧代苯并异噻唑-2-乙烯基-1-酯
67、
68、(e)-n-苄氧羰基-o-叔丁基-l-天冬氨酸-1,1-二氧代苯并异噻唑-2-乙烯基-1-酯
69、
70、(e)-n-叔丁氧羰基-o-叔丁基-l-谷氨酸-1,1-二氧代苯并异噻唑-2-乙烯基-1-酯
71、
72、(e)-n-叔丁氧羰基-n’-叔丁氧羰基-l-赖氨酸-1,1-二氧代苯并异噻唑-2-乙烯基-1-酯
73、
74、(e)-n-叔丁氧羰基-n’-叔丁氧羰基-l-组氨酸-1,1-二氧代苯并异噻唑-2-乙烯基-1-酯
75、
76、(e)-n-叔丁氧羰基-l-蛋氨酸-1,1-二氧异噻唑-2-乙烯基-1-酯
77、
78、本发明的第二个方面,提供了式ii化合物或其药学上可接受的盐:
79、
80、其中,r2、r3、r4、r5的定义如前所述。
81、在本发明的一些实施方式中,式ii化合物选自下列化合物:
82、2-乙炔基异噻唑烷1,1-二氧化物
83、
84、2-乙炔基-2,3-二氢苯并异噻唑1,1-二氧化物
85、
86、本发明的第三个方面,提供了所述的式i化合物的制备方法,包括以下步骤:
87、
88、将式ii化合物与式iii化合物反应制得式i化合物;
89、其中,r1、r2、r3、r4、r5的定义如前所述。
90、在本发明的一些实施方式中,式ii化合物与式iii化合物的摩尔比为1:(1~2);优选为1:(1~1.5);更优选为1:(1-1.2)。
91、在本发明的一些实施方式中,所述反应的溶剂与式ii化合物的摩尔比为(70~170):1,优选为(90~150):1,更优选为(110~130):1。
92、在本发明的一些实施方式中,所述反应的溶剂有机溶剂;优选为非质子有机溶剂。优选地所述非质子有机溶剂包括二氯甲烷、三氯甲烷、二氯甲烷、乙腈、四氢呋喃、水、乙醚和甲苯中的一种或多种,优选为二氯甲烷、三氯甲烷和二氯甲烷中的至少一种;更优选为二氯甲烷。
93、在本发明的一些实施方式中,所述反应的温度为0℃~100℃;例如为20℃~60℃、30℃~50℃。
94、在本发明的一些实施方式中,所述反应的时间为0.5h~320h;例如为1.0h~240h、5.0h~180h。
95、本发明的第四个方面,提供了一种式ii化合物的制备方法,其特征在于:包括以下步骤:
96、
97、将式iv化合物与式v化合物反应制得式ii化合物;
98、其中,r2、r3、r4、r5的定义如权利要求1~6任一项所述;x为卤素。
99、在本发明的一些实施方式中,式iv化合物与式v化合物的摩尔比为1:(1~2);优选为1:(1~1.5);更优选为1:(1-1.2)。
100、在本发明的一些实施方式中,所述反应的溶剂与式iv化合物的摩尔比为(70~170):1,优选为(90~150):1,更优选为(110~130):1。
101、在本发明的一些实施方式中,所述反应的溶剂有机溶剂;优选为非质子有机溶剂。优选地所述非质子有机溶剂包括二氯甲烷、三氯甲烷、二氯甲烷、乙腈、四氢呋喃、水、乙醚和甲苯中的一种或多种,优选为二氯甲烷、三氯甲烷和二氯甲烷中的至少一种;更优选为二氯甲烷。
102、在本发明的一些实施方式中,所述反应的温度为0℃~100℃;例如为20℃~60℃、30℃~50℃。
103、在本发明的一些实施方式中,所述反应的时间为0.5h~320h;例如为1.0h~240h、5.0h~180h。
104、本发明的第五个方面,提供了一种式vii化合物的制备方法,包括以下步骤:
105、将所述的式i化合物或其药学上可接受的盐与式vi化合物反应制得式vii化合物
106、其中,r1的定义如前所述;
107、r6和r7分别各自独立地选自氢、氨基、c1~c24烃基、具有伯胺和/或仲胺基团的氨基低聚物或氨基聚合物;或者,r6和r7与它们所连接的n原子一起形成c3~c24环状基团;所述烃基任选为非取代,或被一个或多个r31取代;
108、r31选自卤素、氨基、羟基、羧基、巯基、硝基、氰基、c1~c8烃基、卤代c1~c8烃基、c1~c8烃氧基、c1~c8卤代烃氧基、c1~c8烃硫基、c1~c8卤代烃硫基、c1~c8酰基、c1~c8卤代酰基、c1~c8酰氧基、c1~c8卤代酰氧基。
109、本发明中,式i化合物是合成式vi化合物的酰化试剂。
110、在本发明的一些实施方式中,r6和r7分别各自独立地选自氢、氨基、c1~c18烃基、具有伯胺和/或仲胺基团的氨基低聚物或氨基聚合物;或者,r6和r7与它们所连接的n原子一起形成c3~c18环状基团;所述烃基任选为非取代,或被一个或多个r31取代;r31的定义如前所述。
111、在本发明的一些实施方式中,r6和r7分别各自独立地选自氢、c1~c12烃基、具有伯胺和/或仲胺基团的氨基低聚物或氨基聚合物;或者,r6和r7与它们所连接的n原子一起形成c3~c12环状基团;所述烃基任选为非取代,或被一个或多个r31取代;r31的定义如前所述。
112、在本发明的一些实施方式中,所述的氨基低聚物包括多肽链;所述的氨基聚合物包括蛋白质或聚胺。
113、在本发明的一些实施方式中,r6和r7分别各自独立地选自氢、氨基、甲基、乙基、丙基、异丙基、丁基、叔丁基、环戊基、环己基、环庚基、环辛基、环丁烷二基、环戊烷二基、环己烷二基、环庚烷二基、环辛烷二基、羟乙基苯基、苯基、乙基苯基、苯乙基、萘基、3-吲哚乙基、α-酰基c1~c20烷基、β-酰基c2~c20烷基、γ-酰基c3~c20烷基、多肽链c1~c20烷基或多肽链c1~c20链烯基中的一种。
114、在本发明的一些实施方式中,r6和r7不同时为氨基。
115、在本发明的一些实施方式中,式vi化合物是具有至少一个n-h键的化合物。式vi化合物选自氨、肼、含有伯胺和/或仲胺基团的c1~c50有机胺(即,具有至少一个n-h键的有机胺类化合物,优选c1~c32有机胺或氨基酸,更优选c1~c24有机胺,更优选c1~c12有机胺);或,具有伯胺和/或仲胺基团的((例如聚合度在2~1000之间,优选在3~500之间,优选在4~200之间,优选在5~100之间,更优选在6~20之间的)氨基低聚物或氨基聚合物(包括多肽或蛋白质或聚胺)。
116、在本发明的一些实施方式中,式i化合物与式vi化合物的摩尔比为1:(1~2);优选为1:(1~1.5);更优选为1:(1-1.2)。
117、在本发明的一些实施方式中,所述反应的溶剂与式i化合物的摩尔比为(30~180):1,优选为(50~150):1,更优选为(80~120):1。
118、在本发明的一些实施方式中,所述反应的溶剂为有机溶剂,优选为非质子有机溶剂;所述非质子性有机溶剂包括四氢呋喃、二甲基亚砜、n,n-二甲基甲酰胺、乙腈中的至少一种;优选为二甲基亚砜和/或n,n-二甲基甲酰胺;更优选为n,n-二甲基甲酰胺。
119、在本发明的一些实施方式中,所述反应的温度为-40℃~100℃;例如为0℃~60℃、30℃~50℃。
120、在本发明的一些实施方式中,所述反应的时间为0.05h~24h;例如为0.5h~15h、1h~10h。
121、在本发明的一些实施方式中,所述的式vii化合物的制备方法,包括以下步骤:
122、
123、式ii化合物与式iii化合物在第一溶剂中反应制得式i化合物,式i化合物与式vi化合物在第二溶剂中反应制得式vii化合物;
124、其中,r1、r2、r3、r4、r5、r6、r7的定义如前所述。
125、本发明中,上述反应无需加剂和催化剂,还可以采用“一锅两步”法反应得到式vii化合物。
126、本发明中,研究发现,式iii羧酸类化合物可以和式ii炔酰胺化合物发生1,4-加成反应,得到相应的式i化合物(α-羰基烯基酯类化合物),这类烯基酯比较活泼,可以与一级或二级胺发生高效的胺解反应,得到相应的酰胺类化合物。并且,由于该步胺解反应速度快,且无需额外的催化剂和添加剂便可发生反应,可以很好地抑制α-手性羧酸在活化过程中的消旋化。炔酰胺作为缩合试剂,具有制备简单、分子量小、在活化α-手性羧酸时不发生消旋的优点。同时,该反应条件温和,操作简单,其副产物苯甲酰丙酮也在合成中有重要价值,符合现代化学中的绿色化学的方向,具有优良的原子经济性。因此,将炔酰胺用于酰胺键和肽键合成将会是一种新的、高效而且实用的合成方法。
127、在本发明的一些实施方式中,所述第一溶剂与第二种溶剂可相同或不同。
128、在本发明的一些实施方式中,所述第一溶剂与第二种溶剂不同时,所述的式vii化合物的制备方法还包括在式ii化合物与式iii化合物反应后先除去第一溶剂再继续反应。
129、在本发明的一些实施方式中,所述第一溶剂为有机溶剂,优选为非质子有机溶剂;所述第一溶剂为二氯甲烷、三氯甲烷、二氯甲烷、乙腈、四氢呋喃、水、乙醚和甲苯中的至少一种;优选为二氯甲烷、三氯甲烷和二氯甲烷中的至少一种。更优选为二氯甲烷。
130、在本发明的一些实施方式中,所述第二溶剂为有机溶剂,优选为非质子有机溶剂;所述第二溶剂为四氢呋喃、二甲基亚砜、n,n-二甲基甲酰胺、乙腈中的至少一种。优选为二甲基亚砜和/或n,n-二甲基甲酰胺。更优选为n,n-二甲基甲酰胺。
131、本发明的第六个方面,提出了一种多肽的合成方法,包括以下步骤:
132、在树脂固相载体中,依照多肽链序列至少加入一个多肽链序列相对应的端基氨基酸式i化合物(α-羰基烯基酯类化合物)进行偶联反应,制得pg-(aa)q-树脂;脱除侧链保护基和树脂后,制得多肽;
133、其中,q为大于等于2的自然数;pg指代固相载体上多肽链主链末端的保护基,aa指代固相载体上多肽链主链上单个的氨基酸。
134、在本发明的一些实施方式中,所述多肽的合成方法包括以下步骤:在树脂固相载体中,依照多肽链序列至少加入一个多肽链序列相对应的端基氨基酸式i化合物(α-羰基烯基酯类化合物)进行偶联反应,制得pg-(aa)q-树脂;脱保护,裂解,脱除侧链保护基和树脂后,纯化制得多肽。
135、在本发明的一些实施方式中,所述裂解采用的裂解液三氟乙酸:三异丙基硅烷:水=95:2.5:2.5或三氟乙酸:乙二硫醇:三异丙基硅烷:水=92.5:2.5:2.5:2.5。
136、在本发明的一些实施方式中,所述多肽的合成方法还包括以下步骤:1)采用脱保护试剂脱除pg-aa-树脂上的保护基pg,得到h-aa-树脂;2)在催化剂的存在下,加入与pg-aa-oh对应的式i化合物(α-羰基烯基酯类化合物),在溶剂中偶联得到pg-(aa)2-树脂;3)按照目标肽链的序列,依次重复步骤1)和步骤2)制得pg-(aa)q-树脂,脱保护,裂解,脱除侧链保护基和树脂后,纯化制得多肽。
137、在本发明的一些实施方式中,步骤1)中所述脱保护试剂的用量为pg-(aa)q-树脂摩尔量的1~100倍;例如为2~80倍、3~50倍。
138、在本发明的一些实施方式中,当树脂固相载体上多肽链主链末端的保护基为fmoc(芴甲氧羰基)时,脱保护试剂为哌啶的n,n-二甲基甲酰胺溶液,其加入量为pg-(aa)q-树脂的摩尔量的1~100倍;例如为2~80倍、3~50倍;当固相载体上多肽链主链末端的保护基为boc(叔丁氧羰基)时,脱保护试剂为三氟乙酸的二氯甲烷溶液,其加入量为pg-(aa)q-树脂的摩尔量的1~100倍;例如为2~80倍、3~50倍。
139、在本发明的一些实施方式中,所述偶联反应的溶剂为有机溶剂;优选为非质子有机溶剂;优选地,所述非质子性有机溶剂为n,n-二甲基甲酰胺(dmf)和/或二甲基亚砜(dmso);优选为n,n-二甲基甲酰胺(dmf)。
140、在本发明的一些实施方式中,所述偶联反应的溶剂与pg-(aa)q-树脂的质量比为(10~300):1;例如为(20~200):1、(30~100):1。
141、在本发明的一些实施方式中,所述纯化采用反向高效液相色谱进行纯化,色谱柱为c18反向硅胶柱,流动相为水和乙腈。
142、在本发明的一些实施方式中,pg选自芴甲氧羰基(fmoc)、苄氧羰基(cbz)、叔丁氧羰基(boc)、烯丙氧羰基(alloc)、乙酰基(ac)、甲基(me)、乙基(et)、叔丁基(tbu)、三苯甲基(trt)或苄基(bn)中的至少一种;优选地,pg选自芴甲氧羰基(fmoc)或叔丁氧羰基(boc)中的一种;优选为芴甲氧羰基(fmoc)。
143、在本发明的一些实施方式中,树脂固相载体选自marrifield树脂、wang树脂、2-ctc树脂、mbha树脂中的任意一种。
144、在本发明的一些实施方式中,所述偶联反应的催化剂包括hoat(1-羟基-7-偶氮苯并三氮唑)、hobt(1-羟基苯并三唑)、hoobt(3-羟基-1,2,3-苯并三嗪-4(3h)-酮)、hosu(n-羟基琥珀酰亚胺)、comu((2-肟基-氰基乙酸乙酯)-n,n-二甲基-吗啉基脲六氟磷酸酯)、hopht(n-羟基邻苯二甲酰亚胺)中的任意一种;优选为hoat(1-羟基-7-偶氮苯并三氮唑)或hobt(1-羟基苯并三唑);更优选为hobt(1-羟基苯并三唑)。
145、在本发明的一些实施方式中,所述催化剂的用量为树脂固相载体摩尔量的0.3~10倍;例如为1~5倍、1~3倍。
146、在本发明的一些实施方式中,所述偶联反应还可在碱作用下进行,所述碱包括4-二甲氨基吡啶、吡啶、n-甲基咪唑、n,n-二异丙基乙胺(diea)中的至少一种;优选为n,n-二异丙基乙胺(diea)。
147、在本发明的一些实施方式中,所述碱的用量为pg-(aa)q-树脂摩尔量的1~10倍;例如为1~6倍、1~3倍。
148、在本发明的一些实施方式中,所述α-羰基烯基酯类化合物的用量为pg-(aa)q-树脂摩尔量的1~10倍;例如为1~6倍、1~3倍。
149、在本发明的一些实施方式中,当选择的是树脂固相载体(例如2-ctc树脂)和与目标多肽链序列的端部氨基酸进行反应时,该反应优选的是在具有碱存在的反应环境中进行;而当选择的是树脂固相载体(例如mbha树脂)和与目标多肽链序列的端部氨基酸相对应的α-羰基烯基酯类化合物进行反应时,该反应优选的是在具有催化剂存在的反应环境进行;如果选用的是其他的树脂固相载体(例如wang树脂)那么还可以根据树脂固相载体和与目标多肽链序列的端部氨基酸或与端部氨基酸相对应的α-羰基烯基酯类化合物的不同组合方式进行任选地选择使用更适宜的缩合试剂。
150、本发明的第七个方面,提出了所述的式i化合物或其药学上可接受的盐在制备酰胺类化合物和/或多肽中的应用。
151、本发明中,所述保护的α-氨基烷基、保护的β-氨基烷基、保护的γ-氨基烷基和多肽链烷基中的保护指的是对主链上的末端氨基进行保护,所述对主链上的末端氨基进行保护的基团即为主链保护基,所述对主链上的末端氨基进行保护的主链保护基选自fmoc(芴甲氧羰基)、cbz(苄氧羰基)、boc(叔丁氧羰基)、alloc(烯丙氧羰基)、ac(乙酰基)中的一种。对主链上的末端氨基进行保护的目的在于避免末端氨基在使用式ii化合物及式iii化合物合成式i化合物反应过程中的影响。
152、进一步的,保护的α-氨基烷基、保护的β-氨基烷基、保护的γ-氨基烷基和多肽链烷基还可以是在保护主链上的末端氨基的同时也对侧链上的官能团进行保护,所述侧链上需要保护的官能团选自羟基、巯基、氨基、伯酰胺基、羧基中的一种或几种,所述对侧链上的官能团进行保护的基团即为侧链保护基,所述对侧链上的官能团进行保护的侧链保护基选自fmoc(芴甲氧羰基)、cbz(苄氧羰基)、boc(叔丁氧羰基)、alloc(烯丙氧羰基)、ac(乙酰基)、me(甲基)、et(乙基)、tbu(叔丁基)、trt(三苯甲基)、bn(苄基)中的一种或几种。所述带有主链保护基或同时带有主链保护基及侧链保护基的羧酸类化合物,均可通过合成或直接购买得到。对主链上的末端氨基及侧链上的官能团进行保护的目的在于避免末端氨基及侧链上的官能团在使用式ii化合物及式iii化合物合成式i化合物反应过程中的影响(例如基团相互间会发生反应或者会阻止目标反应的进行等)。
153、术语“取代”是指分子中的氢原子被其它不同的原子或基团所替换。
154、术语“多个”是指两个或更多的数量,因而本发明中描述的被多个基团取代,是指被两个或更多的基团取代,具体的取代基个数,受到被取代基团的可取代位点个数及空间位阻的影响,通常是指被两个、三个、四个、五个或六个基团取代,进一步优选被两个或三个基团取代。
155、术语“烃基”或“杂烃基”包括饱和或不饱和的直链或支链或环状的烃基。“杂烃基”任选地含有杂原子如氧、硫或氮。当烃基中包含环状基团时,该环状基团可以是碳环或杂环基团,该杂环基团例如是杂环烷基或杂芳基。烃基优选为烷基、链烯基、炔基、环烷基、芳基或杂芳基。具体来说,烃基包括烷基,杂环烷基,链烯基,炔基,芳基,环烷基,烷基芳基,链烯基芳基,炔基芳基,芳基烷基,芳基环烷基,芳基链烯基或芳基炔基;杂烃基包括杂芳基,烷基杂芳基,链烯基杂芳基,炔基杂芳基,杂芳基烷基,杂芳基链烯基或杂芳基炔基。
156、术语“烷基”是指具有指定数目的碳原子的饱和经基。例如,c1~c18烷基是指具有1至18个碳原子,例如优选具体1至6个碳原子的烷基基团。烷基基团可以是直链或支链的。代表性的支链烷基基团具有一个、两个或三个支链。烷基基团也可任选地被一个或多个如本文所定义的取代基取代。烷基的具体实例包括甲基、乙基、正丙基、异丙基、正丁基、异丁基、仲丁基、叔丁基、正戊基、异戊基、2-甲基丁基、新戊基、1-乙基丙基、正己基、异己基、3-甲基戊基、2-甲基戊基、1-甲基戊基、3,3-二甲基丁基、2,2-二甲基丁基、1,1-二甲基丁基、1,2-二甲基丁基、1,3二甲基丁基、2,3-二甲基丁基、2-乙基丁基、1,2-二甲基丙基、新戊基、己基、2-甲基戊基等。
157、术语“环烷基”指完全饱和的并且可以以呈单环、桥环或螺环存在的碳环。除非另有指示,该碳环通常为3至18元环,或3至10元环。环烷基非限制性实例包括但不限于环丙基、环丁基、环戊基、环己基、降冰片基(双环[2.2.1]庚基)、双环[2.2.2]辛基、金刚烷基等。
158、术语“杂环烷基”是指完全饱和的并且可以以单环、桥环或螺环存在的环状基团。除非另有指示,该杂环通常为含有1至3个独立地选自硫、氧和/或氮的杂原子(优选1或2个杂原子)的3至10元环,或者该杂环通常为含有1至3个独立地选自硫、氧和/或氮的杂原子(优选1或2个杂原子)的3至7元环。杂环烷基可以为含有1或2个独立地选自氧和氮的杂原子的3至6元环。3元杂环烷基的实例包括但不限于环氧乙烷基、环硫乙烷基、环氮乙烷基,4元杂环烷基的非限制性实例包括但不限于吖丁啶基、噁丁环基、噻丁环基,5元杂环烷基的实例包括但不限于四氢呋喃基、四氢噻吩基、吡咯烷基、异噁唑烷基、噁唑烷基、异噻唑烷基、噻唑烷基、咪唑烷基、四氢吡唑基,6元杂环烷基的实例包括但不限于哌啶基、四氢吡喃基、四氢噻喃基、吗啉基、哌嗪基、1,4-噻噁烷基、1,4-二氧六环基、硫代吗啉基、1,3-二噻烷基、1,4-二噻烷基,7元杂环烷基的实例包括但不限于氮杂环庚烷基、氧杂环庚烷基、硫杂环庚烷基。其余多元杂环依此类推。
159、术语“烯基”是指具有指定数目个碳原子且具有至少1个碳碳双键(>c=c<)的直链或支链不饱和烃基基团。例如,ca~cb烯基是指具有a至b个碳原子的含烯基的不饱和烃基,烯基的具体实例包括乙烯基、丙烯基、异丙烯基、1,3-丁二烯基等。
160、“炔基”是指含有至少一个碳碳三键的直链或支链一价烃基。术语“炔基”还意在包括具有一个三键和一个双键的那些烃基基团。例如,c2~c6炔基的具体实例包括乙炔基、丙炔基等。
161、术语“芳基”选自苯基、邻甲苯基、间甲苯基、对甲苯基、2,4-二甲苯基、对枯烯基、均三甲苯基、1-萘基、2-萘基、1-蒽基、2-蒽基、9-蒽基、1-菲基、9-菲基、1-苊基、2-薁基、1-芘基、2-三亚苯基、邻联苯基、间联苯基、对联苯基、三联苯基。
162、术语“杂芳基”选自具有1个或2个氮原子、氧原子或硫原子,并且优选为5~10元的杂环基,例如,可以举出三唑基、3-噁二唑基、2-呋喃基、3-呋喃基、2-噻吩基、3-噻吩基、1-吡咯基、2-吡咯基、3-吡咯基、2-吡啶基、3-吡啶基、4-吡啶基、2-吡嗪基、2-噁唑基、3-异噁唑基、2-噻唑基、3-异噻唑基、2-咪唑基、3-吡唑基、2-喹啉基、3-喹啉基、4-喹啉基、5-喹啉基、6-喹啉基、7-喹啉基、8-喹啉基、1-异喹啉基、2-喹噁啉基、2-苯并呋喃基、2-苯并噻吩基、n-吲哚基、n-咔唑基。
163、术语“有机胺类化合物(oa,organic amines)”,即,具有至少一个n-h键的有机胺类化合物,是选自于下列这些中的有机胺类化合物:
164、氨基酸类;
165、c1~c24烃基胺类(伯胺类),例如甲胺、乙胺、丙胺、丁基胺、戊基胺、己基胺、庚基胺、辛基胺、壬基胺、癸基胺、十二烷基胺、二十四烷基胺、未取代或取代(如卤素取代)的苯胺、甲基环己基胺、n-甲基苄胺,等等;
166、二(c1~c16烃基)胺类(仲胺类,即具有一个仲胺基的单胺类),例如二甲胺,二乙基胺,二(十二烷基)胺,或二(十六烷基)胺,等等;
167、任选在c2~c14亚烃基上被羟基取代的c2~c14亚烃基二胺类(其中两个胺基各自独立地是伯胺基或仲胺基),例如乙二胺、n-甲基乙二胺、n,n’-二甲基乙二胺、1,3-丙二胺、n-甲基,n’乙基-1,3-丙二胺、丁二胺(包括各种异构体,如1,2-或1,3-或1,4-丁二胺)、3,6-二羟基癸二胺、十二烷二胺、p-或m-苯二胺、3,3’-二氯-4,4’-二苯基甲烷二胺(moca)、哌嗪,等等;
168、任选在c4~c16亚烃基上被羟基取代的c4~c16多亚烷基多胺类,例如二亚乙基三胺、三亚乙基四胺、四亚乙基五胺、五亚乙基六胺、二亚丙基三胺、三亚丙基四胺、三(2-羟基-1,3-亚丙基)四胺或四(2-羟基-1,3-亚丙基)五胺;等;
169、具有三个伯胺基的任选被羟基取代的c3~c18有机三胺类或具有四个伯胺基的任选被羟基取代的c5~c18有机四胺类,例如1,3,5-三氨基-环己烷、1,3,5-三(氨基乙基)-环己烷、1,3,5-三(氨基丙基)-1,3,5-六氢化三嗪、1,3,5-三(甲基胺丙基)-1,3,5-六氢化三嗪、三聚氰胺、季戊四胺、等等;或
170、c2~c10醇胺类,例如一乙醇胺、二乙醇胺、一丙醇胺、二丙醇胺、单异丙醇胺、二异丙醇胺、单丁醇胺、二丁醇胺,等。
171、术语“药学上可接受的”是指在化学上或物理上与构成某药物剂型的其它成分相兼容,并在生理上与受体相兼容。
172、术语“盐”是指化合物或其立体异构体,与无机酸、有机酸或碱形成的酸式或碱式盐,也包括两性离子盐(内盐),还包括季铵盐,例如烷基铵盐。这些盐可以是在化合物制备过程中经分离和纯化制得,也可以是通过将上述化合物或其立体异构体,与一定数量的酸或碱适当(例如等当量)进行混合而得到。这些盐可能在溶液中形成沉淀而以过滤方法收集,或在溶剂蒸发后回收而得到,或在水介质中反应后冷冻干燥制得。本发明中所述盐可以是化合物的盐酸盐、硫酸盐、枸橼酸盐、苯磺酸盐、氢溴酸盐、氢氟酸盐、磷酸盐、乙酸盐、丙酸盐、丁二酸盐、草酸盐、苹果酸盐、琥珀酸盐、富马酸盐、马来酸盐、酒石酸盐或三氟乙酸盐等。
173、本发明的有益效果是:
174、1、本发明提供了一种α-羰基烯基酯类化合物及其合成方法,还将该类炔酰胺化合物用于与一级或二级胺反应制备酰胺类化合物,从而发展了一种以羧酸和胺为起始原料,以炔酰胺为缩合剂的酰胺键和肽键形成方法,并将α-氨基酸的α-羰基烯基酯作为多肽合成砌块用于多肽固相合成中。
175、2、本发明中合成方法反应条件温和、操作简单、收率高。与现有酰胺键缩合试剂相比,该类炔酰胺拥有制备简便、稳定性好、分子量小,在活化α-手性羧酸时不发生消旋等优点,符合现代化学中的绿色化学的方向,具有优秀的原子经济性,是一种新型的酰胺键和肽键缩合试剂。
- 还没有人留言评论。精彩留言会获得点赞!