阿纳其根中具有抗炎作用的化合物及其制备和应用
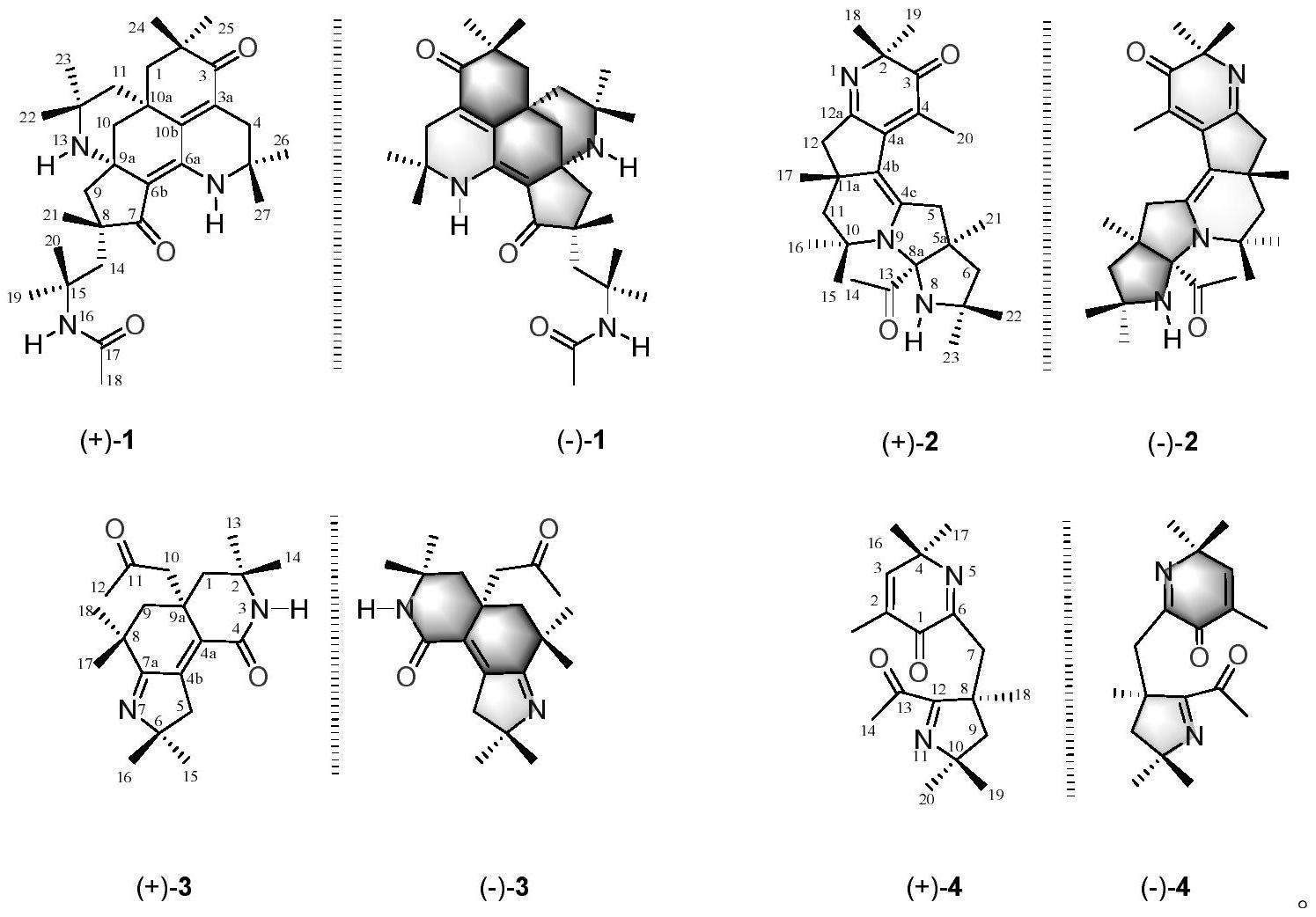
本发明属于医药,具体涉及阿纳其根中具有抗炎作用的化合物(式1、式2、式3或式4的化合物)及其制备和应用。
背景技术:
1、从传统药用植物中探寻显著药效活性的先导化合物是药物研究的热点,因此,从药用植物中发现新颖的具有抗炎作用的化合物是开发新型抗炎药物的有效途径。
2、阿纳其根是罗马除虫菊(anacyclus pyrethrum(l.)dc.)的干燥根,罗马除虫菊是菊科(asteraceae)春黄菊族(anthemideae)anacyclus属多年生草本植物。传统医学的其他用途包括咽炎、扁桃体炎、瘫痪、癫痫、发烧和糖尿病。它具有强有力的刺激特性,可作为唾涎剂和神经系统的补品;根汤可用于治疗扁桃体炎、牙痛、喉咙痛和龋齿。
3、阿纳其根是传统维吾尔医药的经典常用药材,在维药成药制剂中被广泛运用;现代药理学研究表明其具有抗癫痫、免疫调节、改善男性性功能、抗突变、抗炎、保肝、降糖、抗菌等生物活性。研究报道其具有n-烷基酰胺类及哌啶类生物碱,但这些化合物与阿纳其根药理活性的相关性仍未完全明确,阿纳其根的药效物质基础尚未阐明。
技术实现思路
1、本发明人经过潜心研究,从阿纳其根中首次分离出具有抗炎作用的抗炎化合物(式1、式2、式3或式4的化合物),这些化合物为全新骨架生物碱类化合物,对其结构进行了鉴定,并且通过细胞实验,验证了其具有细胞no释放抑制作用,可以用于制备抗炎药物。
2、因此,本发明提供以下各项:
3、1.选自以下的化合物或其异构体:
4、n-(1-(2,2,5,5,8,12,12-七甲基-3,7-二酮-1,2,3,4,5,6,7,8,9,11,12-十氢-6h,13h-9a,14a-甲桥环戊烷并[7,8]氮杂并[4,5,6-ij]异喹啉-2-基)-2-甲丙基-2-基)乙酰胺(式1的化合物或化合物1);
5、8a-乙酰基-2,2,4,5a,7,7,10,10,11a-九甲基-2,5,5a,7,8,8a,10,11,11a,12-十氢吡啶并[3′,2′:3,4]环戊烷并[1,2-g]吡咯并[3,2-b]吲嗪-10(1h)-酮(式2的化合物或化合物2);
6、2,2,6,6,8,8-六甲基-9a-(2-丙酰基)-1,2,3,5,6,8,9,9a-八氢-1h-吡咯并[2,3-h]异喹啉-1-酮(式3的化合物或化合物3);和
7、2-((5-乙酰基-2,2,4-三甲基-3,4-二氢-2h-吡咯-4-基)甲基)-4,6,6-三甲基吡啶-3(6h)-酮(式4的化合物或化合物4)。
8、2.根据以上1所述的化合物或其异构体,其中所述异构体为对映异构体。
9、3.根据以上1或2所述的化合物或其异构体,其选自化合物(+)-1、化合物(–)-1、化合物(+)-2、化合物(–)-2、化合物(+)-3、化合物(–)-3、化合物(+)-4和化合物(–)-4,其中:
10、化合物(+)-1为:n-(1-((8r,9as,10as)-2,2,5,5,8,12,12-七甲基-3,7-二酮-1,2,3,4,5,6,7,8,9,11,12-十氢-6h,13h-9a,14a-甲桥环戊烷并[7,8]氮杂并[4,5,6-ij]异喹啉-2-基)-2-甲丙基-2-基)乙酰胺;
11、化合物(–)-1为:n-(1-((8s,9ar,10ar)-2,2,5,5,8,12,12-七甲基-3,7-二酮-1,2,3,4,5,6,7,8,9,11,12-十氢-6h,13h-9a,14a-甲桥环戊烷并[7,8]氮杂并[4,5,6-ij]异喹啉-2-基)-2-甲丙基-2-基)乙酰胺;
12、化合物(+)-2为:(5ar,8ar,11ar)-8a-乙酰基-2,2,4,5a,7,7,10,10,11a-九甲基-2,5,5a,7,8,8a,10,11,11a,12-十氢吡啶并[3',2':3,4]环戊烷并[1,2-g]吡咯并[3,2-b]吲嗪-10(1h)-酮;
13、化合物(–)-2为:(5as,8as,11as)-8a-乙酰基-2,2,4,5a,7,7,10,10,11a-九甲基-2,5,5a,7,8,8a,10,11,11a,12-十氢吡啶并[3',2':3,4]环戊烷并[1,2-g]吡咯并[3,2-b]吲嗪-10(1h)-酮;
14、化合物(+)-3为:(s)-2,2,6,6,8,8-六甲基-9a-(2-丙酰基)-1,2,3,5,6,8,9,9a-八氢-1h-吡咯并[2,3-h]异喹啉-1-酮;
15、化合物(–)-3为:(r)-2,2,6,6,8,8-六甲基-9a-(2-丙酰基)-1,2,3,5,6,8,9,9a-八氢-1h-吡咯并[2,3-h]异喹啉-1-酮;
16、化合物(+)-4为:(r)-2-((5-乙酰基-2,2,4-三甲基-3,4-二氢-2h-吡咯-4-基)甲基)-4,6,6-三甲基吡啶-3(6h)-酮;和
17、化合物(–)-4为:(s)-2-((5-乙酰基-2,2,4-三甲基-3,4-二氢-2h-吡咯-4-基)甲基)-4,6,6-三甲基吡啶-3(6h)-酮。
18、4.根据以上1至3中任一项所述的化合物或其异构体,其具有选自以下的结构式:
19、
20、5.一种从阿纳其根中提取根据以上1至4中任一项所述的化合物或其异构体的方法,其包括以下步骤:
21、a、将阿纳其根干燥后粉碎,以体积比为50-95%(v/v)的乙醇水溶液、甲醇或者氯仿为溶剂(药材重量(kg)与溶剂(l)比例1:1.5-1:4),采用冷浸、渗漉法提取、加热回流或超声提取,减压浓缩回收溶剂,得到浸膏;
22、b、将步骤a的总浸膏经水混悬后,用酸如浓度为1-5%盐酸或浓度为1-5%硫酸分散处理,得到的酸水层,用二氯甲烷萃取去除非生物碱后用碱如nahco3、na2co3、氨水或naoh调ph至约10-12,再用有机溶剂二氯甲烷、乙酸乙酯或正丁醇萃取,减压浓缩回收有机溶剂,得到总生物碱;和
23、c、将步骤b的总生物碱经硅胶柱层析法、薄层层析法、反相mci柱层析、葡聚糖凝胶lh-20柱层析法、高效液相色谱法或它们的任何组合进行分离,得到所述化合物或其异构体。
24、6.根据以上5所述的方法,其中在步骤c中,使用正相硅胶柱层析和选自反相硅胶或反相mci柱层析或半制备高效液相色谱之一的两者组合来进行分离,优选地,在使用正相硅胶柱层析进行梯度或等度洗脱后,用反相硅胶或反相mci柱层析或半制备高效液相色谱法,得到式1、式2、式3或式4的化合物,其中更优选地,所述正相硅胶柱层析中所用的洗脱剂为体积比为100:0至3:1的石油醚和乙酸乙酯、体积比为500:1至3:1二氯甲烷和甲醇、体积比为50:1至0:1的石油醚和丙酮、或体积比为1:9-1:0的甲醇和水,所述反相硅胶或反相mci柱层析中所用的洗脱剂为体积比10-100%(v/v)的甲醇水溶液或20-100%(v/v)的乙腈水溶液,并且所述半制备高效液相色谱法中所用的等度或梯度洗脱的洗脱剂为体积比99-50%的正己烷/etoh、体积比为99-50%的正己烷/2-异丙醇、体积比为99:1:0.002至50:50:0.002的正己烷/2-异丙醇/二乙胺或浓度20-100%(v/v)的甲醇水溶液。
25、7.根据以上5所述的方法,其中在步骤c中,使用正相硅胶柱层析、反相硅胶或反相mci柱层析、和半制备高效液相色谱的三者组合来进行分离,优选地,在使用正相硅胶柱层析进行梯度或等度洗脱后,用反相硅胶或反相mci柱层析梯度洗脱,再采用半制备高效液相色谱法,得到式1、式2、式3或式4的化合物,其中更优选地,所述正相硅胶柱层析中所用的洗脱剂为体积比100:1至0:1的石油醚和乙酸乙酯、二氯甲烷和甲醇或三氯甲烷和甲醇,所述反相硅胶或反相mci柱层析中所用的洗脱剂为体积比10-100%(v/v)的甲醇水溶液或20-100%(v/v)的乙腈水溶液,并且所述半制备高效液相色谱法中所用的等度或梯度洗脱的洗脱剂为体积比99-50%的正己烷/etoh、体积比99-50%的正己烷/2-异丙醇、体积比为99:1:0.002至50:50:0.002的正己烷/2-异丙醇/二乙胺或浓度10-100%(v/v)的甲醇水溶液。
26、8.根据以上5所述的方法,其中在步骤c中,使用正相硅胶柱层析、葡聚糖凝胶lh-20柱层析、反相硅胶或反相mci柱层析、和半制备高效液相色谱的四者组合来进行分离,优选地,在使用正相硅胶柱层析进行梯度或等度洗脱后,经葡聚糖凝胶lh-20柱层析,用反相硅胶或反相mci柱层析梯度洗脱,再采用半制备高效液相色谱法,得到式1、式2、式3或式4的化合物,其中更优选地,所述正相硅胶柱层析中所用的洗脱剂为体积比100:1至0:1的石油醚和乙酸乙酯、二氯甲烷和甲醇或三氯甲烷和甲醇,所述葡聚糖凝胶lh-20柱层析采用甲醇梯度或等度洗脱,所述反相硅胶或反相mci柱层析中所用的洗脱剂为体积比10-100%(v/v)的甲醇水溶液或20-100%(v/v)的乙腈水溶液,并且所述半制备高效液相色谱法中所用的等度或梯度洗脱的洗脱剂为体积比为99-50%(v/v)的正己烷/etoh、体积比99-50%(v/v)的正己烷/2-异丙醇、体积比99:1:0.002至50:50:0.002(v/v)的正己烷/2-异丙醇/二乙胺或浓度20-100%(v/v)的甲醇水溶液。
27、9.根据以上5至8中任一项所述的方法,其中在步骤c中,所述硅胶柱层析为常压或加压柱层析,和/或所用填料为正相硅胶或反相硅胶;和/或优选地,所述方法还包括将得到的外消旋体(即式1、式2、式3或式4的化合物)经过手性色谱柱进行手性拆分得到对映体化合物的步骤。
28、10.根据以上1至4中任一项所述的化合物或其异构体在制备抗炎药物中的用途,优选地,所述化合物或其异构体是通过抑制细胞一氧化氮(no)释放来发挥抗炎作用。
29、总之,本发明提供了一种从阿纳其根中分离的生物碱类化合物及制备方法和用途,以阿纳其根(anacyclus pyrethrum(l.)dc.)为原料,用溶剂提取,酸碱处理,溶剂萃取,通过硅胶柱层析法、制备薄层层析法、葡聚糖凝胶lh-20柱层析法或高效液相色谱法(phplc)中的两种、三种或四种方式进行分离,采取薄层层析法或高效液相色谱法(hplc)检测分析,得到4个新骨架生物碱化合物。并对所述化合物进行了体外抗炎活性测定,实验结果表明,从阿纳其根中分离的新骨架生物碱化合物具有一定的抗炎活性,可用于制备抗炎症的药物。
30、发明详述
31、本发明的目的是提供具有抗炎作用的化合物以及其分离制备方法及其在制备抗炎药物中的应用价值。
32、根据本发明,第一方面,提供了一种具有抗炎作用的化合物,所述化合物(分别为式1、式2、式3或式4的化合物)的结构式如下所示;
33、
34、
35、其中:
36、化合物(+)-1为:n-(1-((8r,9as,10as)-2,2,5,5,8,12,12-七甲基-3,7-二酮-1,2,3,4,5,6,7,8,9,11,12-十氢-6h,13h-9a,14a-甲桥环戊烷并[7,8]氮杂并[4,5,6-ij]异喹啉-2-基)-2-甲丙基-2-基)乙酰胺(式1的化合物);
37、化合物(–)-1为:n-(1-((8s,9ar,10ar)-2,2,5,5,8,12,12-七甲基-3,7-二酮-1,2,3,4,5,6,7,8,9,11,12-十氢-6h,13h-9a,14a-甲桥环戊烷并[7,8]氮杂并[4,5,6-ij]异喹啉-2-基)-2-甲丙基-2-基)乙酰胺(式1的化合物);
38、化合物(+)-2为:(5ar,8ar,11ar)-8a-乙酰基-2,2,4,5a,7,7,10,10,11a-九甲基-2,5,5a,7,8,8a,10,11,11a,12-十氢吡啶并[3',2':3,4]环戊烷并[1,2-g]吡咯并[3,2-b]吲嗪-10(1h)-酮(式2的化合物);
39、化合物(–)-2为:(5as,8as,11as)-8a-乙酰基-2,2,4,5a,7,7,10,10,11a-九甲基-2,5,5a,7,8,8a,10,11,11a,12-十氢吡啶并[3′,2′:3,4]环戊烷并[1,2-g]吡咯并[3,2-b]吲嗪-10(1h)-酮(式2的化合物);
40、化合物(+)-3为:(s)-2,2,6,6,8,8-六甲基-9a-(2-丙酰基)-1,2,3,5,6,8,9,9a-八氢-1h-吡咯并[2,3-h]异喹啉-1-酮(式3的化合物);
41、化合物(–)-3为:(r)-2,2,6,6,8,8-六甲基-9a-(2-丙酰基)-1,2,3,5,6,8,9,9a-八氢-1h-吡咯并[2,3-h]异喹啉-1-酮(式3的化合物);
42、化合物(+)-4为:(r)-2-((5-乙酰基-2,2,4-三甲基-3,4-二氢-2h-吡咯-4-基)甲基)-4,6,6-三甲基吡啶-3(6h)-酮(式4的化合物);
43、化合物(–)-4为:(s)-2-((5-乙酰基-2,2,4-三甲基-3,4-二氢-2h-吡咯-4-基)甲基)-4,6,6-三甲基吡啶-3(6h)-酮(式4的化合物)。
44、上述生物碱类化合物的提取分离方法,按下列步骤进行:
45、将阿纳其根干燥后粉碎,以体积分数为50-95%(v/v)的乙醇水溶液、甲醇或者氯仿为溶剂(药材重量(kg)与溶剂(l)比例1:1.5-1:4),采用冷浸、渗漉法提取、加热回流或超声提取,减压浓缩回收溶剂,得到浸膏;
46、b、将步骤a的总浸膏经水混悬后,用酸如浓度为1-5%盐酸或浓度为1-5%硫酸分散处理,得到的酸水层,用二氯甲烷萃取去除非生物碱后用碱如nahco3、na2co3、氨水或naoh调ph至10-12,再用有机溶剂二氯甲烷、乙酸乙酯或正丁醇萃取,减压浓缩回收有机溶剂,得到总生物碱;
47、c、将步骤b的总生物碱经硅胶柱层析法、薄层层析法、反相mci柱层析、葡聚糖凝胶lh-20柱层析法、高效液相色谱法中的两种、三种或四种方式进行分离;
48、其中两种分离方式:
49、所用正相硅胶柱层析洗脱剂为体积比100:0-3:1的石油醚-乙酸乙酯、500:1-3:1二氯甲烷-甲醇或体积比50:1-0:1的石油醚/丙酮进行梯度洗脱后,用反相硅胶或mci柱层析或半制备高效液相色谱,得到式1、式2、式3或式4的化合物;
50、三种分离方式:
51、所用正相硅胶柱层析洗脱剂为体积比100:1-0:1的石油醚-乙酸乙酯、二氯甲烷-甲醇或三氯甲烷-甲醇进行梯度洗脱后,经反相硅胶或mci柱层析,以体积比(v/v)的甲醇水溶液或20-100%(v/v)的乙腈水溶液梯度洗脱后,采用半制备高效液相色谱,以体积比为99-50%(v/v)的正己烷/etoh、体积比为99-50%(v/v)的正己烷/2-异丙醇或体积比为99:1:0.002-50:50:0.002(v/v)的正己烷/2-异丙醇/二乙胺作为洗脱剂,得到式1、式2、式3或式4的化合物。
52、四种分离方式:
53、所用正相硅胶柱层析洗脱剂为体积比100:1-0:1(v/v)的石油醚-乙酸乙酯、二氯甲烷-甲醇或三氯甲烷-甲醇进行梯度洗脱后,经葡聚糖凝胶lh-20柱层析,采用甲醇等度洗脱后,经反相硅胶或mci柱层析,以体积比(v/v)的甲醇水溶液或20-100%(v/v)的乙腈水溶液梯度洗脱后,采用半制备高效液相色谱,以体积比为99-50%(v/v)的正己烷/etoh、体积比为99-50%(v/v)的正己烷/2-异丙醇或体积比为99:1:0.002-50:50:0.002(v/v/v)的正己烷/2-异丙醇/二乙胺作为洗脱剂,得到式1、式2、式3或式4的化合物。
54、步骤c所述的阿纳其根中生物碱类化合物的制备方法,其特征在于,所用硅胶柱层析法为常压或加压柱层析,所用填料为正向硅胶或反相硅胶,用体积比500:1-3:1(v/v)的二氯甲烷和甲醇;体积比1:0-3:1(v/v)的石油醚和乙酸乙酯;或体积比1:9-1:0(v/v)的甲醇水为洗脱剂,采用等度或梯度洗脱。
55、步骤c所述的阿纳其根中生物碱类化合物的制备方法,其特征在于上述中的葡聚糖凝胶lh-20柱层析法的洗脱剂为甲醇,采用等度洗脱。
56、步骤c所述的阿纳其根中生物碱类化合物的制备方法,其特征在于所述制备高效液相色谱法的洗脱剂为体积比10-100%(v/v)的甲醇水溶液、以体积比为99-50%(v/v)的正己烷/etoh、体积比为99-50%(v/v)的正己烷/2-异丙醇或体积比为99:1:0.002-50:50:0.002(v/v/v)的正己烷/2-异丙醇/二乙胺作为洗脱剂,采用等度或梯度洗脱。
57、根据本发明另一方面,提供了一种具有抗炎作用的化合物的提取分离方法,将阿纳其根干燥后粉碎,用溶剂为体积比50-95%的乙醇水溶液、甲醇或者氯仿为溶剂(药材重量(kg)与溶剂(l)比例1:1.5-1:4),采用冷浸、渗漉法提取、加热回流或超声提取,减压浓缩回收溶剂,得到浸膏;将所述总浸膏经水混悬后,酸如浓度为1-5%盐酸或浓度为1-5%硫酸分散处理,得到的酸水层,用二氯甲烷萃取去除非生物碱后用nahco3、na2co3、氨水或naoh调ph至10-12,再用有机溶剂为氯仿、乙酸乙酯或正丁醇萃取,减压浓缩回收有机溶剂,得到总生物碱;将所得到的总生物碱经硅胶柱层析法、薄层层析法、葡聚糖凝胶lh-20柱层析法或高效液相色谱法中的两种、三种或四种方式进行分离;采取薄层层析法或高效液相色谱分析法检测分析,得到8个新骨架生物碱化合物。所用硅胶柱层析法为常压或加压柱层析,所用填料为正向硅胶或反相硅胶,用体积比500:1-3:1的二氯甲烷和甲醇;体积比1:0-3:1的石油醚和乙酸乙酯;或体积比10:90-100:0的甲醇水为洗脱剂,采用等度或梯度洗脱。所用的制备薄层层析法为常压层析,展开系统为展开系统为二氯甲烷和甲醇的混合物,石油醚和丙酮的混合物。所用的葡聚糖凝胶lh-20柱层析法的洗脱剂为体积比10:1的氯仿-甲醇或甲醇,采用等度洗脱。所用的制备高效液相色谱法的洗脱剂为体积比为99-50%(v/v)的正己烷/etoh、体积比为99-50%(v/v)的正己烷/2-丙醇、体积比为99:1:0.002至50:50:0.002(v/v)的正己烷/2-异丙醇/二乙胺或浓度20-100%(v/v)的甲醇水溶液,采用等度或梯度洗脱。
58、根据本发明另一方面,提供了所述具有抗炎作用的化合物用于制备抗炎药物的应用。
59、本发明所述的新骨架生物碱类化合物,结合多种波谱分析方法(高分辨质谱、紫外光谱、红外光谱、和核磁共振谱)以及x射线单晶衍射等方法综合分析,确定实施例中制备的化合物1至4的结构。其中化合物1、化合物3和化合物4的相对构型通过x射线单晶衍射确定,如图1、图2和图3所示。
60、化合物1(anacyphrethine c):黄色块状晶体;旋光值[α]25 d 128(c0.092,甲醇,对映异构体化合物(+)-1);[α]25 d-128(c 0.092,甲醇,对映异构体化合物(-)-1);紫外(甲醇)λmax(logε)288(3.92)nm,417(3.74)nm;红外(kbr)max 3291,2973,2936,2871,1714,1667,1563and 1178cm-1;ecd(c 1.86×10-3m,甲醇)λmax215(-1.17),289(2.22),337(-1.97),435(1.67),对映异构体化合物(+)-1;ecd(c 1.86×10-3m,甲醇)λmax(δε)219(1.43),285(-2.15),377(2.17),432(-1.74)nm,对映异构体化合物(-)-1;高分辨质谱m/z496.3532[m+h]+(计算值c30h45o3n3+,496.3534)。其1h和13c nmr谱图数据见表1。
61、表1化合物1的1h和13c nmr数据(氘代氯仿,600mhz)
62、
63、
64、化合物2(anacyphrethine d):黄色粉末;旋光值[α]25 d 92(c 0.08,甲醇,对映异构体化合物(+)-2);[α]25 d-92(c 0.066,甲醇,对映异构体化合物(-)-2);紫外(甲醇)λmax(logε)268(408)nm,453(4.14)nm;红外(kbr)max 3342,2970,2928,2870,1713,1571,1365and 1052cm-1;ecd(c 1.83×10-3m,甲醇)λmax(δε)216(1.32),243(0.75),274(-2.85),306(0.77),381(-1.10),446(1.12),对映异构体化合物(+)-2;ecd(c 1.51×10-3m,甲醇)λmax(δε)219(-1.52),243(-1.44),275(5.01),307(-1.09),383(1.80),446(-1.71),对映异构体化合物(-)-2;高分辨质谱m/z 438.3114[m+h]+(计算值c27h40o2n3+,438.3115)。其1h和13c nmr谱图数据见表2。
65、表2化合物2的1h和13c nmr数据(氘代氯仿,600mhz)
66、
67、
68、化合物3(anacyphrethine e):无色块状晶体;旋光值[α]25 d-34(c0.2,甲醇,对映异构体化合物(-)-3);[α]25 d 34(c 0.2,甲醇,对映异构体化合物(+)-3);紫外(甲醇)λmax(logε)260(4.22)nm;红外(kbr)max2960,2920,1713,1665,1626,1399,1355and1162cm-1;ecd(c 1.21×10-3m,甲醇)λmax(δε)218(0.60),257(-4.05),288(4.78)nm,对映异构体化合物(-)-3;ecd(c 1.21×10-3m,甲醇)λmax(δε)216(-0.54),260(4.39),288(-4.86)nm,对映异构体化合物(+)-3;高分辨质谱m/z 331.2376[m+h]+(计算值c20h31o2n2+,331.2380)。其1h和13c nmr谱图数据见表3。
69、化合物4(anacyphrethine f):无色块状晶体;旋光值[α]25 d 66(c0.2,甲醇,对映异构体化合物(+)-4);[α]25 d-66(c 0.2,甲醇,对映异构体化合物(-)-4);紫外(甲醇)λmax(logε)253(3.86)nm;红外(kbr)max2970,2927,2866,1697,1662,1618,1466,1448and1358cm-1;ecd(c6.62×10-4m,甲醇)λmax(δε)216(22.06),240(-4.91),267(2.98),336(-1.81)nm,对映异构体化合物(+)-4;ecd(c 6.62×10-4m,甲醇)λmax(δε)216(-22.20),241(4.41),272(-2.91),337(2.28)nm,对映异构体化合物(-)-4;高分辨质谱m/z 303.2063[m+h]+(计算值c18h27o2n2+,303.2067)。其1h和13c nmr谱图数据见表3。
70、表3化合物3和4的1h和13c nmr数据(氘代氯仿,600mhz)
71、
72、总体而言,通过本发明所构思的以上技术方案与现有技术相比,主要具备以下的技术优点:
73、(1)本发明中提供的化合物1至4为全新骨架化合物。化合物1是一对高度共轭的二氨基6/6/6/6/5五环生物碱新骨架对映异构体,独特的6,13-二氮杂五环[10.3.31,3.1.02,7.08,12]十九烷环系的骨架结构,具有3个不连续手性立体中心。化合物2是一对三氨基6/5/6/5/5五环生物碱新骨架对映异构体,独特的4,6,17-三氮杂五环[10.7.0.04,11.05,9.013,18]十九烷环系的骨架结构,具有3个不连续手性立体中心。化合物3是一对三氨基6/6/5三环生物碱新骨架对映异构体,独特的5,12-二氮杂三环[7.4.02,6]十九烷环系的骨架结构,具有3个不连续手性立体中心。化合物4是一对新的吡啶酮-吡咯骨架对映异构体,具有1个手性立体中心。
74、(2)本发明中提供的化合物1至4具有抗炎活性,具有制备抗炎症的药物的用途。
75、下面根据附图和实施例对本发明作进一步详细说明,但并不因此而限制本发明的范围。在不背离本发明精神和实质的情况下,对本发明的方法、步骤、条件等所作的修改或替换,均属于本发明的范围。
- 还没有人留言评论。精彩留言会获得点赞!