一种N-甲基氨基酸类化合物及其制备方法
本发明属于氨基酸化学合成的,具体涉及一种n-甲基氨基酸类化合物及其制备方法。
背景技术:
1、赖氨酸(lys)是一种重要的蛋白质生成氨基酸(aa),在控制肽和蛋白质的功能和物理化学性质方面发挥着不可或缺的作用(chem.soc.rev.2015,44,5495)。大自然已经在赖氨酸ε-nh2侧链上构建了一系列酶催化的翻译后修饰(ptm)途径(cell chem.biol.2020,27,953)。其中nε-赖氨酸的甲基化是细胞功能表观遗传学控制领域中最重要的ptm之一(chem rev.2018,118,6656)。除了ptms,肽和蛋白质中的赖氨酸侧链也是各种生物偶联应用中令人垂涎的手柄。尽管在过去的半个世纪里取得了显著的进步,但对选择性修饰赖氨酸的新方法的探索仍有增无减。
2、自然界广泛使用各种α-氨基酸单元的主链n-甲基化来调节肽天然产物的物理化学性质,特别是膜渗透性(acc.chem.res.2008,41,1331)。尽管n-甲基化结构看似简单,然而仲甲基的烷基胺的制备仍然存在问题,这主要由于存在竞争性的n,n-二甲基化副反应以及分离这些同系物的困难所造成的(chem.rev.2004,104,5823)。目前用于伯烷基胺的单选择性n-甲基化的方法主要需要使用保护基团来阻断其中一个n-h键。这种必要性大大增加了合成n-甲基化-氨基酸砌块的成本,并限制了在肽等复杂分子后期修饰中的应用。
3、因此,需要开发一种更好的合成n-甲基氨基酸类化合物的方法。
技术实现思路
1、鉴于以上所述现有的技术缺点,本发明的目的在于提供一种n-甲基氨基酸类化合物及其制备方法。本发明以甲醛作为甲基化的修饰试剂,其与氨基酸的氨基形成的亚胺中间体来作为负氢的受体,同时添加四氢吡咯作为负氢的供体,以及六氟异丙醇溶剂作为质子梭来传递负氢和质子,在温和条件下,实现分子间负氢和质子的协同转移,可以高效地合成单选择性的n-甲基氨基酸类化合物。本发明所需样品简单,用量少,反应体系干净,溶剂可回收利用,反应后只需简单的纯化处理方式,无需柱色谱分离纯化,可适用于不含活性侧链氨基酸的甲基化修饰。本发明中的甲醛/四氢吡咯/六氟异丙醇反应体系为将甲基单选择性引入到不同α,β,γ-氨基酸的氨基提供了一种方便有效的后期修饰方法,具有潜在的合成应用。
2、为实现以上目的,本发明的技术方案为:
3、本发明的目的之一是提供一种制备n-甲基氨基酸类化合物的方法,包括以下步骤:
4、将氨基酸类化合物、甲醛、负氢供体在有机溶剂中反应;
5、其中,氨基酸类化合物中的一个氨基氢被单选择性的用甲基取代,生成所述n-甲基氨基酸类化合物;
6、氨基酸类化合物选自氨基酸或氨基酸衍生物中的至少一种。
7、n-甲基氨基酸类化合物的制备方程式如下:
8、
9、在本发明所述的制备n-甲基氨基酸类化合物的方法中,优选地,
10、氨基酸或氨基酸衍生物选自α-氨基酸类化合物、β-氨基酸类化合物或γ-氨基酸类化合物中的至少一种;
11、优选地,
12、α-氨基酸类化合物选自甘氨酸、丙氨酸、亮氨酸、异亮氨酸、缬氨酸、甲硫氨酸、苯丙氨酸、带有保护基团的酪氨酸、丝氨酸、苏氨酸、谷氨酸或天门冬氨酸衍生物中的至少一种;和/或,
13、β-氨基酸类化合物选自3-氨基-3-苯基丙酸及其衍生物中的至少一种;和/或,
14、γ-氨基酸类化合物选自菲尼布特、普瑞巴林及其衍生物中的至少一种;和/或,
15、赖氨酸类化合物选自fmoc-l-赖氨酸及其类似物中的至少一种。
16、在本发明所述的制备n-甲基氨基酸类化合物的方法中,优选地,
17、所述负氢供体选自四氢吡咯、2,2,5,5-d4-四氢吡咯或2-甲基吡咯烷中的至少一种;和/或,
18、所述甲醛为甲醛水溶液、固体甲醛、氘代固体甲醛中的至少一种;优选甲醛选自浓度为36-38wt%甲醛的水溶液;和/或,
19、所述有机溶剂选自含氟有机醇,优选地,所述有机溶剂选自六氟异丙醇、三氟乙醇中的至少一种。
20、在本发明所述的制备n-甲基氨基酸类化合物的方法中,优选地,
21、反应温度为15℃~100℃;优选为室温~60℃;和/或,
22、反应时间为2小时~8小时;优选为4小时~6小时。
23、在本发明所述的制备n-甲基氨基酸类化合物的方法中,优选地,
24、所述有机溶剂中,氨基酸类化合物的浓度为0.01~1mol/l;优选为0.2~0.6mol/l;和/或,
25、所述负氢供体与氨基酸类化合物的摩尔比为3~9:1;优选为3~4:1;和/或,
26、甲醛与氨基酸类化合物的摩尔比为2~4:1;优选为2~3:1。
27、在本发明所述的制备n-甲基氨基酸类化合物的方法中,优选地,
28、反应结束后对产物进行纯化的方式为:
29、反应完成后,蒸发浓缩,回收溶剂,浓缩后的粗产品置于0~4℃下保存30分钟~1小时,将冷的乙醚加入上述粗产品中,静置10分钟~24小时后,使固体缓慢析出,随后离心分离,分别收集固体和上清液;上清液再旋干后继续至于0~4℃下保存30分钟~1小时,将冷的乙醚加入上述粗产品中,再次静置,使固体缓慢析出,于离心机中离心,富集固体即可得到所述n-甲基氨基酸类化合物。
30、进一步优选地,所述n-甲基-α-氨基酸后处理纯化方式为:反应完成后,于旋转蒸发仪上浓缩,水浴锅温度保持在60℃,在连续抽气下尽可能除去更多六氟异丙醇/四氢吡咯的共沸物,并回收溶剂。随后,浓缩后的粗产品至于0~4℃下保存30分钟~1小时,将冷的乙醚加入上述粗产品中,静置10分钟~24小时后,使固体缓慢析出,在离心机中离心,分别收集固体和上清液。上清液再旋干后继续至于0~4℃下保存30分钟~1小时,将冷的乙醚加入上述粗产品中,静置10分钟~24小时后,使固体缓慢析出,再次于离心机中离心,富集固体即可。
31、所述n-甲基-l-赖氨酸的纯化方式则通过hplc进行纯化分离。
32、本发明的目的之二是提供本发明的目的之一所述的方法制备的n-甲基氨基酸类化合物。
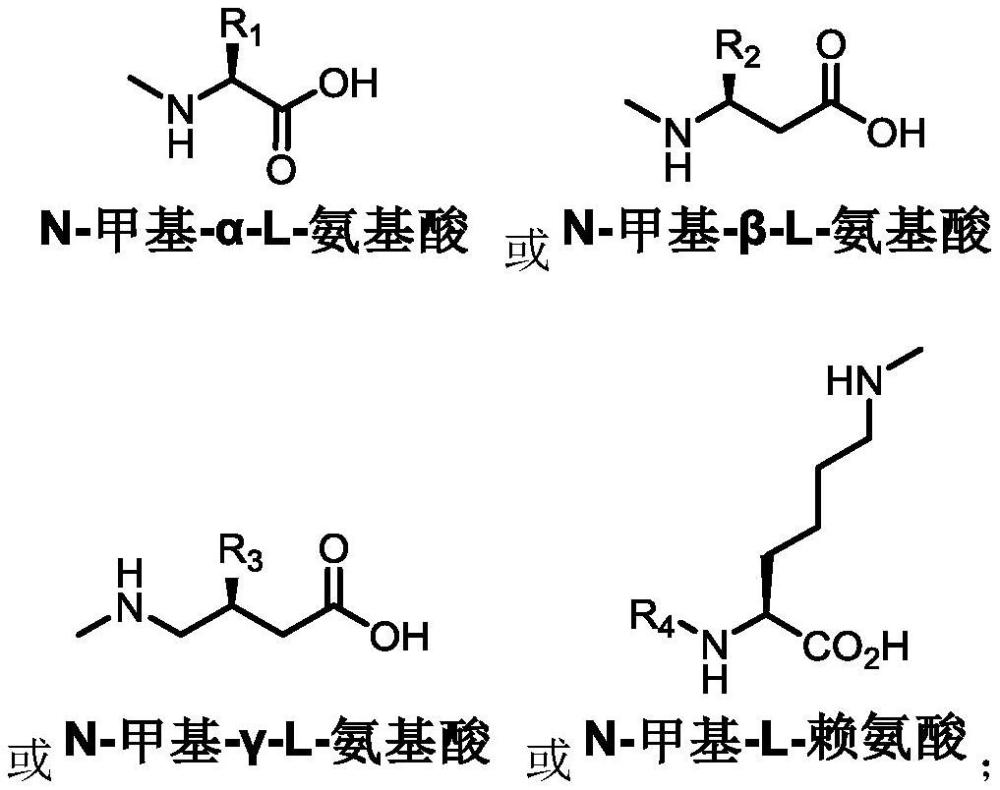
33、在本发明所述的n-甲基氨基酸类化合物中,所述n-甲基氨基酸类化合物为n-甲基-α-l-氨基酸、n-甲基-β-l-氨基酸、n-甲基-γ-l-氨基酸、n-甲基-l-赖氨酸;
34、优选地,所述n-甲基氨基酸类化合物具有以下结构通式:
35、
36、
37、其中r1选自烷基、硫取代的烷基、芳基、羟基、酯基或酚基;
38、r2选自芳基;
39、r3选自烷基或芳基;
40、r4选自酰基。
41、在本发明所述的n-甲基氨基酸类化合物中,优选地,
42、所述n-甲基-α-l-氨基酸选自以下化合物:
43、
44、和/或,所述n-甲基-β-氨基酸选自以下化合物:
45、
46、在本发明所述的n-甲基氨基酸类化合物中,优选地,
47、所述n-甲基-γ-氨基酸选自以下化合物:
48、和/或,
49、所述n-甲基-l-赖氨酸选自以下化合物:
50、
51、本发明以甲醛作为甲基化的修饰试剂,其与氨基酸的氨基形成的亚胺中间体来作为负氢的受体,同时添加四氢吡咯作为负氢的供体,以及六氟异丙醇溶剂作为质子梭来传递负氢和质子,在温和条件下,实现分子间负氢和质子的协同转移,可以高效地合成单选择性的n-甲基氨基酸类化合物。本发明所需样品简单,用量少,反应体系干净,溶剂可回收利用,反应后只需简单的纯化处理方式,无需柱色谱分离纯化,可适用于不含活性侧链氨基酸的甲基化修饰。本发明中的甲醛/四氢吡咯/六氟异丙醇反应体系为将甲基单选择性引入到不同α,β,γ-氨基酸的氨基提供了一种方便有效的后期修饰方法,具有潜在的合成应用。
52、本发明与现有技术相比,至少具有以下有益效果:
53、1、甲醛,四氢吡咯是简单易得的原料,商业可以买到;
54、2、本发明条件温和,反应速度快,十分高效,优秀的选择性,一步就可以得到n-甲基化的氨基酸类化合物;
55、3、本发明的反应采用绿色可回收的溶剂;
56、4、本发明的反应后只需简单的纯化处理方式,无需柱色谱分离纯化;
57、5、本发明的反应适用于不同类型的不同组成和长度的氨基酸类化合物。
58、6、本发明的反应适用于克级制备。
59、综上,本发明开发出了从易得底物出发,简单易行的合成n-甲基氨基酸类化合物方法,使用绿色可回收的溶剂,只需简单的纯化处理方式,对上述n-甲基化的不同组成和长度的氨基酸类化合物进行高效选择性地合成具有较高的应用价值。
- 还没有人留言评论。精彩留言会获得点赞!