一种CHD1Lflox/flox小鼠模型的构建方法与应用
本发明涉及动物模型构建,具体涉及一种chd1lflox/flox小鼠模型的构建方法与应用。
背景技术:
1、目前对于炎症性疾病、癌症的治疗仍是需要克服的难题,需要加大力度对各种特异抗原的寻找,对有关炎症性疾病和癌症等的临床前研究有助于发现疾病检测和治疗的靶标及相关药物研发,有利于对人类的疑难杂症进行攻克。在此过程中构建了大量的基因工程小鼠进行基因功能、疾病发展规律的探索,在药物研发中发挥了重要作用。
2、1q21的扩增是许多实体肿瘤中最常见的遗传改变之一,如膀胱癌、乳腺癌、肝细胞癌、结肠癌、食管癌、骨纤维肉瘤等。在肝癌细胞染色体1q21中发现并命名的色域解旋酶/atp酶dna结合蛋白1样基因(chd1l)(马宁芳等,2008年)在肝细胞癌(hcc)中异常高度扩增,与肿瘤的恶性增殖和预后不良显著相关。目前已发现chd1l在多种肿瘤中高度特异表达,如膀胱癌、乳腺癌、肝细胞癌、结肠癌、食管癌、骨纤维肉瘤等。chd1l基因,又名alc1(染色质域解旋酶/atp酶dna结合1样蛋白基因),位于chr1q21.1,全长53kb,23个外显子。chd1l是通过与dna结合来调节染色体完整性维持、dna修复和转录调节。chd1l的c端具有一段与chd1识别甲基化组蛋白尾巴的染色体结构域不同的macrodomain结构域,macrodomain可以特异性识别聚adp-核糖(par)结构。聚adp-核糖聚合物(poly adp-ribose polymer,par),也称为par化修饰(parylation modification),是由par聚合酶(parps)产生的一种表观修饰形式,当单链dna断裂(ssb)发生时可激活parp活性进行par化标记,以参与dna损伤和修复以及染色质重塑相关的翻译后修饰过程。chd1l的c端的macrodomain宏结构域是一个adp-核糖/par结合元件的聚合物,因此chd1l具有par依赖性染色质重塑活性,促进dna断裂修复。当ssb的发生造成了碱基切除修复,引起染色体构像松弛,激活了parp酶,使在断链处形成聚adp-核糖基化(parylation),chd1l被吸引招募到核小体中,与染色质相关的聚adp-核糖-parp1相互作用促进染色体的修复。
3、chd1l在多种细胞高表达,尤其在肿瘤发生时,肿瘤本身和肿瘤微环境中的免疫细胞中均有高度扩增,对于chd1l的异常表达对肿瘤细胞与免疫细胞各自的作用及它们之间的交互影响机制仍属于未知。现有研究多聚焦于chd1l基因在肿瘤发生中的作用,其在免疫细胞中的作用却鲜有报道。通过查询在线数据库资料和前期实验数据证实,chd1l在b、t、nk等淋巴细胞中有高表达,参与调控免疫细胞的增殖、活化、分化及迁移。
4、b淋巴细胞是一群具有不同功能亚群的异质群体,它能在周围淋巴器官中特异识别抗原并处理、提呈抗原启动适应性免疫应答,通过分化成浆细胞分泌特异抗体、中和抗原参与体液免疫,消灭病原体,维持机体的免疫平衡。为对应抗原的多样化,b淋巴细胞产生抗体的多样化是机体能够识别并有效清除抗原的生物学基础。b淋巴细胞主要依赖两种机制产生多样化抗体,一个是重组激活基因(rag)编码的重组酶等主导的基因重排;另一个是胞苷脱氨酶(aid)等主导的体细胞高频突变(shm)。获得抗原活化的b细胞激活rag重组酶介导了免疫球蛋白(ig)重链基因座内vdj片段的重排导致抗体类别转换(csr),随后在滤泡区aid的活化介导了v区内互补决定区(cdr)基因发生体细胞高频突变(shm),shm不仅能增加抗体类别多样化,而且可导致更高亲和力的抗体产生。在分子水平上,csr是一种体细胞重组反应,通过ig重链(igh)位点内dna双链断裂(dsb)的形成和修复程序来完成,此过程涉及parp酶和chd1l分子的参与。基于chd1l在b细胞的表达在免疫细胞中排名靠前,且b淋巴细胞活化时细胞内发生高频的dsb与修复,同时考虑到chd1l专有的macrodomain结构域,其独特的通过识别par的形式进行dsb修复的方式可能在b淋巴细胞实现csr和shm功能的调节中具有重要作用,其中的详细机制仍需构建b细胞特异敲除chd1l基因模型小鼠来揭示。另外,chd1l在cd4+t细胞、cd8+t和nk细胞中均有表达,并且在细胞分化过程中表达发生改变,在这些细胞的分群演化中chd1l的功能尚未阐明,亦需要构建相应的条件敲除小鼠来开展研究。
技术实现思路
1、本发明的目的在于克服现有技术的不足,提供一种chd1lflox/flox小鼠模型的构建方法与应用。
2、为实现上述目的,本发明采取的技术方案为:一种chd1lflox/flox小鼠模型的构建方法,包括以下步骤:
3、(1)构建同源重组载体;
4、(2)将cas9 mrna、grna和同源重组载体通过显微注射至c57bl/6j小鼠受精卵中,将受精卵移植至假孕母鼠并产出获得f0代子鼠;
5、(3)将f0代小鼠与正常野生型的c57bl/6j小鼠交配繁育获得杂合子f1代小鼠;
6、(4)将杂合子f1代小鼠进行交配繁育得f2代小鼠,即所述chd1lflox/flox小鼠。
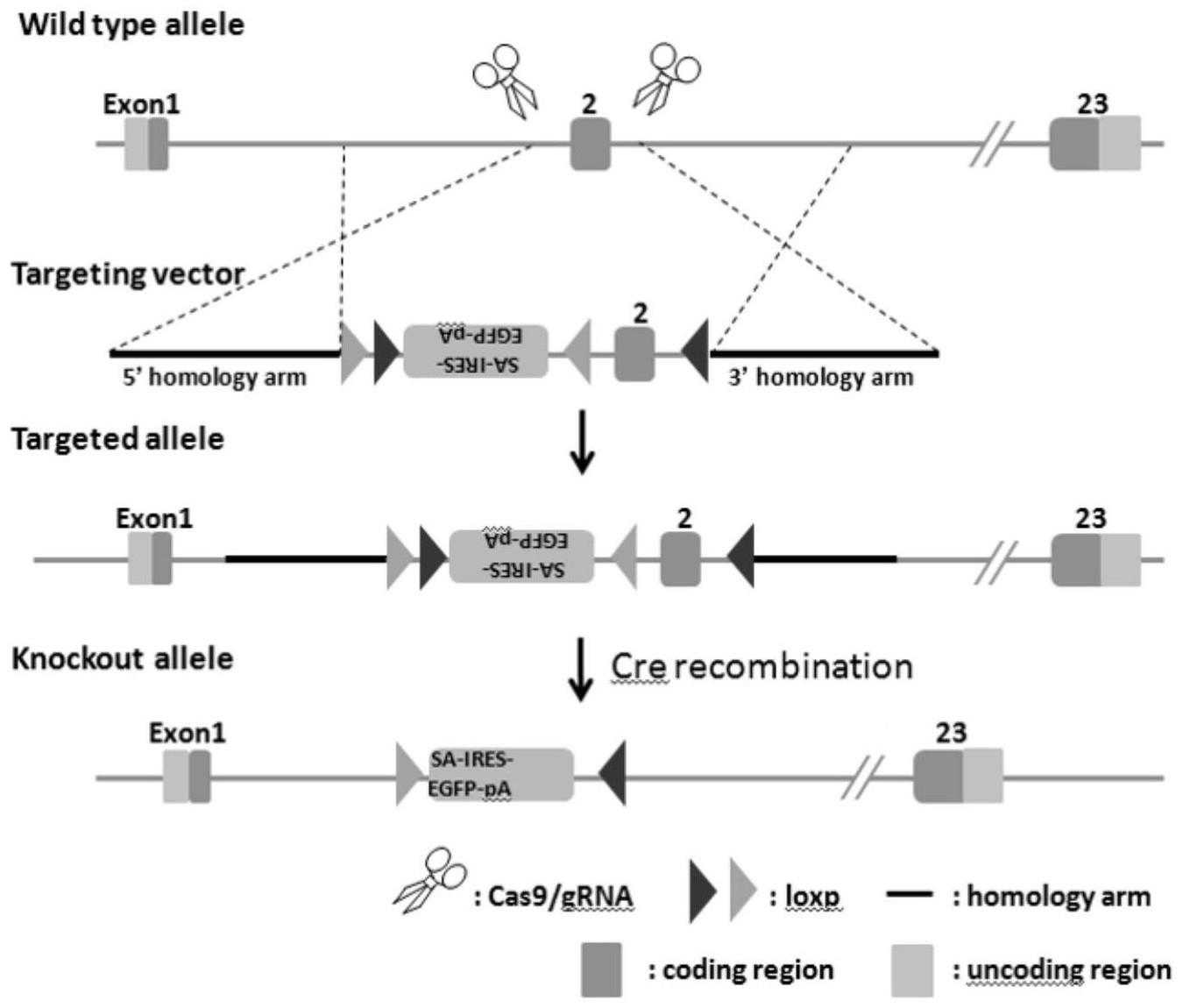
7、作为本发明所述chd1lflox/flox小鼠模型的构建方法的优选实施方式,所述同源重组载体包括包含4.0kb的5'同源臂、sa-ires-egfp-pa、0.7kb的flox区段和3.6kb的3'同源臂。同源重组载体中的sa-ires-egfp-pa将在cre重组酶活化后被激活,表现未绿色荧光蛋白egfp表达,提示两端的loxp位点间的序列被切除。
8、作为本发明所述chd1lflox/flox小鼠模型的构建方法的优选实施方式,所述grna的靶位点位于chd1l基因的第二个外显子的两侧,靶位点grna1和grna2的序列如下:
9、grna1:5'-ataccccttatgatgaagtgtgg-3'
10、grna2:5'-attagagcagccaatgatcctgg-3'。
11、作为本发明所述chd1lflox/flox小鼠模型的构建方法的优选实施方式,还包括对所述f0代小鼠和杂合子f1代小鼠进行基因型鉴定;所述基因型鉴定的pcr引物为:
12、5’同源重组臂引物序列如下:f:agtttgtcctgtcctgtgcctctt;r:gccactcccactgtcctttcct;
13、3’同源重组臂引物序列如下:f:gcggcgttctctctattcca;r:tctccaggttgcctttggtc。
14、作为本发明所述chd1lflox/flox小鼠模型的构建方法的优选实施方式,还包括对所述f2代小鼠进行基因型鉴定;所述基因型鉴定的pcr引物为:
15、p1:gcaaaccagttctgtaaaccacat
16、p2:ggcagcctcacctcccat
17、p3:ggttgtgggttgtggcaagctt
18、p4:tcgccaaaggaatgcaaggtc。
19、本发明采用上述引物对f2代小鼠进行基因型鉴定,其中,野生型小鼠p1,p2扩增出696bp条带,p3,p4无条带;杂合子小鼠p1,p2扩增出696bp条带,p3,p4也扩增出小条带424bp;纯合子小鼠p1,p2无条带,p3,p4可扩增出小条带424bp。
20、本发明还提供采用所述的chd1lflox/flox小鼠模型的构建方法构建得到的chd1lflox/flox小鼠模型。
21、本发明还提供所述的chd1lflox/flox小鼠模型在构建组织细胞特异性条件敲除chd1l小鼠模型中的应用。
22、本发明还提供一种b淋巴细胞chd1l基因敲除模型小鼠的构建方法,包括以下步骤:
23、(1)将所述的chd1lflox/flox小鼠与cd19 cre纯合子小鼠交配,得到得到f3代chd1lflox/+;cd19cre/+杂合小鼠;
24、(2)将f3代chd1lflox/+;cd19cre/+杂合小鼠雌雄交配,经基因型鉴定后代为chd1lflox/flox;cd19cre/cre、chd1lflox/flox;cd19cre/+、chd1lflox/flox;cd19+/+、chd1lflox/+;cd19cre/cre、chd1lflox/+;cd19cre/+、chd1lflox/+;cd19+/+、chd1l+/+;cd19cre/cre、chd1l+/+;cd19cre/+和chd1l+/+;cd19+/+9种基因型小鼠;
25、(3)在步骤(2)获得的基因型小鼠中筛选出雄性chd1lflox/flox;cd19cre/+和雌性chd1lflox/flox;cd19+/+的小鼠并进行兄妹配繁得f4代小鼠,f4代小鼠经基因型鉴定得到chd1lflox/flox;cd19cre/+小鼠即为所述b淋巴细胞chd1l基因敲除模型小鼠。
26、作为本发明所述b淋巴细胞chd1l基因敲除模型小鼠的构建方法,所述基因型鉴定的引物包括:
27、p1:gcaaaccagttctgtaaaccacat
28、p2:ggcagcctcacctcccat
29、p3:ggttgtgggttgtggcaagctt
30、p4:tcgccaaaggaatgcaaggtc
31、p5:agcgatggatttccgtctctgg
32、p6:agcttgcatgatctccggtattgaa
33、p7:cct ctc cct gtc tcc ttc ct
34、p8:tgg tct gag aca ttg aca atc a。
35、本发明的有益效果:本发明提供一种chd1lflox/flox小鼠模型的构建方法,通过基因工程技术设计和成功构建chd1lflox/flox小鼠,并通过与各种组织特异性靶点插入cre基因的工具鼠进行杂交所获得多种组织细胞特异性条件敲除鼠,填补了该领域的技术空白,为开展在肿瘤微环境、免疫微环境中chd1l在不同组织细胞的功能研究,为能在整体水平上阐明chd1l在疾病发展中的功能建立了良好的基础,为以chd1l为靶标的分子治疗、细胞治疗的研发提供了坚实基础。
- 还没有人留言评论。精彩留言会获得点赞!