一种编码NGF蛋白的工程化circRNA、药物组合物及其制备方法和应用
本发明涉及生物医药,更具体地,涉及一种编码ngf蛋白的工程化circrna、药物组合物及其制备方法和应用。
背景技术:
1、神经生长因子(nerve growth factor,ngf),即ngf蛋白,临床上广泛用于用于治疗视神经损伤,角膜炎等。然而现有的动物源性的ngf蛋白有朊病毒感染的风险,重组蛋白发酵工艺及纯化工艺昂贵,且需要每天肌肉注射,给患者带来较大痛苦。
2、circrna是一类没有5’或3’末端的闭合rna。很长时间内被认为是5’剪接点与上游3’剪接点的罕见和异常剪接的副产品。最近由于高通量rna测序和生物信息学分析的快速发展,天然circrna的大量生物学功能被揭示,从蛋白质和基因海绵、细胞活动调节剂到蛋白质翻译模板。此外,随着人们对天然circrnas生理功能的认识不断加深,近年来,人们对开发circrna合成技术和探索合成circrnas在疾病治疗中的应用越来越感兴趣。到目前为止,合成的circrnas不仅被用于治疗,例如替代治疗性蛋白质和多肽以及疫苗,也用作生物传感器。同时,为了在减少副作用的同时优化治疗效果,已经尝试了各种方法来合成circrna。以前circrna主要被认为是非编码rna,但最近的研究表明,它们能够通过天然circrna和合成circrna编码和翻译蛋白质和多肽。circrna在疫苗和核酸药物的开发中有其独特的优势。首先,它不太容易降解,比mrna疫苗和核酸药物更稳定。其次,滚环翻译所需的量比信使核糖核酸低,因此毒性较小。由circrnas包围的共价闭环结构可以保护它免受核酸外切酶的降解,并可以解决mrna疫苗对降解的脆弱性。这些特性使circrna具有作为多肽/蛋白质替代疗法和疫苗的巨大潜力。然而,目前还未见关于ngf蛋白的工程化circrna的相关报道。
技术实现思路
1、本发明的目的在于克服现有技术中存在的上述缺陷和不足,提供一种促进编码ngf蛋白的工程化circrna形成的核酸。
2、本发明的第二个目的在于提供含有所述核酸的重组表达载体
3、本发明的第三个目的在于提供含有所述重组表达载体的重组菌。
4、本发明的第四个目的在于提供一种编码ngf蛋白的工程化circrna的制备方法。
5、本发明的第五个目的在于提供上述制备方法制备得到的编码ngf蛋白的工程化circrna。
6、本发明的第六个目的在于一种包裹有上述编码ngf蛋白的工程化circrna的脂质纳米颗粒。
7、本发明的第七个目的在于所述脂质纳米颗粒的制备方法。
8、本发明的第八个目的在于所述编码ngf蛋白的工程化circrna或所述脂质纳米颗粒的应用。
9、本发明的上述目的是通过以下技术方案给予实现的:
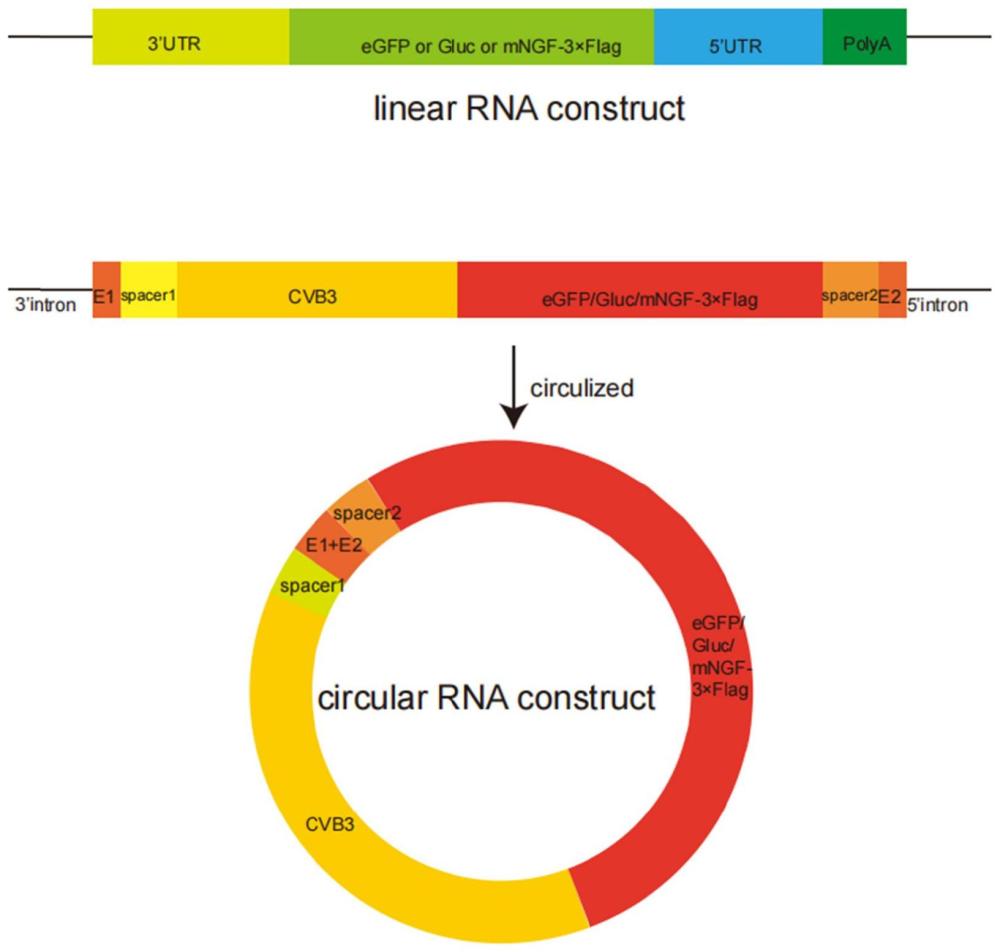
10、一种促进编码ngf蛋白的工程化circrna形成的核酸,其具有如下结构:5’→3’依次为体外转录启动子-3'端i型内含子和3'端同源臂-外显子序列e1-间隔序列(spacer)1-内部核糖体进入位点(ires)-ngf蛋白编码序列-间隔序列(spacer)2-外显子序列e2-5'端i型内含子和5端'同源臂;所述ngf蛋白编码序列为编码人源或鼠源ngf的cds序列,其核苷酸序列分别如seq id no.2或seq id no.4所示。
11、本发明所述核酸可基于i型内含子的自我剪接,可在gtp(鸟嘌呤核苷)催化下,促进circrna的环化,为了进一步提高自剪接前体rna成环效率,其序列结构中的同源臂(homology arm)、间隔序列(spacer),可解决长编码rna序列成环的难题,并且能够得到较好的成环效率。
12、进一步地,所述体外转录启动子为t7、t3或sp6启动子。
13、优选地,所述体外转录启动子为t7启动子。
14、进一步地,所述3'端i型内含子和3'端同源臂-外显子序列e1,外显子序列e2-5'端i型内含子和5端'同源臂来源于鱼腥藻。
15、进一步地,所述外显子序列e1为aaaatccgttgaccttaaacggtcgtgtgggttcaagtccctccaccccca,外显子序列e2为agacgctacggactt。
16、进一步地,所述间隔序列(spacer)1为cgccggaaacgcaatagccgaaaaacaaaaaacaaaaaaaacaaaaaaa aaaccaaaaaaacaaaacaca;间隔序列2为aaaaaacaaaaaacaaaacggctattatgcgttaccggcg。
17、进一步地,所述内部核糖体进入位点为柯萨奇病毒b3的内部核糖体进入位点ires。
18、进一步地,所述ngf蛋白编码序列为人源ngf的cds序列经密码子优化后的序列,其核苷酸序列分别如seq id no.6所示。
19、进一步地,所述ngf蛋白编码序列3’端还连接有蛋白标签序列。
20、优选地,所述蛋白标签序列为3×flag。
21、进一步地,所述ngf蛋白编码序列与相邻两个组件间插入有酶切位点。可用于基因替换,节省成本。
22、进一步地,所述核酸的序列如seq id no.1或seq id no.11或seq id no.12所示。
23、本发明还提供含有上述任一所述核酸的重组表达载体。
24、本发明还提供含有上述重组表达载体的重组菌。
25、本发明还提供一种编码ngf蛋白的工程化circrna的制备方法,包括如下步骤:
26、s1.合成上述任一所述核酸序列;
27、s2.将步骤s1的核酸序列连接到基础质粒模板中,并转化宿主菌,质粒抽提,获得转录模板;
28、s3.将步骤s2转录模板线性化,再体外转录,消化去除dna,沉淀获得circrna前体,在添加gtp孵育,实现环化,再纯化得到环化rna,即得到编码ngf蛋白的工程化circrna。
29、进一步地,所述circrna前体的序列如seq id no:8~10所示。
30、进一步地,步骤s3所述纯化为用rna纯化试剂盒以及rnaser酶对环化后的circrna进行消化和纯化。将纯化后的circrna溶解于酸性柠檬酸钠缓冲液中,并用hplc进行纯化,收集hplc的第二个峰产物,并用rna纯化试剂盒进行纯化。
31、本发明还提供所述制备方法制备得到的编码ngf蛋白的工程化circrna。
32、本发明还提供一种脂质纳米颗粒(lnps),包裹有上述编码ngf蛋白的工程化circrna。
33、本发明还提供所述脂质纳米颗粒的制备方法,是将上述所述编码ngf蛋白的工程化circrna与阳离子或聚阳离子化合物混合后用脂质包装即得。
34、优选地,所述脂质包括但不限于能够促进自组装形成病毒大小的颗粒(~100nm)的脂质、使得circrna从内涵体中释放到胞内的脂质、支撑磷脂双分子层结构的脂质或用作稳定剂的脂质。更优选地,为了增加lnp的半衰期,所述的脂质还可以包含peg化脂质。
35、本发明所述的circrna或包含circrna的脂质纳米颗粒具备的优势在于:1、体外合成,无需细胞培养,无动物源污染的风险;2、研发、生产较快,标准化生产,易于量产和质量控制,同一生产流程适用于多个不同产品;3、可以在一段时间内持续表达;4、支持多种蛋白形式,包括胞内蛋白、跨膜蛋白、vlp等,且可避开vlp产量低而造成的纯化问题;5、无感染、基因组整合风险。
36、本发明研究显示,上述编码ngf蛋白的工程化circrna或所述脂质纳米颗粒(lnps)具有神经保护和治疗神经损伤的效果。因此,本发明还提供所述编码ngf蛋白的工程化circrna或所述脂质纳米颗粒(lnps)在制备预防和/或治疗神经损伤和/或神经退行性疾病的药物中的应用。
37、本发明所述的“预防”指在疾病开始发展之前或之后通过施用本发明所述的产品来避免症状或者延缓特定症状紧张的所有行为。
38、本发明所述的“治疗”指在疾病已开始发展后改善疾病或病理状态的体征、症状等等的治疗干预。
39、与现有技术相比,本发明具有以下有益效果:
40、本发明提供了一种编码ngf蛋白的工程化circrna及包裹该工程化circrna的脂质纳米颗粒,所述编码神经生长因子(ngf)的工程化circrna具有增强ngf稳定性和表达效率的优势。通过包装工程化circrna于纳米脂质颗粒(lnp)中,可以实现药物的有效输送和释放。该药物组合物可通过局部给药、胃肠道给药或非胃肠道给药等方式进行应用,以提供神经保护和治疗神经损伤的效果。一次给药就有显著神经保护效果,不需要持续给药,也避免了动物源性蛋白的病毒感染风险。与病毒基因递送相比,基于circrna的治疗的一个优点是mrna不会转运到细胞核,从而减轻序列插入基因组从而诱变癌变风险。
- 还没有人留言评论。精彩留言会获得点赞!