一种结合宿主去除的纳米孔宏基因组测序方法及其应用
本发明属于基因测序,具体涉及一种结合宿主去除的nanopore宏基因组测序方法,及其在猪和猫等动物临床检测中的应用。
背景技术:
1、宏基因组测序是一种能够对样品中的所有微生物进行无差别检测的测序方法,应用于传染性病原的检测时能够发现样品中存在的细菌、真菌、病毒等,对于非常见病原及新发的传染性病原的检测具有独特的优势。例如,新冠病毒最早就是通过宏基因组测序检测到的;而未知原因引起的人急性脑炎最终也是通过宏基因组测序发现是由感染猪的伪狂犬病毒导致的;尤其是在儿童下呼吸道样品回顾性研究中发现,之前临床诊断为病原微生物阴性的样品通过宏基因组测序发现有一半存在潜在病原体。
2、目前,宏基因组测序已开始应用于动物病原微生物临床检测中,并刚刚开始应用于动物临床诊断中,但受测序设备昂贵、大量宿主基因导致测序时间和成本增加,以及测序准备和数据分析方法复杂等因素的影响,使其应用受到限制。通常情况下,临床样品的宏基因组测序中一个常见的问题是宿主基因占据测序结果的绝大部分(如痰液样品中宿主基因可高达99.999%),影响病原所占比例较小,有时仅有一到两个测序片段来源于病原菌,所以测序数据中绝大部分是无用的。本领域技术人员尝试开发出多种方法致力于降低宿主基因,提高病原基因所占比例。
3、临床上常用的宿主去除方法主要使用研磨结合核酸酶、皂苷结合核酸酶、叠氮溴化丙锭(propidium monoazide,pma)、商品化试剂盒等方法降低宿主基因。其中,研磨结合核酸酶常用于病毒的检测,而皂苷、pma及商品化试剂盒常用于细菌的检测。然而临床检测通常需要一种通用的方法以同时检测样品中可能存在的细菌及病毒。
4、目前,宏基因组测序常用的下一代测序平台(如illuminate和ion torrent)设备价格昂贵,动物临床诊断实验室通常难以负担,而送检测序公司则无法满足临床时效性的要求。minion测序平台作为第三代纳米孔测序设备,具有设备便宜、小巧的特点,适合在动物临床诊断实验室进行部署。另外,传统的测序方法为先测序后分析,而纳米孔测序平台具有边测序边分析的优势,可实时查看检测到了多少病原及其对应的测序片段。因此,如何通过实时检测结果判断何时停止测序是一个值得研究的问题,既要使其数据量满足后续分析需求,避免数据量不足导致重新测序,又尽可能节省测序芯片的消耗,以节省测序时间和成本。本领域期待对nanopore宏基因组测序技术进行优化,进一步提高其应用性能。
技术实现思路
1、为此,本发明所要解决的技术问题在于提供一种结合宿主去除的nanopore宏基因组测序方法;
2、本发明所要解决的第二个技术问题在于提供上述结合宿主去除的nanopore宏基因组测序方法在动物临床检测领域的应用。
3、为解决上述技术问题,本发明所述的一种结合宿主去除的纳米孔宏基因组测序方法,包括如下步骤:
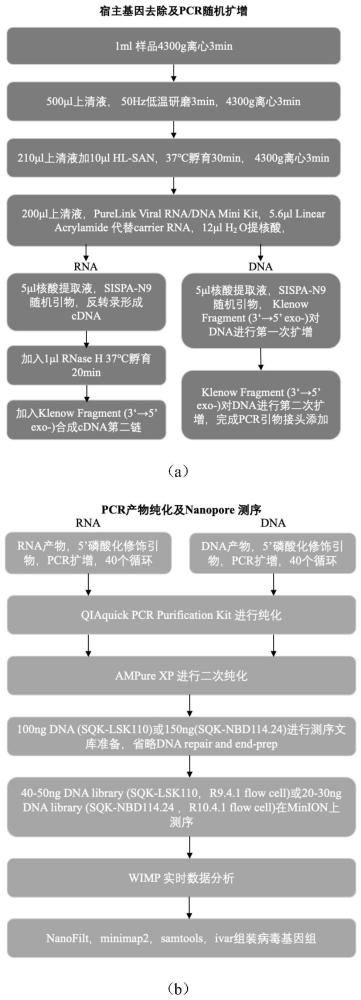
4、(1)宿主基因去除;
5、(2)pcr随机扩增;
6、(3)pcr产物纯化;
7、(4)纳米孔测序。
8、具体的,所述结合宿主去除的纳米孔宏基因组测序方法,所述步骤(1)中,所述宿主基因去除步骤包括:
9、取待测样本经离心后进行低温研磨,再次离心处理并收集上清液;
10、向所述上清液中加入核酸酶进行消化及孵育处理,经离心处理收集酶消化液;
11、取所述酶消化液进行提取rna及dna。
12、具体的,所述结合宿主去除的纳米孔宏基因组测序方法,所述步骤(1)中,所述核酸酶包括hl-san酶和/或benzonase核酸酶;
13、优选的,所述提取rna及dna步骤中,加入linear acrylamide代替carrier rna。
14、具体的,所述结合宿主去除的纳米孔宏基因组测序方法,所述步骤(2)中,所述pcr随机扩增步骤包括进行rna反转录合成第二链的步骤,具体包括:
15、收集步骤(1)获得的核酸提取液进行反转录形成cdna;
16、加入rnase进行孵育处理;
17、收集孵育产物加入klenow fragment合成cdna第二链,得到rna产物;
18、优选的,所述反转录步骤的引物包括sispa-n9引物;
19、sispa-n9:gtttcccactggaggatannnnnnnnn。
20、具体的,所述结合宿主去除的纳米孔宏基因组测序方法,所述步骤(2)中,所述pcr随机扩增步骤包括进行dna链两端引物接头的步骤,具体包括:
21、收集步骤(1)获得的核酸提取液加入klenow fragment对dna进行第一次扩增;
22、收集第一次扩增产物继续加入klenow fragment对dna进行第二次扩增,得到dna产物;
23、优选的,所述第一次扩增步骤的引物包括sispa-n9引物;
24、sispa-n9:gtttcccactggaggatannnnnnnnn。
25、具体的,所述结合宿主去除的纳米孔宏基因组测序方法,所述步骤(2)中,还包括分别收集所述rna产物和dna产物进行pcr扩增的步骤;
26、优选的,所述pcr扩增步骤的引物包括sispa引物,并进行5’磷酸化修饰;
27、sispa:gtttcccactggaggata。
28、具体的,所述结合宿主去除的纳米孔宏基因组测序方法,所述步骤(3)中,所述pcr产物纯化包括使用qiaquick pcr purification kit(qiagen)进行第一次纯化的步骤,以及使用ampure xp reagent(beckman coulter)进行第二次纯化的步骤。
29、具体的,所述结合宿主去除的纳米孔宏基因组测序方法,所述步骤(4)中,所述纳米孔测序步骤包括进行测序建库的步骤;
30、所述测序建库步骤使用ligation sequencing kit,其使用的dna包括rna pcr扩增后纯化产物和dna pcr扩增后纯化产物;
31、优选的,所述rna pcr扩增后纯化产物和dna pcr扩增后纯化产物的质量比为1:1。
32、具体的,所述结合宿主去除的纳米孔宏基因组测序方法,所述步骤(4)中,所述纳米孔测序步骤包括测序步骤和数据分析的步骤;
33、优选的,所述测序步骤使用minlon测序仪;
34、优选的,所述数据分析步骤使用gpu版本的minknow进行碱基判定。
35、本发明还公开了所述结合宿主去除的纳米孔宏基因组测序方法在动物临床检测领域的应用。
36、本发明所述结合宿主去除的纳米孔宏基因组测序方法,基于纳米孔测序第三代测序技术,并通过对纳米孔宏基因组测序及分析方法进行优化,将其应用于猪和猫等动物的临床样品检测领域,进而评估其检测性能、宿主去除效果及数据分析方法。所述结合宿主去除的纳米孔宏基因组测序方法,对于不同类型的样品,优化的宏基因组测序方法作为一种通用的方法,可在24小时内完成对样品中细菌、dna病毒及rna病毒的共同检测,且其结果与pcr检测及细菌培养结果相一致,并额外检测到几种非常见病原或难以分离培养的病原,表现出其在临床检测中的优势。
37、本发明所述结合宿主去除的纳米孔宏基因组测序方法,在进行宿主去除过程中,使用组织研磨结合核酸酶消化去除宿主基因,之后对提取到的dna和rna进行无选择的pcr扩增,以同时检测基因组为dna及rna的病原,并使用r9.4.1或r10.4.1flow cells在minion上进行纳米孔测序,以及epi2m wimp进行病原的实时检测,nanofilt、minimap2、samtools及ivar对病毒基因组进行组装。本发明使用优化的纳米孔宏基因组测序及分析方法,对猪和猫的多种类型样品进行了检测,发现其可明显降低宿主基因,同时检测到样品中的多种细菌、dna病毒及rna病毒,并可根据实时测序结果决定测序时间。本发明为以后宏基因组测序在动物的临床检测提供了参考。
38、本发明所述结合宿主去除的纳米孔宏基因组测序方法,通过对5份猫和4份猪的临床样品中的病原进行检测验证,结果与pcr及细菌培养结果一致,并额外检测到可能引起疾病的4种病毒及3种细菌。所述结合宿主去除的纳米孔宏基因组测序方法,比较了3个样品宿主去除前后的结果,宿主基因降低了9-50%,并进一步比较了6种病毒基因组装效果,3.3-98.3mb数据量即可组装出>90%的病毒基因组。可见,本发明使用优化的纳米孔宏基因组测序和分析方法,降低了宿主基因,减少了测序分析所需的数据量,并可根据实时检测结果判断何时可停止测序,从而节省了测序时间和成本。我们的测序及分析流程降低了宏基因组测序在兽医临床应用中的阻碍,为临床推广使用提供了参考。
39、本发明所述结合宿主去除的纳米孔宏基因组测序方法,使用研磨结合核酸酶消化的方法,结果显示病毒基因富集的效果明显好于细菌,并有效改善了临床样品的中宿主基因通常占据绝大部分的影响。该方法虽不能大大提高细菌基因占比,但并不影响细菌的检出,可满足临床检测的基本需求。
40、本发明所述结合宿主去除的纳米孔宏基因组测序方法,得益于epi2me wimp进行实时检测以及该测序方法对于含有不同病毒的样品进行测序时n50相对稳定性,可快速估计组装病毒所需数据量,这是与其他测序及分析方法的不同之处。
41、本发明所述结合宿主去除的纳米孔宏基因组测序方法,使用nanofilt、minimap2、samtools配合ivar的有参组装方式,ivar原是开发用于病毒的illumina扩增子测序的组装,本发明中发现其也适合用于随机扩增的纳米孔宏基因组测序的有参组装,且能得到较好的组装结果。
42、本发明使用优化的纳米孔宏基因组测序方法,对猪和猫的各种类型样品进行检测,能够较好的检测样品中存在的细菌及病毒,宿主基因得到了明显降低,配合云端实时分析及本地分析,可快速判断何时应停止测序,组装出相对完整的病毒基因组。本发明所述方法适合在中小型动物临床检测实验室应用,为宏基因组测序在兽医临床的普及提供参考。
- 还没有人留言评论。精彩留言会获得点赞!