一种多囊卵巢综合征的标志物及其应用
本发明属于生物医药领域,尤其涉及多囊卵巢综合征的精准医疗领域,更尤其涉及一种多囊卵巢综合征的标志物及其应用。
背景技术:
1、本部分的陈述仅仅是提供了与本发明相关的背景技术信息,不必然构成在先技术。
2、多囊卵巢综合征(polycystic ovary syndrome,pcos)是育龄妇女最常见的生殖内分泌疾病,影响10-12%的育龄妇女,是导致无排卵性不孕症的主要原因。它的典型特点是无排卵性不孕、高雄激素血症和卵巢多囊样改变,卵巢反应性异常等。临床上多囊卵巢综合征的表现多种多样、并不完全相同,区分其具体分型并进行个体化治疗十分必要。
3、关于多囊卵巢综合征的诊断标准,目前广泛应用的是2003年鹿特丹会议提出的诊断标准:1)临床或生化诊断为高雄激素血症:临床上患者有痤疮或多毛的临床表现;或在实验室检查中患者血清中雄激素水平升高或相关产物增加;2)稀发排卵或无排卵:pcos患者常伴月经周期不规律,稀发排卵指每年少于8次排卵,无排卵指超过6个月无月经;3)卵巢多囊样改变:在月经周期的第3-5天进行超声检查,显示双侧卵巢均有≥12个且直径2-9mm的小卵泡,和(或)卵巢体积增大;以上3个指标符合2个及2个以上即可诊断为多囊卵巢综合征。基于此可有多种经验分型如高雄型pcos和非高雄型pcos等,另外上述诊断条目都是基于传统的患者自述、激素检测或者超声检查,目前尚无有效的基因检测方法用于诊断及分子分型。
4、根据临床数据筛选具有适应证的标志物,并建立完善的pcos基因型-表型关联模型,根据基因型对pcos进行分类以实现早预防、早干预,有效避免远期并发症,提高pcos患者生活质量至关重要。
5、pcos是一种复杂的综合征,为了深入认识pcos,构建一个实用有效的动物模型十分必要。由于大鼠和小鼠体型小,繁殖周期短,具有较稳定的动情周期,对于实验研究既经济又方便,是最常用的实验动物之一。目前较常用的pcos动物模型是药物诱导模型,即雄激素注射包括孕期16.5天、17.5天、18.5天连续注射dht,所生子代可以模拟pcos部分生殖异常表型,青春期小鼠持续注射dhea21天,可以模拟pcos代谢异常表型。
6、另外,现有资料公开了dennd1a单碱基变异与pcos发生发展显著相关,以往的研究都是在基因组dna层面的研究,而基因发挥作用是在蛋白质层面。dennd1a具有两个转录本,美国弗吉尼亚州里士满弗吉尼亚联邦大学妇产科,构建了3个dennd1a转录本v2的过表达载体,并在卵巢组织中稳定表达,但同时发现转基因小鼠中,虽然dennd1a的mrna水平升高,但是其蛋白质表达水平较低,对研究及应用带来阻碍(doi:10.3390/ijms21072545)。所以,至今有关pcos的动物模型均无法有效模拟pcos所有表型。
7、从治疗层面而言,探寻并推广更加有效的精准的pcos诊疗方案是生殖医师的重任。目前针对pcos患者缺乏分型治疗方案,所有患者的治疗策略大同小异,并普遍存在着以治疗结局为导向的“头疼医头,脚疼医脚”的相关治疗方式。但在实际临床治疗中,病人对药物治疗反应不同、结局各异。而造成上述情况的主要原因,是对分型治疗方案研究的缺失。因此,目前急需根据pcos亚型靶点,进一步制定临床精准化、个体化治疗方案。
技术实现思路
1、为克服上述现有技术的不足,本发明的目的之一是提供一种可高效检测多囊卵巢综合征pcos的标志物,建立pcos基因型-表型因果关系模型;本发明的目的之二是提供一种能表征多数pcos表型的小鼠模型;本发明的目的之三,是根据所提出的pcos基因型-表型关系模型提供一种高精准预防、治疗pcos的sirna。
2、本发明中通过基因差异表达及特异性分析确定dennd1a转录本v1可以有效表征多囊卵巢综合征pcos,尤其是pcos的高雄分型,建立一个新的pcos基因型-表型关联模型。并通过基因沉默dennd1a转录本v1有效抑制pcos的各种表型。
3、另外本发明中利用crispr-cas9系统,在c57bl/6小鼠的6号染色体的rosa26基因定点敲入带标签的dennd1av1,有效过表达dennd1av1的mrna和蛋白质,获得了高雄激素血症、卵巢对fsh药物反应不良等遗传性动物模型。
4、为实现上述目的,本发明的一个或多个实施例提供了如下技术方案:
5、本发明的第一方面,提供一种用于多囊卵巢综合征诊断的标志物,所述标志物为dennd1a转录本v1;
6、具体的,dennd1a转录本v1的多核苷酸序列如seq id no.1所示。
7、在本发明的具体实施方式中,所述多囊卵巢综合征为高雄分型。
8、在本发明的具体实施方式中,所述标志物取自卵巢;进一步为卵泡;更进一步为颗粒细胞。
9、本发明的第二方面,提供一种用于检测第一方面所述的标志物的试剂,所述试剂包括引物和/或探针,
10、其中,检测dennd1a转录本v1的引物或探针分别为dennd1av1-f、dennd1av1-r;所述引物序列分别如seq id no.2、seq id no.3所示。
11、本发明的第三方面,提供一种检测产品,包括第二方面所述的引物、探针其组合及可接受的助剂;
12、优选的,所述产品包括芯片、试剂盒中的一种或多种。
13、本发明的第四方面,提供抑制dennd1a表达的物质在制备治疗多囊卵巢综合征药物中的应用;
14、所述应用具体表现为:
15、1)逆转转基因小鼠中fshr的分布紊乱;
16、2)恢复fsh信号通路的异常传导;
17、3)提高颗粒细胞对fsh的敏感性;
18、优选的,所述抑制dennd1a表达的物质包括靶向dennd1a的sirna;优选的,所述sirna的正义链序列为:gccagaacuucacauuugutt,反义链序列为:acaaaugugaaguucuggctt。
19、本发明的第五方面,提供一种多囊卵巢综合征的小鼠模型的构建方法,包括以下步骤:
20、将rosa26 grna、含有小鼠dennd1a的载体与cas9 mrna等摩尔比混匀为溶液,使用显微注射仪将所得溶液注射到已受精小鼠的受精卵胞浆中,将成活的受精卵移植到代孕母鼠体内,产生后代筛选获得。
21、在本发明的具体实施方式中,所述rosa26 grna的序列如seq id no.4所示;
22、所述小鼠dennd1a的载体含有cag启动子-小鼠dennd1a cdna-3xflag-polya的基因表达框;
23、所述小鼠dennd1a的序列如seq id no.5所示;
24、优选地,所述小鼠为与c57雄鼠合笼交配后的c57bl/6雌鼠;
25、优选地,所述筛选具体为:提取后代dna,鉴定有dennd1a基因的即为构建成功的模型。
26、通过以上方法构建了dennd1a的全身转基因小鼠(dennd1a tg c57bl/6小鼠),同时该小鼠带有flag标签,有效解决了dennd1a有效抗体缺乏导致的生化分析难题。
27、本发明的第六方面,提供一种由第五方面所述的方法获得的多囊卵巢综合征模型小鼠,所述模型小鼠表现为:
28、1)生育率下降,具体为:动情周期不规则、促性腺激素刺激下获得卵母细胞数量显著减少;
29、2)卵泡发育受损;
30、3)高雄激素血症;
31、4)糖代谢异常;
32、5)促卵泡激素fsh靶基因表达异常;
33、6)卵泡刺激素受体fshr内吞异常。
34、本发明的第七方面,提供第七方面所述多囊卵巢综合征小鼠在耐药性研究、代谢通路研究及个性化治疗中的应用。
35、以上一个或多个技术方案存在以下有益效果:
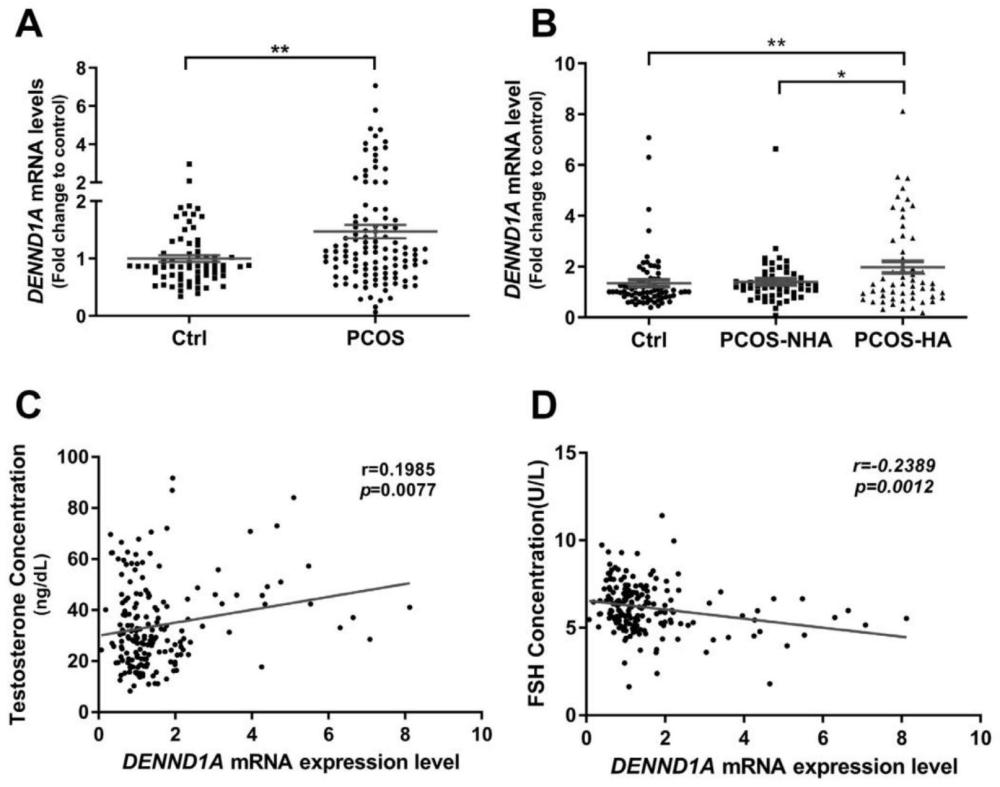
36、本发明对采集临床患者109例pcos组患者和68名对照组卵巢颗粒细胞进行数据验证,发现pcos组卵巢颗粒细胞中dennd1av1 mrna水平较对照组显著升高,高雄型pcos组表达升高更明显,且dennd1av1的表达量与雄激素水平成正相关,与卵泡刺激素(fsh)的水平成负相关关系。且灵敏度、特异性高。表明dennd1a尤其是dennd1av1 mrna可作为诊断pcos的一种标志物。
37、本发明借助crispr-cas9技术构建了一种充分模拟pcos生殖与代谢表型的小鼠模型。通过分析发现小鼠模型中,dennd1a主要定位于卵巢颗粒细胞,dennd1a的mrna和蛋白质表达均升高。转基因小鼠表现出动情周期不规律、卵巢质量下降、高雄激素血症、卵泡发育异常、卵巢对促性腺激素不敏感、葡萄糖代谢异常等。
38、本发明中充分结合动物模型,针对dennd1av1设计了系列sirna,利用过表达dennd1av1的卵巢颗粒细胞进行挽救实验研究,发现其中1条sirna可以有效抑制dennd1a基因表达、改善卵巢颗粒细胞对fsh药物的敏感性,初步实现了以dennd1a为靶点的精准干预,为后续临床研究提供精细化治疗方案。
39、本发明还发现,dennd1a通过增强颗粒细胞中fshr内转运、在溶酶体中裂解fshr,阻碍了fshr的细胞内循环过程,导致颗粒细胞对卵泡刺激素(fsh)反应不敏感。dennd1a的敲降逆转颗粒细胞对fsh敏感性的降低。这些发现有助于了解多囊卵巢综合征的病理生理学,并可能有助于发现新的治疗靶点,改善患者临床表型及生育。
40、本发明附加方面的优点将在下面的描述中部分给出,部分将从下面的描述中变得明显,或通过本发明的实践了解到。
- 还没有人留言评论。精彩留言会获得点赞!