苯并噻唑类化合物或其盐、其制备方法及应用
本发明具体涉及一类苯并噻唑类化合物或其盐、其制备方法及制药用途,属于医药化合物。
背景技术:
1、组蛋白脱乙酰酶(hdacs)催化从组蛋白氨基末端的赖氨酸残基中去除乙酰基,导致染色质浓缩和转录抑制。已在人类中鉴定出18种hdacs,根据它们与酵母hdacs的同源性、亚细胞定位和酶活性,将它们分为四类。i类hdacs(1、2、3和8)与酵母rpd3蛋白同源,通常可在细胞核中检测到,并在各种人类细胞系和组织中普遍表达。ii类hdacs(4、5、6、7、9和10)与酵母hda1蛋白具有同源性,可以在细胞核和细胞质之间穿梭。iib类hdacs,hdac6和10存在于细胞质中并包含两个脱乙酰酶结构域。hdac6具有独特的底物特异性,具有对细胞骨架蛋白α-微管蛋白具有特异性的α-微管蛋白脱乙酰酶(tdac)结构域。iii类hdacs(sirt1、2、3、4、5、6和7)是酵母蛋白sir2的同系物,需要nad+才能发挥调节基因表达的活性,以响应细胞氧化还原状态的变化。sirt1已被证明与p53相互作用并使p53去乙酰化,从而抑制p53介导的转录活性。hdac11是iv类hdacs的唯一成员。它与i类和ii类酶的催化核心区域具有序列相似性,但没有足够强的同一性来归入任何一类。
2、研究表明,hdacs拮抗剂在治疗多发性骨髓瘤,急性髓性白血病,弥漫性大b细胞淋巴瘤,阿尔茨海默病,乳腺肿瘤,非霍奇金淋巴瘤,结直肠肿瘤,皮肤t细胞淋巴瘤,胶质母细胞瘤,艾滋病毒感染,炎症性疾病,胰腺肿瘤,外周t细胞淋巴瘤以及常染色体显性多囊肾病中有积极作用。伏立诺他(vorinostat)、罗米地辛(romidepsin)、贝利司他(belinostat)、帕比司他(panobinostat)等为美国fda批准上市,用于临床治疗外周t细胞淋巴瘤、皮肤t细胞淋巴瘤和多发性骨髓瘤;西达本胺(tucidinostat/chidamide)由我国nmpa批准上市,用于外周t细胞淋巴瘤和乳腺癌。以上这些hdacs抑制剂的开发已成为治疗上述疾病药物研发的热点方向。这类化合物具有拮抗组蛋白去乙酰化酶受体的活性,并因此可应用于治疗上述疾病。
3、目前上市的hdacs抑制剂大多数都是非选择性抑制剂,具有副作用大、不良反应多等缺陷。研究表明,hdac6被敲除的小鼠能够存活并且hdac6选择性抑制剂能够应用于adpkd疾病治疗。目前临床上唯一被fda(美国食品药品监督管理局)认证的adpkd有效治疗药物是托伐普坦,但是在临床试验中,托伐普坦减缓患者肾功能下降的同时,部分患者血清肝转氨酶上升至正常水平三倍以上,这表明托伐普坦的使用会引起肝损伤。因此需要开发新的hdac6选择性抑制剂,研发出治疗效果更好、毒副作用更小的药物来缓解疾病的发生。
技术实现思路
1、本发明的目的之一是提供一类苯并噻唑类化合物或其盐,其能作为有效的hdac6激酶抑制剂,治疗与hdac6激酶介导的增殖相关疾病,具有应答率高、副作用小、不良反应少等特点,满足临床用药的需求,从而克服现有技术的缺陷。
2、本发明的目的之二是提供所述苯并噻唑类化合物或其药学上可接受的盐在制备用于预防和/或治疗增殖性疾病的药物中的应用。
3、本发明的目的之三是提供所述苯并噻唑类化合物或其盐的制备方法。
4、为实现上述发明目的,本发明采用了如下技术方案:
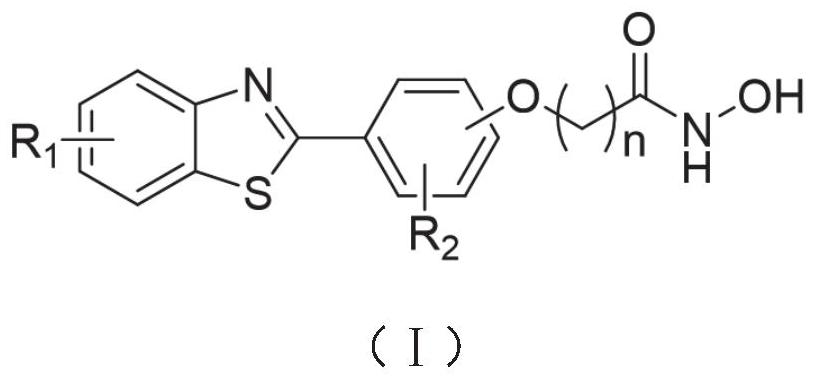
5、本发明的第一个方面提供了一类苯并噻唑类化合物或其盐,所述苯并噻唑类化合物具有式(i)所示结构,
6、
7、其中r1、r2至少独立地选自氢、卤素、氰基、硝基、c1-6烷基、c1-6烷氧基、c3-8环烷基、芳基、杂芳基和杂环基中的任一者,n为1~7中的任一整数。
8、其中,若定义式(i)中苯并噻唑基团为a单元,与苯并噻唑基团连接的苯环基团为b单元,与b单元通过醚键连接的基团为c单元,则b单元中r2连接在苯环的2、3或6位,c单元是连接在b单元中苯环的4位或者5位。
9、在一个实施例中,r1选自氢、卤素、c1-6烷基或c1-6烷氧基,r2选自氢、卤素、c1-6烷基或c1-6烷氧基。
10、较为优选的,r1选自氢、卤素、c1-6烷基或c1-6烷氧基,r2选自氢、卤素、甲氧基、乙氧基或甲基。
11、更为优选的,r1为氢,r2选自氢、卤素、甲氧基、乙氧基或甲基中的任一者。
12、较为优选的,r1为氢,r2选自氢、卤素、甲氧基、乙氧基或甲基中的任一者。
13、较为优选的,所述r1为氢,r2选自氢、卤素、甲氧基、乙氧基或甲基中的任一者。
14、其中,所述卤素优选为氟或氯。
15、较为优选的,r1为卤素,r2选自氢或甲氧基。
16、更为优选的,r1为氟或氯,r2选自氢或甲氧基。
17、较为优选的,r1为c1-6烷基,r2选自氢或甲氧基。
18、更为优选的,r1为甲基,r2选自氢或甲氧基。
19、较为优选的,r1为c1-6烷氧基,r2选自氢或甲氧基。
20、更为优选的,r1为甲氧基,r2选自氢或甲氧基。
21、在一个实施例中,所述苯并噻唑类化合物包括2-(4-(苯并[d]噻唑-2-基)苯氧基)-n-羟基乙酰胺、6-(4-(苯并[d]噻唑-2-基)苯氧基)-n-羟基己酰胺、7-(4-(苯并[d]噻唑-2-基)苯氧基)-n-羟基庚酰胺、8-(4-(苯并[d]噻唑-2-基)苯氧基)-n-羟基辛酰胺、7-(4-(苯并[d]噻唑-2-基)-2-氟苯氧基)-n-羟基庚酰胺、7-(4-(苯并[d]噻唑-2-基)-2-甲基苯氧基)-n-羟基庚酰胺、7-(4-(苯并[d]噻唑-2-基)-2-氯苯氧基)-n-羟基庚酰胺、7-(4-(苯并[d]噻唑-2-基)-2-甲氧基苯氧基)-n-羟基庚酰胺、7-(4-(苯并[d]噻唑-2-基)-2-乙氧基苯氧基)-n-羟基庚酰胺、7-(4-(苯并[d]噻唑-2-基)-3-氯苯氧基)-n-羟基庚酰胺、7-(4-(苯并[d]噻唑-2-基)-3-氟苯氧基)-n-羟基庚酰胺、7-(4-(苯并[d]噻唑-2-基)-2,6-二甲氧基苯氧基)-n-羟基庚酰胺、2-(3-(苯并[d]噻唑-2-基)苯氧基)-n-羟基乙酰胺、4-(3-(苯并[d]噻唑-2-基)苯氧基)-n-羟基丁酰胺、5-(3-(苯并[d]噻唑-2-基)苯氧基)-n-羟基戊酰胺、6-(3-(苯并[d]噻唑-2-基)苯氧基)-n-羟基己酰胺、7-(3-(苯并[d]噻唑-2-基)苯氧基)-n-羟基庚酰胺、8-(3-(苯并[d]噻唑-2-基)苯氧基)-n-羟基辛酰胺、7-(3-(苯并[d]噻唑-2-基)-2-氯苯氧基)-n-羟基庚酰胺、7-(5-(苯并[d]噻唑-2-基)-2-甲氧基苯氧基)-n-羟基庚酰胺、n-羟基-7-(2-甲氧基-5-(6-甲氧基苯并[d]噻唑-2-基)苯氧基)庚酰胺、7-(5-(6-氯苯并[d]噻唑-2-基)-2-甲氧基苯氧基)-n-羟基庚酰胺、7-(5-(6-氟苯并[d]噻唑-2-基)-2-甲氧基苯氧基)-n-羟基庚酰胺、n-羟基-7-(2-甲氧基-5-(6-甲基苯并[d]噻唑-2-基)苯氧基)庚酰胺、7-(5-(5-氯苯并[d]噻唑-2-基)-2-甲氧基苯氧基)-n-羟基庚酰胺、n-羟基-7-(4-(6-甲氧基苯并[d]噻唑-2-基)苯氧基)庚酰胺、7-(4-(6-氟苯并[d]噻唑-2-基)苯氧基)-n-羟基庚酰胺、7-(4-(6-氯苯并[d]噻唑-2-基)苯氧基)-n-羟基庚酰胺、n-羟基-7-(4-(6-甲基苯并[d]噻唑-2-基)苯氧基)庚酰胺、7-(4-(5-氯苯并[d]噻唑-2-基)苯氧基)-n-羟基庚酰胺、8-(5-(苯并[d]噻唑-2-基)-2-甲氧基苯氧基)-n-羟基辛酰胺以及7-(3-(苯并[d]噻唑-2-基)-2-氟苯氧基)-n-羟基庚酰胺中的任一者,但不限于次。
22、在一个实施例中,所述苯并噻唑类化合物的盐包括--盐酸盐、对甲苯磺酸盐、硫酸盐、琥珀酸盐、马来酸盐、富马酸盐、醋酸盐、磷酸盐、构橼酸盐、甲磺酸盐、钠盐中的任一者。
23、本发明的第二个方面提供了一类苯并噻唑类化合物的制备方法,其包括:
24、s1、以式(ii)所示化合物为起始原料,与式(iv)所示化合物在第一反应体系中反应形成式(v)所示的第一中间体,所述第一反应体系包含连亚二硫酸钠、乙醇和水。其中,式(ii)所示化合物、式(iv)所示化合物及连亚二硫酸钠的当量比可以为1~2∶1~2∶2~4,优选为1∶1∶2左右。反应的温度可以为50~100℃,优选为80℃左右。乙醇和水主要用作溶剂,乙醇和水的体积比可以为5∶1~2左右,优选为8∶3左右。
25、s2、使所述第一中间体(1eq)在第二反应体系中反应,得到式(vi)所示的第二中间体,所述第二反应体系包含三溴化硼和二氯甲烷。其中,所述第一中间体与三溴化硼的当量比可以为1∶3~8左右,优选为1∶6左右。二氯甲烷主要用作溶剂。所述的反应可以先在0℃左右进行0.5h左右,之后在常温下进行6~12h左右。
26、s3、使所述第二中间体和式(vii)所示的溴代烷基酯类化合物在第三反应体系中反应,得到式(viii)所示的第三中间体,所述第三反应体系包括碳酸钾、碘化钾以及n,n-二甲基甲酰胺或乙腈。其中,所述第二中间体、式(vii)所示的溴代烷基酯类化合物、碳酸钾和碘化钾的当量比可以为1~2∶1~2∶2~4∶0.1~0.5,优选为1∶1.5∶2∶0.1左右。n,n-二甲基甲酰胺或乙腈主要用作溶剂。所述反应的温度可以为50~100℃,优选为80℃左右,时间可以为8~12h左右。
27、s4、使所述第三中间体在第四反应体系中反应,制得式(i)所示的苯并噻唑类化合物,所述第四反应体系包括羟胺的甲醇溶液。其中,所述第三中间体与羟胺的当量比可以为1∶3~3∶1。所述反应的温度可以为常温,时间可以为1-2h左右。
28、
29、
30、其中r1、r2至少独立地选自氢、卤素、氰基、硝基、c1-6烷基、c1-6烷氧基、c3-8环烷基、芳基、杂芳基和杂环基中的任-者,n为1~7中的任-整数,n1的取值为1、3、4、5、6或7,n2的取值为0或1。
31、本发明的第三个方面提供了一种药物组合物,其包括:
32、治疗有效量的所述苯并噻唑类化合物或其药学上可接受的盐;
33、以及,一种或多种药学上可接受的载体。
34、本发明的第四个方面提供了所述苯并噻唑类化合物或其药学上可接受的盐或者所述药物组合物在制备hdac6激酶抑制剂中的用途。
35、本发明的第五个方面提供了所述苯并噻唑类化合物或其药学上可接受的盐或者所述药物组合物在制备用于预防和/或治疗增殖性疾病的药物中的用途。
36、在一个实施例中,所述增殖性疾病包括急性髓性白血病、慢性髓性白血病、甲状腺癌、胃癌、胃肠基质肿瘤、结肠直肠癌、前列腺癌、乳腺癌、卵巢癌、胰腺癌、肺癌、非小细胞肺癌、淋巴瘤、肾癌、常染色体显性多囊肾病和骨髓瘤中的任一种,且不限于此。
37、本发明的第六个方面提供了所述苯并噻唑类化合物或其药学上可接受的盐或者所述药物组合物在制备用于预防和/或治疗常染色体显性多囊肾病的靶向药物中的用途。
38、本发明提供的一类苯并噻唑类化合物或其药学上可接受的盐在用作hdac6激酶抑制剂时,对mdck细胞和组织胚胎肾实验有很好的抑制作用,且在给药剂量为1mg/kg时,对adpkd小鼠的抑制活性与tolvaptan与相当,为常染色体显性多囊肾病的治疗和预防提供了一类新型先导化合物。
- 还没有人留言评论。精彩留言会获得点赞!