一种维生素MK-4的生物酶法制备工艺的制作方法
本发明涉及生物合成,特别涉及一种维生素mk-4的生物酶法制备工艺。
背景技术:
1、维生素k对于维护骨骼健康、预防心血管疾病以及免疫调节等方面具有重要作用。维生素k有三个类型,分别是k1、k2和k3,在人体内,维生素k1和k3必须转化为k2才能被人体吸收。维生素k2本身也分为几个不同的亚型,包括mk-4、mk-6、mk-7和mk-8,它们之间是根据化学结构上异戊二烯侧链长度不同进行分类。其中mk-4是其中比较重要的一类维生素k2,市场需求广泛,具有巨大的药用价值。
2、目前mk-4主要的工业制备方法有两种,一种是化学合成法,另一种是生物发酵法。化学合成法是最普遍应用的mk-4工业合成方案,生物发酵法则是以产黄杆菌作为发酵菌株经过发酵后分离纯化获得mk-4。
3、1979年化学合成法相关报道的整体反应以2-甲基萘为原料,经过氧化、溴化、还原、保护以及金属试剂加侧链和去保护氧化成mk-2,该反应首次在最后一步用硝酸铈铵脱除甲氧基氧化成醌,但该方法最终产物杂质较多,难以纯化。到了2003年,mk-4的化学合成路线得到了改进,通过砜基作用使两个短链连接,从而获得目的产物,但是在脱除矾基过程中会发生一定数目双键迁移。该方法路线也是目前工业上化学合成mk-4的主流生产工艺,目前国内企业主要采用化学法合成mk-4。
4、日本在1980年开始进行mk-4的微生物发酵生产尝试,主要是采用产黄杆菌进行自然发酵获得mk-4产品。通过对发酵菌株进行不断的优化筛选,时至今日mk-4的发酵生产产率仅为0.5%,而微生物法发酵生产mk-4也是日本目前的主流生产方法。
5、化学法合成mk-4主要采用烯丙基配合物为起始物料,经过十几步反应获得维生素k2,均使用金属催化剂引入侧链,成本较贵,后处理复杂;也有的合成路线采用苯并四元环酮作为核心步骤,反应步骤超过20步,关键中间体有剧毒,金属氧化剂以及保护剂等对环境污染较大;另有一些反应过程需要添加culi以及其他保护剂,反应条件较为苛刻,另外需要额外添加卤素试剂,后处理成本高。
6、目前工业上化学法合成维生素mk-4的过程中,主要有三个关键技术环节,每个环节都存在瓶颈和技术难点。第一个关键技术环节是醌官能团的保护,在化学法合成mk-4的早期研究中,一般直接用萘醌和烷基化试剂反应,由于醌在反应中结构不稳定,结果都不理想,后期进行改进后使用甲氧基作为保护剂进行基团保护,但是甲氧基也存在脱除困难的问题,而继续改进改为采用氧化银或硝酸铈作氧化剂,发现副产物较多,收率不高。目前仍然没有寻找到合适的保护基团。
7、第二个关键技术环节是反应过程中母核与侧链的连接问题,目前工业上采用两种主流方法实现母核与侧链连接:f-c烷基化和格氏反应。烷基化反应要求酸性条件,会使不饱和侧链发生成环反应,并且在萘环2位和3位存在反应性特异性低的问题,会产生大量异构体,有一部分侧链会由反式异构成顺式结构,失去生物活性。格氏反应虽然可以避免烷基化的相关弊端,但是萘环结构的格氏试剂制备较为困难,反应的引发也是一个难点。
8、第三个关键技术环节是侧链全反式结构的保持,对于维生素mk-4,只有全反式侧链才具有生物活性。目前的相关烷基化方法均不利于全反式结构的保持,导致产出无生物活性的产品。
9、对于微生物发酵法生产mk-4,与化学合成法相比,微生物发酵法具有污染低,操作简便等优点,但目前微生物发酵法生产mk-4的缺点也很明显,主要有以下几点:(1)产率低,日本经过40多年的优化选育,最高报道产率仅为0.5%;(2)发酵周期较长,为6~7天;(3)菌株优化改进方法繁杂且周期很长,日本对菌株的优化改进策略采用传统的自然诱变筛选,该优化方法费时费力,筛选周期非常长,往往需要几十年时间进行不断的选育;(4)无法获得mk-4纯品,因为产黄杆菌本身也产mk-6,发酵完后所获得的是mk-4和mk-6混合物,无法快速高效将两种物质分离开,因此发酵法所获得的mk-4均是含有mk-6杂质的混合物,以上种种弊端导致mk-4的成本居高不下。
技术实现思路
1、本发明的目的在于提供一种维生素mk-4的生物酶法制备工艺,大大缩短了合成路线,同时采用廉价原料作为出发底物,大大降低了mk-4的生产成本,且兼具生物法的相关优势比如污染少、操作简便等。相比于化学合成法和传统的微生物发酵法,本发明在产率和生产成本方面具有极大优势,另外本发明的新生物合成路线所得mk-4产品并不掺杂有mk-6,产品纯度高,减少了后续分离纯化的难度。
2、本发明解决其技术问题所采用的技术方案是:
3、一种维生素mk-4的生物酶法制备工艺,包括以下步骤:
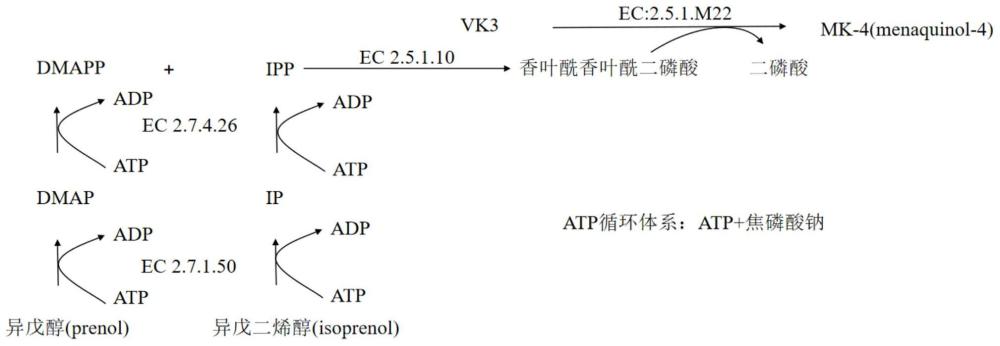
4、(1)二甲基烯丙基二磷酸的合成:异戊烯醇在羟乙基噻唑激酶(ec 2.7.1.50,ncbigene id: 945142)催化下生成二甲基烯丙基单磷酸(dmap);二甲基烯丙基单磷酸(dmap)在磷酸异戊烯基激酶(ec 2.7.4.26,ncbi gene id: 1450882)催化下生成二甲基烯丙基二磷酸(dmapp);
5、(2)异戊烯基二磷酸的合成:异戊二烯醇在羟乙基噻唑激酶(ec 2.7.1.50)催化下生成异戊烯基单磷酸(ip);异戊烯基单磷酸(ip)在磷酸异戊烯基激酶(ec 2.7.4.26)催化下生成异戊烯基二磷酸(ipp);
6、(3)香叶酰香叶酰二磷酸的合成:二甲基烯丙基二磷酸和异戊烯基二磷酸在法尼酰二磷酸合酶(ec 2.5.1.10,ncbi gene id: 945064)催化下生成香叶酰香叶酰二磷酸;
7、(4)mk-4的合成:香叶酰香叶酰二磷酸和维生素k3一起在香叶酰香叶酰转移酶(ec2.5.1.m22,ncbi gene id: hs04454)催化下生成目标产物mk-4。
8、本发明主要解决了两个关键技术问题:1.解决了目前微生物发酵法mk-4生物合成路线过长导致的产率过低的难题,通过通路重新设计大大缩短mk-4的生物合成路线,有效地提高了产率;2.解决了目前微生物发酵法生产mk-4时掺杂有mk-6杂质的问题,本发明通过更换催化反应的相关酶,使最终产物只有mk-4,而没有mk-6的生成。进而,本发明技术内容有望应用于工业规模生产mk-4。
9、本发明通过四步酶法催化即可获得mk-4。本反应体系共涉及5个酶,其中一个酶是参与建立辅因子atp循环体系,其余四个酶参与合成mk-4的催化过程。由于更换了最后一步催化反应的酶,与日本的微生物发酵法相比,本发明并不会产生mk-6杂质。
10、作为优选,步骤(1)和步骤(2)中,添加atp作为辅因子和提供能量。
11、作为优选,所述atp由atp循环系统提供,atp循环系统包括adp激酶、循环启动用atp和焦磷酸钠。
12、作为优选,所述atp由atp循环系统生成,atp循环系统包括adp激酶、循环启动用atp和焦磷酸钠,其中adp激酶浓度为0.1~10mg/l,循环启动用atp初始添加浓度为50~1000mg/l,焦磷酸钠初始添加浓度为50~1000mg/l,在酶促反应温度下进行循环,焦磷酸钠每隔1.5~2小时补加一次。
13、作为优选,步骤(1)中,酶促反应体系各原料添加量为:底物异戊烯醇1~100ml/l,羟乙基噻唑激酶0.5~50mg/l,磷酸异戊烯基激酶0.5~50mg/l;催化反应温度为20~40℃,ph控制在6-8。
14、作为优选,步骤(2)中,酶促反应体系各原料添加量为:底物异戊二烯醇1~100ml/l,羟乙基噻唑激酶0.5~50mg/l,磷酸异戊烯基激酶0.5~50mg/l;催化反应温度为20~40℃,ph控制在6-8。
15、作为优选,步骤(3)中,酶促反应体系各原料添加量为:二甲基烯丙基二磷酸和异戊烯基二磷酸的总用量为1~100g/l,其中二甲基烯丙基二磷酸和异戊烯基二磷酸的质量比为1:1~1:3,法尼酰二磷酸合酶的用量为0.5~50mg/l;催化反应温度为20~40℃,ph控制在6-8。
16、作为优选,步骤(4)中,还添加有抗坏血酸,酶促反应体系各原料添加量为:香叶酰香叶酰二磷酸1~200g/l,维生素k3 1~40g/l,抗坏血酸0.1~5g/l,香叶酰香叶酰转移酶0.5~50mg/l;催化反应温度为20~40℃,ph控制在6-8,全程避光。抗坏血酸用于防止生成的mk-4氧化。
17、作为优选,香叶酰香叶酰二磷酸和维生素k3的质量比为1:1~5:1。
18、作为优选,步骤(1)至步骤(4)中,酶促反应所用的缓冲体系为磷酸缓冲液或tris-hcl缓冲液。
19、作为优选,步骤(1)至步骤(4)中使用的酶采用大肠杆菌、枯草芽孢杆菌、酿酒酵母、毕赤酵母中的一种工程菌株表达生产。
20、本发明的有益效果是:
21、(1)本发明所设计的mk-4全新合成路线,既可以将其应用于细胞内合成mk-4,即通过代谢工程构建细胞工厂的来发酵生产mk-4,又可以进行体外全酶法合成mk-4,应用环境更加灵活;
22、(2)由于与传统生物发酵法的细胞内合成路线不同,所采用的酶也不同,因此最终产物并无mk-6杂质生成,大大简化了后期的分离纯化过程,进一步降低成本,并且操作更为简便可控;
23、(3)目前微生物发酵法由于细胞内合成路线过长,即使经过40年的优化选育,mk-4产率也是极低的,仅有0.5%,而本发明通过对mk-4合成路线进行重新设计,大大缩短了mk-4的合成路线,使产率大为提升。
- 还没有人留言评论。精彩留言会获得点赞!