一种苯并吡喃类化合物的晶型及其制备方法与流程
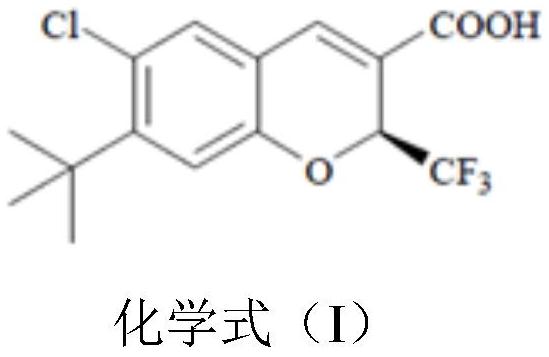
本发明属于生物医药领域,具体地,本发明涉及作为环氧合酶-2抑制剂的(2s)-7-叔丁基-6-氯-2-(三氟甲基)-2h-苯并吡喃-3-羧酸的三种晶型及其制备方法。
背景技术:
1、前列腺素在发炎过程中发挥重要作用,抑制前列腺素的生成,尤其是pgg2、pgh2及pge2的生成成为抗炎剂开发中共同的目标。但是,对减轻前列腺素诱发的疼痛和发炎过程相关的肿胀起作用的常用非甾体抗炎药(nsaids),对与发炎过程并不相关的其他前列腺素-调节过程也起作用。因此,较高剂量的使用nsaids,会产生诸如威胁生命的溃疡之类的副作用,从而限制了它们潜在的治疗性。而作为nsaids的代替方案使用皮质类固醇,尤其在长期治疗中,会具有更极端的副作用。
2、nsaids通过抑制人花生四烯酸/前列腺素路径中的酶(包括酵素环氧合酶(cox))来抑制前列腺素的生成。具体而言,在诸如炎症、疼痛及癌症之类的病理学病症中诱发环氧合酶-2(cox-2)的表达,其与病症的发生及维持有关联。从而开发出了诸如塞来昔布、罗非昔布、伐地昔布、帕瑞昔布及依他昔布之类的被称作昔布的一系列药物。
3、专利文献1(cn1257489a)中公开了一类化学式(i)表示的苯并吡喃、二氢喹啉、苯并硫吡喃及二氢萘(dihydronapthalene)衍生物,其选择性地抑制环氧合酶-2。其中,苯并吡喃衍生物比传统药物中的布洛芬具有更强的镇痛性,起效更快。而且在临床研究中确认到,苯并吡喃衍生物为传统的cox-2抑制剂和nsaids中肾脏问题较少的衍生物。
4、昔布-药物对诸如炎症、疼痛、癌症、发烧、骨关节炎、类风湿性关节炎、偏头痛、神经退行性疾病、心血管疾病、骨质疏松症、气喘、狼疮及银屑病、痛经、早产、青光眼、痛风、僵直性脊椎炎、滑囊炎、烧伤、扭伤及挫伤之类的由环氧合酶-2介导的疾病的治疗是有效的。
5、一般包含于昔布-药物的活性成分都具有磺酰胺基,相对的,化学式(i)的化合物没有磺酰胺基也没有烷磺酰基,而具有羧酸基的独特的化学结构(以下,本说明书中将没有磺酰胺基也没有烷磺酰基而具有羧酸基之类的昔布-药物或昔布化合物称作第三代昔布药物或昔布-化合物)。
6、化合物(i)的化学名为:(2s)-7-叔丁基-6-氯-2-(三氟甲基)-2h-苯并吡喃-3-羧酸,结构式如下:
7、
8、专利文献2(cn1196692c)公布了包括式i化合物在内的“用于治疗发炎的取代的苯并吡喃衍生物”,文中还公开了式i化合物的制备方法。本发明人在实验研究过程中,发现式i化合物存在新晶型a、b和c,本发明提供了式i化合物的新晶型a、b和c,这对式i化合物的应用提供了更多的选择。
9、应理解,同一药物的不同晶型在外观、溶解度、熔点、溶出度、生物有效性等方面可能会有显著不同,从而影响了药物的稳定性、生物利用度及疗效,该种现象在口服固体制剂方面表现得尤为明显。
技术实现思路
1、本发明的一个目的是提供一种苯并吡喃类化合物(2s)-7-叔丁基-6-氯-2-(三氟甲基)-2h-苯并吡喃-3-羧酸的晶型a、晶型b和晶型c及其制备方法。
2、在本发明的第一方面,提供了一种式i化合物的晶型a,
3、
4、所述的晶型a具有以下x-射线粉末衍射特征峰:9.382°±0.2°、14.908°±0.2°、16.602°±0.2°、17.847°±0.2°、18.876°±0.2°、19.563°±0.2°。
5、在另一优选例中,所述的晶型a还具有一个或多个(如2个、3个、5个、8个或10个)选自下组的x-射线粉末衍射特征峰:10.622°±0.2°、14.367°±0.2°、17.183°±0.2°、20.153°±0.2°、20.704°±0.2°、22.315°±0.2°、29.946°±0.2°。
6、在另一优选例中,所述的晶型a的x-射线粉末衍射特征峰包括:9.382°±0.2°、14.908°±0.2°、16.602°±0.2°、17.847°±0.2°、18.876°±0.2°、19.563°±0.2°、10.622°±0.2°、14.367°±0.2°、17.183°±0.2°、20.153°±0.2°、20.704°±0.2°、22.315°±0.2°、25.784.°±0.2°、26.106°±0.2°、29.946°±0.2°。
7、在另一优选例中,所述的晶型a的dsc谱图在起始温度为141-145℃和172-176℃处分别存在吸热峰;和/或
8、所述的晶型a的tga谱图在178-182℃处失重1-2wt%。
9、在另一优选例中,所述的晶型a还具有一个或多个选自下组的特征:
10、(a)所述的晶型a具有基本如表1所示的特征峰;
11、(b)所述的晶型a具有基本如图1所示的xrpd谱图;和/或
12、(c)所述的晶型a具有基本如图2所示的dsc&tga图;和/或
13、(d)所述的晶型a具有基本如图3所示的ir图;和/或
14、(e)所述的晶型a具有基本如图4所示的dvs图;和/或
15、(f)所述的晶型a具有基本如表2所示的红外吸收峰数据。
16、在本发明得到第二方面,提供了一种本发明第一方面所述的晶型a的制备方法,包括方法(a)、(b)或(c):
17、所述的方法(a)包括步骤:
18、(1a)在化合物(i)的l-苯丙氨盐溶于游离萃取溶剂和水的混合物中形成的第一溶液中加入酸,然后分离有机相;
19、(2a)对所述的有机相进行浓缩后,用第一溶剂置换,然后控温下加入第二溶剂;
20、(3a)对上述混合物保温搅拌析晶,得到晶型a;或
21、(b)在化合物(i)溶于第一溶剂中形成的第二溶液中加入第二溶剂,进行析晶并收集析出固体,得到晶型a;或
22、(c)在化合物(i)溶于第一溶剂中形成的第二溶液中加入第二溶剂,然后对混合溶液进行浓缩,用第二溶剂置换得到单一溶剂的溶液,再次进行浓缩,然后继续加入第二溶剂并进行析晶,从而得到晶型a。
23、在另一优选例中,所述的游离萃取溶剂选自下组:c1-c6酮类溶剂、c2-c6醚类溶剂、c2-c6酯类溶剂、c1-c6烷烃类溶剂,或其组合。
24、在另一优选例中,所述的游离萃取溶剂选自下组:乙酸乙酯、乙酸异丙酯、二氯甲烷、四氢呋喃、2-甲基四氢呋喃、丙酮、甲基叔丁基醚,或其组合。
25、在另一优选例中,在所述的方法(a)、(b)和(c)中,所述第一溶剂选自下组:c1-c6醇类溶剂、c1-c6酮类溶剂、c2-c6醚类溶剂、c2-c6酯类溶剂、c2-c6腈类溶剂、c1-c6烷烃类溶剂,或其组合。
26、在另一优选例中,在所述的方法(a)、(b)和(c)中,所述第一溶剂选自下组:甲醇、乙醇、异丙醇、正丁醇、乙酸乙酯、乙酸异丙酯、二氯甲烷、四氢呋喃、2-甲基四氢呋喃、甲基叔丁基醚、丙酮、乙腈,或其组合;较佳地为甲基叔丁基醚、甲醇、乙酸乙酯,或其组合。
27、在另一优选例中,在所述的方法(a)、(b)和(c)中,所述第二溶剂选自下组:水、c1-c6醇类溶剂、c1-c6酮类溶剂、c2-c6醚类溶剂、c2-c6酯类溶剂、c2-c6腈类溶剂、c1-c6烷烃类溶剂,或其组合。
28、在另一优选例中,在所述的方法(a)、(b)和(c)中,所述第二溶剂选自下组:水、乙醇、异丙醇、正丁醇、乙酸乙酯、乙酸异丙酯、二氯甲烷、四氢呋喃、2-甲基四氢呋喃、丙酮、乙腈、正庚烷、正己烷、甲基叔丁醚、异丙醚,或其组合;较佳地为乙醇、乙腈、二氯甲烷、正庚烷,或其组合。
29、在另一优选例中,在所述的方法(a)、(b)和(c)中,所述第一溶剂与所述第二溶剂是不同的。
30、在另一优选例中,所述的步骤(1a)中,所述的酸为盐酸溶液,较佳地为3-5mol/l的盐酸溶液。
31、在另一优选例中,所述的步骤(1a)中,所述化合物(i)的l-苯丙氨盐与酸的用量比(g/ml)为1:(1-4);较佳地为1:2。
32、在另一优选例中,所述的步骤(1a)中,所述游离萃取溶剂与水的体积比为1:(0.2-1);较佳地为1:(0.4-1)。
33、在另一优选例中,所述的步骤(2a)中,控制温度为≤40℃;较佳地为≤35℃。
34、在另一优选例中,所述步骤(2a)中,控制温度为10~40℃,较佳地为20~30℃在另一优选例中,所述的步骤(2a)中,所述化合物(i)的l-苯丙氨盐与所述第二溶剂的质量体积比(g/ml)为1:(2~15);较佳地为1:(4~10)。
35、在另一优选例中,所述的步骤(2a)中,分液浓缩后,有机相的体积是化合物(i)的l-苯丙氨盐质量的两倍。
36、在另一优选例中,方法(2a)中,浓缩后,用结晶溶液置换,保温析晶,其中,所述结晶溶液为第一溶剂与第二溶剂所形成的混合体系。
37、在另一优选例中,所述的方法(2a)中,所述第一溶剂为乙醇,所述第二溶剂为水。
38、在另一优选例中,所述的方法(2a)中,所述第一溶剂为乙醇,所述第二溶剂为正丁醇。
39、在另一优选例中,所述的方法(2a)中,所述第一溶剂为乙腈,所述第二溶剂为正丁醇。
40、在另一优选例中,所述的方法(2a)中,所述第一溶剂为乙腈,所述第二溶剂为水。
41、在另一优选例中,所述的步骤(3a)中,析晶时间为8-16h;较佳地为10-12h。
42、在另一优选例中,所述的步骤(3a)中,析晶温度为10~40℃;较佳地为20~30℃。
43、在另一优选例中,方法(b)中,所述的第二溶剂分批次加入或一次性加入。
44、在另一优选例中,在方法(b)中,所述析晶温度为20-30℃。
45、在另一优选例中,在方法(b)中,当所述混合物中,所述的第一溶剂为乙醇,所述的第二溶剂为水时,所述化合物(i)与乙醇的质量体积比为1:(3~20);所述化合物(i)与水的质量体积比为1:(6~40);
46、较佳地,所述化合物(i)与乙醇的质量体积比为1:(3~8);所述化合物(i)与水的质量体积比为1:(6~16)。
47、在另一优选例中,在方法(b)中,当所述混合物中,所述的第一溶剂为乙腈,所述的第二溶剂为水时,所述化合物(i)与乙腈的质量体积比为1:(1.5~6);所述化合物(i)与水的质量体积比为1:(6~24);较佳地,所述化合物(i)与乙腈的质量体积比为1:(1.5~4.5);所述化合物(i)与水的质量体积比为1:(6~18)。
48、在另一优选例中,在方法(c)中,析晶温度为-10-0℃。
49、在另一优选例中,在方法(c)中,析晶时间为8-36h,较佳地为10-24h。
50、在另一优选例中,在方法(c)中,当所述混合物中,所述的第一溶剂为甲基叔丁基醚,所述的第二溶剂为正庚烷时,所述化合物(i)与甲基叔丁基醚的质量体积比为1:(4~20);所述化合物(i)与正庚烷的质量体积比为1:(10~30);浓缩后,置换为4~5倍的正庚烷;较佳地,所述化合物(i)与甲基叔丁基醚的质量体积比为1:(4~8),所述化合物(i)与正庚烷的质量体积比为1:(10~15)。
51、在另一优选例中,所述的晶型a为白色至类白色固体状。
52、在另一优选例中,所述方法还包括对所得的晶型过滤干燥。
53、在另一优选例中,在所述方法(a)中,所述化合物(i)的l-苯丙氨盐与游离萃取溶剂/水混合物的质量体积(g/ml)比为1:(2~10),较佳地为1:(3~5);和/或
54、所述化合物(i)的l-苯丙氨盐与第一溶剂的质量体积比(g/ml)为1:(0.5~10),较佳地为1:(1~5);和/或
55、所述化合物(i)的l-苯丙氨盐与第二溶剂的质量体积比(g/ml)为1:(2~15),较佳地为1:(4~10)。
56、在另一优选例中,在所述方法(b)中,所述的化合物(i)与第一溶剂的质量体积比为1:(1.5~6);所述化合物(i)与水的质量体积比为1:(6~24)。
57、在另一优选例中,在所述方法(c)中,所述化合物(i)与第一溶剂的质量体积比为1:(4~20);
58、所述化合物(i)与第一次浓缩前,加入的第二溶剂的质量体积比为1:(5-15);
59、所述化合物(i)与第一次浓缩后,加入的第二溶剂的质量体积比为1:(5-15);和/或
60、所述化合物(i)与第二次浓缩后,加入的第二溶剂的质量体积比为1:(1-3);。
61、在本发明的第三方面,提供了一种式i化合物的晶型b,
62、
63、所述晶型b具有以下x-射线粉末衍射特征峰:18.6°±0.2°,19.5°±0.2°,16.1°±0.2°、20.3°±0.2°,25.4°±0.2°,29.0°±0.2°。
64、在另一优选例中,所述晶型b还具有一个或多个(如2个、3个、5个、8个或10个)选自下组的x-射线粉末衍射特征峰:24.1°±0.2°、29.8°±0.2°、32.5°±0.2°、9.3°±0.2°。
65、在另一优选例中,所述晶型b还具有以下x-射线粉末衍射特征峰:18.6°±0.2°、19.5°±0.2°、16.1°±0.2°、20.3°±0.2°、25.4°±0.2°、24.1°±0.2°、29.0°±0.2°、29.8°±0.2°、32.5°±0.2°、9.3°±0.2°。
66、在另一优选例中,所述的晶型b的dsc谱图在起始温度为172-176℃处存在吸热峰。
67、在另一优选例中,所述的晶型b具有一个或多个选自下组的特征:
68、(g)所述的晶型b具有基本如图6所示的xrpd谱图;和/或
69、(h)所述的晶型b具有基本如图7所示的dsc图;和/或
70、(i)所述的晶型b具有基本如图8所示的tga图;和/或
71、(j)所述的晶型b具有基本如图9所示的ir图;和/或
72、(k)所述的晶型b具有基本如图10所示的dvs图。
73、在本发明的第四方面,提供了一种本发明第三方面所述的晶型b的制备方法,包括方法(d)、(e)或(f):
74、所述的方法(d)包括步骤:
75、将化合物(i)溶于第三溶剂中,得到样品溶液;使用0.45μm孔径的聚四氟乙烯滤膜将样品溶液过滤到新容器中,用封口膜将所述新容器密封,在封口膜上扎几个小孔,放置在室温条件下挥发析晶至有固体析出,得到晶型b;或
76、所述的方法(e)包括步骤:
77、将化合物(i)溶于第四溶剂中,得到样品溶液;使用0.45μm孔径的聚四氟乙烯滤膜将样品溶液过滤到新容器中,随后磁力搅拌(转速约为1000转/分钟)得澄清溶液,并向其中逐滴加入第五溶剂,析晶,待固体析出,离心分离所得固体,得到晶型b;或
78、所述的方法(f)包括步骤:
79、将化合物(i)溶于第三溶剂中,得到样品溶液;使用0.45μm孔径的聚四氟乙烯滤膜将样品溶液过滤到新容器中,将装有样品溶液的新容器敞口放置在70-90℃(优选为80℃)加热平板上挥发析晶至有固体析出,得到晶型b。
80、在另一优选例中,在所述的方法(d)和(f)中,所述的第三溶剂选自下组:c1-c6酮类溶剂、c2-c6醚类溶剂、c2-c6酯类溶剂、c1-c6烷烃类溶剂,或其组合;较佳地,所述第三溶剂选自乙酸乙酯、乙酸异丙酯、二氯甲烷、四氢呋喃、2-甲基四氢呋喃、丙酮、甲基叔丁基醚,或其组合。
81、在另一优选例中,所述第四溶剂选自下组:c1-c6醇类溶剂、c1-c6酮类溶剂、c2-c6醚类溶剂、c2-c6酯类溶剂、c2-c6腈类溶剂、c1-c6烷烃类溶剂,或其组合。
82、在另一优选例中,所述第四溶剂选自下组:甲醇、乙醇、异丙醇、正丁醇、乙酸乙酯、乙酸异丙酯、二氯甲烷、四氢呋喃、2-甲基四氢呋喃、丙酮、甲基叔丁基醚、乙腈、甲基异丁基酮、2-丁酮,或其组合;较佳地为甲基叔丁基醚、甲醇、乙酸乙酯,或其组合。
83、在另一优选例中,所述第五溶剂选自下组:水、甘油c1-c6醇类溶剂、c1-c6酮类溶剂、c2-c6醚类溶剂、c2-c6酯类溶剂、c2-c6腈类溶剂、c1-c6烷烃类溶剂,或其组合。
84、在另一优选例中,所述第五溶剂选自下组:水、乙醇、异丙醇、正丁醇、乙酸乙酯、乙酸异丙酯、二氯甲烷、四氢呋喃、2-甲基四氢呋喃、丙酮、乙腈、正庚烷、正己烷、甲基叔丁醚、异丙醚、甘油、三氟乙醇,或其组合;较佳地为正庚烷、甘油、三氟乙醇,或其组合。
85、在另一优选例中,所述第四溶剂与所述第五溶剂是不同的。
86、在另一优选例中,所述第四溶剂为乙醇,所述第五溶剂为水。
87、在另一优选例中,所述第四溶剂为乙醇,所述第五溶剂为正丁醇。
88、在另一优选例中,所述第四溶剂为乙腈,所述第五溶剂为正丁醇。
89、在另一优选例中,所述第四溶剂为乙腈,所述第五溶剂为水。
90、在另一优选例中,所述的方法(f)中,析晶温度为50~90℃;较佳地为75~85℃。
91、在另一优选例中,方法(e)中,所述的第五溶剂分批次加入或一次性加入。
92、在另一优选例中,在方法(e)中,所述析晶温度为20-30℃。
93、在另一优选例中,所述的晶型b为白色至类白色固体状。
94、在另一优选例中,所述方法还包括对所得的晶型过滤干燥。
95、在另一优选例中,在所述方法(d)中,所述化合物(i)与第三溶剂的质量体积(g/ml)比为1:(10~100),较佳地为1:(40-100)。
96、在另一优选例中,所述方法(e)中,所述的化合物(i)与第四溶剂的质量体积比为1:(4~10);所述化合物(i)与第五溶剂的质量体积比为1:(10~250)。
97、在另一优选例中,所述方法(f)中,所述化合物(i)与第三溶剂的质量体积比为1:(5~50)。
98、在本发明的第五方面,提供了一种式i化合物的晶型c,
99、
100、所述的晶型c具有以下x-射线粉末衍射特征峰:11.253°±0.2°,19.673°±0.2°,21.052°±0.2°,18.456°±0.2°,14.193°±0.2°,8.008°±0.2°。
101、在另一优选例中,所述的晶型c还具有一个或多个(如2个、3个、5个、8个或10个)选自下组的x-射线粉末衍射特征峰:28.947°±0.2°、15.965°±0.2°、29.285°±0.2°、12.147°±0.2°、17.634°±0.2°、17.993°±0.2°、20.788°±0.2°。
102、在另一优选例中,所述晶型c的的x-射线粉末衍射特征峰包括:8.008°±0.2°、14.193°±0.2°、21.052°±0.2°、28.947°±0.2°、11.253°±0.2°、15.965°±0.2°、19.673°±0.2°、29.285°±0.2°、12.147°±0.2°、17.634°±0.2°、17.993°±0.2°、18.456°±0.2°、20.788°±0.2°。
103、在另一优选例中,所述的晶型c具有一个或多个选自下组的特征:
104、(l)所述的晶型c具有基本如表4所示的特征峰;
105、(m)所述的晶型c具有基本如图12所示的xrpd谱图。
106、在本发明得到第六方面,提供了一种本发明第五方面所述的晶型c的制备方法,其步骤如下:
107、(1c)在化合物(i)的l-苯丙氨盐溶于游离萃取第六溶剂和水的混合物中形成的第二溶液中加入酸,然后分离有机相;
108、(2c)对所述的有机相进行浓缩后,加入第七溶剂后浓缩进行溶剂置换后,控温下加入水;
109、(3c)对上述混合物保温搅拌析晶,得到晶型c。
110、在另一优选例中,在所述晶型c的制备方法中,所述第六溶剂选自下组:c1-c6醇类溶剂、c1-c6酮类溶剂、c2-c6醚类溶剂、c2-c6酯类溶剂、c2-c6腈类溶剂、c1-c6烷烃类溶剂,或其组合。
111、在另一优选例中,在所述的方法中,所述第六溶剂选自下组:甲醇、乙醇、异丙醇、正丁醇、乙酸乙酯、乙酸异丙酯、二氯甲烷、四氢呋喃、2-甲基四氢呋喃、甲基叔丁基醚、丙酮、乙腈,或其组合;较佳地为甲基叔丁基醚、乙酸乙酯,或其组合。
112、在另一优选例中,在所述的方法中,所述第七溶剂选自下组:水、c1-c6醇类溶剂、c1-c6酮类溶剂、c2-c6醚类溶剂、c2-c6酯类溶剂、c2-c6腈类溶剂、c1-c6烷烃类溶剂,或其组合。
113、在另一优选例中,在所述的方法中,所述第七溶剂选自下组:水、乙醇、异丙醇、正丁醇、乙酸乙酯、乙酸异丙酯、二氯甲烷、四氢呋喃、2-甲基四氢呋喃、丙酮、乙腈、正庚烷、正己烷、甲基叔丁醚、异丙醚,或其组合;较佳地为乙醇、乙腈、二氯甲烷、正庚烷,或其组合。
114、在另一优选例中,在所述的方法中,所述第六溶剂与所述第七溶剂是不同的。
115、在另一优选例中,所述的方法中,所述第六溶剂为甲基叔丁醚,所述第七溶剂为乙醇。
116、在另一优选例中,所述的方法中,所述第六溶剂为二氯甲烷,所述第七溶剂为乙醇。
117、在另一优选例中,所述的方法中,所述第六溶剂为甲基叔丁醚,所述第七溶剂为乙腈。
118、在另一优选例中,所述的方法中,所述第六溶剂为二氯甲烷,所述第七溶剂为乙腈。
119、在另一优选例中,方法中,所述的水分批次加入或一次性加入。
120、在另一优选例中,所述的晶型c为白色至类白色固体状。
121、在另一优选例中,所述方法还包括对所得的晶型过滤干燥。
122、在另一优选例中,在所述方法(1c)步骤中,所述化合物(i)的l-苯丙氨盐与第六溶剂/水混合物的质量体积(g/ml)比为1:(0.6~10),较佳地为1:(2~5);和/或
123、所述化合物(i)的l-苯丙氨盐与第六溶剂的质量体积比(g/ml)为1:(0.4~10),较佳地为1:(1~5);和/或
124、所述化合物(i)的l-苯丙氨盐与第七溶剂的质量体积比(g/ml)为1:(2~15),较佳地为1:(4~10)。
125、在另一优选例中,步骤(2c)中,加入的水的体积为化合物(i)的l-苯丙氨盐的5-15倍。
126、在本发明的第七方面,提供了一种药物组合物,所述的药物组合物中包括:
127、(i)作为活性成分的本发明第一方面所述的化合物(i)的晶型;和
128、(ii)药学上可接受的载体。
129、在本发明的第八方面,提供了一种本发明第一方面所述的晶型和/或本发明第七方面所述的药物组合物的用途,用于制备药物或制剂,所述的药物或制剂用于治疗环氧合酶-2介导的疾病。
130、在另一优选例中,所述的疾病选自下组:炎症、疼痛、癌症、发烧、骨关节炎、类风湿性关节炎、偏头痛、神经退行性疾病、心血管疾病、骨质疏松症、气喘、狼疮及银屑病、痛经、早产、青光眼、痛风、僵直性脊椎炎、滑囊炎、烧伤、扭伤、挫伤,或其组合。
131、在另一优选例中,所述的炎症为前列腺素诱发的炎症。
132、应理解,在本发明范围内中,本发明的上述各技术特征和在下文(如实施例)中具体描述的各技术特征之间都可以互相组合,从而构成新的或优选的技术方案。限于篇幅,在此不再一一累述。
- 还没有人留言评论。精彩留言会获得点赞!