寡核苷酸组合物及其用于外显子跳跃的方法与流程
背景技术:
1、肌肉营养不良(md)是一组肌肉病症、疾病或障碍,据报道,随着时间的推移,会导致(增加)骨骼肌衰弱和分解。主要影响肌肉的病症、疾病或障碍,当症状开始时的无力程度以及症状恶化的速度。许多md受试者最终将无法行走。在许多情况下,肌肉营养不良是致命的。一些类型也与其他器官(包括中枢神经系统)的问题有关。在一些实施例中,肌肉营养不良是杜氏肌肉营养不良(dmd)。在一些实施例中,肌肉营养不良是贝克肌肉营养不良(bmd)
技术实现思路
1、虽然美国食品和药物管理局(fda)已经批准了针对dmd的治疗,包括寡核苷酸戈罗迪生(golodirsen)和维托拉生(viltolarsen),但对于治疗包括dmd在内的肌肉营养不良的更多技术的需求仍未得到满足。除其他外,在本发明之际,尚未确定批准的寡核苷酸药物的临床益处。
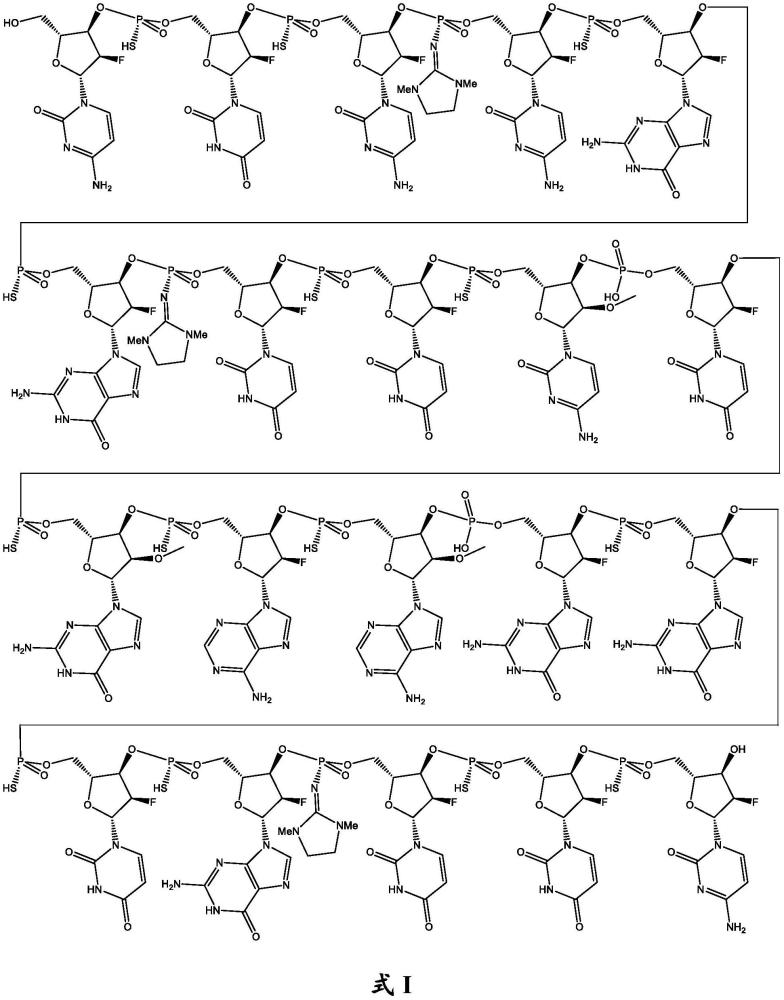
2、wve-n531是一种寡核苷酸化合物,它在体外和小鼠模型中已显示出外显子跳跃活性和dmd功能恢复。在结构上,wve-n531与戈罗迪生和维托拉生属于不同的寡核苷酸类型。例如,戈罗迪生和维托拉生均是磷酸二酰胺吗啉代寡聚物(pmo),而wve-n531是2'-f和2'-ome修饰的寡核苷酸,其中核苷酸间键联独立地是硫代磷酸酯键联、n001键联和天然磷酸酯键联。此外,手性键联磷中心未被立体定义,并且戈罗迪生和维托拉生均是作为立体随机组合物进行提供和施用,其中它们的手性键联磷中心以两种可能构型(rp或sp)随机存在:组合物是戈罗迪生和维托拉生的分别超过3300万(225)和100万(220)个非对映异构体的随机混合物。相比之下,wve-n531中的手性键联磷各自独立地被立体定义:每个硫代磷酸酯键联的键联磷是sp,而每个n001键联的键联磷是rp。如本文所证明的,wve-n531组合物是手性控制的组合物,其中与其他非对映异构体或其盐相比,wve-n531或其盐被高度富集。此外,据申请人在本披露之前所知,含有磷酸胍键联(如n001)的寡核苷酸未被系统地施用于人受试者并对其进行评估以用于治疗用途。寡核苷酸苏沃迪森(suvodirsen)包含某些化学部分,如2'-f、2'-ome、硫代磷酸酯键联等,苏沃迪森比戈罗迪生和维托拉生更相似于wve-n531,并且也是作为手性控制的寡核苷酸组合物进行制造和施用,但在评估剂量(包括约4.5mg/kg)的人临床试验中失败了。
3、除其他外,本披露提供了用于治疗肌肉营养不良(例如dmd)的技术。在一些实施例中,本披露提供了剂量和剂量方案,这些剂量和剂量方案足够安全的用于向受试者临床施用,并且有效地提供dmd外显子53跳跃、产生截短的dmd多肽(与缺乏wve-n531相比,该多肽可以发挥野生型dmd蛋白的提高水平的一个或多个功能)、dmd功能恢复或改善和/或临床益处。在一些实施例中,如本文所证明的,与苏沃迪森相比,wve-n531可以在包括人在内的灵长类动物受试者中提供改善的特性和/或活性,例如auc、cmax、组织分布和/或血浆半衰期。本文呈现的各种结果支持wve-n531可以安全且有效地用于包括在人受试者中治疗与适合于外显子53跳跃的dmd突变相关的病症、障碍或疾病。
4、在一些实施例中,本披露提供了一种用于治疗肌肉营养不良(例如dmd)的方法,该方法包括向患有该疾病的受试者施用wve-n531,施用的剂量相当于约1-20(例如约1-5、约5-10、约10-15、约15-20或约1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19或20)mg/kg(mg/kg体重)wve-n531游离酸形式,其中该受试者具有适合于外显子53跳跃的dmd基因突变。在一些实施例中,wve-n531作为药学上可接受的盐形式施用。在一些实施例中,wve-n531作为wve-n531十六钠盐形式施用。在一些实施例中,wve-n531作为一种或多种形式施用,包括一种或多种药学上可接受的盐形式,并且所有wve-n531形式的总量相当于约1-20(例如约1-5、约5-10、约10-15、约15-20或约1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19或20)mg/kg游离酸形式。在一些实施例中,wve-n531在药物组合物中施用。
5、在一些实施例中,本披露提供了一种用于治疗肌肉营养不良(例如dmd)的方法,该方法包括向患有该疾病的受试者施用包含wve-n531和药学上可接受的载剂的药物组合物,施用的剂量相当于约1-20(例如约1-5、约5-10、约10-15、约15-20或约1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19或20)mg/kg wve-n531游离酸形式,其中该受试者具有适合于外显子53跳跃的dmd基因突变。在一些实施例中,药学上可接受的载剂是或包含缓冲溶液。在一些实施例中,药学上可接受的载剂是磷酸盐缓冲溶液。在一些实施例中,wve-n531溶解在溶液中并以一种或多种形式存在,其中所有wve-n531形式的总量相当于约1-20(例如约1-5、约5-10、约10-15、约15-20或约1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19或20)mg/kg游离酸形式。
6、在一些实施例中,本披露提供了一种用于在受试者中提供dmd外显子53跳跃的方法,该方法包括向受试者施用wve-n531或包含wve-n531和药学上可接受的载剂的药物组合物,施用的剂量相当于约1-20(例如约1-5、约5-10、约10-15、约15-20或约1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19或20)mg/kg wve-n531游离酸形式。在一些实施例中,本披露提供了一种用于恢复受试者中dmd rna阅读框的方法,该方法包括向受试者施用wve-n531或包含wve-n531和药学上可接受的载剂的药物组合物,施用的剂量相当于约1-20(例如约1-5、约5-10、约10-15、约15-20或约1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19或20)mg/kg wve-n531游离酸形式。在一些实施例中,本披露提供了一种用于在受试者中提供截短的dmd多肽的方法,该方法包括向受试者施用wve-n531或包含wve-n531和药学上可接受的载剂的药物组合物,施用的剂量相当于约1-20(例如约1-5、约5-10、约10-15、约15-20或约1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19或20)mg/kg wve-n531游离酸形式。在一些实施例中,截短的(与野生型dmd蛋白相比)dmd多肽由外显子53跳跃的dmd mrna编码。在一些实施例中,这样的mrna除了外显子53外,可能缺少一个或多个另外的外显子。在一些实施例中,这样的截短的dmd多肽提供了野生型dmd蛋白的一个或多个功能(部分或全部)。在一些实施例中,本披露提供了一种用于在受试者中提供增加水平的dmd功能的方法,该方法包括向受试者施用wve-n531或包含wve-n531和药学上可接受的载剂的药物组合物,施用的剂量相当于约1-20(例如约1-5、约5-10、约10-15、约15-20或约1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19或20)mg/kg wve-n531游离酸形式。在一些实施例中,受试者具有适合于外显子53跳跃的dmd基因突变。在一些实施例中,受试者患有或易患肌肉营养不良,例如dmd。
7、在一些实施例中,施用两个或更多个剂量,每个剂量独立于本文所述的量,例如相当于约1-20(例如约1-5、约5-10、约10-15、约15-20或约1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19或20)mg/kg wve-n531游离酸形式。在一些实施例中,施用约2-10个剂量。在一些实施例中,施用10个或更多个剂量。在一些实施例中,每个剂量约是相同的。
8、在一些实施例中,约每周施用两个或更多个(例如约2、3、4、5、6、7、8、9或10或更多个)剂量。在一些实施例中,约每两周施用两个或更多个(例如约2、3、4、5、6、7、8、9或10或更多个)剂量。在一些实施例中,约每3、4、5、6、7、8、9或10周施用两个或更多个(例如约2、3、4、5、6、7、8、9或10或更多个)剂量。在一些实施例中,约每周施用剂量。在一些实施例中,约每两周施用剂量。在一些实施例中,约每三周施用剂量。在一些实施例中,约每四周施用剂量。在一些实施例中,约每月施用剂量。在一些实施例中,约每5、6、7、8、9或10周施用剂量。在一些实施例中,约每两周施用三个或更多个剂量。在一些实施例中,首先以较短的间隔(例如,约每两周)施用剂量,然后以较长的间隔(例如,约每3、4、5、6、7、8、9或10周)施用剂量。在一些实施例中,约每两周施用两个或更多个剂量,例如约2、3、4、5、6、7、8、9或10个剂量,随后施用一个或多个剂量,每个剂量从其先前剂量后约3、4、5、6、7、8、9或10周独立地施用。在一些实施例中,约每两周施用约2、3、4、5、6、7、8、9或10个剂量,以及约每3、4、5、6、7、8、9或10周或约每月施用一个或多个剂量。在一些实施例中,从第一剂量起,约每两周施用剂量,持续约2、3、4、5、6、7、8、9、10、11、12、13、14、15或16周或更多周数,然后约每3、4、5、6、7、8、9或10周施用剂量。在一些实施例中,从第一剂量起,每两周施用剂量,持续约4、8、12或16周或更多周数,然后约每4周施用剂量。在一些实施例中,从第一剂量起,每两周施用剂量,持续约4、8、12或16周或更多周数,然后约每月施用剂量。在一些实施例中,首先约每两周施用剂量,然后从第一剂量起约4周、8周、12周或16周后,约每四周或约每月施用剂量。在一些实施例中,每个剂量独立地是约相同的,例如约10mg/kg。
9、在一些实施例中,wve-n531或其组合物静脉内施用。在一些实施例中,wve-n531或其组合物肌内施用。在一些实施例中,剂量以约20-60,例如约20、25、30、35、40、45、50、55或60分钟静脉输注施用。在一些实施例中,输注施用约1、2、3或4小时。在一些实施例中,如果错过了剂量,则可在预定剂量之后尽快施用。
10、在一些实施例中,受试者是儿科受试者。在一些实施例中,受试者是男孩受试者。在一些实施例中,受试者年龄不小于5岁。在一些实施例中,受试者年龄不超过18岁。在一些实施例中,受试者符合实例中描述的一个或多个或所有纳入标准。在一些实施例中,根据实例中描述的一个或多个或所有纳入和排除标准选择受试者。
11、在一些实施例中,wve-n531以可达到临床上显著的最大血浆浓度的剂量进行施用。
12、在一些实施例中,受试者在wve-n531或其组合物第一剂量前至少约六个月(或24周)施用类固醇。在一些实施例中,受试者在wve-n531或其组合物第一剂量前至少约六个月(或24周)施用皮质类固醇。在一些实施例中,受试者接受稳定的皮质类固醇治疗方案。在一些实施例中,皮质类固醇是地夫可特(deflazacort)。在一些实施例中,受试者在wve-n531或其组合物的第一剂量前至少约一个月施用类固醇。
13、在一些实施例中,提供的技术(寡核苷酸、组合物、方法、剂量、剂量方案等)提供了一个或多个所期望的生物学效应。在一些实施例中,提供的技术提供了外显子53跳跃。在一些实施例中,提供的技术提供了临床显著水平的外显子53跳跃。在一些实施例中,提供的技术提高了内部截短但具功能性的dmd多肽(例如,由外显子53跳跃的dmd mrna编码)的水平。在一些实施例中,提供的技术提供了一个或多个恢复的dmd功能,例如,通过截短但具功能性的dmd多肽。在一些实施例中,提供的技术提供了临床益处。在一些实施例中,疾病进展得到延迟、减缓或预防。在一些实施例中,疾病进展得到延迟、减缓或预防,如通过10米步行测试评估的。在一些实施例中,提供的技术减少了肺功能丧失(相对于基线)。在一些实施例中,受试者的肌无力得到延迟、减缓或预防。在一些实施例中,受试者的肌肉质量损失得到延迟、减缓或预防。在一些实施例中,受试者在肌肉肌营养不良蛋白评估中得到改善。在一些实施例中,受试者在dmd评估中得到改善。在一些实施例中,在一个或多个功能评估中实现了改善,包括北极星移动评估(nsaa)2.0、上肢性能(pul)2.0、四梯攀爬、手持肌测量和肺功能测试。在一些实施例中,此类评估按这样的顺序进行。在一些实施例中,评估是或包括定时功能测试(包括10米步行/跑步时间、四梯攀爬时间和从地面起来的时间)的下肢运动功能。在一些实施例中,评估是或包括利用手持式肌测仪评估的上肢近端强度。在一些实施例中,评估是或包括肺功能测试(峰流速[pfr]、咳嗽峰流量[cpf]和fvc)。在一些实施例中,在一个或多个或所有这些评估中独立地实现了改善。在一些实施例中,评估是在实例中披露的评估。在一些实施例中,将改善与基线进行比较。在一些实施例中,将改善与wve-n531施用之前进行比较。在一些实施例中,将改善与预测的wve-n531施用后水平、严重程度和/或功能进行比较。在一些实施例中,将改善与未施用wve-n531进行比较。在一些实施例中,将改善与施用参考组合物进行比较。在一些实施例中,参考组合物与施用的wve-n531组合物相当,但不包含wve-n531或包含较少数量的wve-n531。
14、在一些实施例中,提供的技术减少了行走丧失(相对于基线)。
15、在一些实施例中,提供的技术在施用一定时间段后或施用一定数量的剂量后,使肌营养不良蛋白水平相对于基线增加正常水平的约1%或更多。在一些实施例中,增加约1%或更多。在一些实施例中,增加约2%或更多。在一些实施例中,增加约3%或更多。在一些实施例中,增加约4%或更多。在一些实施例中,增加约5%或更多。在一些实施例中,增加约6%或更多。在一些实施例中,增加约7%或更多。在一些实施例中,增加约8%或更多。在一些实施例中,增加约9%或更多。在一些实施例中,增加约10%或更多。在一些实施例中,增加约11%或更多。在一些实施例中,增加约12%或更多。在一些实施例中,增加约13%或更多。在一些实施例中,增加约14%或更多。在一些实施例中,增加约15%或更多。在一些实施例中,增加约16%或更多。在一些实施例中,增加约17%或更多。在一些实施例中,增加约18%或更多。在一些实施例中,增加约19%或更多。在一些实施例中,增加约20%或更多。在一些实施例中,时间段为约10-60周。在一些实施例中,时间段为约4周。在一些实施例中,时间段为约8周。在一些实施例中,时间段为约10周。在一些实施例中,时间段为约12周。在一些实施例中,时间段为约13周。在一些实施例中,时间段为约14周。在一些实施例中,时间段为约15周。在一些实施例中,时间段为约16周。在一些实施例中,时间段为约20周。在一些实施例中,时间段为约24周。在一些实施例中,时间段为约25周。在一些实施例中,时间段为约28周。在一些实施例中,时间段为约30周。在一些实施例中,时间段为约32周。在一些实施例中,时间段为约35周。在一些实施例中,时间段为约36周。在一些实施例中,时间段为约37周。在一些实施例中,时间段为约38周。在一些实施例中,时间段为约40周。在一些实施例中,时间段为约45周。在一些实施例中,时间段为约48周。在一些实施例中,时间段为约49周。在一些实施例中,时间段为约50周。在一些实施例中,时间段为约72周。在一些实施例中,时间段为约73周。在一些实施例中,时间段为约74周。在一些实施例中,时间段为约96周。在一些实施例中,时间段为约97周。在一些实施例中,时间段为约98周或更长时间。在一些实施例中,时间段为约1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19或20个月。在一些实施例中,一定数量的剂量为约5个剂量。在一些实施例中,一定数量的剂量为约6个剂量。在一些实施例中,一定数量的剂量为约7个剂量。在一些实施例中,一定数量的剂量为约8个剂量。在一些实施例中,一定数量的剂量为约9个剂量。在一些实施例中,一定数量的剂量为约10个剂量。在一些实施例中,一定数量的剂量为约11个剂量。在一些实施例中,一定数量的剂量为约12个剂量。在一些实施例中,一定数量的剂量为约13个剂量。在一些实施例中,一定数量的剂量为约14个剂量。在一些实施例中,一定数量的剂量为约15个剂量。在一些实施例中,一定数量的剂量为约16个剂量。在一些实施例中,一定数量的剂量为约17个剂量。在一些实施例中,一定数量的剂量为约18个剂量。在一些实施例中,一定数量的剂量为约19个剂量。在一些实施例中,一定数量的剂量为约20个剂量。在一些实施例中,一定数量的剂量为约21个剂量。在一些实施例中,一定数量的剂量为约22个剂量。在一些实施例中,一定数量的剂量为约23个剂量。在一些实施例中,一定数量的剂量为约24个剂量。在一些实施例中,一定数量的剂量为约25个剂量。在一些实施例中,一定数量的剂量为约30个剂量。在一些实施例中,一定数量的剂量为约35个剂量。在一些实施例中,一定数量的剂量为约40个剂量。在一些实施例中,一定数量的剂量为约45个剂量。在一些实施例中,一定数量的剂量为约48个剂量。在一些实施例中,一定数量的剂量为约49个剂量。在一些实施例中,一定数量的剂量为约50个或更多个剂量。在一些实施例中,wve-n531每两周施用。
16、在一些实施例中,提供的技术不会导致不良事件或低水平的不良事件,或者不会导致重度和/或严重不良事件或低水平的重度和/或严重不良事件。在一些实施例中,与提供的技术相关的不良事件是可接受或可控制的。
17、在一些实施例中,本披露提供了用于制造wve-n531的技术。在一些实施例中,本披露提供了用于制造wve-n531药物物质的技术。在一些实施例中,本披露提供了用于制造wve-n531药物产品的技术。在一些实施例中,本披露提供了用于表征wve-n531药物物质和/或产品的技术。在一些实施例中,本披露提供了用于表征wve-n531药物物质和/或产品的发布规格。在一些实施例中,本披露提供了wve-n531、其组合物、通过所提供的方法制造的其药物物质和/或产品。
- 还没有人留言评论。精彩留言会获得点赞!