一种特异性结合红细胞膜的多肽或其突变体的制作方法
本发明公开了一种多肽。
背景技术:
1、药物的半衰期是描述药物在生物体内的传递、代谢和排泄过程的重要参数,反映了药物在体内消除的速度,并决定了用药物的次数和剂量,是衡量药物作用效果的有效工具。半衰期短的药物,在血液中的浓度会很快下降,给药次数相对较多;半衰期长的药物,在血液中的浓度衰减较慢,给药次数减少并能维持稳定的药物浓度,达到更理想的疾病控制。长效药物的技术开发不仅意味着患者治疗成本的下降,可以在减少剂量的同时,降低护理成本和安全风险,而且还能提高患者的依从性和治疗效果。例如生长激素和glp-1受体(胰高血糖素样肽-1受体,glucagon-like peptide-1 receptor)激动剂的长效化,不仅给患者带来了更便利的治疗体验,安全性和疗效也显著提高。目前增加蛋白质药物循环的方法仍然主要集中在三种策略上,1)增加分子的表观流动力学半径,减少肾小球滤除速率,例如,化学偶联聚乙二醇(polyethylene glycol, peg)或其他水溶性聚合物(如xten等);2)调节与血浆蛋白结合和释放的平衡,缓慢释放药物,进而延长半衰期,例如通过化学偶联脂肪酸链(如司美格鲁肽),借助脂肪酸链与血清白蛋白结合而延长半衰期;3)与抗体的fc融合(如阿巴西普),不仅通过增大分子体积,降低肾清除率,还利用fcrn(fc受体)介导的保护作用延长半衰期,血浆半衰期能达到10天。
2、成熟红细胞在人体内循环时间长达120天,因此被认为是潜在的延长药物半衰期的优秀载体。此外红细胞是血液中数量最多的细胞,无细胞核,可异体回输,并且具有极高的生物相容性,能够完全降解,以及免疫逃逸和免疫耐受,基于红细胞的这些特征,目前很多研究正在进行药物的开发和药物递送,但是目前还没有较大的突破。利用红细胞延长半衰期的方法主要有两种策略,1)利用物理化学方法将药物封闭于红细胞内部,2)将药物富集于红细胞的表面。将药物封闭于红细胞内部的方法,相关研究很多,例如低渗法、化学法、胞吞法和脂质融合法等。其主要机理是在低渗条件下或者通过物理挤压,主动或被动地使得药物进入红细胞内,而后在高渗条件修复红细胞膜,封装药物;进入到人体循环中,再利用红细胞膜的通透性进行药物释放。这种方法对红细胞的损伤较大,难以维系正常的红细胞循环寿命。将药物富集于红细胞的表面的方法相对比较柔和,如利用纳米聚合物颗粒,将其附着在红细胞的表面,这些附着的纳米颗粒会随着红细胞进行循环,并逐渐脱落,从而在一定程度上延长药物的作用(nanoscale.2019, 11:1636–46; acta pharmacol sin 2021,42:1040–1054)。此外研究较多的则是红细胞膜特异性的结合,例如靶向补体受体一型分子(cr1),也称为c3b受体或c3b/c4b受体,红细胞上的cr1数约为50~1400个/细胞。利用抗体靶向cr1抗体与治疗性蛋白融合,可以通过与红细胞结合显著提高药物的半衰期,如sergeizaitsev等将cr1抗体和tpa融合,在增加药物半衰期的同时,可以减轻副作用(blood.2006,108:1895–902)。但是因为cr1在红细胞上的拷贝数相对较低,携带的药物较少,同时cr1作为免疫粘附受体,靶向cr1会影响红细胞体内携带、运输及清除循环免疫复合物的重要功能。b3p(band 3 protein)又名阴离子交换蛋白1( anion exchanger 1, slc4a1),也主要表达在红细胞表面,大约有120万个拷贝,约占红细胞细胞膜蛋白的25%。balthasar jp等利用靶向b3p的纳米抗体和靶向tnf-α的抗体融合,可以在小鼠体内显著的延长半衰期,同时具有很好的安全性(int j mol sci. 2022 dec 28:475.)。但红细胞的b3p通过与锚蛋白和细胞骨架网络的物理连接,对于红细胞的双凹圆碟形起到重要的机械支持,并调节红细胞内的ph值,与红细胞的弹性、可塑性、维持气体交换面积等生理功能直接相关,靶向b3p可能会引起红细胞物理性状改变而缩短寿命。
3、噬菌体展示技术是通过基因工程技术把外源的多肽库或蛋白库表达在噬菌体表面,通过与锚定在固体表面的靶蛋白结合与否的筛选,经过3~5轮的淘洗和富集,逐步提升特异性识别靶分子的噬菌体比例,最终获得与靶分子特异性结合的多肽或者蛋白。jeffreya. hubbell和stephan kontos在多篇文献中(mol pharm. 2010 dec 6, 2141-7; chemsoc rev.2012 apr 7,41:2686-95; curr opin immunol. 2015 aug,35:80-8)以及pct/us2011/047078中描述了用完整的红细胞作为靶点筛选噬菌体库,分别得到了系列多肽。利用完整红细胞作为靶点筛选噬菌体库,但细胞作为靶点不仅固化困难,而且在筛库过程中红细胞容易发生破裂,细胞浆内的血红蛋白会造成筛选过程的污染。在上述专利和文献中描述了命名为ery1的多肽,与小鼠红细胞特异性结合,但与人红细胞无结合力;在小鼠模型中,ery1与抗原蛋白进行偶联后抗原的血清半衰期延长,免疫原性减弱。但由于ery1与人红细胞无法结合,因此在转化医学上存在空白。此外,利用红细胞特殊的膜蛋白作为靶点,用基因工程方法表达纯化得到重组的蛋白质,例如靶向cr1(complement receptor 1,补体受体一型分子)和gypa(glycophorin-a),筛选针对它们的多肽。但这种方法忽略了红细胞最为特殊的细胞类型,对所有的蛋白质分子都有相对独特的翻译后修饰,包括磷酸化、乙酰化、甲基化、糖基化、泛素化等。
4、通过靶向红细胞而达到延长半衰期的目的,首先要满足几个条件,1)与红细胞之间的结合一定是可逆的,即亲和力不能过高,药物要从红细胞膜上解离成游离状态后才能发挥药效;2)高特异性,与其它血细胞(如淋巴细胞等)无结合,不会由于和其它细胞结合而穿越血管内皮进入组织。此外,与红细胞的结合最好不会影响红细胞的功能。结合位点不一定是膜蛋白上的氨基酸序列,也可以是蛋白质翻译后的特殊修饰及其组合。
5、因此本发明的目的就是提供一种符合上述描述,能与小鼠和人的红细胞膜特异结合的多肽。与重组蛋白药物融合后,利用多肽与红细胞结合的特性,延长药物的循环半衰期。
技术实现思路
1、基于上述目的,本发明首先提供了一种特异性结合红细胞膜的多肽或其突变体,所述多肽的氨基酸序列如seq id no.1所示,所述多肽在本发明中被命名为rhm-6。
2、所述多肽的突变体的氨基酸序列为在seq id no.1所示氨基酸序列的基础上任意位点的其它氨基酸残基突变为丙氨酸的突变体或者第8-9位氨基酸残基被删除的截短突变体。
3、为了进一步优化rhm-6,本发明对序列中的9个氨基酸进行了定点突变研究。首先发现c末端的两个氨基酸去除后,对人红细胞的结合功能影响不大。随后逐一对氨基酸进行了丙氨酸(ala,a)置换突变,研究发现v2a(n端第2位氨基酸缬氨酸v置换突变为丙氨酸a)、d4a(n端第4位氨基酸天冬氨酸d置换突变为丙氨酸a)和w6a(n端第6位氨基酸色氨酸w置换突变为丙氨酸a)三个突变体对人红细胞的结合力有明显提高。
4、在一个优选的实施方案中,所述突变体的氨基酸序列选自seq id no.2-10中的任意一种。
5、其中,氨基酸序列如seq id no.2所示的突变体被命名为rhm-6 (l1a)、氨基酸序列如seq id no.3所示的突变体被命名为rhm-6 (v2a)、氨基酸序列如seq id no.4所示的突变体被命名为rhm-6(e3a)、氨基酸序列如seq id no.5所示的突变体被命名为rhm-6(d4a)、氨基酸序列如seq id no.6所示的突变体被命名为rhm-6 (l5a)、氨基酸序列如seqid no.7所示的突变体被命名为rhm-6 (w6a)、氨基酸序列如seq id no.8所示的突变体被命名为rhm-6 (i7a)、氨基酸序列如seq id no.9所示的突变体被命名为rhm-6 (v9a);氨基酸序列如seq id no.10所示的第8-9位氨基酸残基被删除的截短突变体被命名为rhm-6(delgv)。
6、在一个更为优选的实施方案中,所述红细胞包括人红细胞、小鼠红细胞、大鼠红细胞和食蟹猴红细胞。
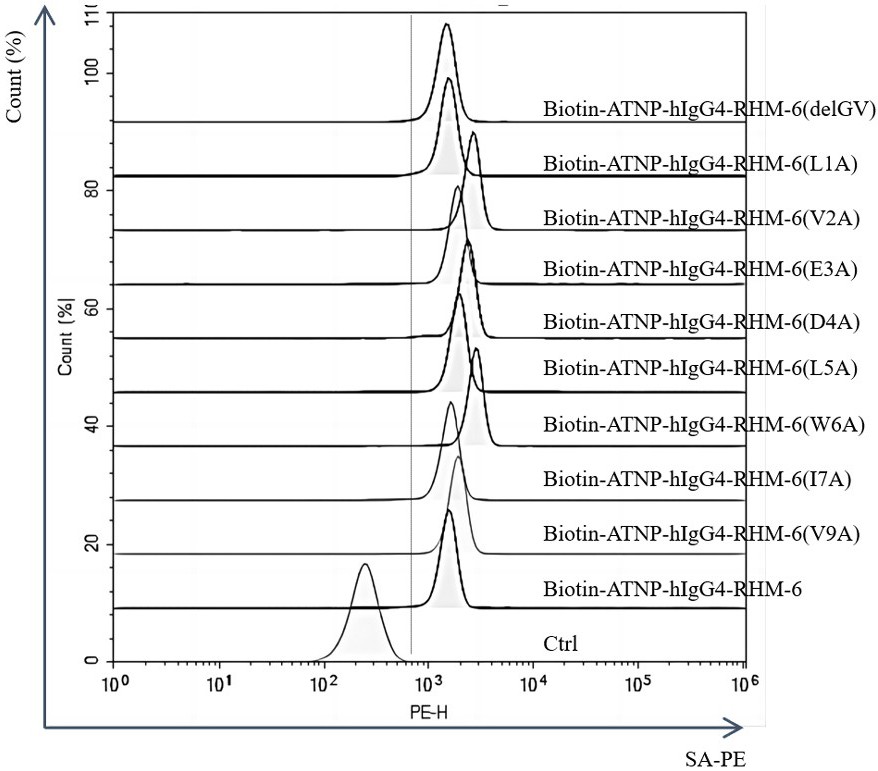
7、在本发明中,合成上述多肽时,在n端偶联生物素(biotin)用于后续的检测。合成的多肽,分别与人和小鼠的新鲜红细胞进行体外孵育,通过流式细胞仪(facs)和荧光标记的链霉素(如streptavidin-pe)检测,进一步确定筛选得到的多肽能够与完整的红细胞结合。其中,多肽rhm-6能够与人和小鼠的红细胞结合,并且具有相似的亲和力(kd值介于20~40 μm),属于弱亲和力。rhm-6不仅能与人和小鼠红细胞结合,与大鼠红细胞、食蟹猴的红细胞及比格犬的红细胞均可以结合。但rhm-6与血液循环中的淋巴细胞,中性粒细胞,nk细胞等都无明显结合,与常见的小鼠和人类的肿瘤细胞系也没有明显结合。对rhm-6进行序列同源分析,在已知的蛋白序列数据库中未找到与其全长一致的序列,相似的序列均为细菌的酶或者未知蛋白的部分序列(约占蛋白全序列的10%)。
8、在本发明中,为了进一步了解rhm-6在红细胞膜上的结合位点,本发明进行了液相色谱-质谱联用分析 (liquid chromatography mass spectrometry, lc-ms):用链霉亲和素磁珠(streptavidin beads,sa beads)与biotin-rhm-6结合后,再与人的红细胞蛋白提取物进行结合,分离纯化出与rhm-6特异性结合的红细胞膜提取物中的组分,然后利用lc-mass进行分析和鉴定。鉴定得到的蛋白主要包括ephrin type-a receptor 2(epha2),mansc domain-containing protein 4(mansc4),beta-1,4-galactosyltransferase 1(b4galt1),long-chain fatty acid transport protein 6(slc27a6),transferrinreceptor protein 2(tfr2),fer-1-like protein 6(fer1l6),membrane proteinfam174a(fam174a)等。虽然这些蛋白并不是红细胞特异的,但并没有发现rhm-6与其它类型细胞有特异性结合,因此猜测,这些蛋白在红细胞上有特殊的翻译后修饰,包括磷酸化、乙酰化、甲基化、糖基化、泛素化等。这些发现也证明了,用红细胞膜提取物而不是用重组蛋白作为筛选靶点,是更为有效的筛选策略。
9、在一个优选的实施方案中,所述多肽或其突变体特异性结合于红细胞膜的ephrintype-a receptor 2、mansc domain-containing protein 4、beta-1,4-galactosyltransferase 1、long-chain fatty acid transport protein 6、transferrinreceptor protein 2、fer-1-like protein 6和membrane protein fam174a中的一种或多种。
10、红细胞与rhm-6共同孵育后,未发现红细胞膜完整性遭到破坏,表现为红细胞内2,3-dpg(2,3-二磷酸甘油酸),以及游离血红蛋白与天然红细胞无明显差异(结果未显示)。在小鼠实验中,也未发现与rhm-6共同孵育后的红细胞半衰期改变。因此rhm-6本身不会引起红细胞功能的改变。
11、其次,本发明提供了一种含有上述的多肽或其突变体的融合蛋白。
12、在一个优选的实施方案中,所述融合蛋白还含有生物功能分子或生物标志物。
13、在一个更为优选的实施方案中,所述生物功能分子或生物标志物为抗体、酶、核酸或多肽。在本发明的一个具体实施方案中,所述抗体为抗三硝基苯酚(trinitrophenyl,tnp)的重组单克隆抗体(atnp-higg4),其与所述的多肽或其突变体的融合蛋白分别命名为:atnp-higg4-rhm-6,atnp-higg4-rhm-6(l1a),atnp-higg4-rhm-6(v2a),atnp-higg4-rhm-6(e3a),atnp-higg4-rhm-6(d4a),atnp-higg4-rhm-6(l5a),atnp-higg4-rhm-6(w6a),atnp-higg4-rhm-6(i7a),atnp-higg4-rhm-6(v9a),atnp-higg4-rhm-6 (delgv)。
14、在另一个具体实施方案中,所述生物功能分子为人生长因子,所述融合蛋白被命名为“hgh-rhm-6”。
15、再次,本发明提供了一种缀合物,所述缀合物为缀合了上述的多肽或其突变体的生物功能分子或生物标志物。
16、在一个优选的实施方案中,所述生物功能分子或生物标志物为抗体、酶、核酸或多肽。
17、在本发明的一个具体实施方案中,在rhm-6的n端加入游离的半胱氨酸(cystine,cys), 同时偶联生物素(biotin),方便后续检测。在胺-巯基交联剂sulfo-smcc的介导下,将biotin-cys-rhm-6随机偶联到hgh(human growth hormone)上的赖氨酸上(hgh有9个赖氨酸),缀合物称为hgh-rhm-6×n 。质谱分析后,每个hgh携带2~3个rhm-6。
18、根据本发明的发现,本发明提供了一种药学上可延长生物功能分子或生物标志物半衰期的策略,其包含将特异性结合患者红细胞的“红细胞结合部分”即本发明披露的红细胞膜结合多肽与发挥药效的蛋白质分子,例如重组蛋白、抗体或抗体片段融合或者缀合的方法。例如在本发明中,rhm-6分别融合在抗体重链的c末端,或者重组蛋白如生长激素(growth hormone, gh)的c末端,或者将rhm-6与生长激素缀合。首先在体外利用流式细胞术对融合蛋白和缀合物结合红细胞的能力进行了检测,然后将融合蛋白或缀合物通过静脉注射给小鼠,检测融合蛋白或缀合物在小鼠体内的半衰期,本发明发现,两者均能够延长半衰期。
19、最后,本发明提供了一种筛选特异性结合红细胞膜的多肽的方法。红细胞作为特殊的细胞类型,对所有的蛋白质分子都有相对独特的翻译后修饰,包括磷酸化、乙酰化、甲基化、糖基化等,红细胞膜的提取物保留了独特的翻译后修饰,使得筛选得到的多肽能够特异性识别红细胞膜上的蛋白质分子,即便是该分子也同样表达在别的类型的细胞膜上,但现有技术方法筛选出来的某些多肽却仅仅识别红细胞上的蛋白质分子,例如,manscdomain-containing protein 4表达在多种细胞和组织中包括鳞状上皮细胞、神经元细胞、滋养细胞,其原因可能是在第407和435位上的糖基化类型不同。本发明利用了序贯筛选的方法,例如,先用小鼠的红细胞膜作为靶点,筛选得到的亚库再以人的红细胞膜作为靶点进行筛选,反之亦然,得到同时可以结合小鼠和人的红细胞膜的多肽,所述方法包括以下步骤:
20、(1)制备8-15个氨基酸长度的混合线性肽库、12个氨基酸长度的线性肽库,以及基于所述8-15个氨基酸长度的混合线性肽库并排除了对筛选有影响的非特异性序列重新构建的肽库;
21、(2)将小鼠红细胞膜作为固相,步骤(1)获得的肽库作为流动相,筛选出来的噬菌体命名为一级亚库;再以人红细胞膜作为固相,一级亚库作为流动相,筛选得到的噬菌体命名为二级亚库;以及
22、将人红细胞膜作为固相,步骤(1)获得的肽库作为流动相,筛选出来的噬菌体命名为一级亚库;再以小鼠红细胞膜作为固相,一级亚库作为流动相,筛选得到的噬菌体命名为二级亚库;
23、(3)用免疫学方法确定阳性噬菌体克隆,得到能够同时结合小鼠和人红细胞膜的候选噬菌体;
24、(4)通过测序确定阳性克隆的多肽序列。
25、在本发明提供的上述方法中,靶点选择的是红细胞膜提取物,充分去除了细胞内的所有成分,但保留了所有可能的红细胞独特的蛋白质翻译后修饰,更大几率上能获得与红细胞特异性结合的多肽。
26、在步骤(1)中,使用了三种不同的人工合成噬菌体库进行筛选,包括8~15个氨基酸的混合线性肽库(lib p),12个氨基酸的线性肽库(lib p trimer),以及lib p-qy多肽库。lib p多肽库针对多种不同靶点蛋白进行筛选,如果库中同一种多肽作为阳性多肽反复出现,则说明这个多肽可能是因为非特异性的黏性与不同靶点蛋白结合,被认为是非特异性序列,而从lib p中剔除。因此,lib p-qy多肽库是基于lib p多肽库,排除了对筛选有影响的非特异性序列重新构建的肽库,lib p-qy多肽库提升了对于靶点的针对性。这三个库都是通过kunkel突变方法构建的全合成多肽库。kunkel突变是一种研究基因突变的实验方法(methods mol biol.2012, 907:195–209),原理是利用dna聚合酶的错误扩增机制,在体外特定条件下引入突变,从而改变目标基因的序列。本发明使用的kunkel突变效率能达到100%,有利于保证库的多样性,进而提高筛选的成功率。
27、步骤(2)中,为了方便转化医学的实施,获得能够同时结合小鼠和人红细胞膜的多肽,用两种策略进行了多轮筛选:首先将小鼠红细胞膜作为固相,噬菌体库作为流动相,筛选出来的噬菌体命名为一级亚库;再以人红细胞膜作为固相,一级亚库作为流动相,筛选得到的噬菌体命名为二级亚库;对二级亚库进行噬菌体-酶联免疫吸附实验(phage elisa)检测,确定阳性噬菌体克隆,并对其扩增。类似上述操作,先将人红细胞膜作为固相筛选得到一级亚库,再以小鼠红细胞膜作为固相筛选得到二级亚库,并用phage elisa确定阳性噬菌体克隆。通过这种交叉筛选策略得到能够同时结合小鼠和人红细胞膜的候选噬菌体。
28、步骤(3)中,所述免疫学方法为elisa,分别用人和小鼠的红细胞膜包被elisa平板,以空噬菌体作为阴性对照,对上述得到的噬菌体克隆株进行亲和力半定量的检测并排序,选择亲和力高、且与人和小鼠红细胞膜都结合的噬菌体克隆。
29、步骤(4)中,通过pcr确定阳性克隆的多肽序列。经过对三个噬菌体库进行筛选,得到12条单一多肽序列。
30、综上,本发明通过特异性结合红细胞膜的多肽的筛选方法筛选到的多肽可以与蛋白质药物融合表达,药物注射到外周血中,通过与红细胞的可逆性结合,以红细胞作为载体,延长药物的血浆半衰期。多肽片段小,且没有特定的功能,不会影响药物本身的药效。同时,本发明的多肽能够同时结合人和小鼠的红细胞,且具有相似的亲和力,因此药物在小鼠模型中的表现可以用于预测在人体中的表现,具有良好的医学转化特点。
- 还没有人留言评论。精彩留言会获得点赞!