成纤维细胞和角质细胞分化成3D皮肤模型及血管内皮细胞和肝细胞培养方法
本发明涉及生物医药应用,具体涉及成纤维细胞和角质细胞分化成3d皮肤模型及血管内皮细胞和肝细胞的培养方法。
背景技术:
1、许多外源化学品会经皮暴露,它们与机体有较强的反应性并可明确产生各种毒性作用,但它们经皮暴露后,先会被皮肤中的n-乙酰化酶代谢,因此会与传统毒理学评价方法中为了达到最大暴露量采用的经口暴露体内试验产生很大的毒性差异;而皮肤和肝代谢系统的差异也会让使用肝脏s9代谢活化系统进行的2d培养细胞系体外毒性试验产生误导性结果。因此,考虑到减少、替代和优化原则和人体相关性,人们开发了皮肤芯片。皮肤芯片也称作皮肤微流控设备,是一种动态灌注的体外3d皮肤模型,它能使营养物质的运输更加生理化,可模拟天然人皮肤的3d微环境,能观察到传统2d模型无法重建的体内多重3d细胞间的相互作用,并对化学品的毒性、疗效和输送进行高通量和低成本的快速筛选。但现有的皮肤微流控芯片多数结构复杂,管路长,辅助设备多,易污染,样本数多时需多人操作,使用便捷性差;同时它们都没有代谢产物的毒性靶细胞,因此都无法评价可能存在的经皮代谢后有肝细胞毒性的代谢产物。
2、有鉴于此,本发明提供成纤维细胞和角质细胞分化成3d皮肤模型及血管内皮细胞和肝细胞的培养方法。
技术实现思路
1、本发明的目的在于针对现有技术的不足,提供成纤维细胞和角质细胞分化成3d皮肤模型及血管内皮细胞和肝细胞的培养方法。
2、为了解决上述技术问题,采用如下技术方案:
3、成纤维细胞和角质细胞分化成3d皮肤模型及血管内皮细胞和肝细胞的培养方法,所述方法培养的成纤维细胞和角质细胞放置在芯片中完成培养,包括以下步骤:
4、s1.先配制成纤维细胞胶原混合物,然后取200-500μl成纤维细胞胶原混合物加到芯片的第一培养室内,最后在37℃凝胶0.5-2h使所述纤维细胞胶原混合物固化,接着在芯片的其它腔室加满10% fbs dmem培养液,培养6-8天。
5、s2.在上述培养6-8天后,将所述10% fbs dmem培养液更换为epidermalizationⅰ,往所述成纤维细胞胶原混合物表面滴加10-100μl角质细胞悬液,控制所述角质细胞在第一培养室的终密度为500-5000个/mm2,静置5-20min后,放入培养箱,37℃孵育0.5-2h;最后往第一培养室中缓慢滴加epidermalizationⅰ至满,所述芯片的其它腔室也加满epidermalizationⅰ,培养2-4天。
6、s3.在上述培养2-4天后,先将芯片中的epidermalizationⅰ吸去,然后加满epidermalizationⅱ,培养1-3天。
7、s4.在上述培养1-3天后,将芯片中的epidermalizationⅱ吸去,在第二培养室和第三培养室、第一储液室中加满cornification,进行气-液界面培养,并开始流动,培养6-9天,得到3d皮肤模型。
8、在所述的技术方案基础之上再做进一步的改进的是,还包括
9、s5.在所述s4的气-液界面培养进行4-6天后,继续进行气-液界面培养,并将所述芯片中的cornification吸去,用pbs润洗1次,在第二培养室和第三培养室中加满即用型基质胶,在37℃孵育0.5-2h;
10、s6.先吸去步骤s5中的即用型基质胶,在第二培养室中加入血管内皮细胞悬液,在第三培养室中加入肝细胞悬液,控制血管内皮细胞和肝细胞在培养室的终密度为500-5000个/mm2,将芯片倒置,37℃孵育0.5-2h;然后将芯片中的血管内皮细胞悬液和肝细胞悬液吸去,用pbs润洗1次,在第二培养室中加入血管内皮细胞悬液,在第三培养室中加入10% fbsdmem培养液,37℃孵育0.5-2h;接着将芯片中的血管内皮细胞悬液吸去,用pbs润洗1次,在芯片的各腔室中加入10% fbs dmem培养液,37℃孵育过夜。
11、s7.在步骤s6中过夜的第二天,将芯片中的10% fbs dmem培养液吸去,替换为cornification,并开始流动,保持时间为1天。
12、s8.细胞生长完成,芯片可用于暴露试验。
13、在所述的技术方案基础之上再做进一步的改进的是,所述角质细胞、成纤维细胞、肝细胞和血管内皮细胞包括人原代细胞、细胞系、干细胞分化所得细胞中任意一种。
14、在所述的技术方案基础之上再做进一步的改进的是,在步骤s1中,所述成纤维细胞胶原混合物的配制方法如下:按顺序将10×dmem,1m naoh,dh2o,高浓度鼠尾ⅰ型胶原,胎牛血清和成纤维细胞混合均匀并置于冰上,得到成纤维细胞胶原混合物。
15、在所述的技术方案基础之上再做进一步的改进的是,在步骤s5中,所述3d皮肤模型的浸没过程中,所述芯片中流动培养液产生的液体交换刚好浸没3d皮肤模型的边缘,保证了胶原湿润、成纤维细胞浸没培养,胶原表面的角质细胞接触到空气继续分化。
16、在所述的技术方案基础之上再做进一步的改进的是,在步骤s5中,所述3d皮肤模型的检测通过石蜡切片he染色表明3d皮肤可分化形成具有明显角质层的皮肤样结构。
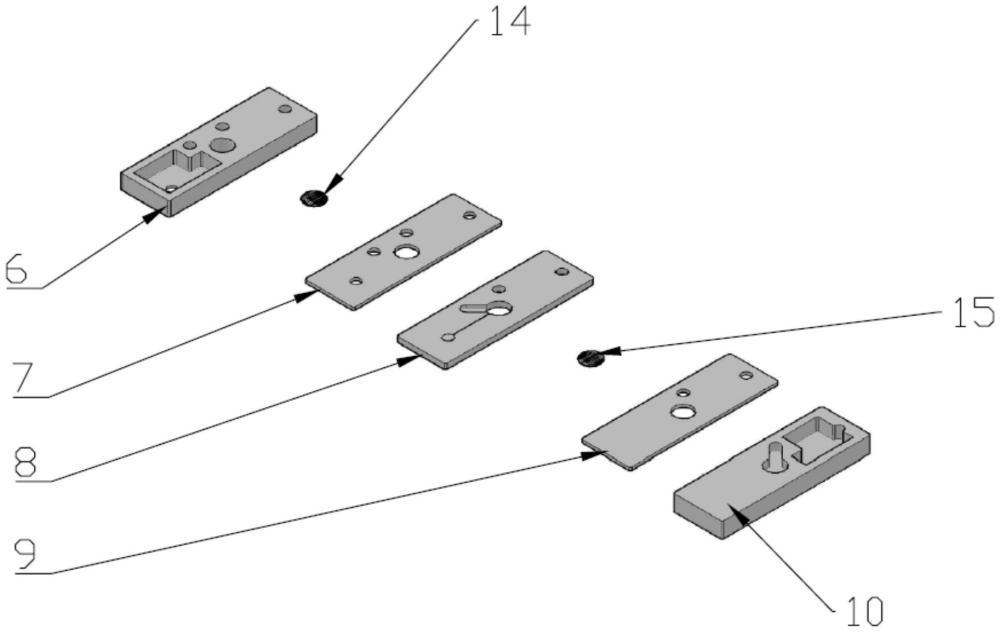
17、在所述的技术方案基础之上再做进一步的改进的是,所述芯片包括培养室、储液室和微流通路,所述储液室包括第一储液室和第二储液室,所述微流通路包括第一微流通路和第二微流通路。
18、所述培养室设置于所述芯片的中部,所述培养室的一侧设有流体流入的第一微流通路,所述第一微流通路连通所述第一储液室,所述培养室的另一侧设有流体流出的第二微流通路,所述第二微流通路连通所述第二储液室。
19、所述第一储液室和第二储液室在竖直方向上形成有高度差。
20、在所述的技术方案基础之上再做进一步的改进的是,所述流体在重力作用下从所述第一储液室流出,先通过所述第一微流通路流向所述培养室,再通过所述第二微流通路流向所述第二储液室;当所述第二储液室快满时,将流体吸出并重新加入所述第一储液室进行流动循环。
21、在所述的技术方案基础之上再做进一步的改进的是,所述培养室按上、中和下排列,所述培养室包括第一培养室、第二培养室和第三培养室,所述培养室内设有多孔滤膜,所述多孔滤膜包括第一多孔滤膜和第二多孔滤膜,所述第一培养室与第二培养室之间设有第一多孔滤膜,所述第二培养室与第三培养室之间设有第二多孔滤膜,在流动过程中,所述流体通过所述多孔滤膜进行物质交换。
22、在所述的技术方案基础之上再做进一步的改进的是,所述多孔滤膜的材料包括硅基膜、纤维素基膜、合成聚合物膜、壳聚糖基膜或合成膜。
23、由于采用上述技术方案,具有以下有益效果:
24、本发明通过提供成纤维细胞和角质细胞分化成3d皮肤模型及血管内皮细胞和肝细胞的培养方法,本发明的芯片具备3层培养室结构,并采用重力驱动,结构简单,无任何辅助设备。本发明的方法包括在芯片中由成纤维细胞和角质细胞分化成的3d皮肤模型,及芯片中的血管内皮细胞和肝细胞的培养。
25、本发明的芯片培养的3d皮肤模型、血管内皮细胞和肝细胞,可同时模拟复杂的三维组织结构和细胞微环境的多功能人源化组织。以此可以实现对体外皮肤组织的制备与评价研究,从而进一步促进皮肤相关疾病发生机制的阐明以及治疗策略的选择。
26、本发明的芯片培养的3d皮肤模型、血管内皮细胞和肝细胞,本发明的方法可模拟外源化学品经皮暴露代谢后入血,再至肝产生毒性的体内暴露过程,无论从种属相似性、3r原则或暴露水平上都表明本芯片在评估外源化学品毒性,特别是经皮代谢后具有肝毒性的外源化学品方面比动物模型更有优势。因此,本发明可以为生物医学工程等领域提供新的思路和方法。
27、本发明的芯片培养的3d皮肤模型、血管内皮细胞和肝细胞可与其他器官联合,将几种不同毒理学靶器官的试验结合起来,构建一个能完全模拟体内环境的用于毒理学评价的皮肤芯片,并达到令人满意的预测性,在研究细胞相互作用的基础上,对各种化学品进行高通量和低成本的快速筛选。与单一的角质细胞模型相比,3d皮肤模型与人皮肤更相似,在角质细胞层下方增加一层含成纤维细胞的胶原层,相当于模拟了“真皮层”,它会增加角质细胞对毒物的抵抗力。3d皮肤模型还适用于外源化学品代谢研究,因为三维组织结构增加了角质细胞中生物转化酶的代谢能力。除代谢研究外,由于3d皮肤模型比角质细胞模型增加了屏障功能,因此也被用于局部暴露物质的皮肤渗透研究。
- 还没有人留言评论。精彩留言会获得点赞!