表达CRISPR/Cas9基因编辑系统的重组痘苗病毒及应用
本发明涉及生物,尤其涉及一种在靶细胞内递送并表达crispr/cas9基因编辑系统的重组痘苗病毒及应用。
背景技术:
1、成簇规律间隔短回文重复序列(clustered regularly interspaced shortpalindromic repeats,crispr),是细菌中发现的特殊dna序列,它与细菌的天然免疫防御有关。近年,基于crispr原理,将相关元件及蛋白酶加以基因工程改造,创造出方便且强效的基因编辑工具,其中应用最广的是crispr/cas9系统,为修饰庞大的基因组序列这一此前操作极为困难的工作提供了颠覆性工具。
2、要使crispr/cas9系统发挥基因编辑作用,首先需将crispr/cas9系统的相关元件cas9蛋白酶基因和grna(即指导rna,系通过碱基互补决定被剪切的靶序列)特异性递送进靶细胞并表达,递送的方式及其效率成为制约基因编辑效率甚至成败的关键和“瓶颈”。
3、递送crispr/cas9系统的方式包括非病毒载体和病毒载体两类,前者包括脂质体转染法、电穿孔法及显微注射法等,后者迄今用到腺相关病毒(aav)载体、腺病毒(adv)载体、慢病毒(lv)载体及噬菌体等。
4、一般而言,非病毒载体递送方式中脂质体转染法操作简单,但递送效率相对较低且变异大,而电穿孔法及显微注射法精准高效,但涉及昂贵的仪器且需训练有素的专业人员操作。所有的非病毒载体递送方式都不适用于大规模样本处理,且往往不适用于活体内递送。相对而言,病毒载体递送效率很高,可适用于活体递送,但病毒载体本身可激发宿主的免疫反应,且病毒载体递送倾向于持久过强表达crispr/cas9,可导致增强的脱靶效应。
5、各病毒载体各有其优缺点。例如,aav载体是最常用的递送crispr/cas9的病毒载体,它递送效率高而基因组整合风险低,但aav载体容量太小(仅4.7kb),通常需要两个甚至三个aav载体联合应用,才能完成整个crispr/cas9系统的递送。adv载体递送效率也很高,但它有较强的免疫原性。lv载体免疫原性很低,但它有整合进宿主基因组潜在致癌风险。
6、痘苗病毒(vaccinia virus)是迄今发现的最大、最复杂的病毒之一,它是预防天花的活疫苗病毒。经过多年大规模人群接种,证明痘苗病毒具有良好的生物安全记录。天花在全球根除后,痘苗病毒作为基因工程表达载体得到深入研究和广泛应用。基于该病毒以下特点,其在基因治疗领域得到越来越广泛的应用:
7、1.安全:痘苗病毒是唯一能在胞浆内复制的dna病毒,它不会整合进宿主细胞基因组,无致癌性等安全问题;
8、2.表达效率高:痘苗病毒可培养到很高滴度(>109pfu/ml),通常感染1-3小时,无需任何药物抗性筛选,可使90%以上的受感染细胞表达目的基因产物;
9、3.感染细胞范围广泛:可感染几乎所有类型的哺乳动物细胞;
10、4.对分裂和非分裂细胞均能感染/转导;
11、5.基因组容量大:至少可插入25kb的外源基因而不影响其遗传稳定性;
12、6.天然的肿瘤靶向性:在注射体内后,绝大多数痘苗病毒将聚集在肿瘤部位。
技术实现思路
1、本发明的目的在于针对现有技术的不足,提供一种递送和表达crispr/cas9基因编辑系统的重组痘苗病毒及应用。
2、为了达到上述目的,本发明采用以下技术方案实现:一种表达crispr/cas9基因编辑系统的重组痘苗病毒,作为验证本发明原理可行性的模型,剪切mcherry红荧光蛋白标志基因的crispr/cas9元件表达盒被插入痘苗病毒tk基因区,由人工合成的痘苗病毒早/晚期启动子(p-se/l)驱动cas9基因表达;由痘苗病毒修饰的h5启动子(mh5)驱动grna表达。所述重组痘苗病毒是基于重组痘苗病毒表达质粒pcb-cas9-dmcz转染vero细胞后,用野型痘苗病毒wr株感染vero细胞,通过细胞内同源重组机制而构建的。
3、进一步地,所述重组痘苗载体表达质粒pcb-cas9-dmcz的核酸全序列如seq idno.1所示。
4、进一步地,重组痘苗病毒的母体病毒是痘苗病毒wr株。
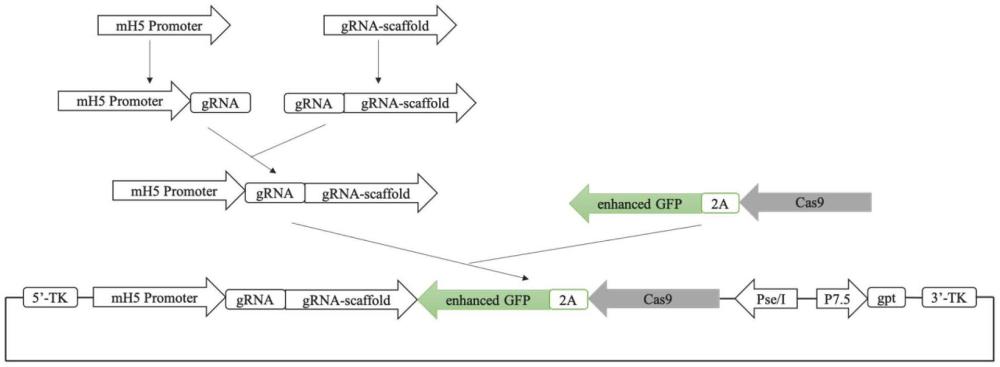
5、进一步地,所述重组痘苗表达质粒pcb-cas9-dmcz的结构包含cas9基因及其上游的人工合成的痘苗病毒早/晚期启动子p-se/l、grna及其上游的痘苗病毒修饰的h5启动子mh5、与目的基因表达盒串联的可选择标志基因表达盒;所述p-se/l驱动cas9基因表达,所述mh5驱动grna表达;其中,所述grna为指导剪切mcherry红荧光蛋白标志基因的rna,所述可选择标志基因为egfp基因和gpt抗性基因,所述目的基因为cas9基因及grna。
6、进一步地,所述cas9基因的核酸序列如seq id no.3所示,所述p-se/l的核酸序列如seq id no.4所示,所述grna的核酸序列如seq id no.2所示,所述mh5的核酸序列如seqidno.5所示。
7、进一步地,所述可选择标志基因包括增强型绿荧光蛋白(egfp)基因与gpt药物抗性基因。
8、进一步地,所述可选择标志基因gpt药物抗性基因的核酸序列如seq id no.6所示;可选择标志基因egfp的核酸序列如seq id no.7所示。
9、进一步地,所述egfp基因通过2a肽与cas9基因融合,所述gpt药物抗性基因由痘苗病毒p7.5早/晚期启动子(p7.5)驱动表达。
10、进一步地,所述cas9基因编码蛋白的氨基酸序列如seq id no.8所示;可选择标志基因egfp编码蛋白的氨基酸序列如seq id no.9所示;可选择标志基因gpt药物抗性基因编码蛋白的氨基酸序列如seq id no.10所示。
11、本发明还提供一种上述任一重组痘苗病毒在靶向细胞递送并表达crispr/cas9系统及在靶细胞内基因编辑任一内源或外源目的基因中的应用。
12、其中,所述“基因编辑”一词的含义包括但不限于:通过重组痘苗病毒载体向肿瘤等靶细胞递送并表达crispr/cas9相关元件,导致靶细胞内的内源性基因或外源性基因(如标志基因)发生剪切、失活、插入或突变等基因改变的效应。
13、本发明的有益效果是:本发明首先构建重组痘苗病毒载体质粒pcb-cas9-dmcz,采用该质粒转染、继而用野型痘苗病毒wr株感染vero细胞,通过细胞内同源重组机制产生重组痘苗病毒,再通过与目的基因表达盒串联的可选择标志基因egfp的表达,基于其表达产物产生的绿荧光表型,和表达药物抗性蛋白产生gpt抗性表型,可方便地筛选出重组痘苗病毒。本发明产生的重组痘苗病毒vv-cas9-dmcz感染细胞后,可有效表达产生grna和cas9蛋白。上述重组痘苗病毒vv-cas9-dmcz在感染稳定表达或瞬时转染mcherry红荧光蛋白的肿瘤细胞模型中,可有效表达crispr/cas9相关元件cas9蛋白和grna序列,并剪切mcherry靶基因序列,导致靶细胞内红荧光减弱的基因编辑效应。
- 还没有人留言评论。精彩留言会获得点赞!