纯化重组带状疱疹蛋白的方法与流程
本发明属于蛋白纯化,尤指纯化重组带状疱疹蛋白的方法。
背景技术:
1、带状疱疹由潜伏在神经元内的水痘-带状疱疹病毒(varicella-zoster virus,vzv)重新激活,表现为成簇集型水泡,通常出现在老年人、儿童免疫力低下或患有慢性皮肤病的人群。vzv由双链dna、核衣壳及其表面包膜附着的糖蛋白组成,其中糖蛋白在侵染细胞并发挥免疫原性的过程中起到重要作用。vzv病理学的一个标志是在皮损中形成多核细胞,这种多核细胞是由糖蛋白gb、gh和gl介导的细胞间融合构成的。糖蛋白e(ge)是最丰富的一类蛋白,具有高度免疫原性,也是研究重组带状疱疹蛋白的重要对象。经基因重组技术改造后的ge蛋白在中国仓鼠卵巢细胞(cho)中表达特异性抗原制成重组亚单位疫苗,刺激机体产生th1型免疫应答,对免疫力低下的人群有很好的保护效果。
2、近些年来,围绕重组带状疱疹蛋白上游工艺及免疫原性的探究层出不穷,但下游纯化工艺尚不成熟。在生物制品生产过程中,宿主细胞系中表达目标蛋白时会产生来自宿主细胞的结构蛋白和分泌蛋白(hcp),刺激人体免疫系统产生不良反应。因此开发纯化工艺时需要检测hcp残留,特别对于重组带状疱疹蛋白,hcp残留往往需要从几十万ppm降低至几百ppm。
3、在目标蛋白上携带标签,采用亲和层析来纯化能够获得较纯的产物,但后续需要切除标签,操作难度大,并且在酶切的过程容易产生难以去除的副产物,往往适用于小批量纯化来探究重组带状疱疹的生物学功能。日益精进的层析介质给纯化方式带来更多的选择,经疏水、离子交换或分子筛等层析方式能够纯化出目标产物。传统的纯化工艺采用阴离子交换层析进行捕获,疏水作用层析进行中度纯化,多模式弱阳离子交换介质进行精细纯化,uf/df换液后使用分子筛来去除痕量杂质。传统工艺所使用的介质中包含分子筛使得纯化成本高、步骤繁琐,操作难度大,亟需探索出新的纯化工艺来进行国产化介质替换并有效去除hcps。
技术实现思路
1、针对以上技术问题,本发明的目的在于提供一种纯化重组带状疱疹蛋白的方法,具有流程短、操作简便且质量稳定的特点,纯化后的蛋白可达质量要求:纯度≥95%及宿主细胞蛋白残留<500ppm。
2、为了实现上述目的,本发明所采用的技术方案如下:
3、技术方案1
4、一种纯化重组带状疱疹蛋白的方法,包括:
5、将重组带状疱疹蛋白的粗分离样品溶液依序经过diamond mix-a、butylbestarose 4ff、diamond mmc mustang和diamond mix-a mustang作为层析介质的纯化步骤。
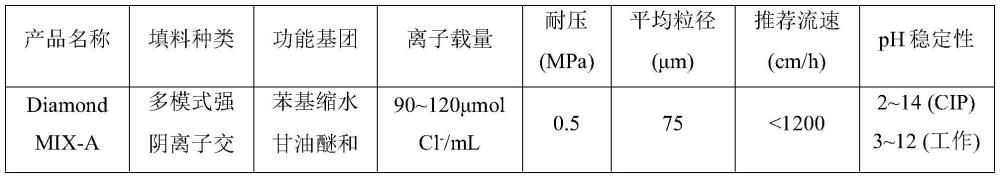
6、上述方案中,diamond mix-a是通过两次交联分别将苯基缩水甘油醚和2,3-环氧丙基三甲基氯化铵两种基团偶联在高刚性琼脂糖微球上形成的一种多模式强阴离子交换介质,该种介质不仅具有离子交换功能,还具有疏水和氢键作用,可以有效地去除聚体、dna、宿主蛋白、内毒素、proteina等杂质。
7、上述方案中,butyl bestarose 4ff是在4%的琼脂糖基架上偶联丁基脂肪链而成的,琼脂糖基架的高物理和化学稳定性,使其具有良好的压力流速性能,成为规模纯化工艺的理想选择,特别是在需要高流速分离过程的捕获或中度纯化阶段,优化后的配基密度适合疏水性较强的生物分子的分离纯化。
8、上述方案中,diamond mmc mustang是将带有苯环和羧基的复合基团偶联在平均颗粒大小为40μm的高刚性琼脂糖微球上形成的一种多模式弱阳离子交换介质,该种介质结合了阳离子交换和疏水作用,适用于生物分子的捕获和纯化。
9、上述方案中,diamond mix-amustang是通过两次交联分别将苯基缩水甘油醚和2,3-环氧丙基三甲基氯化铵两种基团偶联在颗粒较小的高刚性琼脂糖微球上形成的一种多模式强阴离子交换介质,这种介质可以用于生物分子的纯化,特别是在抗体纯化中作为精纯步骤。
10、作为优选方案,所述重组带状疱疹蛋白粗分离样品过0.45μm滤膜后直接进行diamond mix-a多模式强阴离子层析。
11、作为优选方案,将diamond mix-a作为层析介质的纯化步骤1,工艺条件包括:所述重组带状疱疹蛋白的上样量为7~9mg/ml、接触时间为5~7min、上样蛋白浓度为≤1.5mg/ml;使用缓冲液组合1,所述缓冲液组合1包括平衡缓冲液1、清洗缓冲液1及洗脱缓冲液1,具体组成及参数控制为:
12、平衡缓冲液1:15~25mm pb,ph6.5~7.5;
13、清洗缓冲液1:15~25mm pb+0.40~0.60m精氨酸盐酸盐,ph5.5~6.5;
14、洗脱缓冲液1:15~25mm pb+0.60~0.80m精氨酸盐酸盐,ph5.5~6.5。
15、在更换洗脱缓冲液后约1cv,洗脱峰明显上升时开始收集洗脱液约3cv,得到diamond mix-a的洗脱液。
16、作为优选方案,所述diamond mix-a层析的洗脱液用饱和硫酸铵和1mtris分别调节电导和ph与butyl bestarose 4ff的平衡缓冲液保持一致后进行butyl bestarose 4ff疏水作用层析。
17、作为优选方案,将butyl bestarose 4ff作为层析介质的纯化步骤2,工艺条件包括:将调节电导和ph的diamond mix-a层析的洗脱液进行上样,上样量为6~8mg/ml、接触时间为5~7min;使用缓冲液组合2,所述缓冲液组合2包括平衡缓冲液2、清洗缓冲液2及洗脱缓冲液2,具体组成及参数控制为:
18、平衡缓冲液2:15~25mm pb+0.50~0.70m硫酸铵,ph6.0~7.0;
19、清洗缓冲液2:15~25mm pb+0.30~0.40m硫酸铵,ph6.0~7.0;
20、洗脱缓冲液2:15~25mm pb+0.05~0.15m硫酸铵,ph6.0~7.0。
21、在更换洗脱缓冲液后约1cv,洗脱峰明显上升时开始收集洗脱液约3cv,得到butylbestarose 4ff的洗脱液。
22、作为优选方案,所述butyl bestarose 4ff层析的洗脱液用纯水和0.5m柠檬酸分别调节电导和ph与diamond mmc mustang的平衡缓冲液保持一致后进行diamond mmcmustang多模式弱阳离子交换层析。
23、作为优选方案,将diamond mmc mustang作为层析介质的纯化步骤3,工艺条件包括:将调节电导和ph的butyl bestarose 4ff的洗脱液进行上样,上样量为3~4mg/ml、接触时间为5~7min;使用缓冲液组合3,所述缓冲液组合3包括平衡缓冲液3及洗脱缓冲液3,具体组成及参数控制为:
24、平衡缓冲液3:15~25mm pb+0~0.10m氯化钠,ph5.5~6.5;
25、洗脱缓冲液3:15~25mm pb+0~0.10m氯化钠,ph6.5~7.0。
26、在洗脱过程中收集洗脱峰25~25mau/mm,得到diamond mmc mustang的洗脱液。
27、作为优选方案,将diamondmix-amustang作为层析介质的纯化步骤4,工艺条件包括:将diamond mmc mustang的洗脱液直接进行上样,上样量为3~4mg/ml、接触时间为5~7min;使用缓冲液组合4,所述缓冲液组合4包括平衡缓冲液4、清洗缓冲液4及洗脱缓冲液4,具体组成及参数控制为:
28、平衡缓冲液4:15~25mm pb,ph6.5~7.0;
29、清洗缓冲液4:15~25mm柠檬酸+0.30~0.50m精氨酸盐酸盐,ph4.5~5.5;
30、洗脱缓冲液4:15~25mm柠檬酸+0.60~0.70m精氨酸盐酸盐,ph4.5~5.5。
31、在更换洗脱缓冲液后约1cv,洗脱峰明显上升时开始收集洗脱液约3cv,得到纯化后的重组带状疱疹蛋白原液。
32、技术方案2
33、一种纯化重组带状疱疹蛋白的方法,包括:
34、将重组带状疱疹蛋白的粗分离样品溶液依序经过diamond q、diamond mix-amustang、butyl bestarose 4ff和diamond q mustang作为层析介质的纯化步骤。
35、上述方案中,diamond q是将季铵基偶联在高刚性琼脂糖微球上形成的一种强阴离子交换介质,具有较高的耐压性与载量。
36、上述方案中,diamond q mustang是将季铵基偶联在颗粒较细的高刚性琼脂糖微球上形成的一种强阴离子交换介质,分辨率比diamond q高,适合于层析步骤中的精细纯化或者中度纯化阶段。
37、作为优选方案,所述重组带状疱疹蛋白粗分离样品过0.45μm滤膜后直接进行diamond q阴离子层析。
38、作为优选方案,将diamond q作为层析介质的纯化步骤1,工艺条件包括:所述重组带状疱疹蛋白的上样量为7~9mg/ml、接触时间为5~7min、上样蛋白浓度为≤1.5mg/ml;使用缓冲液组合5,所述缓冲液组合5包括平衡缓冲液5、清洗缓冲液5及洗脱缓冲液5,具体组成及参数控制为:
39、平衡缓冲液5:15~25mm pb,ph5.5~6.5;
40、清洗缓冲液5:15~25mm pb+0.20~0.30m氯化钠,ph5.5~6.5;
41、洗脱缓冲液5:15~25mm pb+0.30~0.40m氯化钠,ph5.5~6.5。
42、在更换洗脱缓冲液后约1cv,洗脱峰明显上升时开始收集洗脱液约3cv,得到diamond q的洗脱液。
43、作为优选方案,将diamondmix-amustang作为层析介质的纯化步骤2,工艺条件包括:将diamond q的洗脱液直接进行上样,上样量为6~8mg/ml、接触时间为5~7min;使用缓冲液组合6,所述缓冲液组合6包括平衡缓冲液6、清洗缓冲液6及洗脱缓冲液6,具体组成及参数控制为:
44、平衡缓冲液6:15~25mm pb,ph5.5~6.5;
45、清洗缓冲液6:15~25mm柠檬酸+0.30~0.50m精氨酸盐酸盐,ph4.5~5.5;
46、洗脱缓冲液6:15~25mm柠檬酸+0.60~0.70m精氨酸盐酸盐,ph4.5~5.5。
47、在更换洗脱缓冲液后约1cv,洗脱峰明显上升时开始收集洗脱液约3cv,得到diamond q的洗脱液。
48、作为优选方案,所述diamond mix-amustang层析的洗脱液用饱和硫酸铵和1mtris分别调节电导和ph和butyl bestarose 4ff的平衡缓冲液保持一致后进行butylbestarose 4ff疏水作用层析。
49、作为优选方案,将butyl bestarose 4ff作为层析介质的纯化步骤3,工艺条件包括:将调节电导和ph的diamond mix-amustang层析的洗脱液进行上样,上样量约为3~4mg/ml、接触时间为5~7min;使用缓冲液组合2,具体组成及参数控制见技术方案1。
50、在更换洗脱缓冲液后约1cv,洗脱峰明显上升时开始收集洗脱液约3cv,得到butylbestarose 4ff的洗脱液。
51、作为优选方案,所述butyl bestarose 4ff层析的洗脱液用纯水调节电导为10ms/cm,用0.5m柠檬酸调节ph和diamond q mustang的平衡缓冲液保持一致后进行diamond qmustang阴离子交换层析。
52、作为优选方案,将diamond q mustang作为层析介质的纯化步骤4,工艺条件包括:将调节电导和ph的butyl bestarose 4ff层析的洗脱液进行上样,上样量约为3~4mg/ml、接触时间为5~7min;使用缓冲液组合7,所述缓冲液组合7包括平衡缓冲液7、清洗缓冲液7及洗脱缓冲液7,具体组成及参数控制为:
53、平衡缓冲液7:15~25mm pb,ph5.5~6.5;
54、清洗缓冲液7:15~25mm pb+0.10~0.20m氯化钠,ph5.5~6.5;
55、洗脱缓冲液7:15~25mm pb+0.20~0.40m氯化钠,ph5.5~6.5。
56、在更换洗脱缓冲液后约1cv,洗脱峰明显上升时开始收集洗脱液约2cv,得到纯化后的重组带状疱疹蛋白原液。
57、技术方案3
58、一种纯化重组带状疱疹蛋白的方法,包括:
59、将重组带状疱疹蛋白的粗分离样品溶液依序经过diamond q、diamond mix-amustang、butyl bestarose 4ff和diamond mmc mustang作为层析介质的纯化步骤。
60、作为优选方案,纯化步骤1、2和3及其工艺条件和技术方案2中的纯化步骤1、2和3及其工艺条件一致。
61、作为优选方案,将diamond mmc mustang作为层析介质的纯化步骤4,工艺条件包括:将调节电导和ph的butyl bestarose 4ff层析的洗脱液进行上样,上样量为3~4mg/ml、接触时间为5~7min;使用缓冲液组合3,具体组成及参数控制见技术方案1。
62、在洗脱过程中收集洗脱峰25~25mau/mm,得到纯化后的重组带状疱疹蛋白原液。
63、作为优选方案,各纯化步骤中,保持样品、溶液和环境温度均在22~24℃之间。
64、所述重组带状疱疹蛋白的无糖基化修饰的分子量为57kda,有糖基化修饰的分子量为60~75kda,两种形式的蛋白均为纯化的目标产物;表达量为0.5~1.5g/l,等电点为5.2,消光系数为1.59。
65、本发明采用以上技术方案至少具有如下的有益效果:
66、1.对于本发明所纯化的重组带状疱疹蛋白,多模式强阴离子交换介质diamondmix-a和diamond mix-a mustang、多模式弱阳离子交换介质diamond mmc mustang、强阴离子交换介质diamond q和diamond qmustang以及疏水作用介质butyl bestarose 4ff能够协同去除hcp和杂质,其中diamond q和butyl bestarose 4ff效果显著;
67、2.本发明提供三套优选方案纯化重组带状疱疹蛋白。粗分离样品经diamond mix-a、butyl bestarose 4ff、diamond mmc mustang和diamond mix-amustang纯化的样品纯度>98%,hcp残留降低至300ppm左右;粗分离样品经diamond q、diamond mix-a mustang、butyl bestarose 4ff和diamond q mustang纯化的样品纯度约97%,hcp残留降低至350ppm左右;粗分离样品经diamond q、diamond mix-amustang、butyl bestarose 4ff和diamond mmc mustang纯化的样品纯度约98%,hcp残留降低至200ppm以下。本发明提供的纯化重组带状疱疹蛋白的方法不包括分子筛,具有流程短、操作简便且质量稳定的特点,纯化后的蛋白可达质量要求:纯度≥95%及宿主细胞蛋白残留<500ppm;不同类型的带状疱疹,种类不同,质量要求不同,因此,层析介质的属性要求也会存在差异。
- 还没有人留言评论。精彩留言会获得点赞!