快速检测实体肿瘤相关基因突变的引物组和方法与流程
本发明属于分子生物学,具体是涉及快速检测实体肿瘤相关基因突变的引物组和方法。
背景技术:
1、随着肿瘤研究的不断深入和肿瘤药物研发越来越“基因化”,肿瘤治疗已经进入个体化治疗时代。在肿瘤个体化治疗之前,肿瘤患者需要接受系列的基因检测,根据患者的基因特点,采用不同的药物和治疗方案,实施个体化治疗。肿瘤手术组织是我们能获得的第一类肿瘤样本,对手术样本的基因靶标检测,有助于术后治疗方案的确定。肿瘤在生长过程中,经过多次分裂增殖,其子细胞呈现出分子生物学或基因方面的改变,从而使肿瘤的生长速度、侵袭能力、对药物的敏感性、预后等各方面产生差异,由于肿瘤异质性广泛存在,对肿瘤内的多个部位在多个时间点进行检测,就有可能鉴定出突变导致的肿瘤异质性,从而为个体化治疗提供重要线索。与传统的组织活检相比,液体活检有着快速、便捷、无创等众多优势,液体活检技术作为常规组织活检的有效补充,并将其用于检测靶点、监测肿瘤治疗反应、预测肿瘤复发等。
2、研究证实,越来越多的基因变异与各种形式的癌症有关联,也有越来越多的靶向药物被证实对某种类型的癌症有治疗效果。以晚期nsclc为例,目前临床常用的靶向治疗药物易瑞沙、特罗凯、凯美纳等均是表皮生长因子受体(epidermal growth factorreceptor,egfr)酪氨酸激酶抑制剂(tyrosine kinase inhibitors,tkis)。研究显示,当nsclc患者egfr基因发生19号外显子缺失、21号外显子l858r、l861q突变和18号外显子g719x突变时,对tkis靶向治疗敏感,但当20号外显子770-775位发生插入突变后,提示发生tkis耐药。kras是egfr下游的靶分子,egfr生长信号需经kras蛋白传递,携带kras基因突变的患者tkis治疗无效。因此tkis治疗前必须对kras基因进行检测,因此,临床上检测这些通路中特定基因的扩增/突变/表达情况,能针对性地为每位患者“量身定做一套最适合的治疗方案,从而最大程度地提高治疗的有效率,减少药物的毒副作用,避免用药不当贻误治疗时机。通过检测肿瘤相关的基因热点区域信息,可以反映肿瘤的发生发展,同时分析这些基因的突变特征,根据患者的个体差异性,结合药物基因组学相关信息,辅助临床医生为癌症患者选择合适的治疗药物,制定完善的治疗方案,有利于实现“因人因时”的肿瘤个体化治疗。
3、肿瘤患者突变主要包括单个核苷酸变异(snv,single nucleotide varients)、小片段插入缺失(1ndel,insertion-deletion)、拷贝数变异(cnv,copy numbervariations)、dna融合(fusion)等;实时荧光定量pcr、一代测序、基因芯片方法等传统检测方法一次只能检测个别及部分位点,不能检测出未知突变。因此,提供一种能快速准确地检测多个肿瘤相关基因多个位点突变的产品和方法对于实现“因人因时”的肿瘤个体化治疗非常重要。
技术实现思路
1、基于此,本发明的目的是提供快速检测实体肿瘤相关基因突变的引物组,所述引物组可快速准确地扩增出所述实体肿瘤相关基因的特异性核酸序列,再经过文库构建和测序,实现相关基因突变的检测。
2、本发明的第一个方面,是提供一种检测实体肿瘤相关基因突变的引物组,所述引物组包括针对13个相关基因40个区域内突变中的至少两个基因的引物对,所述引物对选自如下:
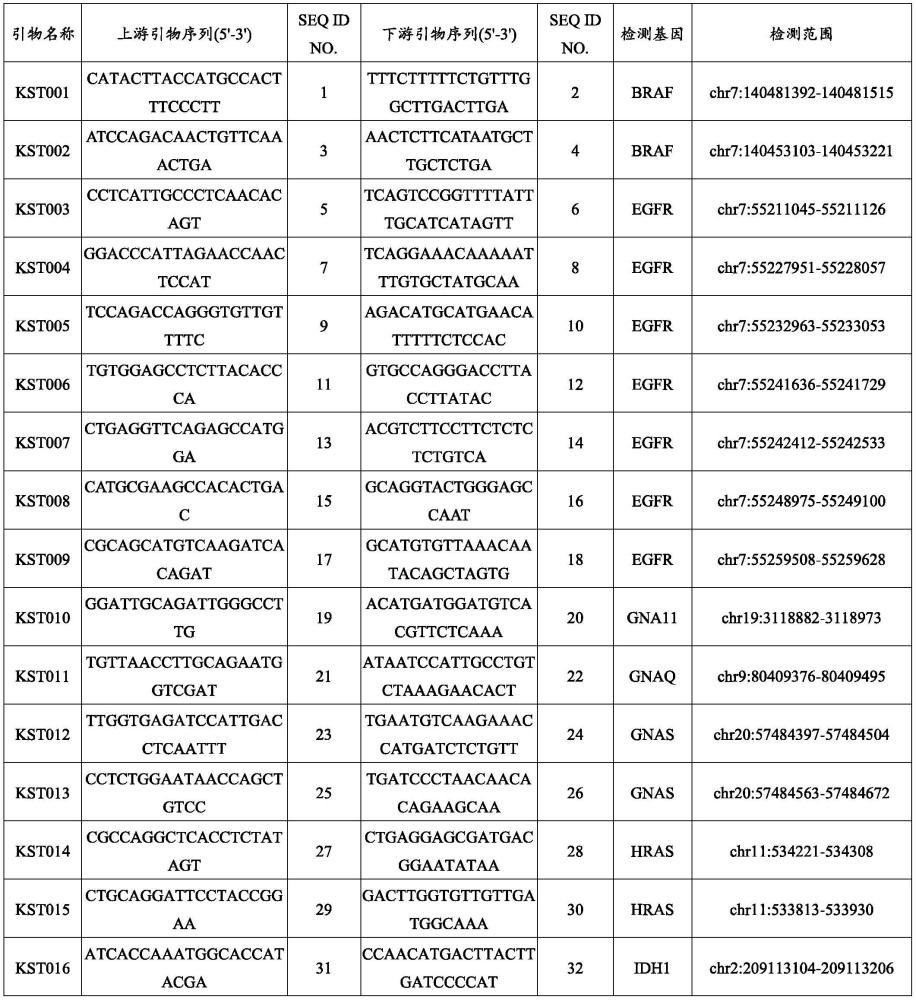
3、检测braf基因突变的引物对,所述引物对选自:序列如seq id no.1所示的上游引物和序列如seq id no.2所示的下游引物;序列如seq id no.3所示的上游引物和序列如seq id no.4所示的下游引物;
4、检测egfr基因突变的引物对,所述引物对选自:序列如seq id no.5所示的上游引物和序列如seq id no.6所示的下游引物;序列如seq id no.7所示的上游引物和序列如seq id no.8所示的下游引物;序列如seq id no.9所示的上游引物和序列如seq id no.10所示的下游引物;序列如seq id no.11所示的上游引物和序列如seq id no.12所示的下游引物;序列如seq id no.13所示的上游引物和序列如seq id no.14所示的下游引物;序列如seq id no.15所示的上游引物和序列如seq id no.16所示的下游引物;序列如seq idno.17所示的上游引物和序列如seq id no.18所示的下游引物;
5、检测gna11基因突变的引物对,所述引物对包括:序列如seq id no.19所示的上游引物和序列如seq id no.20所示的下游引物;
6、检测gnaq基因突变的引物对,所述引物对包括:序列如seq id no.21所示的上游引物和序列如seq id no.22所示的下游引物:
7、检测gnas基因突变的引物对,所述引物对选自:序列如seq id no.23所示的上游引物和序列如seq id no.24所示的下游引物;序列如seq id no.25所示的上游引物和序列如seq id no.26所示的下游引物;
8、检测hras基因突变的引物对,所述引物对选自:序列如seq id no.27所示的上游引物和序列如seq id no.28所示的下游引物;序列如seq id no.29所示的上游引物和序列如seq id no.30所示的下游引物;
9、检测idh1基因突变的引物对,所述引物对包括:序列如seq id no.31所示的上游引物和序列如seq id no.32所示的下游引物;
10、检测idh2基因突变的引物对,所述引物对包括:序列如seq id no.33所示的上游引物和序列如seq id no.34所示的下游引物;
11、检测kras基因突变的引物对,所述引物对选自:序列如seq id no.35所示的上游引物和序列如seq id no.36所示的下游引物;序列如seq id no.37所示的上游引物和序列如seq id no.38所示的下游引物;序列如seq id no.39所示的上游引物和序列如seq idno.40所示的下游引物;
12、检测nras基因突变的引物对,所述引物对选自:序列如seq id no.41所示的上游引物和序列如seq id no.42所示的下游引物;序列如seq id no.43所示的上游引物和序列如seq id no.44所示的下游引物;序列如seq id no.45所示的上游引物和序列如seq idno.46所示的下游引物;
13、检测pik3ca基因突变的引物对,所述引物对选自:序列如seq id no.47所示的上游引物和序列如seq id no.48所示的下游引物;序列如seq id no.49所示的上游引物和序列如seq id no.50所示的下游引物;序列如seq id no.51所示的上游引物和序列如seq idno.52所示的下游引物;序列如seq id no.53所示的上游引物和序列如seq id no.54所示的下游引物;序列如seq id no.55所示的上游引物和序列如seq id no.56所示的下游引物;序列如seq id no.57所示的上游引物和序列如seq id no.58所示的下游引物;序列如seq id no.59所示的上游引物和序列如seq id no.60所示的下游引物;序列如seq idno.61所示的上游引物和序列如seq id no.62所示的下游引物;序列如seq id no.63所示的上游引物和序列如seq id no.64所示的下游引物;序列如seq id no.65所示的上游引物和序列如seq id no.66所示的下游引物;序列如seq id no.67所示的上游引物和序列如seq id no.68所示的下游引物;
14、检测tert基因突变的引物对,所述引物对选自:序列如seq id no.69所示的上游引物和序列如seq id no.70所示的下游引物;序列如seq id no.71所示的上游引物和序列如seq id no.72所示的下游引物;序列如seq id no.73所示的上游引物和序列如seq idno.74所示的下游引物;
15、检测erbb2基因突变的引物对,所述引物对选自:序列如seq id no.75所示的上游引物和序列如seq id no.76所示的下游引物;序列如seq id no.77所示的上游引物和序列如seq id no.78所示的下游引物;序列如seq id no.79所示的上游引物和序列如seq idno.80所示的下游引物。
16、在其中一些实施例中,所述引物组包括针对nras、pik3ca基因的引物对。
17、在其中一些实施例中,所述引物组还包括针对braf、egfr、kras、gna11、gnaq、gnas、hras、idh1、idh2、tert、erbb2基因的引物对中的至少一种。
18、在其中一些实施例中,所述引物组包括针对braf、egfr、gna11、gnaq、gnas、hras、idh1、idh2、kras、nras、pik3ca、tert、erbb2基因的引物对。
19、本发明的第二个方面,是提供如上所述的引物组在制备检测实体肿瘤相关基因突变的产品中的应用。
20、在其中一些实施例中,所述产品为试剂盒。
21、本发明的第三个方面,是提供一种检测实体肿瘤相关基因突变的试剂盒,所述试剂盒包含如上所述的引物组。
22、本发明的第四个方面,是提供一种检测实体肿瘤相关基因突变的方法,所述方法包括以下步骤:以待测样本的dna为模板,使用如上所述的引物组或如上所述的试剂盒进行多重pcr扩增,构建文库,测序。
23、在其中一些实施例中,所述多重pcr扩增包括第一轮pcr扩增和第二轮pcr扩增;
24、所述第一轮pcr扩增的反应体系包含以下组分:multiplex pcr master mix、dmso、所述引物对混合物和dna模板;
25、所述第二轮pcr扩增的反应体系包含以下组分:multiplex pcr master mix、所述第一轮pcr扩增的产物、接头。
26、在其中一些实施例中,所述引物对seq id no.1~2、seq id no.25~26、seq idno.53~54、seq id no.77~78、seq id no.79~80在所述第一轮pcr扩增的反应体系中的浓度各为0.035um;
27、所述引物对seq id no.3~4、seq id no.17~18、seq id no.35~36、seq idno.39~40、seq id no.47~48、seq id no.63~64在所述第一轮pcr扩增的反应体系中的浓度各为0.06um;
28、所述引物对seq id no.5~6、seq id no.7~8、seq id no.9~10、seq id no.15~16、seq id no.19~20、seq id no.41~42、seq id no.55~56、seq id no.57~58在所述第一轮pcr扩增的反应体系中的浓度各为0.05um;
29、所述引物对seq id no.11~12、seq id no.29~30、seq id no.45~46、seq idno.49~50、seq id no.51~52、seq id no.59~60在所述第一轮pcr扩增的反应体系中的浓度各为0.045um;
30、所述引物对seq id no.13~14、seq id no.21~22、seq id no.33~34、seq idno.37~38、seq id no.67~68在所述第一轮pcr扩增的反应体系中的浓度各为0.04um;
31、所述引物对seq id no.23~24在所述第一轮pcr扩增的反应体系中的浓度各为0.055um;
32、所述引物对seq id no.27~28在所述第一轮pcr扩增的反应体系中的浓度各为0.075um;
33、所述引物对seq id no.31~32、seq id no.61~62、seq id no.65~66在所述第一轮pcr扩增的反应体系中的浓度各为0.03um:
34、所述引物对seq id no.43~44、seq id no.69~70、seq id no.71~72、seq idno.73~74在所述第一轮pcr扩增的反应体系中的浓度各为0.065um;
35、所述引物对seq id no.75~76在所述第一轮pcr扩增的反应体系中的浓度各为0.02um。
36、在其中一些实施例中,所述第一轮pcr扩增的反应程序为:1)95℃,5min;2)95℃,10s;60℃,30s;72℃,15s;20个循环;3)72℃,1min;
37、所述第二轮pcr扩增的反应程序为:1)95℃,10min;2)95℃,30s;65℃,90s;10个循环。
38、在其中一些实施例中,所述dna包括gdna和/或ctdna。
39、在其中一些实施例中,所述构建文库的方法为扩增子捕获法。
40、在其中一些实施例中,所述测序基于illumina测序平台。
41、本发明经过大量的研究和筛选获得了一种针对实体肿瘤13个相关基因突变检测的引物组,这些引物可以单独扩增,更可在同一pcr反应体系和反应程序下对待测dna模板进行高效的扩增,一次多重pcr扩增即可快速准确地扩增出所述实体肿瘤13个相关基因40个区域的特异性核酸序列。将扩增产物连上接头构建文库,然后进行测序,即可实现所述实体肿瘤13个相关基因40个区域内突变的检测,辅助临床医生为癌症患者选择合适的治疗药物,制定完善的治疗方案,实现“因人因时”的肿瘤个体化治疗。
42、本发明通过对多重pcr扩增条件的反复探索和优化,包括引物组中每条引物在扩增体系中的浓度和扩增程序等,建立了针对所述引物组的合适的多重pcr扩增条件,可高效、准确地实现每个相关基因检测区域的扩增,从而保证后续测序的深度均一性、准确性和灵敏度。
43、本发明检测方法快速简便,可实现自动化检测,从dna提取到结果报告发放仅需3天。并且通量高,成本低,适用于实体肿瘤的相关基因筛查,应用前景广阔。
- 还没有人留言评论。精彩留言会获得点赞!