识别人MSLN蛋白的单克隆抗体及其制备方法与应用与流程
本发明涉及一种识别人msln蛋白的单克隆抗体及其制备方法与应用,属于单克隆抗体。
背景技术:
1、间皮素(mesothelin,msln)最初发现是一个能被单克隆抗体k1特异性识别的抗原,从与k1发生反应的hela细胞系基因文库中提取cdna并克隆出了msln基因,由于该基因编码生成的膜结合蛋白主要位于正常间皮细胞表面,故命名为间皮素。间皮素基因位于染色体16p13,间皮素基因msln包含17个外显子,cdna长约2138bp,含有1884bp的开放阅读框,编码628个氨基酸的前体蛋白(69kda)。该前体蛋白可被弗林(furin)蛋白酶水解为两个部分:40kda大小片段的间皮素和31kda大小的分泌片段,称为巨核细胞增强因子(megakaryocyte-potentiating factor,mpf)。msln是40kda的膜结合蛋白,通过糖基化磷脂酰肌醇锚定于细胞膜,其细胞外结构域由区域ⅰ(n末端区域,残基296~390),区域ⅱ(残基391~486)和区域ⅲ(c末端区域,残基487~598)组成。目前关于msln的生物学功能尚不完全清楚,但是近年来发现msln作为一种肿瘤分化抗原,在恶性间皮瘤、肺癌、食管癌、胰腺癌、宫颈癌以及卵巢癌等恶性肿瘤中呈过度表达,其中msln蛋白在85%至90%的间皮瘤,80%至85%的胰腺癌和60%至65%的肺癌,卵巢癌和胆管癌中有表达,而在正常组织中几乎不表达(仅少量表达在腹膜、心包膜等位置),使其成为靶向疗法中的优秀靶点。
2、目前以msln为靶点的靶向药物研发有多种,包括癌症疫苗、adc药物、car-t/nk细胞疗法、单抗药物等,总体来看抗体相关类药物居多。市面所用抗体多数靶向msln胞外区域ⅰ(n末端区域,残基296~390)和区域ⅲ(c末端区域,残基487~598)。
技术实现思路
1、针对上述现有技术,本发明提供了一种针对人msln蛋白的单克隆抗体,此抗体靶向msln胞外区域(非胞外区域ⅰ和区域ⅲ),特异性良好,可用于靶向抗体类药物或者用于生物检测类实验。
2、本发明是通过以下技术方案实现的:
3、识别人msln蛋白的单克隆抗体的制备方法,包括以下步骤:
4、(1)免疫:利用义翘神州商品化产品13128-h08h1(296aa~580aa)作为免疫原免疫小鼠;
5、(2)检测:于三次免疫后一周取血,利用包被免疫原13128-h08h1(296aa~580aa)进行血清效价elisa检测,以及利用ovcar-3细胞进行流式检测;
6、(3)杂交瘤细胞的获得:选取检测结果最优的1只小鼠进行杂交瘤融合筛选及有限稀释,取免疫后小鼠脾细胞,按1:1比例与sp2/0骨髓瘤细胞混合,利用电融合法进行融合,获得杂交瘤细胞;
7、(4)单克隆抗体的制备和纯化:培养杂交瘤细胞,进行纯化,得识别人msln蛋白的单克隆抗体。
8、进一步地,所述步骤(1)的具体操作方式为:首次免疫将免疫原与等体积的完全弗氏佐剂制成乳化剂,腹部皮下多点注射;间隔2周后,取相同剂量免疫原与等体积不完全弗氏佐剂制成乳化剂,腹部皮下多点注射;再次间隔2周后,取相同剂量免疫原与等体积不完全弗氏佐剂制成乳化剂,腹部皮下多点注射;每只小鼠单次免疫剂量50μg。
9、进一步地,所述步骤(2)中,以小鼠血清1:8000倍稀释时od450-blank大于0.8为效价合格标准,elisa检测的步骤如下:
10、(1)包被:取适量合成蛋白msln(296aa~580aa)、抗原区域ⅰ(296aa~390aa)和抗原区域ⅲ(487aa~605aa),用包被缓冲液溶解并稀释成5μg/ml,然后用移液器在96孔板每孔中加入100μl,轻拍板子使样品混匀,用保鲜膜封严,4℃下包被过夜;
11、(2)洗板:用洗涤液按300μl/孔洗板1次,扣干酶标板;
12、(3)封闭:用封闭液按300μl/孔封闭酶标板,室温下封闭1h;
13、(4)洗板:用洗涤液按300μl/孔洗板2次,扣干酶标板;
14、(5)加样:将经过梯度稀释的血清样品及样品稀释剂以100μl/孔加样;
15、(6)加二抗:加入检测抗体,以100μl/孔加至96孔板内,室温下共同孵育2h;
16、(7)洗板:用洗涤液按300μl/孔洗板5次,扣干酶标板;
17、(8)显色:以200μl/孔加入显色液室温放置12min;
18、(9)终止与检测:以50μl/孔加入终止液终止反应,而后用酶标仪进行检测,测定波长为450nm。
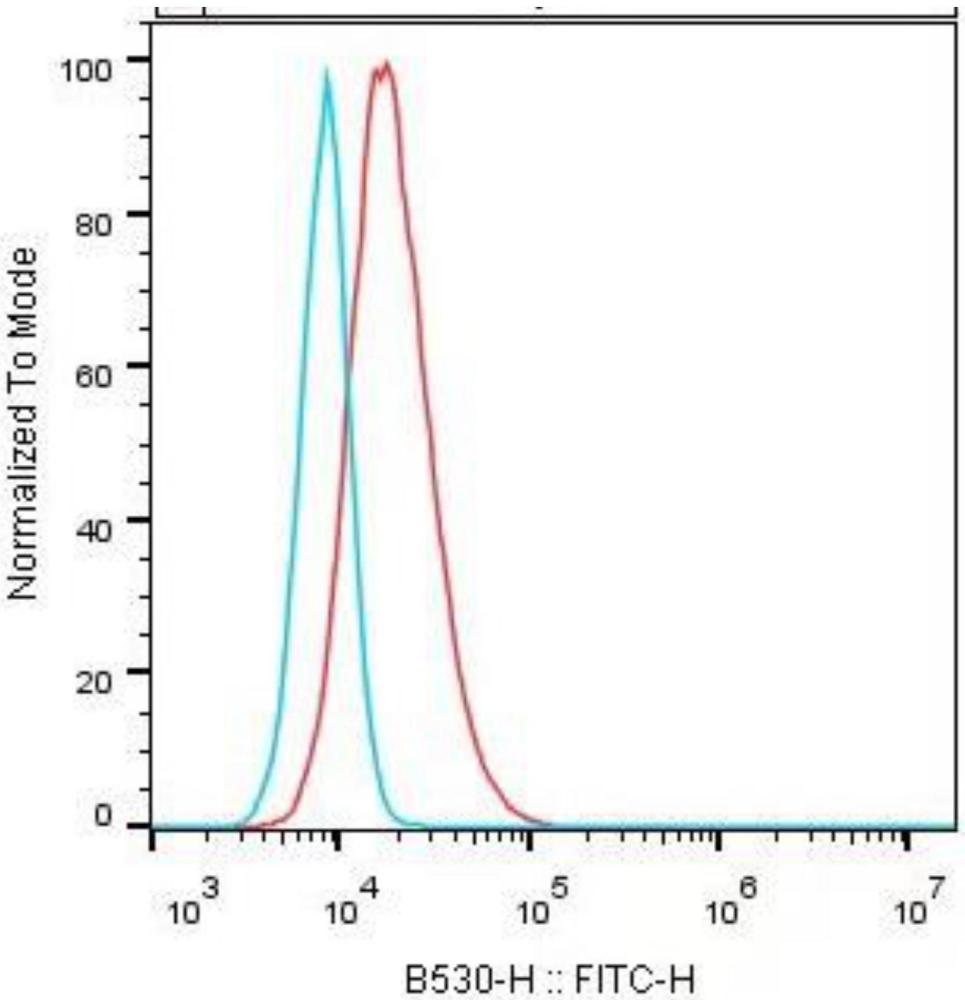
19、进一步地,所述步骤(2)中,流式检测的步骤如下:
20、(1)细胞重悬:细胞离心弃上清,加入洗液,重悬,400目滤网过滤,离心洗细胞1次,加入适量洗液重悬细胞调整密度至1×107cells/ml,分装至流式管,每管50μl;
21、(2)一抗孵育:加入稀释后小鼠血清,混匀,4℃、避光孵育20min,加入洗液离心洗细胞1次;
22、(3)二抗孵育:加入2μl小鼠二抗,混匀,4℃、避光孵育20min,加入洗液离心洗细胞1次;
23、(4)上机检测:加入50μl洗液重悬细胞,当日上机检测。
24、进一步地,所述步骤(3)的具体操作方式为:取免疫后小鼠脾细胞,按1:1比例与小鼠骨髓瘤细胞混合,利用电融合法进行融合,获得杂交瘤细胞;于融合后第6天、第8天使用hat选择培养基各进行一次细胞换液;于细胞融合后第10天,取主克隆阶段细胞上清进行筛选检测,使用间接elisa方法筛选获得与抗原蛋白结合的阳性主克隆细胞;主克隆经过连续2~3轮有限稀释及相应筛选,直至获得稳定的单克隆细胞株。
25、进一步地,所述步骤(4)中,培养杂交瘤细胞的具体操作方式为:将1ml杂交瘤细胞转入100ml培养瓶中,定期加入一定量的培养基进行细胞扩增,将细胞扩增至所需生产体积。之后加杂交瘤加料液,隔天加料。培养6~8天后收料。
26、进一步地,所述步骤(4)中,纯化的具体操作方式为:使用蛋白a亲和纯化方法对离心后的杂交瘤细胞培养上清进行纯化,收获单克隆抗体。更进一步地,操作步骤如下:
27、(1)根据表达量选取合适规格的蛋白a柱;
28、(2)水平衡:超纯水清洗2cv,将25%乙醇保存液置换掉;
29、(3)平衡层析柱:ac binding+1/5stock buffer平衡10cv;
30、(4)上样:倒入上样;
31、(5)淋洗:淋洗液淋洗5-10cv至蛋白柱平衡;
32、(6)洗脱:ac elution洗脱,前1cv舍弃,收后1.5cv;
33、(7)中和:加入2m tris,ph 8.0中和洗脱抗体;
34、(8)平衡:ac binding平衡5cv至中性;
35、(9)cip清洗:cip清洗5cv以上;
36、(10)冲洗碱:ac binding冲碱,直至出口处ph为中性;
37、(11)保存:25%乙醇平衡2cv,保存柱子。
38、利用上述方法制备得到的识别人msln蛋白的单克隆抗体,可变区vl的核苷酸序列如seq id no.1所示,可变区vh的核苷酸序列如seq id no.2所示,可变区vl的氨基酸序列如seq id no.3所示,可变区vh的氨基酸序列如seq id no.4所示。
39、上述识别人msln蛋白的单克隆抗体在特异性识别间皮素中的应用,在制备特异性识别间皮素的制剂中的应用。
40、本发明的单克隆抗体的制备方法,首先利用义翘神州商品化产品13128-h08h1(296aa~580aa)作为免疫原免疫5只小鼠,免疫后的小鼠进行血清效价检测。利用包被免疫原13128-h08h1(296aa~580aa)进行血清效价elisa检测,以及利用ovcar-3细胞进行流式检测。血清效价elisa和流式检测合格后,选取检测结果最优的1只小鼠进行杂交瘤融合筛选及有限稀释,取免疫后小鼠脾细胞,按1:1比例与sp2/0骨髓瘤细胞混合,利用电融合法进行融合,获得杂交瘤细胞。筛选阳性克隆后通过1~2步有限稀释进行亚克隆化,直至得到稳定分泌单克隆抗体的杂交瘤细胞株,并获取抗体可变区序列,获得的单克隆抗体分别进行elisa和流式验证。
41、本发明得到了稳定分泌单克隆抗体的杂交瘤细胞株,并获取了抗体可变区序列,获得的单克隆抗体具有良好的特异性,可用于靶向抗体类药物或者用于生物检测类实验。
- 还没有人留言评论。精彩留言会获得点赞!