一种用于sul1、sul2、sul3的光驱动扩增-光热分析的方法及装置
本发明涉及一种用于sul1、sul2、sul3的光驱动扩增-光热分析的方法及装置,属于分析检测。
背景技术:
1、抗生素抗性基因是编码一系列蛋白质或其他分子机制,使细菌能够对抗生素产生耐药性的基因,其存在和传播对公共健康、食品安全和环境安全构成了严重威胁。其中,磺胺类抗生素抗性基因是细菌等微生物在面临磺胺类抗生素压力时,通过基因突变或水平基因转移等方式获得的,能够赋予细菌对磺胺类抗生素产生抗性的基因。随磺胺类抗生素广泛使用,其残留物在环境中普遍存在,经食物链传递,导致细菌及人体内的致病菌对磺胺类抗生素产生抗性,严重威胁人体健康。因此,为了应对磺胺类抗性基因带来的挑战,迫切需要开发磺胺类抗生素抗性基因的现场快速检测方法。
2、抗生素抗性基因的检测方法主要基于核酸扩增,包括聚合酶链式反应(pcr)以及等温扩增技术。因pcr扩增时间长且依赖于专业人员及设备,并不适用于现场快速检测。环介导等温扩增即lamp技术能够在等温(通常是60℃~65℃)条件下,利用链置换dna聚合酶(如bst dna聚合酶)和一套特异引物,通过自循环的链置换dna合成完成目标核酸的快速扩增。lamp技术针对靶基因的6个特定区域设计4种特异引物,这4种引物分别为fip(正向内引物)、bip(反向内引物)、f3(正向外引物)和b3(反向外引物)。这些引物在扩增反应中起着关键作用,能够确保扩增的特异性和高效性。
3、lamp的扩增过程主要分为两个阶段:
4、(1)起始阶段:在此阶段,内引物和外引物均参与反应,它们与目标dna的特定区域结合,并在dna聚合酶的作用下进行延伸,形成双哑铃结构dna,这种结构为后续的循环扩增提供了模板;
5、(2)循环扩增阶段:进入此阶段后,只有内引物参与反应,内引物通过链置换dna合成反应,不断产生新的茎环结构dna产物,这些产物又可以作为模板继续参与反应,从而实现靶序列的指数扩增。
6、光驱动扩增,通过将各种光激活剂加入扩增体系中,用发光二极管(led)或激光等作为光源,光激活剂均匀分散于扩增体系,经led激发,为核酸扩增提供能量供应。chen等人建立了一种聚吡咯包覆氧化铁粒子介导的光驱动lamp,可在约1小时内检测大肠杆菌中低至8cfu的malb基因(biosensors and bioelectronics 2022,215,114574)。
7、目前尚未有利用光驱动扩增技术实现多个基因同时lamp扩增的报道。使用光激活剂介导、光驱动lamp的挑战在于需要具有更高活性的光激活剂,操作难点在于光激活剂需要与lamp体系兼容且不干扰反应;需有可精确控制的光源和光驱动条件以避免影响扩增稳定性;需开发高灵敏度、高特异性的检测方法。
8、外同轴反射led光源与其他led光源在多个方面存在显著的区别,主要体现在结构设计、光线特性、应用场景以及光学效率上。外同轴反射led光源主要由侧向光源和分光镜组成,光源发出的光线首先经过分光镜,然后被平行反射至待测物上。其他led光源如环形光源、条形光源、线型光源等,它们的结构设计各不相同,但通常不包含分光镜这一组件。例如,环形光源直接照射被测物体上方,条形光源则提供直射、斜射及测光等多种照射效果。外同轴反射led光源由于采用了分光镜设计,光线经过分光镜后能够均匀照射在物体表面,减少阴影和反射造成的干扰。同时,这种光源通常具有较高的亮度和均匀性,能够突出物体的外形轮廓特征。其他led光源虽然也具备各自的光线特性,如环形光源能够解决对角照射阴影问题,条形光源照射角度与安装随意可调等,但相比之下,外同轴反射led光源在光线均匀性和减少阴影方面更具优势。外同轴反射led光源分光镜设计减少光损失,从而提高光学效率。
9、目前尚未有利用外同轴反射led光源激发-光驱动多重lamp扩增结合光热试纸技术同时检测磺胺类基因的相关报道。
技术实现思路
1、技术问题:现有光驱动扩增光激活剂的效率不理想;光驱动扩增技术尚未应用于同时扩增多个抗性基因;外同轴反射led光源虽具有光线均匀性和减少阴影的优势,但尚未与光驱动扩增及光热试纸技术结合用于检测磺胺类抗性基因。使用光激活剂介导、光驱动lamp的挑战与操作难点在于光激活剂需与lamp体系兼容且不干扰反应;需有可精确控制的光源和光驱动扩增条件以避免影响扩增稳定性;需开发高灵敏度、高特异性的检测方法。
2、发明目的:为了克服上述的现有技术的不足与缺陷,本发明提供一种用于sul1、sul2、sul3的光驱动扩增-光热分析的方法及装置,采用光激活剂sb2moo6@nifes2作为光热材料,利用其光致活性产生光电子和光热效应,在808nm外同轴反射led光源照射下,实现快速控温且与lamp扩增体系在分子层面直接接触,光热效率显著提高,然后再进行光热试纸显色检测,从而实现光驱动扩增和光热侧流层析试纸检测两个环节的集约化高效扩增及检测。
3、技术方案:本发明采用以下技术方案。
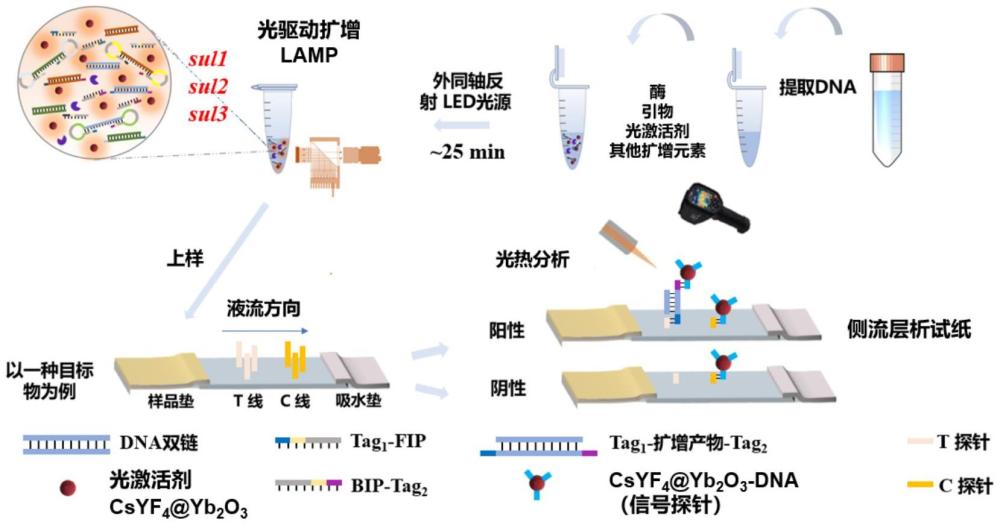
4、本发明的第一个目的是,提供一种利用光激活剂sb2moo6@nifes2及光热侧流层析试纸实现抗性基因sul1、sul2和sul3光驱动lamp及检测的方法。该方法包括光驱动扩增和光热侧流层析试纸检测两个环节。首先,利用808nm外同轴反射led光源照射光驱动扩增体系,激发光驱动扩增体系中的光激活剂sb2moo6@nifes2产生光电子和热,为lamp提供能量,使sul1、sul2和sul3作为模板引发扩增反应,获得大量双链dna扩增产物;以三种核酸链修饰光激活剂sb2moo6@nifes2得到三种光热信号探针,并分别在光热侧流层析试纸的检测区和质控区固定t探针和c探针,得到针对目标基因sul1、sul2、sul3的光驱动lamp产物的多靶标光热侧流层析试纸;然后,通过光热侧流层析试纸以夹心形式捕获扩增产物和信号探针,给出与扩增产物含量正相关的光热温变信号,实现目的基因的定量检测。所述lamp等温扩增体系包括以下组分:引物组、光激活剂sb2moo6@nifes2、dna模板、bst3.0 dna聚合酶以及等温扩增缓冲液。
5、使用光激活剂介导、光驱动lamp的挑战在于需要具有更高活性的光激活剂,操作难点在于光激活剂需要与lamp体系兼容且不干扰反应;需有可精确控制的光源和光驱动条件以避免影响扩增稳定性;需开发高灵敏度、高特异性的检测方法。
6、具体的,本发明一种用于sul1、sul2、sul3的光驱动扩增-光热分析的方法,包括以下步骤:
7、s1、制备光激活剂sb2moo6@nifes2
8、s2、光驱动扩增
9、在光激活剂sb2moo6@nifes2介导下,使用808nm外同轴反射led光源的照射,待测样品经光驱动环介导等温扩增即光驱动lamp等温扩增体系进行扩增反应,得到扩增产物,其中,
10、所述lamp等温扩增体系包括以下组分:引物组、光激活剂sb2moo6@nifes2、dna模板、bst3.0 dna聚合酶以及等温扩增缓冲液,所述dna模板为抗性基因sul1、sul2和sul3;
11、s3、光热试纸检测
12、在试纸的t区和c区固定捕获探针,得到针对目标基因sul1、sul2、sul3光驱动lamp产物的多靶标光热侧流层析试纸;
13、分别以sul1、sul2、sul3的核酸链修饰光激活剂sb2moo6@nifes2得到光热信号探针;
14、使用所述光热信号探针及所述光热侧流层析试纸检测所述扩增产物,光热侧流层析试纸的检测区以夹心形式捕获扩增产物和光热信号探针,并在808nm外同轴反射led光源照射下给出与扩增产物含量正相关的光热温变信号,根据该温变信号对待测样品中sul1、sul2、sul3定性和/或定量。
15、作为一种可选的实施方式,所述808nm外同轴反射led光源的照射参数为功率4.5-6w,照射时间10-30min。
16、作为一种可选的实施方式,所述光激活剂sb2moo6@nifes2的制备方法包括以下步骤:
17、(1)将ni(no3)2·6h2o、fecl2和ch4n2s按1:1:8-1:1:10摩尔比溶解于去离子水中,搅拌1-2h,得混合溶液。
18、(2)将所述混合溶液注入sb2moo6的水溶液中,sb2moo6与硝酸镍的摩尔比为1:2-1:4,在反应釜中160-180℃加热1-2h,反应结束后,得初产物;
19、(3)将产物经离心、洗涤及干燥后,得到sb2moo6@nifes2。
20、作为一种可选的实施方式,步骤(1)中,所述硝酸镍溶解于水中的浓度为0.4-0.5mm。优选为0.4mm。
21、作为一种可选的实施方式,步骤(2)中,所述sb2moo6溶解于水中的浓度为0.1-0.25mm。优选为0.2mm。
22、作为一种可选的实施方式,步骤(3)中,所述离心包括,在10000-12000rpm离心10-15min。优选为在10000rpm离心15min。
23、作为一种可选的实施方式,所述干燥包括,在烘箱中50-55℃干燥20-24h。优选为在烘箱中50℃干燥24h。
24、作为一种可选的实施方式,所述lamp等温扩增体系中,每组dna模板的浓度为4%-8%v/v。
25、作为一种可选的实施方式,所述引物组包括三组引物,每组引物包括两个外部引物f3和b3、两个内部引物fip和bip,及两个环引物loop f和loop b。
26、作为一种可选的实施方式,所述lamp等温扩增体系中,每组引物中两个外部引物f3和b3的浓度为2%-6%v/v,两个内部引物fip和bip的浓度为2%-6%v/v,两个环引物loop f和loop b的浓度为0%-4%v/v。
27、作为一种可选的实施方式,所述lamp等温扩增体系还包括以下组分:bsa、dntps、甜菜碱及ddh2o。
28、作为一种可选的实施方式,所述lamp等温扩增缓冲液包括tris-hcl,(nh4)2so4,kcl,mgso4,tween-20。
29、作为一种可选的实施方式,光热信号探针独立于光热侧流层析试纸主体使用,或者滴加并干燥在结合垫上并将结合垫整合于试纸上。
30、本发明的第二个目的是,提供一种用于sul1、sul2、sul3的光驱动扩增-光热分析的装置,用于实现上述方法的集成化、便捷化操作,具体的,该装置包括808nm外同轴反射led光源、光驱动扩增装置及光热侧流层析试纸组件,其中,
31、所述光驱动扩增装置包括:避光保温外壳,及设置于所述避光保温外壳内部的光驱动扩增组件,其中,
32、所述光驱动扩增组件包括样品支架,其上设有n个贯穿的pcr管孔道,用于放置pcr管,其中n≥1;所述pcr管用于盛放光驱动扩增体系,所述光驱动扩增体系含有引物组、光激活剂sb2moo6@nifes2、dna模板、bst3.0 dna聚合酶以及等温扩增缓冲液,所述dna模板为抗性基因sul1、sul2和sul3;
33、所述避光保温外壳的前部具有横向设置的样品孔道,所述光驱动扩增组件插入并固定在所述样品孔道中;所述808nm外同轴反射led光源位于所述避光保温外壳的后部,朝向所述光驱动扩增组件和光热侧流层析试纸组件设置;
34、所述光热侧流层析试纸组件包括竖直或横向设置的光热侧流分析试纸和光热信号探针,所述光热信号探针分别以sul1、sul2、sul3的核酸链修饰光激活剂sb2moo6@nifes2得到,其中,
35、当光热侧流分析试纸竖直设置时,具体包括,在所述避光保温外壳的前侧内底部设有竖直的试纸槽道,所述光热侧流分析试纸竖直插入并固定在所述试纸槽道中;
36、当光热侧流分析试纸横向设置时,具体包括,所述光热试纸组件包括试纸支架和光热侧流分析试纸,所述试纸支架插入并固定在所述样品孔道中,所述试纸支架上含有矩形凹槽,所述光热侧流分析试纸固定在所述矩形凹槽中。
37、作为一种可选的实施方式,所述808nm外同轴反射led光源包括led光源、分光镜及平凸柱透镜,所述平凸柱透镜竖直设置于所述避光保温外壳内部,其平面一侧朝前,所述led光源水平置于所述平凸柱透镜后侧底部位置,所述分光镜呈45°倾斜设置于所述平凸柱透镜与所述led光源之间,led光源经过分光镜及平凸柱透镜后聚集为线性光斑,构成外同轴反射led光源。
38、作为一种可选的实施方式,所述led光源的波段在800-810nm。
39、作为一种可选的实施方式,所述led光源的照射参数为功率4.5-6w,照射时间10-30min。
40、作为一种可选的实施方式,所述避光保温外壳的两侧相对具有分光镜槽道、平凸柱透镜槽道,分别用于插入分光镜、平凸柱透镜。
41、作为一种可选的实施方式,所述避光保温外壳的顶部设有观测孔道,位于平凸柱透镜的平面前侧,用于观测光驱动扩增组件和/或光热侧流分析试纸。
42、有益效果:本发明提供的光驱动扩增-光热分析的方法和装置,应用光激活剂sb2moo6@nifes2的光致活性产生光电子和光热效应,能快速控温且与扩增体系在分子层面直接接触,比传统水浴、金属浴效率显著提高,同时,以该光激活剂为光热试纸的信号探针,提供了灵敏且可定量的信号。整套方法可以快速实现多种目标dna的高效扩增和检测。
- 还没有人留言评论。精彩留言会获得点赞!