一种环己烯衍生物的不对称催化氢化方法与流程
本发明涉及有机化合物的氢化领域,具体涉及一种环己烯衍生物的不对称催化氢化方法。
背景技术:
1、在化合物合成领域,特别是在药物中间体的合成过程中,不对称氢化还原双键是一项至关重要的反应步骤。这一步骤旨在通过特定的催化过程,将含有双键的底物转化为具有特定构型的化合物。目前,不对称催化氢化还原双键最常用的方法是利用金属或金属络合物作为催化剂,然而,这种方法在实际应用中面临着一系列挑战。首先,金属或金属络合物催化剂在催化还原底物时,往往存在选择性较差的问题,这意味着催化还原反应可能产生多种还原产物,而目标构型的化合物只是其中之一。因此,为了获得纯净的目标构型化合物,后续通常需要繁琐的拆分步骤,这不仅增加了生产成本,还降低了生产效率。其次,底物转化效率也是影响不对称催化氢化还原双键应用效果的关键因素,特别是当底物和还原产物结构差别较小时,两者的分离变得尤为困难,导致底物转化效率显著降低。这种情况下,即使催化剂本身具有一定的活性,也难以实现高效的催化转化。此外,催化剂的选择对于待还原底物来说至关重要。理想的催化剂应具有高转化率和高选择性,即能够将待还原底物几乎完全转化为目标构型的化合物(例如,转化率达到99%或以上),并且生成的还原产物具有高度的对映选择性(例如,ee值达到99%或以上)。然而,现有的金属或金属络合物催化剂往往难以满足这些要求。
2、为了解决上述问题,研究者们尝试采用基于溶解度差异分离/拆分技术或酶法拆分等方法来分离非对映异构体或制备单独的立体异构体。然而,这些方法的应用范围有限,仅适用于含有特殊结构的化合物,且酶法拆分对应异构体通常对反应条件要求较为苛刻,如温度、ph值等,这在一定程度上限制了其后续应用。中国专利cn117362142a采用金属铱类催化剂进行催化,虽然取得了一定的效果,但金属铱的昂贵价格限制了其广泛应用。
3、因此,当前迫切需要开发一种新型的不对称催化氢化还原双键方法,该方法应能够使用价格更为便宜易得的催化剂,同时实现高转化率和高选择性。
技术实现思路
1、为解决上述技术问题,本发明提供一种环己烯衍生物的不对称催化氢化方法。
2、本发明通过以下技术方案实现:
3、本发明提供一种环己烯衍生物的不对称催化氢化方法,包括以下步骤:
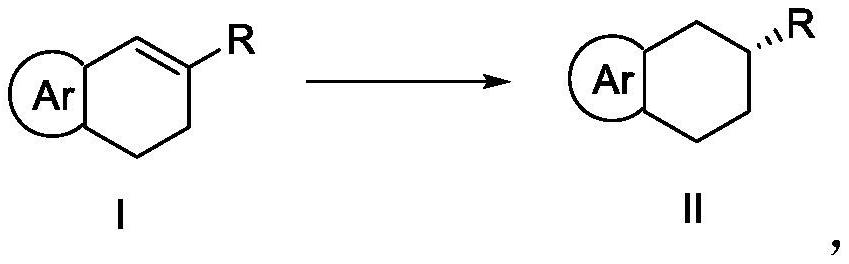
4、在氢气氛围下,式i所示的化合物(即环己烯衍生物)在催化剂、酸以及溶剂的存在下进行不对称氢化还原反应,形成式ⅱ所示的化合物,反应式如下所示:
5、
6、其中,ar选自芳基或杂芳基,所述芳基或杂芳基任选地被一个或多个选自烷基、烷氧基、环烷基、芳基、卤素、硝基、含酰基的基团、含磺酰基的基团或杂芳基的取代基所取代;
7、r选自烷基、烷氧基、环烷基、杂环基、芳基或杂芳基,所述烷基、烷氧基、环烷基、杂环基、芳基、杂芳基任选地被一个或多个选自卤素、硝基、氰基、氨基、烷基、烷氧基、环烷基、杂环基、含酰基的基团、含磺酰基的基团、芳基、杂芳基的取代基所取代;
8、所述催化剂由配体和钌盐反应得到,所述配体选自下式所示的化合物:
9、
10、式ⅲ中,r1、r2、r3和r4各自独立地选自氢、卤素、烷基、烷氧基、环烷基或芳基,其中所述烷基、烷氧基、环烷基、芳基任选地被一个或多个选自卤素、硝基、氰基、烷基、烷氧基、环烷基、含酰基的基团、含磺酰基的基团或芳基的取代基所取代;
11、式ⅳ和v中,r5独立地选自氢、烷基、烷氧基、环烷基或芳基,其中所述烷基、烷氧基、环烷基或芳基任选地被一个或多个选自卤素、硝基、烷基、烷氧基、环烷基、含酰基的基团、含磺酰基的基团或芳基的取代基所取代;
12、式ⅵ中,r6和r7各自独立地选自氢、卤素、烷基、烷氧基、环烷基或芳基,或者r6和r7连同其连接的碳形成5至6元环,或者两个苯环上的r7连同其连接的碳形成7至12元环,其中所述烷基、烷氧基、环烷基、芳基、5至6元环、7至12元环任选地被一个或多个选自卤素、硝基、氰基、烷基、烷氧基、环烷基、含酰基的基团、含磺酰基的基团或芳基的取代基所取代;r8为芳基,其中所述芳基任选地被一个或多个选自卤素、硝基、氰基、烷基、烷氧基、环烷基、含酰基的基团、含磺酰基的基团或芳基的取代基所取代;
13、所述钌盐选自对伞花烃二碘化钌(ⅱ)二聚体、二氯双(4-甲基异丙基苯基)钌(ⅱ)二聚体、二羰基环戊二烯基二钌(ⅱ)二聚体、二氯(五甲基环戊二烯基)钌(ⅱ)二聚体、二氯苯基钌(ⅱ)二聚体、(六甲基苯)合二氯化钌(ⅱ)二聚体、(1,5-环辛二烯)二氯化钌(ⅱ)和三羰基二氯代钌二聚物中的一种或几种;
14、所述酸选自盐酸、甲酸、硫酸、醋酸、三氟乙酸、三氟甲磺酸、苯甲酸和柠檬酸的一种或几种。
15、优选地,式i和式ⅱ中,ar为苯环,其中所述苯环被一个或多个选自卤素、烷基、烷氧基的取代基所取代。
16、优选地,式i和式ⅱ中,r为苯环,其中所述苯环被一个或多个选自卤素、硝基、氰基、氨基、烷基、烷氧基的取代基所取代。
17、优选地,式ⅲ中,r1、r2、r3和r4各自独立地选自氢、烷基、环烷基或苯基,其中所述烷基、环烷基、苯基任选地被一个或多个选自烷基、烷基、环烷基、苯基的取代基所取代。
18、优选地,式ⅳ和v中,r5独立地选自氢、烷基、环烷基或苯基,其中所述烷基、环烷基或苯基任选地被一个或多个选自烷基、环烷基、苯基的取代基所取代。
19、优选地,式ⅵ中,r6和r7各自独立地选自氢、烷基、环烷基或苯基,或者r6和r7连同其连接的碳形成5至6元环,其中所述烷基、环烷基或苯基任选地被一个或多个选自烷基、烷基、环烷基、苯基的取代基所取代,所述5至6元环被苯环取代并与取代的苯环共用两个碳原子。
20、进一步地,所述溶剂选自甲醇、乙醇、异丙醇、丙醇、氯甲烷、乙腈、甲苯、二甲苯、叔丁醇、丁醇、异丁醇、丙酮、1,4-二氧六环、四氢呋喃、甲基叔丁基醚、二乙酸乙酯和乙酸甲酯中的一种或几种。
21、进一步地,所述式i所示的化合物与溶剂的用量比为(5-40)mg:1ml,优选为(10-20)mg:1ml。
22、进一步地,所述式i所示的化合物的结构如下式i-1所示:
23、
24、其中,r9为氢或羟基保护基;
25、r10和r11各自独立地选自氢、烷基或含酰基的基团,所述烷基任选地被一个或多个选自卤素、硝基、氰基、氨基、烷基、烷氧基、环烷基、苯基、含酰基的取代基所取代;
26、r12选自氢、烷基或环烷基,所述烷基、环烷基任选地被一个或多个选自卤素、硝基、氰基、氨基、烷基、烷氧基、苯基的取代基所取代。
27、优选地,所述羟基保护基选自tms(三甲基硅基)、tips(三异丙基硅基)、tbs(叔丁基二甲基)、me(甲基)、et(乙基)、pr(丙基)、bn(苄基)、ch3co(乙酰基)、ch3ch2co(丙酰基)、phco(苯甲酰基)、ch3so2(甲磺酰基)或phso2(苯磺酰基)。
28、进一步地,式i-1所示的化合物选自如下结构中的一种:
29、
30、进一步地,所述不对称氢化还原反应的温度为0-130℃,优选为50-100℃,更优选为60-90℃。
31、进一步地,所述不对称氢化还原反应在氢气压力为1-100bar的条件下进行,氢气压力优选为50-80bar。
32、进一步地,所述式i所示的化合物与催化剂的摩尔比为(100-10000):1,优选为(200-3000):1。
33、进一步地,所述催化剂的制备方法包括以下步骤:所述配体和钌盐反应形成络合物,即得所述催化剂。
34、进一步地,所述配体和钌盐的摩尔比为1:(0.8-1.2)。
35、进一步地,所述催化剂选自以下结构所示的化合物:
36、
37、
38、本发明还保护上述催化剂在不对称催化还原双键中的应用。
39、在具体实施方式中,本发明提供一种式i-1所示的化合物的不对称催化氢化方法,包括以下步骤:
40、在氢气氛围下,式i-1所示的化合物在催化剂、酸以及溶剂的存在下进行不对称氢化还原反应,形成式ⅱ-1所示的化合物,反应式如下所示:
41、
42、其中,r9选自h、bn、cbz或ac,所述催化剂选自以下结构所示的化合物:
43、
44、
45、本发明的有益效果:
46、1.本发明提供的环己烯衍生物的不对称催化氢化方法中,针对环已烯衍生物底物,实现了高转化率和优异的选择性,所得还原产物的对映体过量(ee)值高,可达到99%,适合于工业化放大生产,能够有效提升生产效率和产品纯度,满足大规模生产的需求。
47、2.相较于现有技术中常用的手性拆分方法,本发明采用催化剂对环己烯衍生物进行不对称催化氢化,其成本更低。同时,本发明采用钌催化剂替代现有技术中的铱催化剂进行不对称催化氢化,由于钌相较于铱更为廉价且易得,因此进一步降低了生产成本。
- 还没有人留言评论。精彩留言会获得点赞!