一种鉴定分枝杆菌菌种的引物探针组合、试剂盒及其鉴定方法和应用
本发明属于生物,尤其涉及一种鉴定分枝杆菌菌种的引物探针组合、试剂盒及其鉴定方法和应用。
背景技术:
1、分枝杆菌感染引起的结核病和非结核病是世界范围内的公共卫生问题。结核病是由结核分枝杆菌复合群(mycobacterium tuberculosis complex,mtbc)引起的慢性传染病,根据世界卫生组织发布的《2023年全球结核病报告》,2022年,全球结核病估算发病患者为1060万,约有130万例患者死于结核病,我国新发患者数约为74.8万,位列全球第三。
2、非结核分枝杆菌(non-tuberculous mycobacteria,ntm)与mtbc同属分枝杆菌属,是一大类广泛存在于土壤、自来水或空气中的环境细菌。一些ntm可侵犯人体器官和组织,引起各种疾病,主要包括肺病、淋巴结炎、皮肤和软组织感染以及全身播散性疾病等,免疫缺陷或免疫功能不全的人群更容易感染非结核病并引发疾病。其中,ntm肺病和肺结核的临床症状相似,只有通过菌种鉴定才能做出诊断。然而,传统的涂片抗酸染色和结核实验室的分枝杆菌分离培养均无法区分结核分枝杆菌复合群(mtbc)和ntm。如果ntm肺病被误诊为肺结核,并用抗结核药物治疗,治疗效果往往较差,因为ntm天生对抗结核药物有耐药性,非结核病和肺结核的治疗方案存在差异。此外,不同ntm菌株对药物的敏感性也各不相同。因此,为了指导临床治疗方案的选择,分枝杆菌菌种的鉴定具有重要意义。
3、近年来,由于培养周期长、操作繁琐、准确性差,传统的生化鉴定已逐渐被分子生物学方法所取代。目前,常见的分子鉴定方法包括线性探针分析(lpa)、实时荧光pcr、基质辅助激光解吸串联飞行时间质谱仪(maldi-tof ms)和dna sanger测序法等。其中,lpa需要pcr后处理,存在扩增产物被污染的风险,操作步骤繁琐,至少需要6个小时才能产生结果。实时荧光pcr是一种针对待测样本特异性靶基因设计引物探针,通过pcr反应过程中荧光信号的变化来实现检测的方法,实时荧光pcr检测时间短、特异性强、灵敏度高,但其检测通量往往受限于荧光通道的数量,目前市面上大多数荧光pcr仪仅有4~6个通道,这使得实时荧光pcr单管同时检测多重靶标的能力有限。近年来,maldi-tof ms技术发展迅速,广泛应用于细菌感染的鉴定,但它只能鉴定临床分离株。由于大多数ntm是生长缓慢的细菌,在maldi-tof ms鉴定之前至少需要几周的分离和培养,这严重影响了该方法的及时性。dnasanger测序法是基因检测方法的“金标准”,但它需要专门的测序设备,价格昂贵,无法在临床实验室广泛应用。
4、目前,关于分枝杆菌菌种鉴定已有相关的商品化试剂盒,其中包括亚能生物技术(深圳)有限公司的《分枝杆菌菌种鉴定基因检测试剂盒(pcr-反向点杂交法)》和成都博奥晶芯生物科技有限公司的《分枝杆菌菌种鉴定试剂盒(dna微阵列芯片法)》,这两款试剂盒的基本原理均为将扩增产物与dna探针进行杂交,利用杂交条带的显色/发光反应来进行分枝杆菌菌株鉴定。该方法与测序法相比,在一定程度上简化了操作,因此在临床中得到了进一步的应用,但该方法存在一定的局限性,如检测灵敏度较差(分别为105个细菌/ml和103个细菌/pcr反应)、鉴别能力较弱等(如两款试剂盒均无法区分龟分枝杆菌和脓肿分枝杆菌等)。基于荧光pcr熔解曲线法,厦门致善生物科技股份有限公司开发了《分枝杆菌鉴定试剂盒(荧光pcr熔解曲线法)》,该试剂盒鉴别能力较强,可准确鉴定19种临床常见的分枝杆菌,但该方法非全自动化检测产品,检测时间相对较长(4h),且无法直接对临床痰液样本进行检测,而是需要对痰液样本进行培养后方可检测,因此仍然限制了其在临床中的应用。
技术实现思路
1、为了解决上述技术问题,本发明提供了一种鉴定分枝杆菌菌种的引物探针组合、试剂盒及其鉴定方法,可在2小时内同时鉴定临床常见多种分枝杆菌,且特异性好、检测灵敏度高。
2、本发明的鉴定分枝杆菌菌种的引物探针组合,包括以下引物和探针中的一种或几种,分别为:
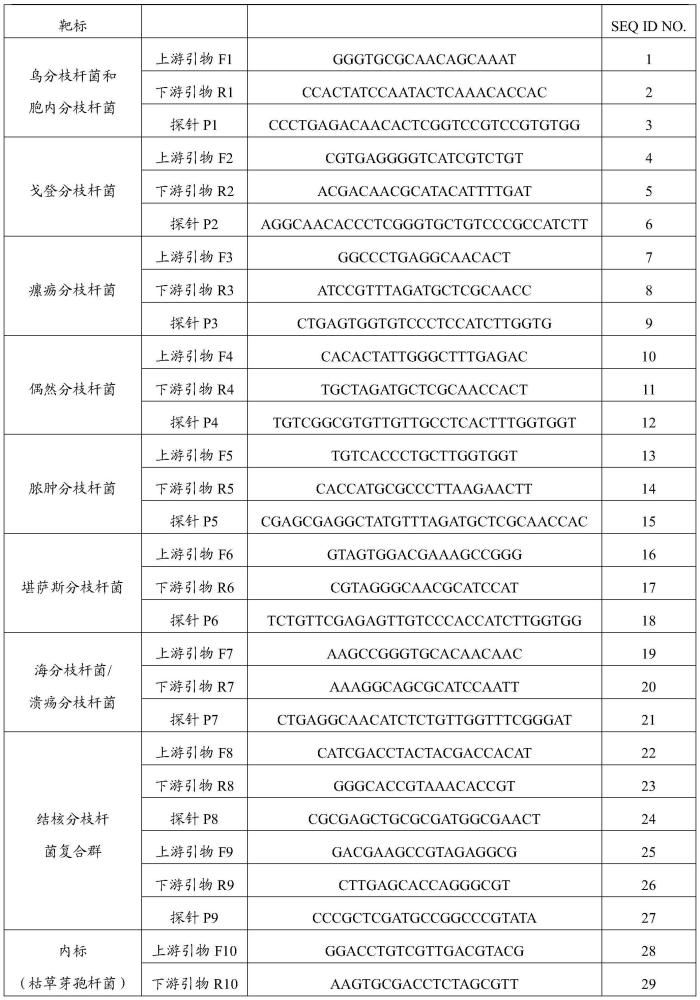
3、鉴定鸟分枝杆菌和胞内分枝杆菌的引物的核苷酸序列如seq id no.1和seq idno.2所示,探针如seq id no.3所示;
4、鉴定戈登分枝杆菌的引物的核苷酸序列如seq id no.4和seq id no.5所示,探针如seq id no.6所示;
5、鉴定瘰疬分枝杆菌的引物的核苷酸序列如seq id no.7和seq id no.8所示,探针如seq id no.9所示;
6、鉴定偶然分枝杆菌的引物的核苷酸序列如seq id no.10和seq id no.11所示,探针如seq id no.12所示;
7、鉴定脓肿分枝杆菌的引物的核苷酸序列如seq id no.13和seq id no.14所示,探针如seq id no.15所示;
8、鉴定堪萨斯分枝杆菌的引物的核苷酸序列如seq id no.16和seq id no.17所示,探针如seq id no.18所示;
9、鉴定海分枝杆菌或溃疡分枝杆菌的引物的核苷酸序列如seq id no.19和seq idno.20所示,探针如seq id no.21所示;
10、鉴定结核分枝杆菌复合群的包括2对引物和2条探针,第1对引物的核苷酸序列如seq id no.22和seq id no.23所示,探针如seq id no.24所示;第2对引物的核苷酸序列如seq id no.25和seq id no.26所示,探针如seq id no.27所示。
11、优选的是,还包括1对引物和探针鉴定内标;所述引物的核苷酸序列如seq idno.28和seq id no.29所示,探针如seq id no.30所示。
12、更优选的是,所述分枝杆菌和内标的检测探针5’端修饰有荧光基团,3’端修饰有淬灭基团;
13、所述荧光基团选自fam、vic、tet、joe、hex、cy3、cy5、tamra、rox、texas red、cy5.5或cy7中的任意一种;
14、所述淬灭基团选自bhq0、bhq1、bhq2、bhq3或mgb中的任意一种。
15、本发明还提供了一种鉴定分枝杆菌菌种的试剂盒,所述试剂盒包括所述的引物探针组合。
16、本发明还提供了一种利用所述试剂盒鉴定分枝杆菌菌种的方法,包括以下步骤:(1)提取待测样品的核酸;(2)以提取的核酸作为模板进行pcr扩增,对pcr扩增的结果进行判读,鉴定出待测样品中的分枝杆菌菌种。
17、优选的是,所述pcr扩增的体系为:模板0.1~50μl,pcr扩增试剂5~50μl;所述pcr扩增试剂的配制为:2×扩增mix 1×;所述的引物各0.01~10μm,探针各0.01~10μm。
18、优选的是,所述pcr扩增的程序为:95℃预变性1~3min,95℃变性3~120s,55~65℃退火延伸5~100s共40~60个循环,95℃变性1~3min,35~45℃保温1~3min,40℃~90℃做熔解曲线分析,每步升温0.1~10℃。
19、优选的是,所述鉴定分枝杆菌菌种的方式为:通过不对称pcr的特异性熔解曲线tm值鉴定非结核分枝杆菌,通过对称pcr的扩增曲线ct值鉴定结核分枝杆菌复合群。
20、更优选的是,所述鉴定非结核分枝杆菌时,瘰疬分枝杆菌的tm值判读区间为65.0~69.0,戈登分枝杆菌的tm值判读区间为69.1~75.0,偶然分枝杆菌的tm值判读区间为73.0~78.0,脓肿分枝杆菌的tm值判读区间为65.0~76.0,鸟分枝杆菌的tm值判读区间为63.0~70.0,胞内分枝杆菌的tm值判读区间为70.1~76.0,堪萨斯分枝杆菌的tm值判读区间为66.0~73.0,海分枝杆菌或溃疡分枝杆菌的tm值判读区间为66.0~78.0,内标的tm值判读区间为79.0~82.0;所述鉴定结核分枝杆菌复合群时,结核分枝杆菌复合群的ct≤42。
21、本发明还提供了一种所述引物探针组合或所述试剂盒在鉴定分枝杆菌菌种或制备鉴定分枝杆菌菌种试剂中的应用。
22、相较于现有技术,本发明的有益效果如下:
23、本发明的引物探针组合或试剂盒可实现1个样本同步检测多个指标(最多可同步检测9个指标),同时鉴定结核分枝杆菌复合群和8种非结核分枝杆菌;且在多重体系下检测灵敏度高,结核分枝杆菌复合群最低检出限为50cfu/ml,非结核分枝杆菌最低检出限为500cfu/ml。
- 还没有人留言评论。精彩留言会获得点赞!